重视急性胰腺炎后糖尿病的发生与发展
2022-06-01钱苏皖童智慧
钱苏皖 童智慧
南京医科大学金陵医学院重症医学科,南京 210002
【提要】 急性胰腺炎后糖尿病(PPDM-A)是AP患者常见的并发症。与其他类型的糖尿病相比,其发病机制、诊断标准及治疗方法均有特殊之处。本文系统性阐述PPDM-A的命名变迁、诊断标准、流行病学、发病机制、危险因素、临床特征及治疗方法等,以期引起临床医师对PPDM-A发生与发展的重视。
AP是临床常见的急危重症,20%的患者会发展为重症急性胰腺炎,出现胰腺坏死组织感染、器官功能衰竭等并发症。近年来,随着治疗理念和综合救治水平的提高,由胰腺坏死组织感染和器官功能衰竭所致AP患者的病死率已显著下降,但其远期并发症引起越来越多的关注,其中一个并发症就是急性胰腺炎后糖尿病(post-acute pancreatitis diabetes mellitus, PPDM-A)。PPDM-A给AP患者的生活质量和预期寿命带来巨大影响,与其他类型的糖尿病相比,其发病机制、诊断标准及治疗方法均有特殊之处[1-2]。但目前对PPDM-A的认识仍显不足,缺乏专门的管理方案。本文对PPDM-A的发生与发展进行阐述,以期在临床及研究工作中有所借鉴。
一、PPDM-A的命名
国际上对胰腺外分泌疾病后糖尿病的命名还未完全统一,目前主要有3c型糖尿病(type 3c diabetes mellitus,T3cDM)和外分泌胰腺糖尿病(diabetes of the exocrine pancreas, DEP)两个名称。T3cDM最早在2008年德国两次小型研讨会上提出[3-4],2020年美国糖尿病协会(American Diabetes Association, ADA)在“糖尿病医疗保健”一文中正式提及“3c型糖尿病”一词[5]。DEP是新西兰学者Petrov在2017年提出的,主要包括胰腺炎后糖尿病(post-pancreatitis diabetes mellitus, PPDM)、胰腺癌相关糖尿病(pancreatic cancer-related diabetes,PCRD)、囊性纤维化相关糖尿病(cystic fibrosis-related diabetes, CFRD)等[6],其中PPDM又包含PPDM-A和慢性胰腺炎后糖尿病(post-chronic pancreatitis diabetes mellitus,PPDM-C)(图1)。相比较而言,两个名称各有特点,T3cDM是1型糖尿病(type 1 diabetes mellitus,T1DM)和2型糖尿病(type 2 diabetes mellitus,T2DM)概念的延续,但这一名称包含甚广,急、慢性胰腺炎,胰腺创伤,胰腺切除术,胰腺肿瘤,胰腺囊性纤维化,血色素沉着症,纤维结石性胰腺病等胰腺外分泌疾病后的糖尿病均包括在内,而DEP相对独立,其下有专门的PPDM-A这一分类,可与PPDM-C相区分。
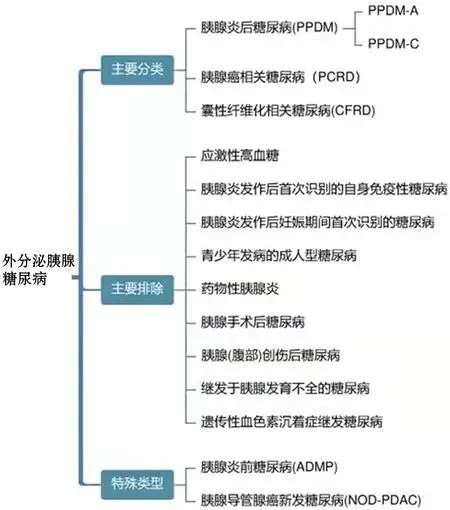
图1 外分泌胰腺糖尿病分类(引自文献[7])
此外,在临床上还需区分“胰腺炎后新发糖尿病(new onset diabetes after pancreatitis,NODAP)”与“PPDM”这两个概念的差别。当AP或CP首次发作时,若通过检测糖化血红蛋白(hlycatedhaemoglobin,HbA1c)确认胰腺炎发病之前无糖尿病,则使用NODAP来描述更为准确。然而,若胰腺炎患者首次发作时未做HbA1c检验,基线HbA1c和血糖的数据缺失,胰腺炎发病之前是否存在糖尿病不得而知,则采用PPDM描述更为合适。鉴于临床上AP患者首次发作入院前及入院时HbA1c的数据常有缺失,所以使用PPDM-A表示急性胰腺后糖尿病较为恰当[7]。在此,也呼吁临床医师在AP患者首次发作入院时需完善糖尿病的相关检查。
二、PPDM-A的诊断标准和发病率
目前认为,所有符合ADA糖尿病诊断标准且有AP病史的成年人都应考虑PPDM-A,排除标准为已确诊的T1DM、AP首次发作前的T2DM、或AP发病后3个月内的应激性高血糖。之所以采用3个月阈值,是因为HbA1c水平反映了患者测定前8~12周的平均血糖水平,具体诊断流程见图2[1]。需要注意的是,PPDM-A的诊断并不一定要依赖于胰腺外分泌功能不全的存在,因为只有40%的PPDM-A患者存在胰腺外分泌功能不全,且在T1DM和T2DM患者中也发现胰腺外分泌功能降低的情况[8]。
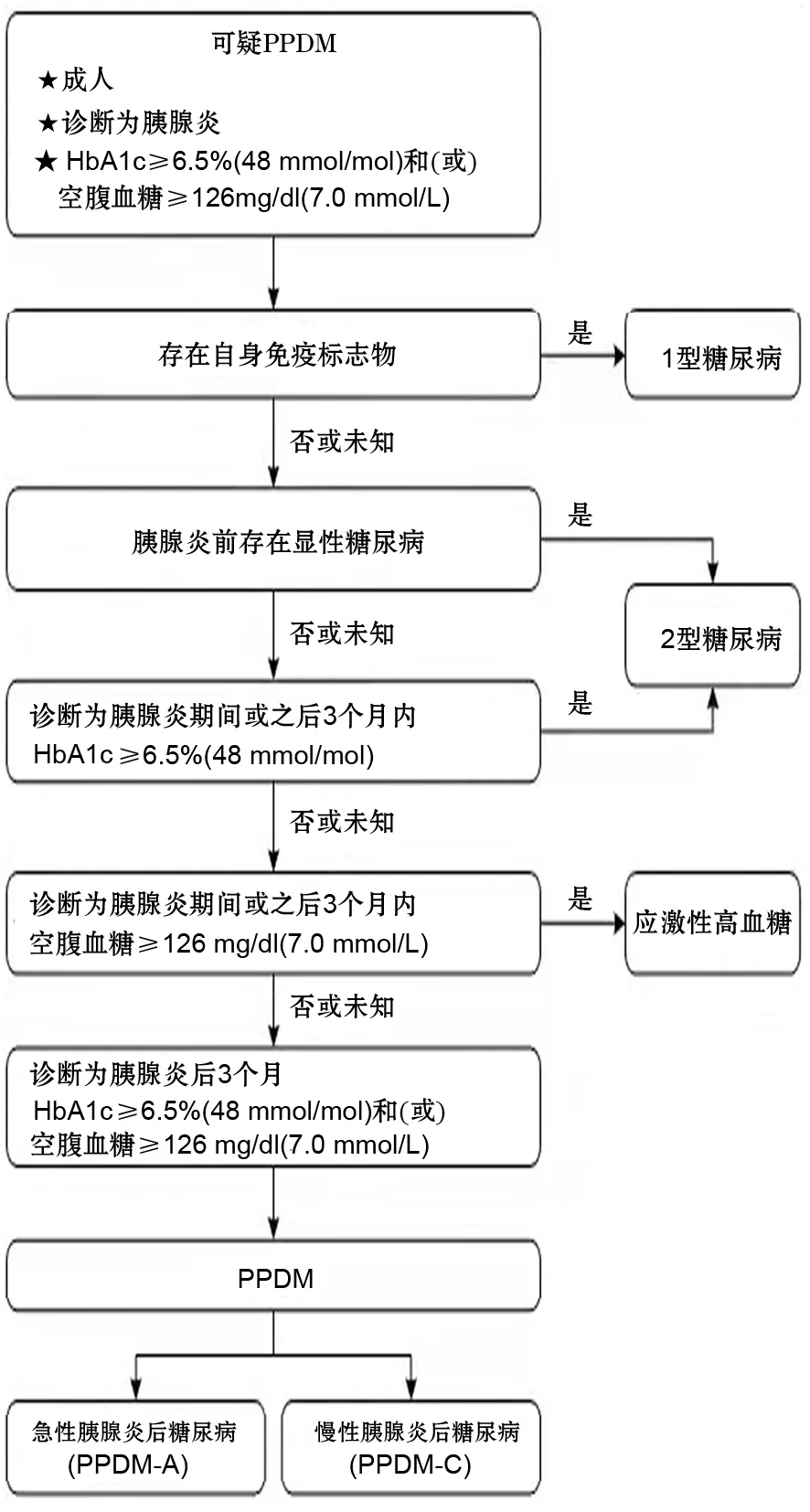
注:PPDM为胰腺炎后糖尿病;HbA1c为糖化血红蛋白
PPDM是DEP最常见的亚型,PPDM-A约占PPDM的4/5[1]。2010年新西兰PPDM-A的发病率为1.8/100 000[9],我国尚无确切的发病率报道。2014年代谢、营养和胰腺疾病的临床流行病学调查(clinical and epidemiological investigations in metabolism, nutrition, and pancreatic diseases,COSMOS)小组发表的一项Meta分析显示,AP首次发作后约23%患者会发生PPDM-A[10],我国台湾省2015年的一项研究调查显示,有AP病史的人群患糖尿病的终生风险至少是普通人群的2倍[11]。2020年Bharmal等[12]随访了AP发作后2年内新发糖尿病的累积发生率,结果显示NODAP的累积发生率在6个月时为3.3%,12个月时为7.2%,18个月时为9.2%,24个月随访时为11.2%,其发病率随时间延长而增加,提示临床医师需在AP发作后对PPDM-A高危人群进行定期随访。
三、PPDM-A的发病机制
目前研究发现,PPDM-A的发病机制主要包括β细胞破坏、胰腺内脂肪沉积、IL-6介导的慢性低度炎症状态、脂质代谢紊乱、铁代谢失调以及胰-肠-脑轴功能障碍所致胰腺激素和肠道激素异常[13]。肠道菌群紊乱是T2DM明确的发病机制之一,然而其在PPDM-A发生、发展中的作用目前尚不明确,有待进一步研究验证。
1.β细胞破坏:笔者所在团队对出院AP患者的内、外分泌功能进行了随访研究,发现胰腺坏死患者的糖尿病发生率较未发生胰腺坏死患者的糖尿病发生率高(38.2%比0,P=0.001),多因素logistic回归分析显示胰腺坏死程度>50%是PPDM-A的独立危险因素[14]。广泛的胰腺坏死后β细胞大量被破坏,进而导致胰岛素严重缺乏,从而产生糖尿病。因此,出现胰腺坏死的AP患者中,β细胞破坏在PPDM-A的发生中起到重要作用。然而无胰腺坏死的AP患者也会发生PPDM-A,其β细胞破坏较少,胰岛素的缺乏程度不至于使其发展成为糖尿病,提示无胰腺坏死的AP后糖尿病潜在的发病机制不限于β细胞破坏,炎症因子降低β细胞对高糖的反应性所致的胰岛素抵抗、胰多肽分泌减少导致肝脏胰岛素受体表达减弱可能是其主要发病机制[15]。
2.胰腺内脂肪沉积:既往研究表明,PPDM-A患者的胰腺内脂肪沉积显著增加,为PPDM-A的危险因素[16-18]。胰腺内脂肪沉积导致胰腺周围持续存在一种慢性低度炎症状态,进而导致胰岛素分泌不足、胰岛素信号转导受损以及胰岛素抵抗,以致糖代谢异常[19]。
3.IL-6:Lesina等[20]研究发现IL-6与PPDM-A显著相关,并将IL-6确定为PPDM-A的主要细胞因子。循环IL-6通过降低胰岛素刺激的胰岛素受体β、胰岛素受体底物-1和蛋白激酶B(protein kinase B,PKB)的磷酸化来负向调节胰岛素信号,还可以通过诱导巨噬细胞募集到组织来促进炎症的发展和随后胰岛素信号的中断,从而导致糖尿病的发生[21]。
4.胰腺激素:2018年Pendharkar等[22]研究发现PPDM-A患者混合膳食试验后,血液中的胰岛素、C肽水平显著升高,但胰岛素敏感性下降,餐后胰高血糖素和胰多肽水平无显著变化。可能的解释为在PPDM-A患者中存在早期β细胞代偿机制,胰岛素及C肽分泌增多,但胰岛素敏感性会降低,且随着病程进展,β细胞开始发生凋亡、坏死,导致胰岛素分泌减少。
5.脂质代谢:研究发现PPDM-A患者的脂质代谢标志物甘油与游离脂肪酸水平显著上升,表明脂肪分解是PPDM-A重要发病机制。脂肪分解增加异位脂质积聚会损害胰岛素信号转导;肝脏脂质的增加也会损害胰岛素调节糖异生和激活糖原合成的能力;脂肪组织中脂解增加会促进其他组织中脂质的再酯化,并进一步加剧胰岛素抵抗,从而导致糖代谢紊乱[23]。
6.肠道激素:与T2DM相比,PPDM-A患者的餐后胃泌酸调节素、胰高血糖素样肽-1(glucagon-like peptide-1, GLP-1)和YY肽水平显著降低,具体机制尚不明确,可能包括GLP-1信号通路受损、炎症持续状态、肠道免疫轴紊乱。另一个值得注意的是,在PPDM-A患者中,肠肽与促炎因子呈显著负相关,这与T2DM患者截然相反[24]。
7.铁代谢:PPDM-A患者的铁调素水平显著升高,肠道铁吸收下调,循环铁蛋白水平显著降低,表明PPDM-A个体铁代谢发生显著改变为发病机制之一[25],其原因可能为炎症反应减少细菌对铁的利用,过量的铁在线粒体中积累,导致线粒体功能障碍,从而抑制三磷酸腺苷的产生,最终抑制胰岛素的分泌[26]。
8.肠道菌群紊乱:在T2DM中肠道菌群通过影响主要代谢器官中的葡萄糖稳态和胰岛素抵抗,以及控制肠道激素的产生而影响糖代谢[27]。然而其是否为PPDM-A的发病机制目前尚不明确。但Petrov[28]认为,AP的慢性炎症和免疫系统激活可能通过改变肠道代谢环境、肠道通透性和肠-脑-胰轴来促进肠道菌群改变,同时外分泌胰腺功能障碍也会通过影响十二指肠PH值引起肠道菌群改变,从而影响糖代谢。
四、PPDM-A的危险因素
PPDM-A的发病危险因素与T1DM及T2DM存在一定区别,男性、青年、肥胖、胰腺炎反复发作、胰腺外分泌功能障碍等均是其患病的危险因素。值得注意的是,无论是轻症还是重型AP都有发展成为PPDM-A的高风险,AP发作的严重程度与发展为PPDM-A的风险大小无关。
1.性别:研究表明,男性DEP的患病率显著高于女性(1.32‰比0.93‰),且PPDM-A和PPDM-C的发病率在男女性之间的差异均有统计学意义,提示男性患PPDM-A的风险比女性更高。然而胰腺癌相关糖尿病的患病率在男女之间的差异无统计学意义[29]。
2.年龄:年龄在20~29岁和30~39岁、有胰腺外分泌疾病病史的患者,新诊断糖尿病的风险显著高于普通人群,40~59岁患DEP和T2DM的风险相当,而60~79岁患T2DM的风险往往高于DEP[30],表明青壮年和中年人患PPDM-A的风险最高。
3.体重指数:英国的一项研究使用了常规体重指数范围,结果表明与T1DM患者相比,PPDM-A及T2DM患者中肥胖个体比例显著增高[31],说明肥胖个体患PPDM-A的风险增加。
4.胰腺炎反复发作:2次或2次以上AP复发的患者胰腺总体积显著降低,β细胞质量显著减少,患PPDM-A的风险显著增加。但在复发1次或无复发的个体中,胰腺总体积没有显著减少,患PPDM-A风险并未增加[32-34]。
5.胰腺外分泌功能障碍:糖尿病患者胰腺外分泌功能障碍的发生率较高。囊性纤维化CTFR基因突变致使胰腺外分泌功能障碍,导致CFRD。2020年一项研究调查胰腺外分泌功能不全与PPDM-A之间间隔超过1年的个体,发现胰腺外分泌功能障碍与PPDM-A的风险呈显著相关[34]。
6.其他:有AP病史的患者无论发作时病情的严重程度如何,都有发展为PPDM-A的高风险倾向,轻症AP患者发展为PPDM-A的风险也很高。痛风会增加女性患PPDM-A的风险,然而在男性当中痛风并非PPDM-A的危险因素[35-36]。
五、PPDM-A的临床特征与治疗方法
PPDM-A的临床特征为胰腺内分泌及外分泌功能均受损,胰岛损伤影响β、α和PP细胞分泌激素,低胰岛素、胰高血糖素和胰多肽的结合导致血糖水平波动大,从而导致血糖控制较差,从轻度损害到低血糖频繁发作,即脆性糖尿病,其胰岛素用量、HbA1c水平、重度低血糖和低血糖昏迷发生率显著高于T2DM;其远期特征为患癌症的风险较高,死亡年龄较低,病死率较高[37-39]。
由于疾病复杂程度不同,胰岛素缺乏程度不同,目前尚无治疗PPDM-A统一的实践指南。药物治疗方面大多是经验治疗。目前推荐二甲双胍为最佳一线治疗药物,因其可以提高PPDM-A患者生存率,但由于脆性血糖难以控制,有时又需要早期启动胰岛素治疗。其他一些经典降糖药物在临床使用中需要关注的问题也颇多。
1.二甲双胍:在糖尿病早期血糖仅轻度升高或伴有明显的胰岛素抵抗时,推荐二甲双胍。新西兰全国胰腺和代谢疾病流行病学(nationwide epidemiology of pancreatic and metabolic diseases,NORMA)项目的一项研究表明,患有PPDM-A的个体中使用二甲双胍者与从不使用抗糖尿病药物者相比生存率显著提高,但二甲双胍对PCRD患者无效。目前二甲双胍单药剂量1 000 mg/d是PPDM-A最佳的一线药物治疗[40]。
2.胰岛素:由于胰腺炎症后β细胞功能障碍,肠道消化吸收障碍及肠促胰素分泌减少,机体对高血糖反应敏感性降低,有时口服降糖药很难控制PPDM-A血糖水平,导致启用胰岛素时机较早。研究表明胰岛素作为PPDM-A的一线治疗与显著降低病死率无关,且与首次AP发作进展为复发性AP或慢性胰腺炎的风险增加相关;可能的生物学机制包括胰腺内脂肪沉积驱动的胰腺组织低度炎症和纤维化[41]。
3.其他降糖药物:磺脲类和格列奈类属于胰岛素促泌剂,可增加胰岛素的分泌,导致低血糖风险增高,而慢性高胰岛素血症可能成为胰腺癌发生的高危因素;噻唑烷二酮类药物有增加骨折风险可能,而胰腺外分泌功能障碍患者容易合并骨质疏松;α-糖苷酶抑制剂可能加剧现有的胰腺外分泌功能不足所致的消化不良;GLP-1受体激动剂和二肽基肽酶4抑制剂属于肠促胰素类药物,这些药物虽能促进胰岛素分泌,但胃肠道不良反应明显;钠-葡萄糖协同转运蛋白2抑制剂可增加尿糖排泄,降低血压、血糖、血脂和血尿酸水平,但同时可能会导致营养物质丢失,有脱水及酮症酸中毒的风险[42]。
4.拮抗抑胃肽(gastric inhibitory peptide,GIP)受体:随着PPDM-A发生机制研究的不断深入,由其发病机制驱动的一些新药物靶点为治疗带来新的希望。PPDM-A的一个特征是GIP水平升高和胃泌酸调节素水平降低[43]。Gasbjerg等[44]研究表明,GIP(3-30)NH2是一种有效和特异的GIP受体拮抗剂,能导致GIP诱导的胰岛素分泌等受到82%的抑制。未来的研究可关注混合餐饮试验后给予GIP(3-30)NH2刺激对餐后胰岛素分泌的影响,GIP对脂肪组织中三酰甘油沉积的重要性,以及GIP对餐后抑制骨吸收的重要性等问题。
5.胃泌酸调节素模拟物(oxyntomodulin mimetics, OXM):OXM是胰高血糖素原肽的衍生物,主要由肠道L细胞分泌, 其主要作用为调节饱腹感、胃排空和控制葡萄糖代谢。一项病例对照研究对葡萄糖依赖的胰岛素肽、胰高血糖素样肽-1、OXM和YY肽进行检测,结果发现与T2DM患者和健康对照者相比,PPDM-A患者中OXM水平显著降低,其显著增加了胰岛素抵抗并减缓了血糖波动[45],目前认为合成具有最佳比例的GLP-1和胰高血糖素受体激活的OXM作为抗糖尿病药物比修饰一种“母体”肽(即GLP-1和胰高血糖素)更有希望[46]。
6.酮症模拟物:PPDM-A患者酮体和空腹血糖之间反向关联,抑制酮体生成是AP发作后葡萄糖代谢紊乱的最早变化之一[47]。研究发现PPDM-A患者摄入含酮单酯β-羟丁酸(ketone monoester β-hydroxybutyrate,KEβHB)的饮料会急剧升高血酮体浓度并降低血糖浓度,外源性补充酮体是有前景的一种降糖治疗[48]。然而值得注意的是,腹部脂肪分布会影响外源性补酮对PPDM-A的治疗效果,特别是胰腺内脂肪沉积高的个体,补酮可能无法获得良好的血糖控制效果[49]。
六、总结与展望
综上所述,PPDM-A临床表现个体差异较大,诊断及治疗均存在一定难度,应引起临床医师的高度重视。随着PPDM-A发病机制的研究,特别是对胰腺外分泌和内分泌如何通过分泌递质IL-6、GIP、OXM等与其他器官相互作用研究的不断深入,基于其发病机制中关键致病靶点的新型治疗方法有望实现,GIP受体、GLP-1受体和胰高血糖素受体活性的操纵以及外源性酮补充诱导等有望成为PPDM-A治疗的重要策略。未来需要制定多学科的循证医学指南,引领PPDM-A进入规范化、系统化、精准化以及个体化的诊疗新时代。
利益冲突所有作者声明无利益冲突
