禽网状内皮组织增生病病毒感染对SPF雏鸡法氏囊细胞Bcl-2和C-myc基因表达及凋亡的影响
2022-06-01顾先哲吕晓萍高雪丽刘超男吴文杰郑世民
顾先哲,侯 宁,吕晓萍,高雪丽,刘超男,吴文杰,郑世民
(东北农业大学动物医学学院,黑龙江省实验动物与比较医学重点实验室,哈尔滨 150030)
禽网状内皮组织增生病病毒(Reticuloendotheliosis virus,REV)是引起禽网状内皮组织增生病(reticuloendotheliosis disease,RE)的病原,该病毒于1958年在美国被首次发现[1]。REV常见的宿主有鸡、鸭、鹅、火鸡等,一些野生鸟类也会成为其宿主,携带病毒在自然界和养殖场之间交叉传播,使得该病预防难上加难[2-4]。REV感染的宿主会产生以淋巴-网状细胞增生为主要特征的一系列病理综合征,常见有生长抑制综合征、急性网状内皮细胞瘤、免疫器官萎缩、淋巴细胞分化成熟受阻等,给家禽养殖业带来了巨大经济损失[5-7]。REV的传播方式多种多样,既能通过粪便、精液在禽类群体之间直接传播,也能通过受污染人员、物品甚至疫苗进行间接传播[8]。毕研丽等[9]证实,REV还可通过反转录将病毒的DNA插入宿主DNA中,进行垂直传播。禽类动物被REV感染之后,其法氏囊、胸腺等免疫器官发生不同程度的萎缩,使淋巴细胞的发育成熟受阻,导致患禽产生免疫抑制。国内外已有大量研究报道指出,这与REV感染后调控了家禽的免疫细胞发生凋亡有关[8,10-12],尽管国内外学者作了大量研究工作,但REV调控细胞凋亡过程的详细机制迄今仍不十分清楚。Bcl-2蛋白家族是细胞凋亡相关蛋白中研究最充分的,目前已鉴定出20多种[13]。多数成员对细胞凋亡起到促进作用,但也有部分成员可抑制细胞凋亡,Bcl-2蛋白就是其中之一。C-myc是原癌基因,隶属于核蛋白类调控基因家族,在细胞增殖、分化、恶性转化及凋亡等过程中起重要调节作用[14]。Hatzl等[15]研究发现,Bcl-2和C-myc之间存在着协同作用,可共同诱导肿瘤产生和免疫抑制。因此,推断REV可能通过调控Bcl-2与C-myc基因,进而影响家禽法氏囊内淋巴细胞凋亡,降低其免疫反应。本研究基于上述科学问题展开试验,以期为进一步探索REV的免疫发生机制和免疫抑制途径完善理论基础。
1 材料与方法
1.1 材料
1.1.1 试验动物 1日龄SPF雏鸡100只,购自中国农业科学院哈尔滨兽医研究所SPF试验动物中心。
1.1.2 病毒 REV-T毒株购自中国兽医微生物菌种保藏管理中心,菌种号为:CVCC No.CACCAV107。经9~11胚龄SPF鸡胚增毒后使用,使用时将之稀释105倍。
1.1.3 主要试剂及仪器 APES购自武汉博士德生物工程有限公司;TUNEL细胞凋亡检测试剂盒购自南京凯基生物有限公司;Oligo(dT)15购自天根生化科技(北京)有限公司;Axy Prep DNA 凝胶回收试剂盒和Axy Prep质粒 DNA小量试剂盒均购自爱思进生物技术(杭州)有限公司;Bcl-2和C-myc抗体均购自Abcam公司;5×First Strand Buffer、0.1 mol/L DTT和M-MLV Reverse Transcriptase均购自Invitrogen公司;DL2000 DNA Marker、RNA 酶抑制剂、dNTP Mixture、10×PCR Buffer、TaqDNA聚合酶和pMD18-T载体均购自宝生物工程(大连)有限公司。LightCycler 2.0荧光定量PCR仪购自罗氏公司;H600L显微病理切片成像系统购自Nikon公司;ELx808酶标仪购自伯腾仪器有限公司。
1.2 方法
1.2.1 REV复苏及病毒50%组织细胞感染量(TCID50)测定 取10胚龄SPF鸡胚,消毒后于超净台内敲开蛋壳气室,取出胚胎,除去头、四肢及内脏,PBS冲洗3次洗去红细胞。剩余组织在无菌平皿中剪碎,PBS冲洗3次后弃去液体。使用5 mL 0.25%的胰酶在锥形瓶中37 ℃水浴消化25 min,加入等量37 ℃预热的含10%胎牛血清的DMEM培养液终止消化,经过8层无菌纱布过滤后分装入玻璃试管中,1 100 r/min离心10 min,弃上清液。以 1 mL含10%胎牛血清的 DMEM培养液重悬细胞,并吹打均匀以计数。 用培养液稀释到1×106/mL,然后分装于细胞培养瓶中,每瓶5 mL细胞悬浮液,37 ℃、5% CO2培养箱中培养24 h,细胞汇合度为80%~90%时用于接毒。
接毒前弃掉细胞培养液,PBS冲洗3次,每个细胞瓶中接种100 μL稀释后的病毒液,37 ℃恒温箱感作1 h。弃掉感作液,换入5 mL 2%胎牛血清的细胞维持液,重新放入37 ℃、5% CO2培养箱中继续培养。维持培养7 d,然后取出,于-80 ℃超低温冰箱内反复冻融3次,收集细胞及上清液。将病毒原液稀释105倍,用于正式试验。
1.2.2 试验动物处理及样品采集 将100只SPF雏鸡随机分为2组,即对照组和感染组。其中感染组雏鸡经腹腔注射途径感染REV稀释液,500 μL/只,对照组雏鸡经相同途径注射等量经高压灭菌的生理盐水。于病毒感染雏鸡后第1、7、14、21、28和42天,从感染组和对照组分别随机抽取5只雏鸡,心脏采血处死后,迅速摘取法氏囊,做如下处理。一部分置于4 ℃预冷的 10%中性福尔马林固定液中固定,用于凋亡细胞数量、细胞核浆比值与Bcl-2、C-myc阳性细胞数量的检测。 另一部分于液氮中迅速冷冻后,转移至-80 ℃冰箱中保存,用于Bcl-2与C-myc基因mRNA 表达检测。剩余部分与裂解液按每100 mg组织与900 μL预冷的裂解液混合,用玻璃匀浆器在低温下充分研磨,将得到的组织匀浆液放入1.5 mL预冷的离心管中,4 ℃、10 000 r/min离心5 min。将上清液放入新的离心管中,置于-80 ℃冰箱中保存,用于Bcl-2与C-myc蛋白含量检测。
1.2.3 测定指标及方法
1.2.3.1 法氏囊凋亡细胞数量 制作组织石蜡切片[16]并按照TUNEL细胞凋亡检测试剂盒说明书进行染色,于油镜下随机选取5个视野,计数凋亡细胞阳性数。
1.2.3.2 法氏囊细胞核浆比 雏鸡心脏釆血处死后,快速釆取法氏囊,经10%中性福尔马林缓冲液固定后的组织块,常规乙醇脱水、二甲苯透明、浸蜡、包埋、切片(3 μm),HE染色,光学显微镜下观察。利用病理切片成像系统软件NIS-Elements BR 3.0计算细胞核与细胞浆的面积比[17]。
1.2.3.3 法氏囊Bcl-2与C-myc阳性细胞数量 应用组织石蜡切片[16]及免疫组织化学染色法(DAB显色),将法氏囊组织石蜡切片常规脱蜡水化,PBS漂洗3次后滴加3% H2O2+甲醇,湿盒内避光反应20 min。于组织切片上滴加1%的胰酶,置于37 ℃恒温箱内消化30 min。将正常山羊血清稀释20倍后滴加于载玻片上,封闭20 min。滴加50倍稀释的兔抗鼠Bcl-2或C-myc多克隆抗体,切片置于湿盒内,于37 ℃恒温箱孵育1 h,PBS洗3次,5 min/次。结束后滴加按1∶2 000稀释的辣根过氧化物酶标记的山羊抗兔IgG,于37 ℃恒温箱中孵育1 h。PBS洗3次,5 min/次,滴加DAB,室温下避光显色5 min,再用苏木素复染5 min。盐酸+乙醇分化、逐级乙醇脱水、二甲苯透明、中性树胶封片后,于油镜下随机取5个视野,统计Bcl-2或C-myc阳性细胞数。
1.2.3.4 法氏囊Bcl-2和C-myc蛋白含量及mRNA表达测定 取法氏囊组织裂解上清,按照ELISA试剂盒说明书检测Bcl-2和C-myc含量,每个样本设3个重复,同时设空白对照组孔。以空白对照组孔调零,用酶标仪测定D490 nm值。应用实时荧光定量PCR法[17]测定法氏囊Bcl-2和C-myc蛋白含量及mRNA表达量。
1.3 数据统计分析
所有试验数据均应用SPSS 16.0软件处理,进行单因素方差分析(One-Way ANOVA)及LSD多重比较,结果以平均值±标准误表示,再应用GraphPad Prism 9.0.2作图。P<0.05为差异显著;P<0.01为差异极显著。
2 结 果
2.1 REV感染SPF雏鸡法氏囊凋亡细胞数量变化
SPF雏鸡感染REV后21和28 d,其法氏囊中凋亡细胞数量均极显著高于相应对照组雏鸡(P<0.01),在病毒感染后42 d,凋亡细胞数量依然显著高于对照组雏鸡(P<0.05)(图1)。

①A,感染后21 d REV感染组凋亡细胞阳性染色(TUNEL染色,40×,箭头所指);B,感染后21 d对照组凋亡细胞阳性染色(TUNEL染色,40×);C,凋亡细胞密度随时间变化柱形图。②与对照组相比,*,差异显著(P<0.05);**,差异极显著(P<0.01)。下同①A,Positive staining of apoptotic cells of REV infection group 21 days after infection (TUNEL staining,40×,Pointed by arrows);B,Positive staining of apoptotic cells of control group 21 days after infection (TUNEL staining,40×);C,Histogram of apoptotic cell density over time.②Compared with control group,*,Significant difference (P<0.05);**,Extremely significant difference (P<0.01).The same as below图1 雏鸡法氏囊细胞凋亡数量变化Fig.1 Changes of the number of cells apoptosis in bursa of Fabricius of chickens
2.2 REV感染SPF雏鸡法氏囊细胞核浆比的变化
由图2可知,REV感染SPF雏鸡后,其法氏囊细胞核浆比与对照组雏鸡相比均不同程度减小,其中21和28 d显著低于对照组雏鸡(P<0.05)。

图2 雏鸡法氏囊细胞核浆比变化Fig.2 Changes of nucleoplasm ratio in bursa of Fabricius of chikens
2.3 REV感染SPF雏鸡法氏囊Bcl-2和C-myc阳性细胞数量变化
2.3.1 REV感染SPF雏鸡法氏囊Bcl-2阳性细胞数量变化 由图3可知,REV感染SPF雏鸡后21和28 d,其法氏囊中Bcl-2阳性细胞数量较对照组雏鸡显著增加(P<0.05)。
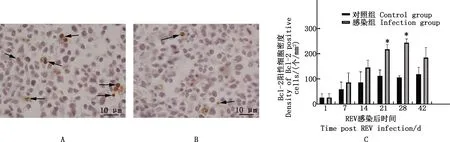
A,感染后21 d REV感染组法氏囊Bcl-2阳性细胞染色(IHC染色,100×,箭头所指);B,感染后21 d对照组法氏囊Bcl-2阳性细胞染色(IHC染色,100×,箭头所指);C,Bcl-2阳性细胞密度随时间变化柱状图A,Positive staining of Bcl-2 positive cells in bursa of REV infection group 21 days after infection(IHC staining,100×,Pointed by arrows);B,Positive staining of Bcl-2 positive cells in bursa of control group 21 days after infection(IHC staining,100×,Pointed by arrows);C,Histogram of Bcl-2 positive cell density over time图3 雏鸡法氏囊中Bcl-2阳性细胞数量变化Fig.3 Changes of the number of Bcl-2 positive cells in bursa of Fabricius of chickens
2.3.2 REV感染SPF雏鸡法氏囊中C-myc阳性细胞数量变化 由图4可知,与对照组雏鸡相比,REV感染SPF雏鸡后,其法氏囊中C-myc阳性细胞数量不同程度的增加,其中,在病毒感染后21和28 d, C-myc阳性细胞数量显著高于对照组雏鸡(P<0.05)。
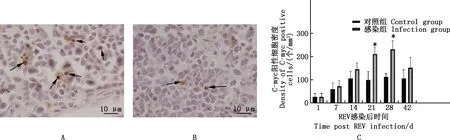
A,感染后21 d REV感染组法氏囊C-myc阳性细胞染色(IHC染色,100×,箭头所指);B,感染后21 d对照组法氏囊C-myc阳性细胞染色(IHC染色,100×,箭头所指);C,C-myc阳性细胞密度随时间变化柱状图A,Positive staining of C-myc positive cells in bursa of REV infection group 21 days after infection (IHC staining,100×,Pointed by arrows);B,Positive staining of C-myc positive cells in bursa of contorl group 21 days after infection (IHC staining,100×,Pointed by arrows);C,Histogram of C-myc positive cell density over time图4 雏鸡法氏囊中C-myc阳性细胞数量变化Fig.4 Changes of the number of C-myc positive cells in bursa of Fabricius of chickens
2.4 REV感染SPF雏鸡法氏囊细胞Bcl-2和C-myc基因mRNA表达变化
由图5可知,REV感染SPF雏鸡后,其法氏囊细胞Bcl-2和C-myc基因mRNA表达量均不同程度高于对照组雏鸡,其中,病毒感染后21和28 dBcl-2基因mRNA表达量极显著高于对照组雏鸡(P<0.01);病毒感染后21 d,C-myc基因mRNA表达量极显著高于对照组雏鸡(P<0.01);28 d时显著高于对照组雏鸡(P<0.05)。
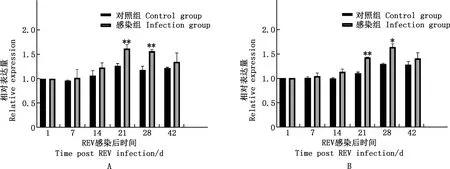
A,Bcl-2;B,C-myc。下同A,Bcl-2;B,C-myc.The same as below图5 雏鸡法氏囊细胞Bcl-2和C-myc基因mRNA表达变化Fig.5 Changes of Bcl-2 and C-myc genes mRNA expression in bursa of Fabricius of chickens
2.5 REV感染SPF雏鸡法氏囊细胞Bcl-2和C-myc蛋白含量变化
REV感染SPF雏鸡后,其法氏囊细胞Bcl-2含量较对照组雏鸡均不同程度增加。其中,病毒感染后21和28 d分别极显著(P<0.01)和显著(P<0.05)增高(图6A)。REV感染SPF雏鸡后,其法氏囊细胞C-myc蛋白含量均不同程度高于对照组雏鸡。在病毒感染后21~42 d极显著(P<0.01)或显著(P<0.05)高于对照组雏鸡(图6B)。
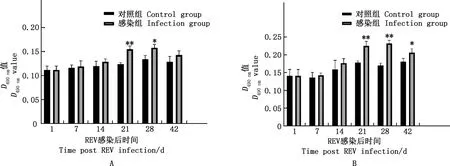
图6 雏鸡法氏囊细胞Bcl-2和C-myc蛋白含量变化Fig.6 Changes of the content of Bcl-2 and C-myc protein in bursa of Fabricius of chickens
3 讨 论
凋亡是细胞最主要的死亡方式之一,其与坏死、自噬、胀亡和焦亡是近年来的研究重点。病毒在感染细胞后会对细胞的凋亡起调控作用,如编码Caspase抑制物,通过抑制Caspase活性阻止宿主细胞凋亡;抑制p53转录为p53肿瘤抑制基因,细胞由于缺乏p53进入无限增殖状态;上调FasL/Fas和TNF-α/TNFR-1的表达,增强死亡受体通路,进而间接诱导细胞凋亡。细胞凋亡后,主要表现为细胞核浓缩、染色质边集,胞浆内Ca2+浓度升高,双链DNA被核酸内切酶切割而断裂,最终形成凋亡小体,导致细胞的核浆比明显减小。因此,检测细胞核浆比变化在一定范围内可较客观地说明细胞死亡方式,且间接反映细胞凋亡程度。本研究发现,SPF雏鸡感染REV后,其法氏囊细胞出现了明显的细胞凋亡现象,法氏囊细胞核浆比与对照组雏鸡相比明显缩小,说明REV感染SPF雏鸡后会导致法氏囊细胞凋亡,该试验结果与相关文献报道一致[18]。与对照组相比,SPF雏鸡感染REV后,雏鸡法氏囊凋亡细胞数在1~28 d逐步增加,细胞核浆比亦不同程度减小。刘畅[17]研究证实,凋亡越明显的细胞,其细胞核浆比减小越显著。发生上述变化可能与免疫器官内的病毒载量先升高后降低有关[19]。上述研究结果表明,REV感染使SPF雏鸡免疫器官细胞发生凋亡,免疫活性细胞数量明显减少,间质结缔组织显著增加,免疫器官萎缩导致雏鸡免疫力下降,无论是先天性免疫还是后天性免疫都被严重抑制,继而使受REV感染的雏鸡对其他病原,尤其是生物性致病因素的易感性增强,易出现混合感染或继发感染。
Bcl-2蛋白主要位于部分亚细胞器(胞核、线粒体和内质网)的生物膜上,通过细胞凋亡的线粒体途径发挥作用[20]。Bcl-2可在3个水平上调控细胞凋亡:①通过调控谷胱甘肽的外泄和降低线粒体巯基的氧化还原状态,以控制线粒体外膜电位从而影响细胞凋亡;②介导线粒体外膜通透转运孔的孔道复合体开放,抑制细胞色素C和凋亡诱导因子(AIF)等促凋亡蛋白的释放阻止凋亡进程;③Bax是Bcl-2活性的主要调控因子,二者间的比率是决定细胞命运的关键因素。Bcl-2可与Bax等结合形成异构二聚体抑制细胞凋亡,Bax表达增加可颉颃Bcl-2的作用,促进细胞凋亡[21]。在某些情况下,该基因表达过量可保护细胞延长寿命,而有些老化细胞未按时凋亡,其基因发生突变导致肿瘤发生。本研究从mRNA表达和蛋白含量两个层面研究了REV感染对法氏囊细胞Bcl-2的影响。结果发现,REV感染SPF雏鸡后21和28 d,其法氏囊细胞Bcl-2 mRNA表达及其蛋白含量均显著高于对照组雏鸡,二者呈现高度一致性,Bcl-2阳性细胞数量也明显增加。分析产生上述现象的主要原因可能与Bcl-2调控因子Bax有关。Bcl-2家族成员之间或与其他凋亡调控分子之间共同构成极其复杂的相互作用网络调控细胞凋亡过程。Brooks等[22]指出,Bax表达增加可对Bcl-2起到颉颃作用,其与Bcl-2结合形成的异构二聚体抑制细胞凋亡。佟美娇[23]研究发现,SPF雏鸡感染传染性法氏囊病病毒(IBDV)后,其法氏囊中Bcl-2、Bax阳性细胞和Bcl-2基因mRNA表达高于对照组雏鸡,且法氏囊细胞凋亡数量亦高于对照组雏鸡。IBDV感染SPF雏鸡后,免疫器官高表达Bcl-2与IBDV所致细胞凋亡密切相关,虽然Bcl-2表达上调,但法氏囊细胞却依然发生了凋亡,且在一定程度上代表了免疫器官病理损伤和免疫抑制的程度,本研究中REV感染SPF雏鸡法氏囊病变程度与其研究结果基本一致,故推测REV感染SPF雏鸡后,虽然Bcl-2表达上升,但法氏囊Bax表达亦上调,Bax上升幅度超过Bcl-2可调控的阈值,导致依然有过多的Bax形成同源二聚体,最终引发了细胞凋亡。雏鸡感染REV后,Bax是否通过表达量超过Bcl-2调控阈值来引起细胞凋亡将是未来研究需解决的问题。
原癌基因C-myc是myc家族中研究最为广泛的一种转录因子,参与调节细胞凋亡、增殖、分化、代谢和血管生成等多种病理和生理过程,具有高度保守性[24]。C-myc基因可诱导肿瘤细胞、成纤维细胞、淋巴细胞及其他细胞发生凋亡。杨莉洁等[25]发现,在B细胞淋巴瘤组织中,细胞凋亡与C-myc表达呈正相关。过表达的C-myc可引起无血清培养的Rat-1纤维细胞和早期鼠胚胎成纤维细胞凋亡[26]。C-myc基因诱导细胞凋亡的确切机制尚未完全阐明,Höfner等[27]指出,C-myc可通过抑制NF-κB活性,使细胞对肿瘤坏死因子(TNF)介导的凋亡更敏感,进而促进细胞凋亡。还可通过生长素响应因子(ARF)间接激活转录因子p53,进而调控凋亡。C-myc与Bcl-2在正常细胞发育、成熟中存在密切联系。在细胞增殖、转化、致癌过程中,Bcl-2与C-myc具有协同作用,而在诱导细胞凋亡过程中,Bcl-2阻碍C-myc诱导细胞凋亡功能的发挥。本研究发现,SPF雏鸡感染REV后,其法氏囊中C-myc mRNA表达在病毒感染后21和28 d显著或极显著高于对照组雏鸡。经ELISA法对其蛋白含量进行了检测,进一步发现,REV感染雏鸡法氏囊中C-myc蛋白含量均高于对照组雏鸡,两者结果虽不完全同步,但在病毒感染后,引起的变化趋势基本呈正相关。从REV致病机制已有的研究资料看,REV在感染禽类后,会将病毒剪切和变异基因插入宿主的C-myc基因中,从而使其致瘤。REV可能通过破坏禽类免疫细胞的DNA,从而引发细胞的凋亡过程。还有研究显示,C-myc可激活Bax,前者与后者形成同源二聚体,通过线粒体途径,促进细胞色素C及其他凋亡相关因子释放到细胞浆中使细胞凋亡,Bax若与Bcl-2结合形成异构二聚体则可阻止这一过程,抑制细胞凋亡,除非二者比例失调[28],王黎霞等[29]指出在Bcl-2与Bax比值较高时,凋亡因子的浓度也更高,引发细胞凋亡。这也进一步解释了为何Bcl-2表达上升却无法抑制细胞凋亡。
4 结 论
REV感染SPF雏鸡导致法氏囊细胞核浆比降低、Bcl-2和C-myc基因mRNA表达量及其蛋白含量升高,细胞凋亡增加是REV感染导致雏鸡免疫机能抑制的病理学基础。
