非基于先验知识的胃癌容积弧形调强治疗自动计划
2022-05-31刘君怡何玲卫治功肖江洪
刘君怡,何玲,卫治功,肖江洪
1.四川大学华西医院肿瘤中心放疗科,四川成都 610041;2.四川大学华西医院肿瘤中心生物治疗科,四川成都 610041
前言
胃癌(包括贲门癌和非贲门癌)仍然是全球范围内高发的一种癌症,是全球第5大最常见的癌症和第3大癌症死亡原因。根据全球癌症统计数据,2018年有超过100 万新发病例和预计78.3 万死亡病例[1]。尽管根治性手术切除是其唯一的治愈手段,然而大量研究表明,术后辅助放疗可降低胃癌局部区域复发率,有利于改善患者生存[2-3]。相较于传统放疗,容积弧形调强治疗(Volumetric Modulated Arc Therapy,VMAT)在满足靶区剂量覆盖的同时能更好地保护周围可能涉及的正常组织,从而在提高肿瘤局部控制率的同时降低正常组织并发症发生率,改善患者的生活质量[4]。
计划设计是VMAT 的核心步骤之一,其质量与患者的治疗效果密切相关。截止目前,人工计划仍然是放疗中占支配地位的计划方式,该过程需要物理师反复试错以获得临床可接受的计划。然而,VMAT 更多的控制点和自由度使其计划设计过程既复杂又耗时,且计划质量往往与物理师的经验和偏好相关[5-7],这导致不同物理师完成的计划质量参差不齐,从而影响肿瘤疗效或增加不良反应。
针对人工计划耗时耗力且质量参差不齐的问题,自动计划是有希望的解决方案之一。放疗自动计划研究主要包括基于先验知识的自动计划[8-9](包括基于机器学习或深度学习预测剂量分布)以及基于自动交互优化程序的自动计划[10-11]。然而,上述方法或多或少需要参考历史计划数据,从而使结果受既往数据的影响。有关深度学习的研究已经证实训练数据的质量对其结果有很大的影响[12]。为此,本研究提出一种非基于先验知识的自动计划方法,其计划参数设置和优化尽可能基于处方和目标函数值而非历史计划,然后通过评估自动计划的质量和效率,探究其在胃癌VMAT中的可行性。
1 资料与方法
1.1 病例资料
本研究回顾性收集了2020年1月至12月于四川大学华西医院放疗科行胃癌术后放疗的患者。患者纳入标准:(1)胃恶性肿瘤切除术后;(2)靶区放疗处方为50.40 Gy/28次;(3)采用VMAT技术。排除标准:(1)多疗程放疗患者;(2)靶区放疗处方为多剂量梯度的患者。最终收集到30例患者,患者基本情况见表1。
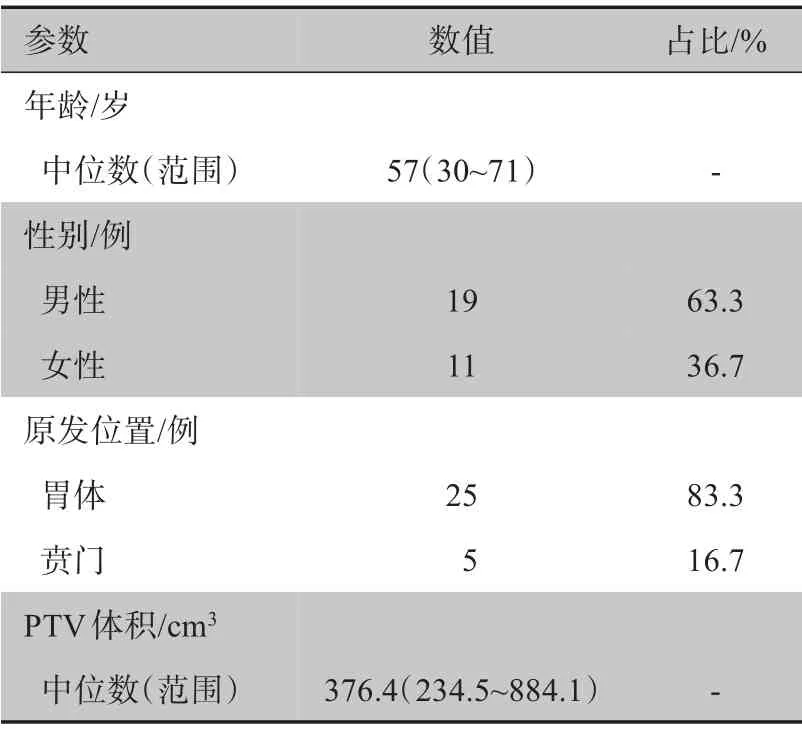
表1 患者基本情况Table 1 Clinical characteristics of the enrolled patients
1.2 模拟定位和体积定义
患者取仰卧位,双手上举,交叉抱头进行体位固定,并于Revolution螺旋CT(GE,Boston,USA)行3 mm增强扫描。图像传输至医生工作站以勾画临床靶区(Clinical Target Volume, CTV)、计划靶区(Planning Target Volume, PTV)及相关危及器官(Organs-at-Risk,OAR)。CTV勾画范围包括瘤床、吻合口及高危淋巴引流区,CTV外扩5 mm形成PTV[13]。OAR 包括脊髓、十二指肠、小肠(十二指肠以外的小肠)、肝脏和双肾等。其中,脊髓三维外扩5 mm 形成脊髓计划危及器官体积(Planning Organs-at-Risk Volume,PRV)。
1.3 处方剂量约束条件
所有患者PTV 照射总剂量50.40 Gy/28 次,每日照射1.80 Gy。计划要求PTV 的D95%(Dx%代表覆盖x%的感兴趣区体积受到的最小吸收剂量)为50.40 Gy,D99%≥47.88 Gy(即95%处方剂量),D1%≤55.44 Gy(即110%处方剂量)。
参考NCCN 胃癌临床诊疗指南[14],计划采用的OAR 约束条件如下:脊髓Dmax≤40 Gy,脊髓PRV 的Dmax≤45 Gy,左、右肾V20Gy≤33%(VxGy代表吸收剂量超过xGy 的感兴趣区百分体积)、Dmean<18 Gy,小肠及十二指肠V45Gy≤195 cc、Dmax≤54 Gy,肝脏V30≤33%、Dmean<25 Gy[15]。
1.4 计划设计
本研究所有计划均在Raystation V4.7.5治疗计划系统(Treatment Planning System, TPS)基于Versa HD 直线加速器(Elekta,Stockholm,Sweden)6 MV 光子束进行计划设计,采用双弧VMAT 技术。首先由一名经验丰富的物理师按照临床常规设计人工计划,针对每名患者靶区及OAR具体解剖位置,确定治疗弧起止角度。然后利用基于Python 语言开发的自动计划程序重新设计胃癌VMAT自动计划。
自动计划的步骤和思路承袭Raystation TPS常规流程和内置的直接机器参数优化(Direct Machine Parameter Optimization,DMPO)算法(图1)。为更好地与临床人工计划对比,人为修改治疗弧起止角度,以便与人工计划保持一致。其余计划初始参数(治疗技术、靶区和OAR 的初始目标、约束等)由程序自动设置。所有目标基于处方剂量约束条件要求设置,如肝脏目标设置Max DVH 和Max EUD(对应V30Gy≤33%和Dmean<25 Gy)。参数设置完成后,程序通过TPS 中预优化得到的目标函数值,判断OAR 和辅助结构的目标及约束合理性。
目标函数值计算思路能简化表述为:
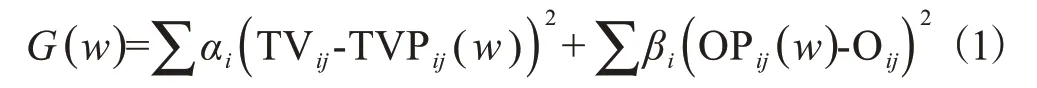
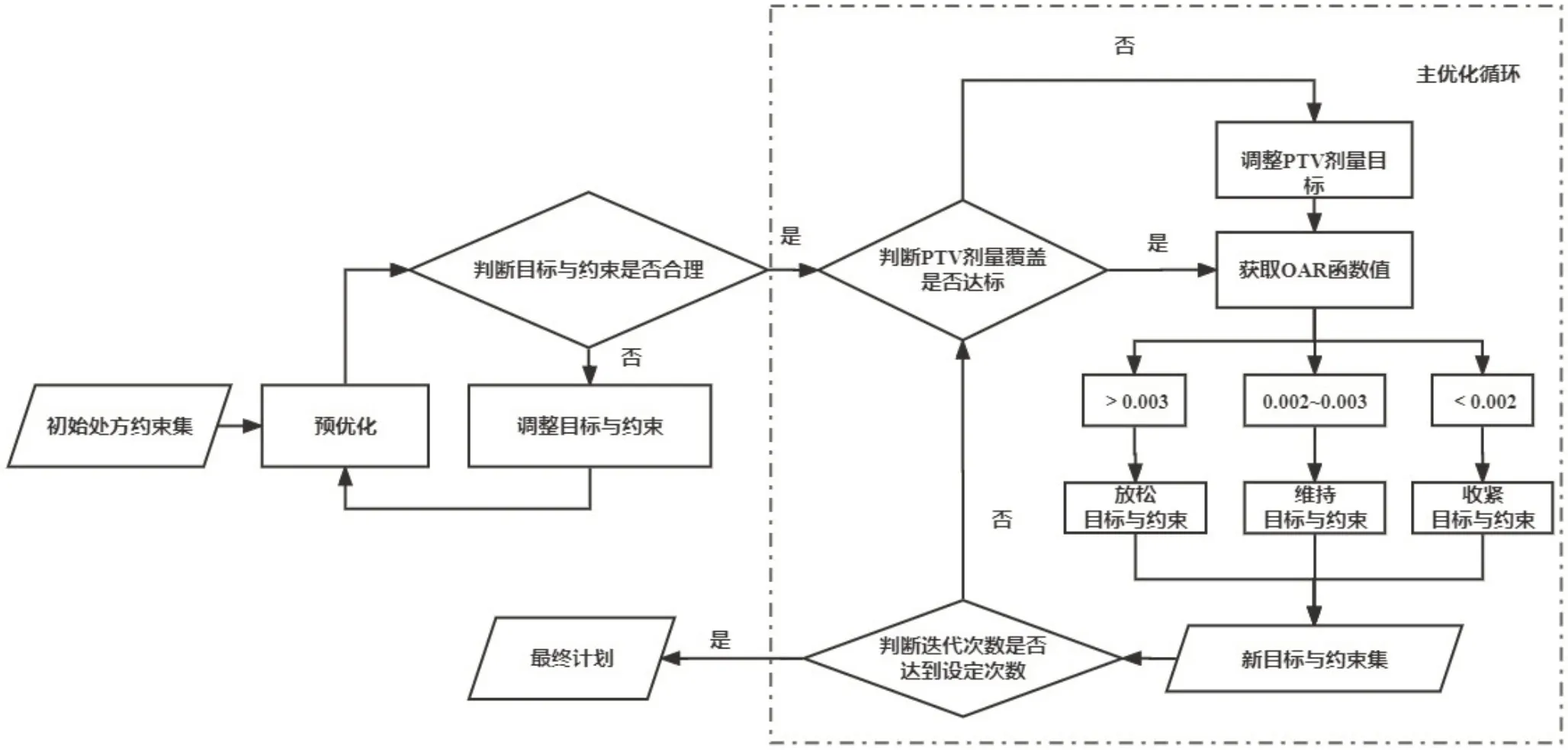
图1 自动计划流程Figure 1 Flowchart of auto-planning
其中,G(w)为计划目标值函数值总和;w为目标的权重因子;αi和βi分别为靶区和OAR 目标的优先级;TVij和Oij分别为靶区和OAR 目标的设定值(如目标剂量或目标体积);j为目标标识符;i为靶区或OAR标识符;TVPij为靶区的实际值;OPij为OAR 的实际值。
目标函数值是反映计划期望剂量目标与实际剂量差异的加权量化值,目标函数值越大,说明差异越大,反之越小。因此本研究将目标函数值作为目标调整的参考并规定在预优化中,函数值>0.000 1为目标或约束不合理,此时,程序自动调整目标与约束后再次进行预优化,直至目标与约束合理,然后进入主优化循环。主优化循环会对靶区覆盖情况进行判断。若靶区欠量则通过增加其Min Dose/Min DVH权重的方式进行调节,反之热点过高则增大Max Dose 权重。在靶区覆盖满足处方剂量要求的情况下,将OAR 和辅助结构的函数值与预设参考值进行比较,并以此作为是否修改目标剂量的评判标准,迭代进行自动优化并根据优化结果调整目标、约束的设定,直到完成指定的循环次数(10 次)后输出并自动保存优化结果。
1.5 评价指标
通过比较靶区与OAR 剂量体积参数、均匀性指数(Homogeneity Index,HI)、适形度指数(Conformity Index,CI)以及机器跳数(Monitor Units,MU)定量比较自动计划与手工计划的优劣。本研究基于ICRU 83报告推荐公式计算HI,基于Paddick 指数[16]计算CI,公式分别如下:


其中,TV 代表靶区绝对体积;TVPIV代表靶区中接受100%处方剂量照射区域的绝对体积;PIV 表示患者外轮廓内100%处方剂量覆盖区域的绝对体积。其中,HI 越接近0,表示靶区剂量均匀性越好;而CI 越接近1,表示靶区剂量分布适形度越好。
1.6 统计学分析
本研究使用IBM 公司SPSS 22.0 软件进行数据处理,数据不完全服从正态分布,描述为中位数(四分位距),对比采用Wilcoxon 符号秩和检验,P<0.05为差异有统计学意义。
2 结果
2.1 计划时间、靶区剂量及MU
自动计划的中位计划时间为30.4 min,相较人工计划(中位计划时间54.3 min),减少23.9 min(P<0.05)。
原发灶位置位于贲门与胃体的计划之间,靶区各指标差值均无统计学意义(P>0.05)。人工计划与自动计划中靶区的剂量学参数对比见表2。尽管自动计划的靶区剂量均匀性略差于人工计划,两种计划的D1%和D99%均满足靶区处方剂量要求。此外,两种计划D95%、CI、MU的差异无统计学意义(P>0.05)。
2.2 OAR保护
自动计划与人工计划中OAR的剂量学参数比较见表3、表4。经统计学分析,原发灶不同病例计划的OAR 指标差值均无统计学差异(P>0.05)。相较于人工计划,自动计划中绝大多数OAR 的剂量得到了改善(图2):其中,脊髓中位D2%与D0.03cc分别下降5.16 Gy和6.10 Gy;小肠的中位D2%、Dmean分别下降0.20 Gy和0.31 Gy,中位V30Gy、V45Gy分别下降4%和1%;右肾中位D2%、Dmean分别降低6.17 Gy 和2.5 Gy,中位V15Gy、V20Gy、V30Gy分别下降9.4%、7.2%和2.0%。左肾中位D2%下降3.21 Gy,中位V30Gy和V45Gy分别下降1.4%和0.4%。然而,十二指肠两组剂量分布无统计学差异(P>0.05);肝脏自动计划中位V45Gy虽然较人工计划下降0.39%,但中位Dmean增加0.93 Gy。

表2 人工计划与自动计划PTV剂量参数对比Table 2 Comparison of PTV dose parameters between manual and automatic plans
3 讨论
胃癌是全球高发的消化道恶性肿瘤[1]。由于剂量学和治疗效率的优势,VMAT逐渐推广到胃癌的综合治疗中以增加患者局部区域控制并改善长期生存[17]。但VMAT 计划设计复杂,需要耗费大量人力、增加计划和患者等待时间,且计划质量受物理师经验和偏好影响[5-7]。为节省人力,提高计划质量、效率和一致性,发展自动计划是当前最有潜力的解决途径。然而,既往的放疗自动计划大多基于历史计划,受已有数据质量的影响。

表3 人工计划与自动计划串行OAR剂量参数比较Table 3 Comparison of serial OAR dose parameters between manual and automatic plans
Raystation TPS 的脚本编辑功能基于IronPython语言,具有强大拓展能力。用户端可通过调用丰富的TPS 内置函数来实现各种操作。本研究基于此平台发展了一种不依赖历史数据的自动计划方法,通过自动设计胃癌VMAT 计划,并与人工计划对比,评估其在胃癌放疗计划中的可行性。研究发现:两种计划中,靶区的D1%、D95%和D99%均满足靶区处方剂量要求;自动计划中脊髓、肾脏及小肠剂量显著降低,但十二指肠与肝脏剂量无显著改善甚至有略微增加;原发灶位置不同对于自动计划结果不产生影响。此外,自动计划中位时间较人工计划缩短23.9 min。
目前主流的几种自动计划包括mdacc AutoPlan系统[18-19]、RapidPlan[20-22]以及基于深度学习的剂量预测方法[23-24]。然而,这些方法或多或少依赖历史计划数据或经验。尤其是基于深度学习的剂量预测方法,对数据库质量和网络训练的要求较高,计划质量受历史计划的影响。临床经验也显示,即便完全按照剂量预测值来设置VMAT 计划的优化目标和约束,仍然得不到与预测一致的计划结果,因此后续的优化调节是必不可少的步骤。相较上述方法,本研究重点在于探索计划调节、优化的过程,对基于预测的计划是一种有力的补充。本研究中靶区与OAR的初始目标参数完全取决于靶区处方和OAR剂量耐受阈值,不受任何历史计划数据的影响;同时,本研究没有试图以完全合理的初始目标开始优化过程,而是通过预优化评估初始目标的合理性并调节后进入主优化循环,整个调节、优化过程完全基于剂量要求和目标函数值自动完成,这样更有利于减小因物理师经验和偏好不同带来的计划质量差异,从而提高计划的一致性。

表4 人工计划与自动计划并行OAR剂量参数比较Table 4 Comparison of parallel OAR dose parameters between manual and automatic plans
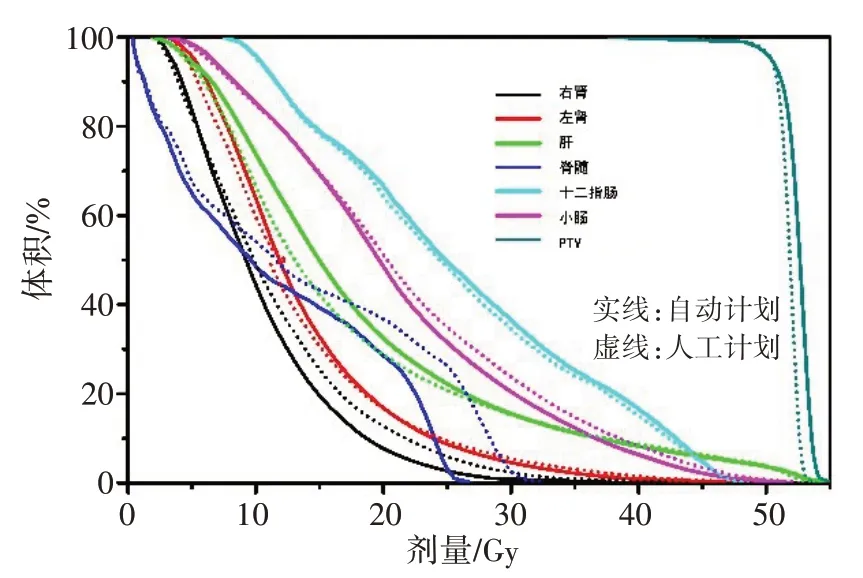
图2 人工计划与自动计划的剂量体积直方图对比Figure 2 Dose-volume histogram comparison between manual and automatic plans
放疗计划中靶区覆盖是肿瘤局控的决定性因素;文献[25-26]证实,靶区Dmin是肿瘤局控的决定性因素。因此在本研究中,D99%作为近最小剂量,在自动计划中被严格要求不小于95%处方剂量;与此同时,D1%均小于110%处方剂量。尽管均匀性稍差于人工计划,但D1%和D99%均满足要求,因此可认为自动计划靶区覆盖满足临床要求,不影响肿瘤的局部控制。
放疗计划的另一个重要方面是OAR保护。相较人工计划,自动计划中脊髓中位D2%与D0.03cc分别下降5.16 Gy 和6.10 Gy。文献[27]提示,超过45 Gy 的放疗剂量使2 级及以上放射性脊髓损伤概率明显增加,本研究中,自动计划将脊髓近最大剂量从30 Gy以上降至约25 Gy,虽然低于45 Gy的剂量耐受阈值,但超过5 Gy 的剂量减少仍会对脊髓的保护带来益处。另外,左肾中位D2%下降3.21 Gy;右肾中位D2%、Dmean分别降低6.17 Gy和2.50 Gy,V15Gy、V20Gy、V30Gy分别平均下降9.4%、7.2%和2.0%。肾脏功能减退发生情况存在剂量-体积依赖性。Klaus等[28]认为,对于分次剂量小于2 Gy 的肾脏局部照射,平均剂量<15 Gy相对安全;Park 等[29]认为V20Gy的下降对于肾脏修复具有重要意义。因此,本研究中肾脏剂量的降低有利于减少其因放疗导致的损伤。此外,多项研究认为十二指肠V30Gy及小肠D2%、V20Gy、V45Gy与其是否出现二级及以上急性肠道损伤密切相关[30-32]。本研究中小肠的D2%、Dmean表现明显的改善,V30Gy、V45Gy也分别下降4%和1%,对于消化道的保护具有积极意义。
尽管自动计划中脊髓、肾脏、小肠等OAR剂量较人工计划显著降低,但十二指肠与肝脏剂量没有显著改善甚至略微增加,原因可能是脊髓、肾脏、小肠距离靶区较远,实际剂量与耐受剂量之间存在一定差距。针对这类OAR,人工计划为了节省时间,在剂量满足耐受剂量要求以后,物理师进一步调节和优化计划有限;而自动计划却会不断地对其进行反复调节和优化,且调整精度可以远高于人工计划(人工计划通常每次调节幅度≥50 cGy,自动计划最小调节幅度为2 cGy),因此更接近调节优化的极限。相较于人工计划,自动计划对于远端OAR的剂量分布改善尤为显著。然而十二指肠、肝脏距离靶区较近,其剂量较高,因此在人工计划中会被物理师充分重视,调节精细度更接近自动计划,使得剂量接近优化极限。物理师为提高计划效率对于远处OAR剂量的放纵也可能成为某些近处较关注的OAR(例如肝脏)剂量略低于自动计划调节结果的原因;但这种剂量降低幅度较小,因为自动计划同样对邻近OAR进行了精细调节,因此人工计划对邻近器官的保护并没有明显优势。远离和邻近OAR的表现不一致进一步说明物理师主观原因会对计划结果产生影响,而自动计划质量更加客观和一致,并有利于降低远离靶区的OAR剂量。
本研究中自动计划的中位运行时间为30.4 min。McIntosh 等[33]基于先验经验的计划设计(包括特征计算、数据库选择及优化)运行时间仅15 min;Wang等[34]基于经验的计划设计完成一个计划却耗时长达3 h;Quan 等[35]应用自动交互优化进行Ⅲ期肺癌VMAT 计划设计,一个周期优化耗时将近30 min,多个周期优化则需要数小时。针对不同研究表现出的较大计划时间差异,推测可能的原因包括计划复杂程度不同以及TPS之间算法和算力的差异。因此,相同情况下的时间比较更有价值。本研究中,自动计划较人工计划中位时间减少23.9 min,自动计划在保证计划质量的基础上,可以显著提高计划效率。
本研究仅为单中心回顾性研究,自动计划未实际执行,因此未能比较自动计划与人工计划的临床疗效和不良反应。未来需要通过多中心前瞻性临床研究进行进一步验证。
综上所述,本研究基于Raystation TPS 平台发展了一种无需依赖先验知识的自动计划方法。该方法能在满足靶区覆盖的同时,减少脊髓、小肠、肾脏等远离靶区的OAR剂量,同时提高计划效率。
