氯气在饱和NaCl溶液中与在水中溶解性差异的实证探究
2022-05-30眭苏奇
眭苏奇


关键词:氯气溶解度;饱和NaCl溶液;手持技术;pH传感器;色度传感器
一、问题的提出
教师在讲授如何在实验室收集氯气时,一般会讲2种收集方式:第一种向上排空气法(氯气密度比空氣大);第二种排饱和食盐水法。根据勒夏特列原理Cl2+H2O?H++Cl-+HClO ,饱和NaCl溶液中c(Cl-)大,会抑制Cl2在水中的溶解,使Cl2难溶于饱和NaCl溶液,所以可以用排饱和食盐水法来收集Cl2。但事实果真如此吗?
笔者首先进行定性实验,分别将Cl2持续通入到饱和NaCl溶液和纯水中,一段时间过后(用pH传感器监测溶液pH变化,pH五分钟内保持不变认为Cl2在水中溶解且与水反应充分),发现两瓶溶液都为黄色,颜色相差无几(见图1,图2),之后用色度计测量(见图3)上述两瓶溶液的透光率(见表1),发现也相差不大,由此带来疑问,饱和NaCl 溶液真的能有效降低氯气在水中的溶解度吗?笔者在中国知网进行相关文献查阅,发现关于这个问题的研究比较少,在2015年《教学仪器与实验》发表的一篇名为“氯气在饱和氯化钠溶液中溶解有多大”的文章中对这个问题有所涉及[1]。此文运用传统实验仪器进行实验,同时结合理论分析,指出氯气在饱和食盐水中溶解度有所减少,但是具体程度如何?文中提到由于实验条件有限,所测量的数据也不是很精确,只能定性进行初步探究,基于此,笔者运用数字化手持技术对这个问题进行了实验探究。
二、实验设计与数据分析
1. 实验原理
根据勒夏特列原理,提高溶液中c(Cl-),平衡左移,抑制Cl2在水中的溶解,通过监测溶液中pH的变化量,探究Cl2在饱和食盐水中的溶解度。
2. 实验仪器及药品
计算机、数据采集器、pH传感器、温度传感器、色度计、磁力搅拌器、锥形瓶、分液漏斗、广口瓶、橡胶塞、导管、铁架台、烧杯等仪器。氯酸钾、浓盐酸、氯化钠、蒸馏水等药品。
3. 实验补充说明
本次制取Cl2采用KClO3+6HCl(浓)== KCl+3H2O+3Cl2↑,此反应常温下能自发进行,且反应速率较快,用分液漏斗将浓盐酸的滴加速率控制为:1滴/s,以确保浓盐酸能充分反应,取10 g KClO3和浓盐酸反应,确保氯气能平稳流畅地持续放出,产生足量Cl2。
4. 实验装置图
实验装置见图4。
5. 实验方案及步骤
实验①:
先将产生的Cl2通入100 mL饱和NaCl溶液中除去挥发出来的HCl后,再通入到40 mL饱和食盐水中,用pH传感器记录溶液pH的变化。
实验步骤:
(1)按图4所示装置组装仪器,用pH=6.86标准缓冲液校准pH传感器。
(2)检查装置的气密性,开始制取Cl2。
(3)同时打开磁力搅拌器,以便Cl2在饱和NaCl溶液中与水充分反应且快速形成Cl2的饱和溶液。
(4)待到pH值稳定(5 min内数值不变)视为达到饱和状态,停止数值采集,清洗pH传感器及其他仪器,剩余药品集中回收处理。
实验②:
先将产生的Cl2通入100 mL饱和NaCl溶液中(目的同实验①),再通入到40 mL蒸馏水中,用pH传感器
记录溶液pH的变化。
实验步骤:同实验①。
实验③:
不用饱和NaCl 溶液去除HCl,直接将制取的Cl2通入到40 mL饱和NaCl溶液中,用pH传感器记录溶液pH的变化。
实验步骤:同实验①。
6. 实验数据分析与结果讨论
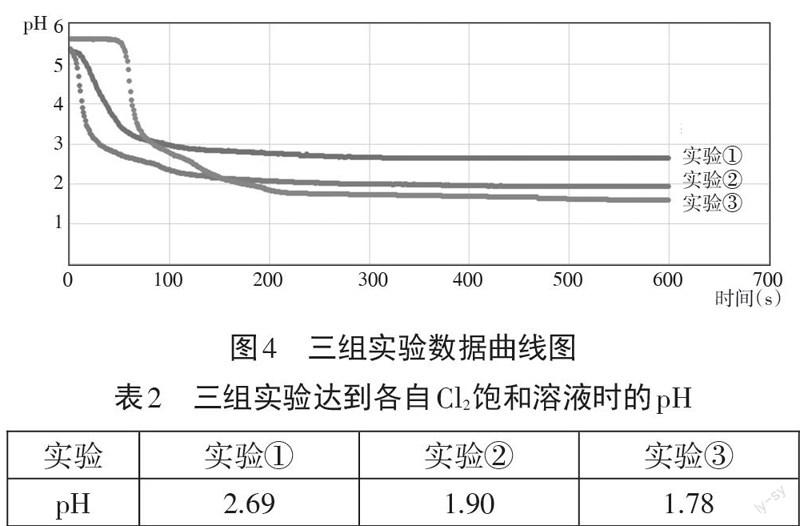
三组实验数据曲线图(见图4)
由表2 分析:实验①c(H+)=2.0×10-3mol/L,实验②c(H+)=1.3×10-2mol/L,即Cl2在实验②中与水反应的物质的量也应该是实验①的6.5倍。查阅相关数据[2]:Cl2+H2O?H++Cl-+HClO 平衡常数为4.2×10-4,逆反应进行程度较大,由此可以得出,在饱和NaCl溶液中由于提高了c(Cl-),平衡左移且进行程度较大,可以看出的确有抑制氯气溶解的作用,也大大减少了Cl2的损耗,可以收集到更多的Cl2。
那如何解释前文所提的疑问及矛盾呢?我们知道Cl2在水中溶解分为物理溶解(只与温度和压强有关)和化学溶解(即与水反应的程度),而实验①与实验②所处的环境基本一致,所以无论肉眼的定性观察还是运用色度计定量测量,其结果不会存在多大差异,只有通过分析Cl2化学溶解才能得出科学的结论和解释。
通过此次探究实验,我们可以看出仅靠定性观察是远远不够的,有时还会产生误导。另外即便是采用定量测量,如果没有测量合理的物理量(变量),也会产生误导。而此次的探究实验,既可以让学生在学的过程中深刻理解Cl2在水中溶解的本质和机理,也可以让教师教得更清晰准确,Cl2 难溶于饱和NaCl 溶液,不是指Cl2 在水中的物理溶解,而是Cl2 在饱和NaCl溶液中更难与水发生化学反应(即化学溶解),从而减少了Cl2损耗。
实验③的数据也能从侧面进行验证,由于实验③没有除去HCl,HCl进入到溶液后电离产生H+,进一步使平衡左移,Cl2 更难与水发生化学反应,但由于挥发出来的HCl 量毕竟少,其抑制效果肯定没有饱和NaCl溶液那么明显,这可以通过实验②和实验③pH 数值比较分析看出,两者相差很小,因此要获得纯净量多的Cl2还是要通过排饱和NaCl 溶液来获得。
同时,通过对比实验①与实验②pH数据,还可以引导学生深刻认识Cl2+H2O?H++Cl-+HClO 为可逆反应,这是高中学生第一次接触可逆反应,让学生理解可逆反应的意义,进而能够理解化学平衡移动原理就显得尤为重要[3]。在常规教学中教师主要是从宏观现象与理论的角度进行讲授,较少从微观和动态变化上让学生学习可逆反应,学生多为机械记忆,没有进行太多的思维活动[4],难以真正理解并记住这一知识点。笔者运用手持技术测量溶液pH的变化,随着溶液c(Cl-)升高,pH也跟着上升,证明平衡向左移动,既然有平衡移动,此反应就一定为可逆反应。实验过程中学生可以把数值与微观粒子(H+)联系在一起,数值变化又是动态变化过程,这样就把可逆反应中微观的、动态的本质展现得淋漓尽致,也把抽象的难以理解和记忆的知识点“数据化、动态化、直观化”,让学生“摸得着、看得见、想得起”,从而达到加深理解和记忆的效果。
由此,教师在课堂讲“因为Cl2难溶于饱和NaCl溶液,所以可以用排饱和NaCl溶液收集Cl2”,这一结论是没有问题的,但在进行解释的时候,应该突出Cl2的化学溶解,再通过平衡理论来分析Cl2在饱和NaCl溶液中与水反应的程度大小。
三、数字化手持技术解决问题的启示
本研究对教材中难以用传统实验仪器表征的知识内容加以补充,突出了实验的基础作用[5],通过手持技术设计实验,测量溶液的pH、透光率进行定量分析。借助数据曲线图,将“数据”指代“微观”来表征“宏观”,使“静态”转化为“动态”,客观真实地展现实验过程,揭开化学微观世界隐藏的规律。这样能够有效降低知识的难度,扫除学生的“盲点”和“误区”。
手持技术的运用使学生探究问题的范围和深度都大大拓展[6],这对提高学生探究能力大有裨益。同时学生在实验过程中,观察现象,采集数据,基于数据和现象建立坐标图,分析解决问题,参与概念的形成。培养了学生收集证据,分析处理数据的能力,促进自身“证据推理与模型认识”“科学探究与创新意识[7]”等化学学科核心素养的发展。
