烟草硝酸盐转运蛋白NtNRT1.7 基因的克隆、亚细胞定位及表达模式分析
2022-05-30尹卓然轩栋栋连文力贾宏昉
尹卓然,王 驰,轩栋栋,罗 勇,连文力,贾宏昉*
1. 河南农业大学烟草学院,郑州市文化路95 号 450002
2. 厦门大学生命科学学院,福建省厦门市翔安区翔安南路4221-120 号 361000
烟草是我国重要的经济作物,在生产过程中常施用硝态氮肥以提升烟叶的产量和品质。硝态氮(NO3-)不仅是一种营养物质还可以作为信号分子调节叶片生长[1]。Tahir 等[2]研究表明植物吸收与利用硝态氮(NO3-)主要是通过硝酸盐转运蛋白(Nitrate transporter,NRT)完成的。当外部硝酸盐浓度小于1 mmol/L 时,主要是NRT2 家族编码的高亲和硝酸盐转运蛋白系统(High-affinity nitrate transporter system,HATS)负责吸收和转运硝酸盐;当外部硝酸盐 浓 度 大 于1 mmol/L 时,NRT1/PTR(Nitrate transporter 1/Peptide transporters,NPF)家族编码的低亲和硝酸盐转运蛋白系统(Low-affinity nitrate transporter system,LATS)负责对外部硝酸盐进行吸收与转运[3-6]。由于适合烟草幼苗根系生长和叶片生物量积累的氮浓度为4 ~6 mmol/L[7],故在适宜植物根系与叶片生长条件下硝酸盐的吸收、转运和再利用主要由NRT1/PTR家族负责,该家族在植物正常的生长发育过程中发挥关键作用[8-9]。
目前植物中关于NRT1 基因家族成员的研究主要集中在拟南芥和水稻中。已发现拟南芥中有53个NRT1/PTR家族成员基因[10],12个基因的功能已经明确[11],其中:AtNRT1.4 参与叶柄中硝酸盐的积累[12];AtNRT1.5 主要参与硝酸根向木质部的装载[13];AtNRT1.6 主要影响拟南芥胚的早期发育[14];AtNRT1.7主要参与介导拟南芥韧皮部硝酸盐再利用的过程[15-16]。水稻中至少有80 个NRT1/PRT 家族成员[17-18],7个基因的功能已经明确[11],其中:OsNPF7.2[19]是水稻中第一个鉴定出的参与液泡NO3-运输的NPF基因,对根细胞内硝酸根的平衡有重要意义;OsNPF2.2[20]参与了根中NO3-向地上部分的运输。而烟草NRT1/PTR 家族成员至少有9 个成员,目前仅Liu 等[21]初步研究了烟草NRT1 家族的2 个基因,其中NtNRT1.1在根系中特异性表达,而NtNRT1.2主要在衰老叶片中强烈表达,其余烟草NRT1家族基因的功能研究还鲜见报道。因此,克隆烟草硝酸盐蛋白家族成员NtNRT1.7,鉴定其同源关系,测定不同氮浓度处理和不同非生物胁迫下基因的表达模式,旨在探究NRT1.7基因在胁迫条件下对氮素的调控机制,为培养氮素高效利用新品种提供理论基础。
1 材料与方法
1.1 供试材料
普通烟草品种K326在培养箱中培养,培养箱周期设置为16 h/8 h(光/暗),光强设置为300 μmol·m-2·s-1,温度设置为28 ℃/22 ℃(光/暗),相对湿度设置为60%。对其进行不同氮素条件、盐处理、干旱处理和低温处理。正常处理所采用的营养液试剂及其浓度为:5 mmol/L NaNO3;1 mmol/L NaH2PO4·2H2O;1 mmol/L K2SO4;0.75 mmol/L CaCl2·2H2O;0.5 mmol/L MgSO4·7H2O;9 µmol/L MnCl2·4H2O;0.03 µmol/L(NH4)2MoO4;46 µmol/L H3BO3;8 µmol/L ZnSO4·7H2O;3 µmol/L CuSO4·5H2O;20 µmol/L FeSO4·7H2O和Na2-EDTA螯合物,pH调至7.0。采用霍格兰营养液水培法,在种子露白后使用1/4正常营养液培养3 d,之后更换为1/2 正常营养液培养3 d,最后更换为正常营养液培养4 d,培养结束后开始处理。氮素处理:设置正常处理(CK:5 mmol/L NO3-)和低氮处理(LN:0.25 mmol/L NO3-)2 个处理,处理时间分别为7 d;盐胁迫处理:150 mmol/L NaCl 处理7 d;干旱处理:10%的PEG-6000处理7 d;低温处理:4 ℃处理3 h。结束后取各处理长势一致的3株幼苗用去离子水洗涤,提取样品的根、茎、幼叶和老叶(幼叶为完全展开的叶片从上往下数第2片,老叶为完全展开的叶片从上往下数第7片),获得检测基因表达模式分析的供试材料。
1.2 目的基因的克隆
参考烟草、拟南芥和水稻等物种在GenBank 收录的NRT1 基因序列,应用Sol Genomics Network 和NCBI网站Blast程序搜索烟草EST序列数据库。使用Primer Premier 6软件设计烟草引物(表1),以烟草cDNA 为模板进行PCR 扩增,扩增条件为:94 ℃5 min;94 ℃30 s,58 ℃30 s,72 ℃2 min,35 个循环;72 ℃5 min。将扩增目的片段连接在中间载体pMD19-T 上,后送Invitrogen 生物公司测序验证,获得全长cDNA序列信息。

表1 RT-PCR和定量PCR扩增引物序列Tab.1 RT-PCR and quantitative PCR amplification primer sequences
1.3 序列分析方法
利 用NCBI 软 件 的ORF finder(https://www.ncbi.nlm.nih.gov/orffinder/)进行基因序列的蛋白翻译。利用Expasy(https://web.expasy.org/protparam/)和PRABI(https://npsa-prabi.ibcp.fr/cgi-bin/npsa_auto mat.pl?page=/NPSA/npsa_sopm.html)分析NtNRT1.7的蛋白结构,利用NetPhos 3.1(https://services.health tech.dtu.dk/service.php?NetPhos-3.1)预测NRT1.7 的磷酸化位点。利用TMHMM 2.0(https://services.hea lthtech.dtu.dk/service.php?TMHMM-2.0)预测NRT1.7蛋白的跨膜结构域。利用DNAMAN 进行蛋白质多序列比对分析;利用MEGA 6.0 制作邻接树(Neighbor-Joining Tree),分析NtNRT1.7 与NRT1 家族成员的亲缘关系;在线网站MEME(https://meme-suite.org/meme/tools/meme)分析序列基序(Motif),利用TBtools[22]将系统进化树和Motif组合,对NRT1.7 与烟草、拟南芥和水稻中的NRT1 家族进行对比分析。
1.4 启动子分析
以烟草NtNRT1.7 基因全长序列为探针,利用Sol Genomics Network 网站进行Blast 搜索基因全长,在起始密码子ATG 上游取一段长1 500 bp 的启动子序列,利用PlantCARE(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/)在线工具分析启动子序列的顺式元件。
1.5 亚细胞定位分析
设计带有酶切位点的特异引物,将扩增得到的PCR 产物连到经内切酶酶切的pBWA(V)HS-GLosgfp 载体上,连接产物转化到大肠杆菌DH5a 中,对阳性克隆进行测序验证,获得融合载体pBWA(V)HS-NtNRT1.7-GLosgfp。采用注射烟草表皮细胞的方法,将表达载体导入烟草表皮细胞,并置于22 ℃培养箱中培养30~60 h 后,利用激光共聚焦显微镜观察荧光蛋白在烟草表皮细胞中的位置,未插入NtNRT1.7基因的pBWA(V)HS-GLosgfp空载体作对照。
1.6 基因表达分析
按 照Invitrogen 公 司 的RealMasterMix(SYBR Green)试剂盒说明书进行实时定量RT-PCR检测,实时定量的实验数据以烟草组成型表达基因NtL25(GenBank:L18908.1)为内参基因,进行3 次重复试验,采用2-ΔΔCT)算法进行分析。假设目的基因在胁迫处理下的表达量是对照(正常培养)的N 倍,N =2-ΔΔCT,ΔΔCT=Treat(CT样品-CTL25)-CK(CT样品-CTL25)[23]。
1.7 数据分析
使用DPS 7.5 软件进行单因素完全随机试验统计分析,运用LSD 法进行多重比较,分析1%水平下的显著性,运用Origin 2018 制作基因相对表达量柱形图。
2 结果与分析
2.1 基因的克隆与序列分析
以K326 的cDNA 作为模板,进行PCR 扩增,琼脂凝胶电泳结果(图1)显示克隆基因全长在1 500 bp和2 000 bp之间。进一步对克隆基因NtNRT1.7的全长进行序列分析,该序列全长为1 839 bp,可编码612个氨基酸。

图1 NtNRT1.7全长基因PCR扩增电泳图谱Fig.1 Electrophoretogram of PCR amplification of full-length NtNRT1.7
2.2 生物学分析
2.2.1 NtNRT1.7蛋白结构
分析NtNRT1.7 蛋白结构可知,其分子式为C3133H4877N793O859S30,分子量为68 358.78,理论等电点(pI)为8.91,含有45 个酸性氨基酸和53 个碱性氨基酸,不稳定性指数(Ⅱ)为40.08,属于不稳定蛋白。该蛋白的二级结构主要包含了46.08%的α螺旋,12.42%的β折叠结构和37.91%的不规则卷曲结构。
由磷酸化位点分析结果可知,NtNRT1.7 中含有37个丝氨酸、16个苏氨酸和7个酪氨酸,推测在这些位点可能发生磷酸化。
2.2.2 NtNRT1.7的跨膜结构域分析
图2(0~1 之间)表示氨基酸位于螺旋、内部或外部的总概率,顶部(1~1.2 之间)表示NtNRT1.7 跨膜结构的最佳预测,也是总体最可能的结构。预测结果显示NtNRT1.7含有12个疏水的跨膜螺旋区,其中在第6 个和第7 个跨膜区之间有一个中央亲水环将其分隔为2组。
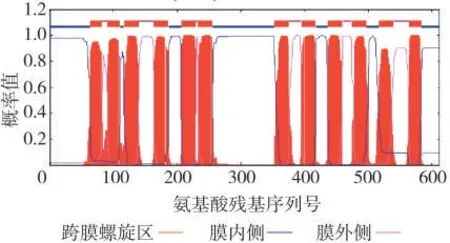
图2 NtNRT1.7蛋白跨膜结构域分析Fig.2 Transmembrane domain analysis of NtNRT1.7 protein
2.2.3 NtNRT1.7同源性与系统发育树分析
NtNRT1.7 与拟南芥、水稻中NRT1 家族成员的同源性分析结果如图3 所示。 NtNRT1.7 与NtNRT1.1 和NtNRT1.2 同源性分别为30.95%和31.43%;与AtNRT1.7 的同源性达到57.23%;与水稻OsNRT1.7 的同源性达35.51%。NtNRT1.7 与拟南芥AtNRT1.7、AtNRT1.6 的亲缘关系较近(图4),同时NtNRT1.7与拟南芥AtNRT1.7含有相似的Motif。
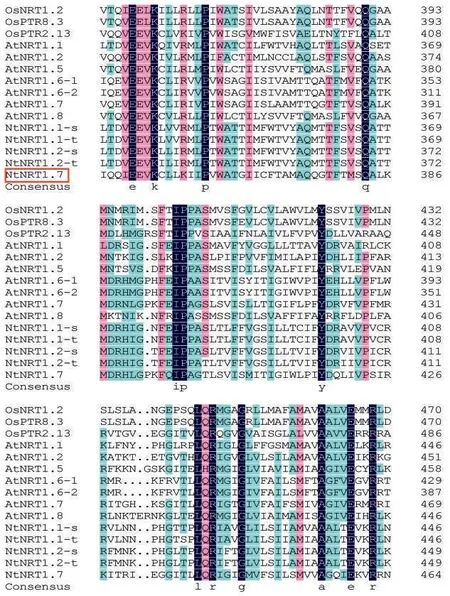
图3 氨基酸序列同源性分析Fig.3 Homology analysis of amino acid sequences

图4 NtNRT1.7系统发育树Fig.4 Phylogenetic tree of NtNRT1.7
2.3 启动子分析
如图5 所示,NtNRT1.7 除含有启动子所必需的TATA-box和CAAT-box外,还含有3个脱落酸反应性涉及的顺式元件(ABRE),1 个生长素反应元件(TGA-element)和3 个MBS。其中,ABRE 与转录因子结合,促进或抑制脱落酸诱导基因的表达,从而表现出加速或减缓植株衰老过程;TGA-element与生长素响应因子结合后可以促进或抑制基因的转录,从而影响植株的生长;MYB 与CAACTG 基序(MBS)结合激活了基因的表达,参与苯丙烷类代谢途径,进而增强抗植株抗逆性。
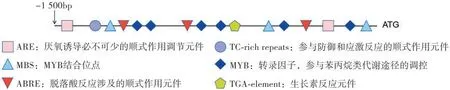
图5 NtNRT1.7启动子克隆及启动子顺式元件分析Fig.5 NtNRT1.7 promoter cloning and analysis of its cis-elements
2.4 亚细胞定位
激光共聚焦显微镜下观察到在细胞膜上存在GFP 信号(图6),说明转pBWA(V)HS-NtNRT1.7-GLosgfp 融合蛋白存在于细胞膜上,NtNRT1.7 为膜蛋白,可作为载体转运物质进出细胞。

图6 NtNRAT1.7亚细胞定位Fig.6 Subcellular localization of NtNRT1.7
2.5 表达特性
2.5.1 氮素处理下不同部位NtNRT1.7 基因的表达特性

图7 可见,在正常处理下(CK:5 mmol/L NO3-),NtNRT1.7 主要在叶片中高表达,老叶相对表达量是根部相对表达量的105倍,叶片与根部的相对表达量间存在极显著差异。在低氮处理下(LN:0.25 mmol/L NO),NtNRT1.7 在幼叶和根中的相对表达量有所增加,老叶中的相对表达量是正常处理下的20%,NtNRT1.7的相对表达量总体不及正常处理。整体来看,NtNRT1.7主要在叶片,尤其是衰老的叶片中高表达,低硝态氮处理时会抑制表达。
2.5.2 不同非生物胁迫下NtNRT1.7基因的表达特性图8 可见,在不同生物胁迫下NtNRT1.7 基因的相对表达量均显著增加。与正常处理相比,盐胁迫、干旱胁迫与低温胁迫条件下NtNRT1.7 相对表达量分别增加1.16 倍、1.29 倍和2.76 倍,存在极显著差异。以上结果表明,NtNRT1.7 在烟草非生物胁迫应答方面发挥着重要的作用。

图8 不同非生物胁迫下NtNRT1.7基因的相对表达量Fig.8 Relative expression of NtNRT1.7 gene under different abiotic stresses
3 讨论
在烟草K326 中克隆出了NtNRT1.7 基因,对NtNRT1.7 进行了生物学分析。结果显示NtNRT1.7包含12个跨膜结构,且在第6和第7个跨膜结构间有1个中央亲水环,这与Tsay等[24]高等植物NRT1/PTR(NPF)在第6和第7个跨膜结构间有1个中央亲水环的研究结果一致。NtNRT1.7与AtNRT1.7高度同源,亲缘关系较近,此外还发现NtNRT1.7蛋白定位在细胞质膜上,Fan 等[16]的研究中也证实AtNRT1.7 蛋白定位于细胞质膜上,参与硝酸盐的再利用,初步猜测NtNRT1.7是具有吸收和转运硝酸盐功能的膜蛋白。
进一步分析烟草NtNRT1.7 的表达特征发现该基因主要在衰老的叶片中表达,其表达量为幼叶的8倍,根部的105 倍;在低氮条件下,NtNRT1.7 在幼叶中表达增强,在老叶和茎中表达减弱,这是因为烟株吸收硝酸盐后优先供给幼叶生长,之后转运至中下部叶,最后到达根部[25]。在老叶中高表达暗示了NtNRT1.7 可能参与硝酸盐的转运和再利用;老叶和茎中表达量降低暗示了低氮条件抑制了NtNRT1.7对硝酸盐的转运。下一步可通过转基因技术获得NtNRT1.7过量表达的转基因株系,研究NtNRT1.7在提高烟草氮素利用效率方面的功能。
NtNRT1.7 的启动子中除含有TATA-box 和CAAT-box等组织特异性元件外,还含有参与防御和应激反应的特异转录因子[26-27]结合的顺式元件。其中MYB 通过调控相关基因的表达来促进特定代谢产物花青素[28]的生成与积累,进而增强抗干旱能力,暗示该基因可能参与各种非生物胁迫的调控。因此,通过qRT-PCR 进一步研究NtNRT1.7 在不同非生物胁迫处理条件下的表达情况,发现NtNRT1.7 基因受干旱、高盐和冷害的胁迫诱导并增强表达,这和启动子序列分析的结果(含有3 个ABRE 基序,3 个MBS基序)一致,表明该基因可能参与了多种非生物胁迫下氮素的吸收与再利用。
4 结论
在烟草中克隆了低亲和硝酸盐转运蛋白基因NtNRT1.7,研究了NtNRT1.7 的蛋白结构、跨膜结构域、同源性和亚细胞定位,发现该蛋白是膜蛋白,可能参与硝酸盐的转运。启动子顺式元件分析与基因的表达模式分析结果显示,正常处理下NtNRT1.7 在老叶中高表达,低氮处理后NtNRT1.7 在老叶的表达量降低,非生物胁迫下表达量增强,说明该基因在受低硝态氮处理时抑制表达,可能参与调控烟叶非生物胁迫下硝酸盐的转运和再利用。
