二维FeCo-MOF催化剂氧析出性能的综合实验教学设计
2022-05-28张树鹏林佳阳杨奇宋海欧
*张树鹏 林佳阳 杨奇 宋海欧
(1.南京理工大学 化学与化工学院,国家级化学化工实验中心 江苏 210094 2.南京师范大学 环境学院 江苏 210023)
近年来,为解决迫在眉睫的环境及能源匮乏问题,开发清洁环保、可持续能源已成当务之急。鉴于高能量密度、无污染性、可持续性等优势,氢能成为新时代理想的绿色能源。电化学分解水作为最有利的制氢方式之一,其包含两个半电极反应,即阴极析氢反应(HER)和阳极析氧反应(OER)。然而,由于氧气与催化剂表面原子的相互作用强于氢气,OER需要一个极高能垒来克服四个质子耦合电子转移步骤的动力学抑制。为加速反应动力学、降低能耗,迫切需要高本征活性和多位点的OER电催化剂。
目前,IrO2、RuO2等贵金属催化剂被认为活性最高。然其高昂成本、有限的耐久性、稀缺的自然资源以及较差的抗中毒能力抑制了大规模市场应用。相较之下,金属有机框架(MOF)拥有巨大的比表面积、高孔隙率以及丰富的活性位点,能最大限度地提高电催化活性。尤其是铁系MOF(Fe、Co、Ni)在地球上分布广泛,且价格低廉,与有机配体的配位数丰富,极大促进了其发展。但由于固有的低导电性和稳定性,铁系MOF表现出的OER性能仍不尽如人意。因此,提高铁系MOF的OER活性是近年来的研究热点。
本实验通过调控MOF电子结构,在一致的测试环境中对比单金属Fe-MOF、Co-MOF和不同维度的双金属FeCo-MOF OER性能。证明了双金属协同效应可提高OER性能,彰显了二维MOF在OER催化领域的优势。本实验不仅涉及到材料合成相关知识,而且涉及材料表征及电化学催化领域的知识,将无机化学、有机化学、电化学及能源化学首次引入到本科生的化学综合实验,可极大地激发学生科研热情。
1.实验目的
(1)了解燃料电池及相关电极材料的应用前景及国内外研究现状,掌握OER反应机制及材料表征方法。(2)了解MOF类材料的结构特征,掌握制备原理、方法及相关实验操作技能。(3)掌握材料表征手段的原理,学会数据处理和图谱分析。(4)培养学生综合运用化学知识的能力,激发系统解决实际问题的能力,提升实验操作能力[2]。
2.实验原理
OER是由氢氧根在碱性电解质或水分子在酸性电解质中的氧化反应产生的[3]。具体的催化过程包括了反应物在活性中心的吸附,反应物通过一些中间体向产物转换,产物从活性中心解吸。据文献报道,在酸性和碱性介质中,其涉及的基本途径因机制不同而有所差异,但两种反应环境均与中间体(*OH,*O,*OOH)的吸附和解吸相关。碱性介质中OER的反应机理[4]如下:

*代表电催化剂的活性位点,可以吸附和解吸反应物、中间体以及产物。一般说来,含氧物质的吸附能极大地决定了反应活性:若电催化剂活性位点的吸附太弱,反应物难以被吸附,直接影响了后续反应的进行;若吸附太强,会阻碍产物的解吸,导致表面有效活性位点的占据。影响OER效率的因素主要包括催化剂的形貌、状态以及基底的选择。为达到理想性能,倾向于构建纳米级、层状、高度开放的结构以暴露更多活性位点。
金属有机框架(MOF)是由金属节点(金属离子和金属簇)与有机配体通过配位键连接而成的多孔材料,通过调节金属节点与有机配体的配位方式可形成不同维度的纳米材料。其中,二维MOF因其表面众多不饱和金属离子配位位点、快速的质量传输和电荷转移,具有高效的电催化活性。界面合成法、表面活性剂辅助合成法、模板辅助合成法和超声剥离法等是典型的二维MOF合成方法,但这些方法均存在一些缺点,如:产率低、表面活性剂与MOF纳米片表面结合阻塞活性位点、所需能量高,限制了二维MOF的大规模应用。因此,我们采用室温搅拌这一温和的合成方法。
3.实验部分
(1)实验试剂
六水合氯化铁(FeCl3·6 H2O)、六水合硝酸钴(Co(NO)2·6H2O)、三乙胺(TEA)和乙醇(AR,国药集团化学试剂有限公司);N,N-二甲基甲酰胺(DMF)、二氧化铱(IrO2)和苯甲酸(BA)(AR,Aladdin);氢氧化钾(KOH)(AR.Macklin)。
(2)实验仪器
CHI600E型电化学工作站(上海辰华仪器有限公司)、TECNAI G2 20 LaB6型透射电子显微镜(TEM)(美国FEI公司)、Bruker D8 Advance型X射线衍射分析仪(XRD)(德国Bruker公司)PHI Quantera II型X射线光电子能谱(XPS)(日本Ulvac-Phi公司)。
(3)实验步骤
Fe-MOF的制备:将270mg六水合氯化铁完全溶解于50mL N,N-二甲基甲酰胺(DMF)中,并加入120mg对苯二甲酸(PTA)。直至PTA全部溶解于DMF后,依次加入适量乙醇(2mL)、水(2mL),并快速加入三乙胺(1mL),室温下反应(800rpm,12h)。将反应所得沉淀用乙醇离心(5000rpm,5min)洗涤3次,并在60℃真空烘箱中干燥。所得橙色产物即为Fe-MOF。Co-MOF的制备:制备方法与Fe-MOF类似,仅将金属离子替换为270mg六水合硝酸钴。所得粉色产物即为Co-MOF。FeCo-MOF的制备:制备方法与Fe-MOF类似,仅将金属离子替换为180mg六水合硝酸钴和90mg六水合氯化铁。所得褐色产物即为FeCo-MOF。
4.结果与讨论
(1)结构分析与表征
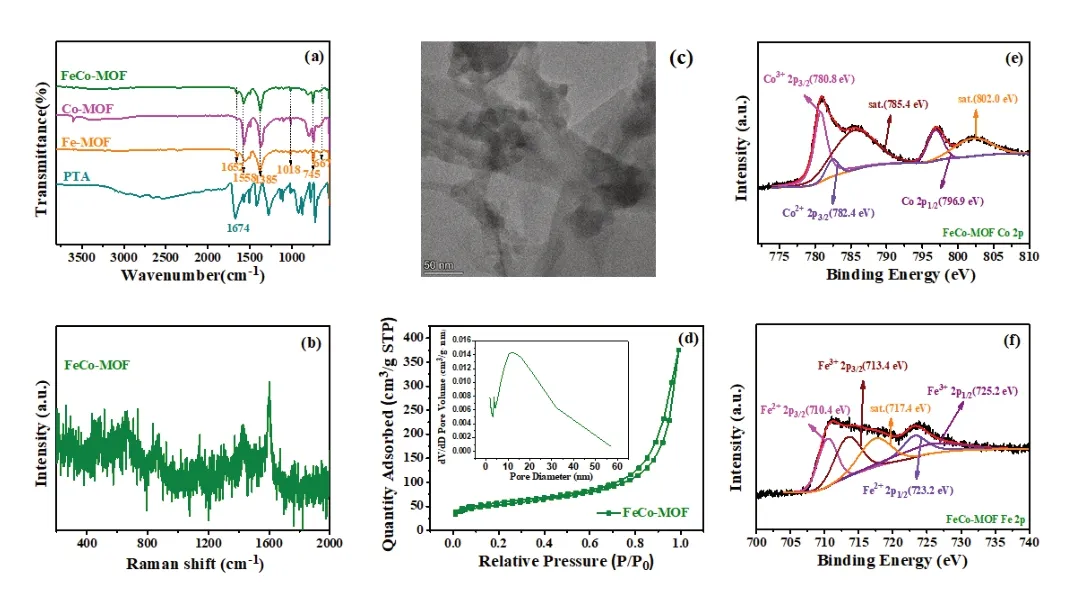
图1 (a)PTA、Fe-MOF、Co-MOF、FeCo-MOF的FT-IR谱图;(b)FeCo-MOF的Raman谱图;(c)FeCo-MOF的TEM图像;(d)FeCo-MOF的N2吸附-脱附等温线(插图为孔径分布曲线);(e)FeCo-MOF中XPS Co 2p高分辨率谱图;(f)Fe 2p高分辨率谱图
由于MOF的低晶态,利用FT-IR技术研究催化剂的分子内化学键。图1a中,与有机配体PTA的-COOH基团吸收峰(1674cm-1)相比,MOF中该特征峰明显削弱且红移至1652cm-1,明显的去质子化作用表明金属离子与PTA的羧酸基团之间存在配位作用。在一系列MOF基催化剂中,1558cm-1和1385cm-1附近均存在强特征峰,分别归属于υas(COO-)和υs(COO-)。而1018cm-1、745cm-1、667cm-1附近的吸收峰依次为O-H面内变形振动、苯环C-H弯曲振动、M-O伸缩振动,进一步证实了金属离子与质子化PTA的成功配位。FeCo-MOF表现出强拉曼散射信号,这可能是因为PTA具有良好的对称性。对于FeCo-MOF,1602cm-1、1425cm-1、1300cm-1、1140cm-1、863cm-1、660cm-1、467cm-1的特征峰分别归属于有机配体中苯环的伸缩振动、υ(COO-)振动、υ(C-O)振动、芳香环的δ(C-H)、芳香环的γ(C-H)、υ(Co-O)振动、υ(Fe-O)振动(图1b)。
FeCo-MOF的TEM图像证明其呈现为极薄的纳米片,边缘发生自然卷曲,表现出其柔性。纳米片形态及边缘的褶皱有利于暴露更多的活性位点,增加与电解质接触的机会(图1c)。为确定催化剂的比表面积和孔径分布能否显著影响催化性能,可以通过N2吸附-脱附等温线测定。观察图1d可知,所有催化剂均呈现Ⅳ型等温线,且存在H4滞后环,证实了催化剂具有介孔特性。FeCo-MOF的比表面积为181.48m2/g,这既有利于反应中间体的扩散和电解质的浸润,又可以暴露更多的活性位点,改善了催化剂总体活性。FeCo-MOF的Co 2p拟合得5个分峰(图1e),依次为:Co3+的2p3/2峰(780.8eV)、Co2+的2p3/2峰(782.4eV)、Co 2p3/2的卫星峰(785.4eV)、Co 2p1/2峰(796.9eV)、Co 2p1/2的卫星峰(802.0eV)。与之对应的是,FeCo-MOF的Fe 2p峰拟合为:Fe2+的2p3/2峰(710.4eV),Fe3+的2p3/2峰(713.4eV),Fe2+的卫星峰(717.4eV),Fe2+的2p1/2峰(723.2eV),Fe3+的2p1/2峰(725.2eV)(图1f)。Co3+/Co2+和Fe3+/Fe2+的比例分别为5.225和1.017。XPS结果表明Co2+/3+和Fe2+/3+不同金属物种的共存,具有充足的不饱和位点,使其具有更高的氧化还原能力。
(2)电催化性能分析
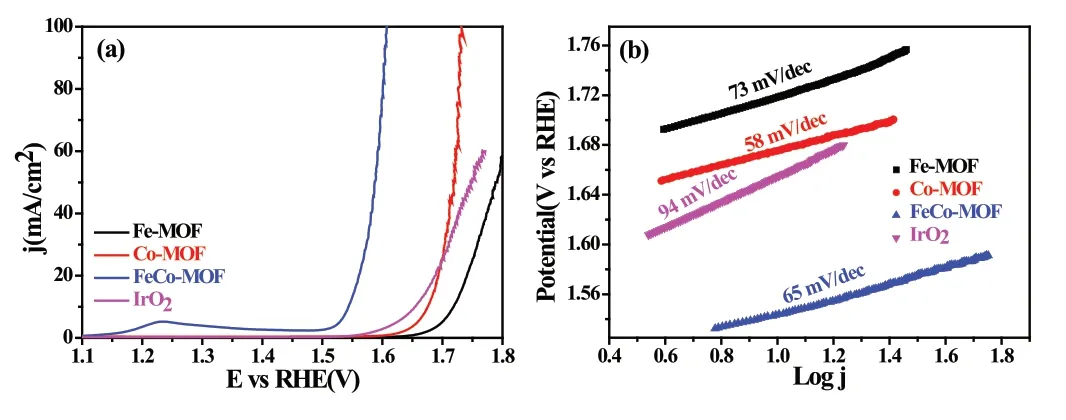
图2 在1 M KOH(饱和O2)、扫速10mV/s、转速1600rpm下Fe-MOF、Co-MOF、FeCo-MOF、IrO2的(a)LSV曲线;(b)Tafel曲线
过电位是评价电催化剂在相同测试条件下OER性能的重要参数之一。有文献指出为电流密度等于10mA/cm2时的过电位,因在一次太阳光照下,10%太阳能-燃料转换效率的太阳能水分解电池的电流密度约为10mA/cm2,而被认为是评估催化剂性能的基准。一般值越小电催化活性越佳。电催化动力学的另一实质性指标为Tafel斜率(b)。在相同电流密度下,值越小,越小,说明电催化动力学越高。此外,Tafel斜率还是判断决速步的重要依据。
在相同测试条件下比较不同过渡金属催化剂Fe-MOF、Co-MOF、FeCo-MOF和贵金属氧化物催化剂IrO2的OER活性。图2a中单金属Fe-MOF、Co-MOF均表现出滞后的起始电位,说明其催化活性较差。而双金属FeCo-MOF则具有较低的,达到10mA/cm2电流密度时所需的过电位为347mV,比Fe-MOF、Co-MOF分别降低了141mV、98mV,也优于商用贵金属催化剂IrO2(425mV)。与单金属Fe-MOF、Co-MOF相比,双金属FeCo-MOF在1.2~1.3V之间出现了明显的阳极峰,这归属于Co离子的自氧化,表明Fe、Co间存在很强的电子耦合作用,改变了催化剂的电子结构。一般来说,Tafel斜率是在电流完全由非质量传递限制决定的电压区域获得的。图2b中双金属FeCo-MOF的斜率为65mV/dec,远低于IrO2(94mV/dec),说明FeCo-MOF具有较快的催化动力学。这可能是由于双金属协同效应,弱化了金属位点和配位水的化学键,显露丰富的不饱和配位中心,提高电化学活化速率;双金属掺杂改变了MOF骨架的主客体相互作用,孔隙度增加,使OH-更易插入,促进金属氧化物中间体的形成。
5.思考题
要求每位同学完成实验后,提交实验报告,并在报告的讨论部分回答以下问题:(1)适合做OER的电极材料还有哪些,优缺点是什么?(2)提升FeCo-MOF电极材料OER性能的控制策略还有哪些?(3)为什么双金属MOF的OER性能会优于单金属MOF?
6.实验组织
教师严格规范同学们实验操作。本实验的开展分为FeCo-MOF的合成、结构表征和OER性能研究3个部分。(1)FeCo-MOF反应期间,学生可以准备OER性能测试需要的玻碳电极抛光、电解液配置等工作,并提交预习报告;(2)材料结构表征及OER性能研究,教师应将碳中和及碳达峰思想与国家能源战略结合起来,培养同学们正确价值观;(3)观察实验现象,详细做好记录,仔细分析遇到的问题和实验结果,并能准确详实记录,如实撰写实验报告。
7.结语
本综合实验采用简单的室温搅拌法制备了FeCo-MOF为代表的OER催化剂,并对其结构和OER性能进行了表征。本综合实验具有操作方法简单、产率高及重复性强的优势。材料制备过程中既包含溶解、搅拌、洗涤及干燥等常规操作,也包含多个重要表征方法的内容,最后阐明了OER的电催化性能。本综合实验的开展不仅提高同学们的实践能力,更能激发学习兴趣,提升工作效率,加强团队合作能力。
