非共价键法构筑C60-Py-GO 用于光热和光动力疗法
2022-05-28张美多李德华刘鸣禹
张美多,李德华,刘鸣禹
吉林警察学院刑事科学技术系,吉林 长春130117
0 引 言
癌症已逐渐成为危害人类生命健康的重要问题之一。纳米技术及生物医学的进步,使得纳米功能材料在癌症治疗中受到越来越多的关注。光热疗法(photothermal therapy,PTT)和 光 动力疗法(photodynamic therapy,PDT)具有微创、低毒,收效快、选择性高,重复应用不会产生耐药性、不破坏正常组织,并可与其他治疗方法联合应用等优点,已成为癌症治疗研究领域的热点之一[1]。光热疗法主要利用光热剂将光能转化为热能,然后依靠热量消融肿瘤而不损害正常组织。光热剂主要包括无机纳米材料类和有机纳米材料类[2~5]。与光热疗法不同,光动力疗法主要使用具有光活化作用的光敏剂,将吸收的能量转移到邻近分子氧上产生活性氧物质(ROS),尤其是具有细胞毒性的单线态氧(1O2)。在光激发下,1O2可对患病细胞和肿瘤组织造成不可逆破坏[6,7]。与单一光疗技术相比,将两种光疗技术相结合可体现出协同作用,并提高治疗准确性和治疗效率[8~10]。
近年来,具有近红外光吸收性质和良好机械性能的氧化石墨烯(GO)引起了人们极大的研究兴趣[11,12]。GO 具有单原子厚度和较大的π 共轭体系,可以用作分子组装或π 电子体系多功能纳米平台,应用于体外和体内光热治疗。然而,GO 可能会抑制1O2的产生,进而阻碍GO 在光动力治疗中的应用[13]。因此,构建一种基于GO 而不影响1O2生成的纳米体系对于肿瘤治疗有重要的研究意义。
富勒烯(C60)是碳的同素异形体,因具有低毒性、高比表面积、易表面功能化和较高的1O2产率而被广泛应用于光动力疗法[14]。Hu 等[15]利用聚多巴胺(PDA)包裹GO 形成PDA-rGO,再借助Schiff 碱反应/ Michael 加成反应,以共价键方式引入叶酸-C60衍生物构筑C60-PDA-rGO 纳米杂化物,该体系表现出光动力和光热协同治疗癌细胞的作用。然而,该纳米杂化物中的C60和GO 均存在水溶性较差等缺点。为了解决水溶性问题,Li 等[16]经过多步反应在GO 表面接枝聚乙二醇(PEG),再接枝乙二胺,暴露出氨基,然后将C60衍生物与裸露氨基结合构成水溶性的GO-C60纳米杂化体系,该体系展现出一定的光热和光动力治疗效果。但上述水溶性GO-C60纳米杂化体系的制备过程较繁复,且共价键修饰的GO 会破坏石墨烯原始的共轭结构,并对其性质产生不利影响。非共价键结合法可有效避免上述问题[17]。芘(pyrene,Py)的多环芳香化合物结构是一种常用的非共价键连接基团,可与GO 发生π-π 非共价键相互作用,实现GO 表面功能化。此外,非共价键结合法还可以有效维持GO 表面碳原子sp2杂化固有的电子结构[18,19]。
本 研 究借助C60-Py 与PEG-GO 之 间的π-π 相互作用,以非共价键构筑水溶性C60-Py-GO 纳米体系,并探讨了该体系对癌细胞的光热和光动力联合治疗效果。图1 为C60-Py-GO 的合成和光热效应、光动力效应示意图。

图1 C60-Py-GO 的合成和光热效应、光动力效应示意图Fig.1 The synthesis, PTT and PDT of C60-Py-GO
1 实验部分
1.1 试剂与仪器
试剂:C60(分析纯,苏州大德碳材料有限公司);碘(分析纯)、H2SO4(分析纯)、高锰酸钾、H2O2溶液(北京化工厂);人宫颈癌HeLa 细胞株(上海中科院细胞库);聚乙二醇2000(PEG-2000)、1-芘丁酸、丙二酰二氯、吡啶、LiAlH4(安耐吉化学);磷酸盐缓冲溶液(PBS,pH 7. 4,赛默飞世尔生物化学制品(北京)有限公司);其他化学试剂均为化学纯或分析纯试剂,无需纯化直接使用;合成过程使用的溶剂通过蒸馏纯化;实验用水为去离子水。
仪器:PL-X500D 氙灯(配置300~700 nm 滤光片,北京普林塞斯科技有限公司);MW-GX-808/1-5000 mW 激光器(长春镭仕光电科技有限公司);Win-IR 型傅里叶红外光谱仪(FT-IR,BIO-Rad 公司);NanoBrook 90Plus 动 态 光 散 射 仪(DLS,Brookhaven 公司);Perkin-Elmer-TGA 热分析系统(TGA,Perkin-Elmer 公司);Avance 400 MHz 型磁共振仪(1H NMR、13C NMR,Bruker 公司);AutoflexⅢTOF/TOF 型质谱仪(HR-MS,Bruker 公司);UV-3600 型分光光度计(UV-Vis,Shimadzu 公司);SPI 3800N 型探针台(AFM,Seiko 公 司);JEM-1011 型透射电子显微镜(TEM,JEOL 公司)。
1.2 实验方法
1.2.1 C60-Py 的制备
化合物C60-Py 的合成路线如图2 所示。

图2 C60-Py 的合成路线Fig.2 Synthesis route of C60-Py
化合物1的合成:氮气保护下,将LiAlH4的无水四氢呋喃(THF,2.50 g,65 mmol)溶液滴加到冰浴冷却的1-芘丁酸(2.00 g,6.9 mmol)的无水THF(100 mL)溶液中,滴毕,回流反应过夜。用水淬灭反应,用二氯甲烷萃取,取有机相经Na2SO4干燥,过滤,滤液减压浓缩,残余物经硅胶色谱柱(石油醚/乙酸乙酯体积比:10/1)纯化得淡绿色固体(化合物1),产率95.2%;磁共振氢谱(1H NMR,CDCl3,400 MHz)化学位移值δ:8.27(d,J=10.8 Hz,1H),8.17(d,J=2.4 Hz,1H),8.15(d,J=2.4 Hz,1H),8.11~8.09(m,2H),8.02~7.96(m,3H),7.87(d,J=9.6 Hz,1H),3.73~3.68(m,2H),3.40~3.35(m,2H),1.99~1.90(m,2H),1.79~1.71(m,2H),1.34(s,1H);磁共振碳谱(13C NMR,CDCl3,100 MHz)δ: 136.58,131.35,130.83,129.71,128.52,127.44,127.13,126.50,125.72,125.00,124.95,124.77,124.70,124.61,123.30,62.42,33.11,32.45,27.84。
化 合 物2的 合 成:将 化 合 物1(1.00 g,3.6 mmol)、丙 二 酰 二 氯(0.291 g,2.0 mmol)和 吡 啶(0.537 g,6.8 mmol)溶于20 mL CH2Cl2中,氮气保护下回流反应过夜。冷却至室温,用水淬灭反应,将反应液倒入0.5 mol/L 盐酸中,用二氯甲烷萃取,取有机相依次用饱和Na2CO3溶液和去离子水洗涤,用Na2SO4干燥后经硅胶柱色谱(二氯甲烷/乙酸乙酯体积比:49/1)分离得到白色化合物2,产率36.4%;1H NMR (CDCl3,400 MHz)δ:8.16 (d,J=9.2 Hz,2H),8.14~8.11(m,4H),8.07(d,J=2.0 Hz,2H),8.02(s,2H),7.98~7.93(m,6H),7.75(d,J=7.6 Hz,2H),4.14(t,J=12.8 Hz,4H),3.36 (s,2H),3.26 (t,J=15.2 Hz,4H),1.84 (m,4H),1.74(m,4H);13C NMR (CDCl3,100 MHz)δ:166.62,135.92,131.45,130.56,129.59,128.43,127.45,127.26,127.12,126.30,125.79,124.87,124.75,124.43,123.02,65.10,41.79,32.56,28.31,27.90。
化 合 物C60-Py 的 制 备:将C60(0.108 g,0.15 mmol)、化合物2(0.103 g,0.17 mmol)、I2(0.093 0 g,0.37 mmol)和1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU,0.154 g,1.01 mmol)溶于30 mL 无水甲苯中,氮气保护下于室温搅拌反应12 h,反应液冷却至0 ℃,倒入去离子水中,用二氯甲烷萃取,取有机相经硅胶柱层析(甲苯/石油醚体积比:10/1)纯化得C60-Py,产率56.3%;1H NMR (CDCl3,400 MHz)δ: 8.16(d,J=9.6 Hz,2H),8.09(d,J=7.6 Hz,4H),8.03(d,J=8.4 Hz,4H),7.96(s,4H),7.93~7.91(m,2H),7.74(d,J=8 Hz,2H),4.43(m,4H),3.28(m,4H),1.85(m,8H);13C NMR (CDCl3,100 MHz)δ:163.89,144.99,144.68,144.49,144.27,143.56,143.05,142.66,141.83,141.53,140.58,138.74,137.82,136.02,131.46,130.84,129.96,128.56,127.40,127.12,126.82,126.20,127.91,124.81,66.70, 32.51, 29.77, 28.41; HR-MS(EI)m/z:C103H34O4理论值1 334.346 9,实验值1 334.230 4;元素分析C103H34O4: 理论值C 92.6、H 2.55,实验室C 83.23、H 2.46。
1.2.2 PEG-GO 的合成
根据文献方法合成PEG-GO[20]。冰浴条件下,将3.00 g 石墨薄片和400 mL 浓H2SO4在1 L 圆底烧瓶中搅拌10 min,缓慢加入3.00 g KMnO4(约30 min),混合液立即变为深绿色。每间隔24 h 向混合液中加入3.00 g KMnO4,共加3 次,待反应结束后,取120 mL(约180 g)反应液倒入300 mL 冰水中,缓慢加入2 mL H2O2,溶液由深紫色变为黄色,以4 400 r/min 离心10 min,用去离子水清洗,再用异丙醇纯化直至溶液pH 值为中性。使用MwCO 透析管(3 500)在异丙醇中透析3 d,以10 000 r/min 离心30 min,收集固体成分,减压蒸发去除异丙醇得GO(1.12 g)。将100 mL GO(3.33 mg/mL 的水溶液)超声处理10 min,加入2.00 g PEG 2000,于120 ℃加热搅拌24 h,制得PEG-GO。
1.2.3 C60-Py-GO 的制备
将50 mL PEG-GO(2.67 mg/mL 的水溶液)与10 mL C60-Py(2.00 mg/mL 的甲苯溶液)混合,超声40 min 至混合均匀,再于60 ℃剧烈搅拌除去甲苯得到C60-Py-GO 水溶液。在进行细胞实验前,将C60-Py-GO 放入透析袋中透析,每6 h 换水一次,透析2 d。
1.2.4 光热处理
在96 孔板内,将Hela 细胞以每孔1.00×104个的密度种在200 μL 的DEME 培养基中,在37 ℃,5% CO2条件下培养24 h。吸出培养基并用PBS(0.01 mol/L,pH 7.4)将细胞清洗3 次,再加入180 μL 新 鲜培养 基 和20 μL 不 同 浓 度的C60-Py-GO 溶液,确保不同孔内C60-Py-GO 的浓度呈梯度分布。分别用808 nm 激光(1~3 W)、可见光(300~700 nm可见光)以及双光源照射细胞5 min,用噻唑蓝(MTT)法测定细胞存活率,考察C60-Py-GO 的光热/光动力治疗效果。
2 结果与讨论
2.1 C60-Py-GO 的表征
图3 为各样品的透射电镜(TEM)图和原子力显微镜(AFM)图。通过TEM 图片可以看出,C60-Py-GO(图3(a))中在薄片板上分布有较均匀的纳米簇点,和文献[16]中C60-GO 的TEM 图的特征形态一致;GO(图3(b))和PEG-GO(图3(c))呈现有褶皱的薄片状且没有团簇点,而C60-Py 图3(d)呈现较明显的团聚形貌。通过AFM 图片可以看出,C60-Py-GO(图3(e))和PEG-GO(图3(g))的边界较模糊,而GO(图3(f))边界较为清晰,与文献[21]中PEG-GO的AFM 图形貌相近,因此推测这种现象是PEG 对GO 表面包裹造成的。

图3 (a)C60-Py-GO、(b)GO、(c)PEG-GO 和(d)C60-Py 的TEM 图;(e)C60-Py-GO、(f)GO 和(g)PEG-GO 的AFM 图Fig.3 The TEM images of (a)C60-Py-GO, (b)GO, (c)PEG-GO and (d)C60-Py;the AFM images of(e)C60-Py-GO, (f)GO and (g)PEG-GO
图4(a)为各样品水溶液的动态光散射图。对比3 个体系粒径分布曲线的峰值,GO 峰值粒径为345 nm,PEG-GO 峰值粒径为225 nm,C60-Py-GO峰值粒径为170 nm。PEG-GO 体系的粒径明显小于GO 的 原 因 主 要 是,GO 经PEG 修 饰 后,PEG 对GO 片层间的范德华力和氢键的弱化作用有利于GO 片层的剥离与延展以及阻止GO 的聚集,从而增 强 了 其 分 散 性[22,23]。而 与PEG-GO 相 比,C60-Py-GO 粒径更小,可能与此体系在合成过程中经过了更长时间的超声振荡,增强了其在水中的分散性有关。此外,通过图4(b) C60-Py-GO 水溶液放置7 d 前后的照片可以看出,该体系在放置7 d 后分散性良好,未出现明显的团聚现象,表现出较好的稳定性。

图4 (a)GO、PEG-GO 和C60-Py-GO 的动态光散射图;(b)C60-Py-GO 体系的分散状态照片Fig.4 (a)The dynamic laser scaterring of GO, PEG-GO and C60-Py-GO;(b)photographs for the dispersion status of C60-Py-GO
图5(a)为GO, PEG-GO,C60-Py 和C60-Py-GO的红外光谱图(FT-IR)。GO 的谱图中,O—H、C=O 和C=C 的特征吸收峰分别位于3 400、1 733、1 620 cm-1处。与GO 相比,PEG-GO 在2 900 cm-1处出现了一个新的吸收峰,归属为PEG 中—CH2—的振动峰,该峰的出现表明PEG-GO 合成成功[24]。C60-Py-GO 谱图中除具有PEG-GO 的特征峰外,在527 cm-1和1 424 cm-1两处还出现了C60的典型特征峰[15]。综合上述分析可知,C60-Py 和PEG-GO 形成了C60-Py-GO 结构体。图5(b)为GO 和C60-Py-GO 的紫外-可见(UV-Vis)吸收光谱。C60-Py-GO谱图在220 nm 处的吸收峰为GO 的特征吸收峰,在图5(b)的插图中可以观察到在270 nm 和350 nm 处的两个弱吸收峰,来源于水溶性较差的C60-Py[25,26]。上述实验结果也证实了C60-Py-GO 制备成功。

图5 (a)GO, PEG-GO,C60-Py 和C60-Py-GO 的FT-IR 谱 图;(b)GO 和C60-Py-GO 的UV-Vis 吸 收 光 谱Fig.5 (a)FT-IR spectra of GO, PEG-GO, C60-Py and C60-Py-GO;(b)the UV-Vis absorption spectra of GO and C60-Py-GO
图6 为各样品的热重分析曲线(TGA)。其中GO 在低于100 ℃的热失重归因于水分的蒸发,160 ℃处显著的热失重归因于GO 表面含氧官能团的热分解[27]。PEG-GO 中200 ℃附近的热失重归因为GO,250~420 ℃阶段的热失重为PEG[28]。因C60在700 ℃下几乎不分解[29],故C60-Py 在200~400 ℃间的热失重归因于Py 基团[30]。C60-Py-GO 的TGA曲线与PEG-GO 相似,可以证实此体系中GO 和PEG 的存在,但在200~400 ℃间C60-Py-GO 的失重率比PEG-GO 多出2.91%,是由体系中少量Py 基团的失重所导致,因此说明此体系中含有Py 基团。以上结果进一步证实C60-Py-GO 制备成功。

图6 GO,C60-Py, PEG-GO, C60-Py-GO 的TGA 曲 线Fig.6 The TGA of GO, C60-Py, PEG-GO,and C60-Py-GO
2.2 C60-Py-GO 的光热/光动力效应
2.2.1 光热效应
图7(a)(b)为C60-Py-GO 浓度和激光功率对C60-Py-GO 溶液光热效应的影响。通过图7(a)可以看出,使用功率为2 W 的808 nm 激光照射纯水10 min后,水的温度从27 ℃升高至31 ℃,未发生显著性变化;而使用功率为2 W 的808 nm 激光照射C60-Py-GO 溶液10 min 后,C60-Py-GO 溶液升温效果明显,且随着C60-Py-GO 浓度的增加升温效果更加显著,尤其是3.00 mg/mL 体系的温度从27 ℃升高至51 ℃。通过图7(b)可以看出,C60-Py-GO 溶液的升温效果随着激光功率的增加更加显著,当激光功率为3 W 时,C60-Py-GO 溶液(3.00 mg/mL)的温度甚至可升高至59 ℃。上述实验现象表明,单位体积的C60-Py-GO 溶液可以吸收更多光能并将其转化为更多的热能,显著升高体系的温度。这一性能使其有望作为光热剂用于癌症的治疗。

图7 溶液浓度(a)和激光强度(b)对C60-Py-GO 光热效应的影响Fig.7 Effects of concentration (a)and laser intensity (b)on the photothermal effect of C60-Py-GO
通过(1)式和(2)式计算C60-Py-GO 纳米体系的光热转换效率[31]。

其中,η(%)代表光热转换效率,h(W/(m2·℃))为热传导系数,S(m2)为样品池表面积,ΔTmax,mix(℃)为溶液体系平衡温度与环境温度的差值(24 ℃),ΔTmax,H2O(℃)为纯水的平衡温度与环境温度的差值(4 ℃),I(W)为激光功率(2 W),A808nm为C60-Py-GO在808 nm 处的吸光度(0.32),mi(g)为样品质量(1 g),Cp,i(J/g)为水的比热容(4.2 J/g),τs(s)为采样系统时间常数。
图8(a)为C60-Py-GO 在(808 nm,2 W)激光照射及停止照射的光热响应曲线,将图8(a)中的降温时间与驱动力温度负对数(-lnθ)作图得到图8(b),通过图8(b)可得τs=212 s。将τs代入(2)式计算hS=0.019 8 W/oC,再将hS代入(1)式计算出C60-Py-GO 光热转换效率η为37.9%。

图8 (a)C60-Py-GO 在激光(808 nm, 2 W)照射及停止照射的光热响应曲线;(b)降温时间与驱动力温度负对数曲线Fig.8 (a)The photothermal response of C60-Py-GO with a laser (808 nm, 2 W)and then the laser shut off;(b)plot of cooling period versus negative natural logarithm of driving force temperature
2.2.2 光动力效应
可见光照射C60后产生的1O2可以有效降低4-亚硝基-N,N′-二甲基苯胺(RNO)在440 nm 处产生的吸光度[13],因此选用RNO 作为生成1O2的指示剂,以RNO 在440 nm 处的吸光度指示1O2的浓度。图9为GO、PEG-GO、C60-Py-GO 随着光照时间变化产生1O2的情况。可以看出,C60-Py-GO 经过可见光照射30 min,在440 nm 处的吸光度为0.718,呈现出明显的下降趋势,而GO 和PEG-GO 在相同条件下吸光度未发生明显变化,表明C60-Py-GO 经过可见光照射后生成了1O2。此前曾有GO 抑制1O2生成的报道[32,33],但本文结果表明,采用非共价键结合方式构建的C60-Py-GO 纳米体系能够有效生成1O2。
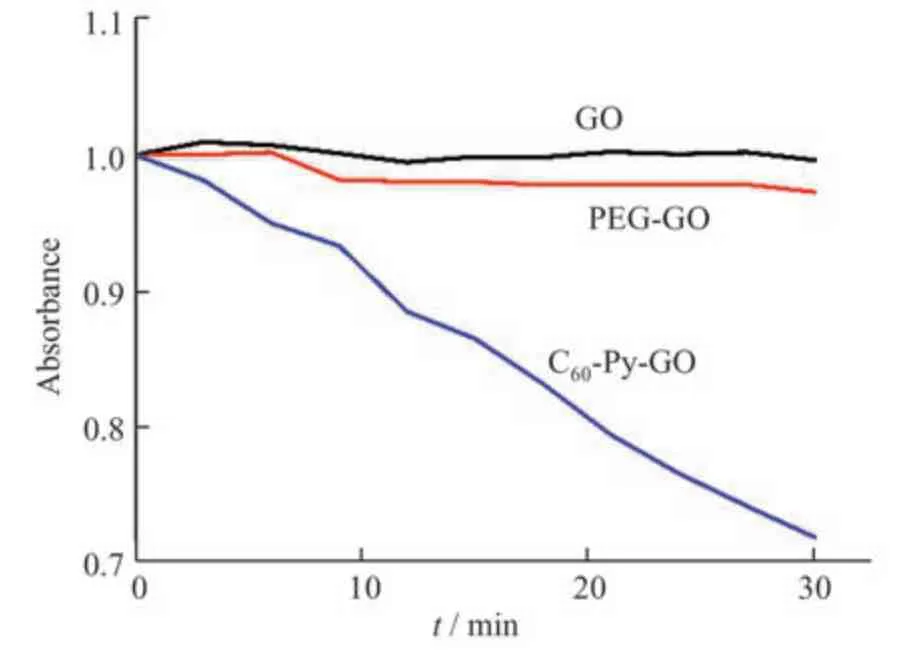
图9 GO, PEG-GO 和C60-Py-GO 随着光照时间变化产生1O2的情况Fig.9 The1O2production by GO, PEG-GO and C60-Py-GO after irradiation for different time periods
2.3 C60-Py-GO 的光热/光动力治疗效果
采用MTT 法检测了C60-Py-GO 体系对Hela细胞的光热/光动力治疗效果。如图10(a)所示,在无光源照射时,C60-Py-GO 体系对Hela 细胞无明显毒性,表明C60-Py-GO 体系具有良好的生物相容性。当在808 nm 激光照射下,C60-Py-GO 体系(140 μg/mL)利用其光热效应可使Hela 细胞存活率降至27.6%;当在可见光照射时,C60-Py-GO 体系(140 μg/mL)利用其光动力效应可使Hela 细胞存活率降至56.5%;而在808 nm 激光和可见光同时照射下,C60-Py-GO 体系由于光热和光动力的共同作用,可以杀死更多的Hela 细胞,使其存活率降至20.7%。通过与PEG-GO 体系(图10(b))进行对照,在同样实验条件下,PEG-GO 仅展示出光热效应,而无光动力效应。这意味着在808 nm 激光和可见光同时照射下,C60-Py-GO 体系可以表现出光热和光动力联合治疗效果。

图10 Hela 细胞在C60-Py-GO 体系(a)和PEG-GO 体系(b)不同处理条件下的存活率Fig.10 Cell viabilities of Hela cells after different treatment C60-Py-GO (a)and PEG-GO (b)
3 结 语
本研究以更加简便、快速、温和的π-π 非共价键相互作用,将C60-Py 与PEG-GO 结合构筑水溶性的C60-Py-GO 纳米体系。该体系基于GO 在808 nm激光照射时的光热效应,能够实现光热治疗效果,同时基于C60在可见光照射下生成1O2,能够实现光动力治疗效果。在808 nm 激光和可见光同时照射下展现出光热和光动力联合治疗效果,可以有效地降低Hela 细胞的存活率。此外,该体系还具有较好的稳定性。该项研究表明,C60-Py-GO 纳米体系具有潜在的应用价值,可进一步开展将其用于杀死其他肿瘤细胞的效果研究。
