高血压性基底节区后部脑出血患者应用不同入路小骨窗开颅术治疗的临床研究
2022-05-25杨万敬
杨万敬
(河南省洛阳市第三人民医院神经外科 洛阳 471002)
高血压脑出血是常见脑外科急症,是所有脑出血中最常见的类型之一[1~3]。高血压动脉硬化所致脑实质内出血以基底节区为高发部位[4],属神经科危急重症,发病率、致死率、致残率较高。高血压性基底节区后部脑出血目前临床主要通过外科手术的方式,清除患者血肿,缓解出血对患者脑组织造成损伤。传统颞叶皮层入路开颅手术能在直视条件下快速清除血肿,改善颅内压迫症状,疗效较好,但由于外侧裂区血管较丰富,走行复杂,经颞叶皮层入路创伤较大,患者出血较多[5~6],故临床应探讨合理微创手术,以减少医源性损伤,从而达到最佳临床疗效。经侧裂下Rolandic 点-岛叶入路小骨窗开颅是一种基于解剖学、外科学的新兴手术入路,该术式能充分利用岛叶与额颞之间的生理间隙完成血肿清除,距离基底节区较短,手术创伤较小,在基底节区脑出血治疗中应用广泛[7]。本研究分析高血压性基底节区后部脑出血患者应用不同入路小骨窗开颅术治疗的效果。现报道如下:
1 资料与方法
1.1 一般资料 纳入我院2018 年5 月至2019 年5 月收治的高血压性基底节区后部脑出血患者84例,随机分为研究组和对照组,各42 例。研究组男22 例,女20 例;年龄45~84 岁,平均(64.52±3.41)岁;格拉斯哥昏迷指数评分(GCS)>12 分9 例,9~12 分23 例,6~8 分10 例;左侧出血25 例,右侧出血17 例。对照组男23 例,女19 例;年龄46~85岁,平均(64.87±3.65)岁;GCS 评分>12 分8 例,9~12 分22 例,6~8 分12 例;左侧出血27 例,右侧出血15 例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。纳入标准:符合基底节区脑出血诊断标准[8];既往有高血压病史;为单侧基底节区后部血肿;对本研究知情且自愿参与,并签署知情同意书。排除标准:伴有其他出血或脏器器质性病变;GCS 评分3~5 分。本研究经医院医学伦理委员会批准(伦理学审查批件编号:IRB-ATT-001-23)。
1.2 治疗方法 对照组采用经颞叶皮层入路手术治疗。患者仰卧位,全麻气管插管,定位颞上或中回后部,切开大脑皮质,约2.0 cm,解剖外侧壁后暴露脑叶,于脑叶皮层上作切口,暴露血肿腔,在显微镜视野下清除血肿,密闭缝合硬脑膜。微骨瓣开颅者行骨瓣复位,脑肿胀、脑皮质塌陷不显著者行向上、向前延伸头皮切口,并去额颞顶大骨瓣以减压。缝合切口,予抗感染、维持水电解质平衡等常规措施。研究组采用经侧裂下Rolandic 点-岛叶入路手术治疗。患者仰卧位,全麻气管插管,头略偏向健侧30°,首先对外侧裂、侧裂前点、Rolandic 点定位,在颞部耳前部位,斜向后上直切口约8 cm,开颅剪开硬脑膜,暴露外侧裂,解剖Rolandic 点,使岛叶中后方充分暴露,再电凝岛叶无血管区,切开1 cm,暴露血肿腔,于显微镜下清除液态与固态血肿,停止出血后采用止血材料置于脑组织表面止血,留置引流管,缝合切口。予抗感染、维持水电解质平衡等常规措施。两组均严密监测患者意识状态、瞳孔及生命体征变化,术后4~6 h 行头颅CT 检查,予尼莫地平(国药准字H20033549)40 ml+生理盐水10 ml 微量泵入,泵速15 μg/(kg·h),并根据血压情况调整泵速,将血压维持在150~160/85~95 mm Hg,同时维持患者脑灌注压,在术后6~8 h 内暂时不予以脱水治疗,保持患者呼吸道通畅,必要时尽早采取气管切开,预防脑卒中相关性肺炎。
1.3 临床疗效评估标准 根据格拉斯哥预后评分(GOS)判定[9],分为良好、中度残疾、重度残疾、植物生存、死亡5 个等级,分值为1~5 分。患者恢复至正常社会活动及工作表示“良好”;患者有独立生活及自理能力,但无法完成正常社会活动及工作表示“中度残疾”;患者意识状态清醒,但生活无法自理,需要他人照料表示“重度残疾”;患者意识状态丧失,但可自主呼吸、睁眼,肢体反射功能及吞咽功能存在表示“植物生存”;死亡。总有效率=(良好例数+中度残疾例数)/总例数×100%。
1.4 观察指标 比较两组手术时间、术中出血量、术后睁眼时间、术后24 h 内再出血发生率、术后24 h 内血肿清除率、术后48 h 内脑水肿增加率、术后并发症发生情况;于术后6 个月比较两组临床疗效。
1.5 统计学分析 采用SPSS19.0 统计学软件分析数据。计数资料以率表示,无序计数资料组间比较采用χ2检验,计量资料以(±s)表示,组间同一时间比较采用独立样本t检验,组内不同时间比较采用配对t检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组手术指标比较 研究组手术时间、术后睁眼时间均显著短于对照组,术中出血量显著低于对照组,差异有统计学意义(P<0.05)。见表1。
表1 两组手术指标比较(±s)
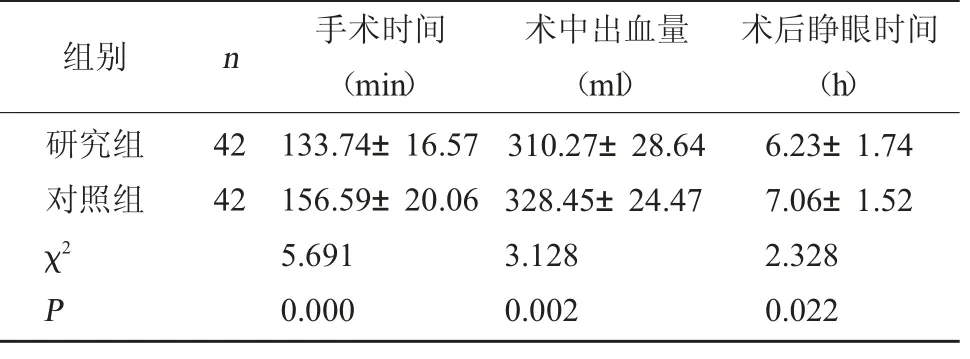
表1 两组手术指标比较(±s)
组别 n 手术时间(min)术中出血量(ml)术后睁眼时间(h)研究组对照组χ2 P 42 42 133.74±16.57 156.59±20.06 5.691 0.000 310.27±28.64 328.45±24.47 3.128 0.002 6.23±1.74 7.06±1.52 2.328 0.022
2.2 两组术后情况比较 研究组术后24 h 内再出血发生率、术后48 h 内脑水肿增加率低于对照组,术后24 h 内血肿清除率明显高于对照组(P<0.05)。见表2。
表2 两组术后情况比较(±s)

表2 两组术后情况比较(±s)
组别 n 术后24 h 内再出血[例(%)]术后48 h 内脑水肿增加率(%)术后24 内血肿清除率(%)研究组对照组t/χ2 P 42 42 0(0.00)4(9.52)4.200 0.040 9.42±0.39 9.76±0.48 3.563 0.001 90.74±4.38 85.26±5.91 4.828 0.000
2.3 两组并发症发生情况比较 研究组并发症总发生率显著低于对照组,差异有统计学意义(P<0.05)。见表3。

表3 两组并发症发生情况比较[例(%)]
2.4 两组临床疗效比较 术后6 个月,研究组治疗总有效率高于对照组(P<0.05)。见表4。

表4 两组临床疗效比较[例(%)]
3 讨论
脑出血属于高血压常见并发症,由于出血部位在大脑,故高血压脑出血具有较高致死率与致残率,以基底节区出血最常见[10]。高血压脑出血后半小时产生血肿,6 h 后出血现象消失,8 h 后病变脑组织发生水肿、坏死[11],因此应早期手术以降低颅内压。经侧裂入路及经颞叶皮层血肿清除术是基底节区脑出血常用治疗手段,该术式由于术中方便直视手术部位,有利于血肿清除,被较多脑外科医生使用,但侧裂入路位于宽大侧裂前点,切口较大,术中易过度牵拉正常组织,干扰手术视野,无法有效控制出血点,血肿不易完全清除[12]。大脑外侧裂位于额顶叶、颞叶及岛叶间的自然蛛网膜间隙,Rolandic 点深面位于脑岛中后部位,与基底节出血部位相对[13]。因此,采用经侧裂下Rolandic 点-岛叶入路可在手术中精准定位,减少脑组织损伤程度,缩短手术路径,易于止血。本研究结果显示,研究组手术时间、术后睁眼时间均短于对照组,术中出血量少于对照组;研究组术后6 个月时随访,临床疗效明显优于对照组。说明该术式用于高血压性基底节区后部脑出血患者可促使患者从重度残疾或植物状态转为中度残疾或良好状态,可明显改善患者预后。经侧裂下Rolandic 点-岛叶入路具有损伤更小的优势,这可能是因为该入路路径较短,可以根据患者血肿情况调整岛叶切口范围,可获得较好的操作空间,进一步提升了血肿清除效果,使患者术后睁眼时间缩短。同时由于经该入路到达血肿部位距离较短,手术切口对脑组织损伤较小,有利于缩短手术时间与降低术中出血量。
清除血肿是高血压脑出血手术的关键所在,可减轻颅内高压状态,提升神经元损伤后修复可能性,预防出血后继发病理变化,切断威胁生命的恶性循环[14]。分离外侧裂下Rolandic 点具有较强可塑性,术中可根据血肿调节分离及岛叶切开方向,保留足够操作区域,便于术后对症治疗及处理,使得继发性脑水肿减轻[15]。本研究结果显示,研究组术后24 h 内再出血发生率、术后48 h 内脑水肿增加率均明显低于对照组,术后24 h 内血肿清除率明显高于对照组。表明经侧裂下Rolandic 点-岛叶入路可减轻高血压性基底节区后部脑出血患者术后出血及脑水肿,提高术后血肿清除率。研究组并发症发生率显著低于对照组,提示经侧裂下Rolandic 点-岛叶入路可以降低高血压基底节区出血患者术后并发症发生率,这可能是因为该入路手术对血肿清除效率较高,同时对患者的损伤降到最低,一定程度上降低了术后再出血的可能,且传统经颞叶皮层入路可能损伤颞上回与颞中回表面的功能区结构,提升失语、癫痫等并发症发生风险[16~17]。研究组选择经侧裂下Rolandic 点-岛叶入路,避免了上述风险的发生,降低了并发症的发生率。综上所述,采用经侧裂下Rolandic 点-岛叶入路小骨窗开颅术治疗高血压性基底节区后部脑出血患者,可获得更好临床疗效,降低术后并发症发生率,有助于改善患者远期预后。
