高考中反应历程(机理)题初探
2022-05-20云南赵旭东
云南 赵旭东
一、化繁为简认识反应历程(机理)
反应历程(机理)试题能较好考查考生获取信息的能力,在近几年的高考中高频出现。为方便教学,符合高中学生的认知水平,笔者在这里对“反应历程(机理)”作化繁为简处理:基元反应就是一步完成的反应;一个复杂反应可以由若干个基元反应按照一定规律组合起来;反应历程是化学中用来描述某一化学变化所经由的全部基元反应的学科名词,所表达的意思就是反应物究竟按什么途径、经过哪些步骤得到了最终产物;反应历程又被称为反应机理。
二、反应历程(机理)题高频出现的原因
1.化学的应用价值使然
化学的应用价值决定了化学必须要研究化学反应来应用于实际生产实践,化学反应要应用于生产实践主要有两个方面的问题:一是要了解反应进行的方向和最大限度以及外界条件对反应平衡的影响;二是要知道反应进行的速率和反应的历程(机理)。
2.《课程标准》的要求
《普通高中化学课程标准(2017年版2020年修订)》(以下简称《课程标准》)在主题2化学反应的方向、限度和速率中提出明确要求“知道化学反应是有历程的,认识基元反应活化能对化学反应速率的影响”。
3.新教材的要求

4.《中国高考评价体系》的要求
《中国高考评价体系》中对高考中反应历程(机理)提出了比《课程标准》、教材更高的要求,通过“立德树人,服务选才,引导教学”的这“一核”将教学、高考、高校人才选拔融合成一个结构严谨的整体系统。《中国高考评价体系说明》在阐述创新性时以化学为例——“高考对化学创新思维能力的考查就包括推测反应现象或物质性质、设计物质合成或分离路线、阐释机理或总结规律等”。足见反应历程(机理)承载创新性的考查要求有独到之处。不仅如此,笔者对照《中国高考评价体系》及其说明分析近年高考化学题中的反应历程(机理)题,发现它还能很好地承载基础性、应用性、综合性的考查要求,包括核心价值、学科素养、关键能力和必备知识的考查内容。此外,反应历程(机理)题还能轻松实现解题向解决问题的转变。
三、反应历程(机理)题的发展
2013年教育部启动了普通高中课程修订工作,2017年《课程标准》颁布,2019年部分地区开始使用新教材,2019年11月《中国高考评价体系》及其说明颁布,2020年落实新高考,这期间高考中的反应历程(机理)题经历了出现、完善、基本定型的发展过程。2018年高考全国卷反应历程(机理)题就闪亮登场,如2018年全国卷Ⅱ第8题,情境是氮氧化物和二氧化硫在形成雾霾时与大气中的氨的关系示意图。彼时未将其称为“反应历程(机理)”,原因是2007年人版教版教材选修4《化学反应原理》中,有“催化剂能加快反应速率,是因为它能改变反应的路径,使发生反应所需的活化能降低”的叙述,未出现“反应历程(机理)”这一名词。也正是因为旧版教材对于《课程标准》和《中国高考评价体系》的考查要求的滞后,导致“反应历程(机理)”题在2019年至2021年的高考全国卷中“犹抱琵琶半遮面”地示人。2019年高考全国卷Ⅰ第28题(3)有“反应历程”的称谓,第10题同样属于反应历程(机理)题,以“表面吸附和溶解过程”谓之;2020年高考全国卷Ⅱ第11题以“反应机理”谓之;2021年高考全国甲卷28题(1)最后两空的考查属于反应历程(机理),高考命题老师用学生容易接受的叙述替换了陌生名词“反应历程(机理)”。这些现象既体现了《中国高考评价体系》以及《课程标准》的要求,又考虑到了2019年版教材尚未全部启用的实际教学情况,同时清晰地传达了反应历程(机理)题将在高考中高频考查的信息。
四、反应历程(机理)题的类型
反应历程(机理)题可以是选择题、也可以是非选择题。反应历程(机理)题多以图像形式呈现信息,也可以是全文字的题。反应历程(机理)题的图像分为能垒图、循环图、直线图。图中可以用物质名称、微粒符号或微粒模型(微粒模型图以下简称“模型图”)来表示所发生的化学反应或变化。2018年至2021年高考全国卷图像题类型统计情况见表1。
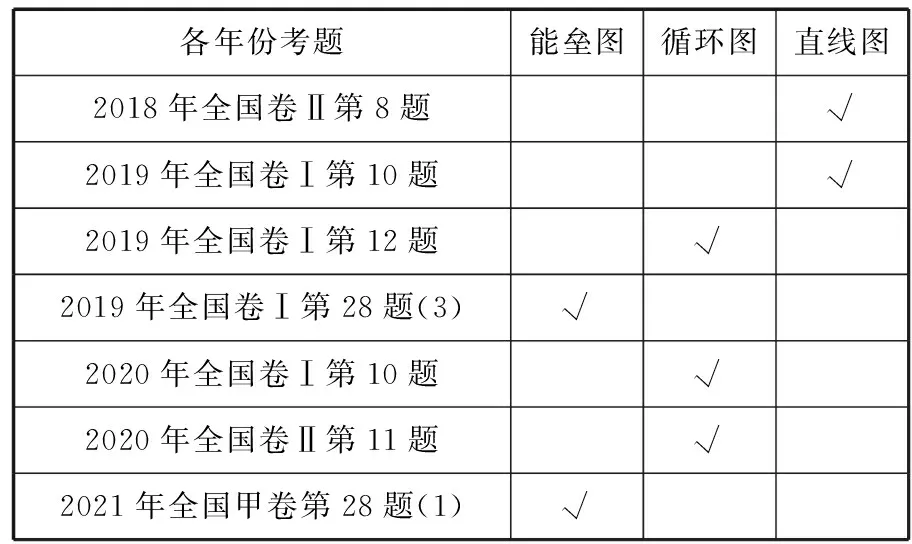
表1 2018年至2021年高考全国卷图像题类型统计表
2019年全国卷Ⅰ第10题情境是HCl气体分子在253 K 冰表面吸附和溶解过程的示意图,从物质变化看是物理过程,因涉及催化领域的研究将其归为反应历程(机理)题,从表达微粒的形式看属于模型图,从反应过程是否闭合看属于直线图。此题与其他年份的反应历程(机理)题相比,较为独特。
五、例析反应历程(机理)题
情境是考查的载体,情境通常分为两类,一是生活实践情境,即与日常生活、生产实践密切相关的试题情境;二是学习探索情境,即源于真实的研究过程或实际的探索过程的试题情境。笔者分析近年反应历程(机理)题的情境,这两类情境都有,题目设问围绕以下考查方向设置:历程中某一陌生方程式的书写,找活化能、催化剂、中间体,判断反应的快慢,判断反应的决速步骤,判断焓变的正负或找焓变值。这些反应历程(机理)题很好地体现了高考评价体系中“四层”“四冀”的要求。下面笔者以2021年全国甲卷第28题(1)为例进行说明。
二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳.回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为

该反应一般认为通过如下步骤来实现:


总反应的ΔH=________kJ·mol-1;若反应①为慢反应,图1示意图中能体现上述反应能量变化的是________(填标号),判断的理由是。
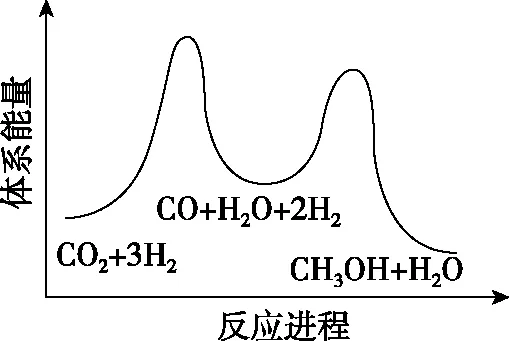
A

B
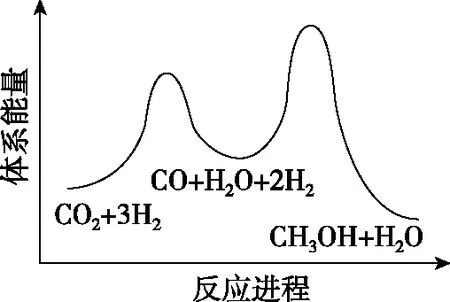
C
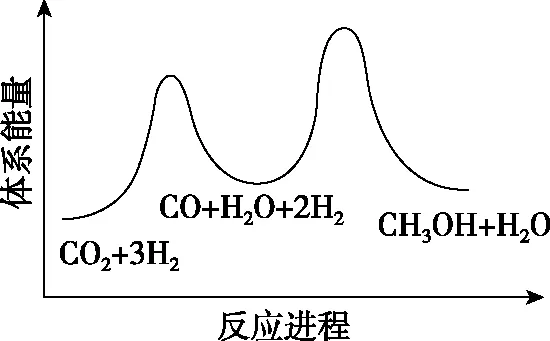
D
【试题情境】属于“生产新能源+环保”情境,利用二氧化碳加氢制得新能源甲醇,同时减少温室气体二氧化碳。
【必备知识】考查了化学用语(热化学方程式)、概念(能垒、活化能)、运用盖斯定律计算反应热、物质转化及利用。
【关键能力】主要考查了学生的理解与辨析能力、分析与推测能力、语言表达能力。第一空利用盖斯定律计算反应热可得出,观察并找到总反应=①+②,计算出反应热ΔH=41+(-90)=-49 kJ·mol-1。第二空图形为能垒图,结合总反应ΔH=-49 kJ·mol-1<0即总反应为放热反应,故能垒图中产物能量低,正确选项在A、C中;由已知“反应①为慢反应”,所以反应①的能垒(活化能)比反应②的高,故选A。第三空考查学生第二空是不是真正懂了、化学学科化的语言表达有没有掌握。
【学科素养】本题考查了证据推理与模型认知化学学科核心素养,侧重考查思维方法。学生利用总反应与①②的关系,联想到用盖斯定律计算反应热;把能垒图和已知信息有机地联系在一起,用图解释已知信息,用已知信息读懂图。
本题很有新意,将盖斯定律求算反应热的结果与能垒图巧妙地综合在一起,层层深入,落实了基础性、应用性、综合性和创新性的考查;教材上学生没有学过的知识高考中也可以考。这对教师的化学新课教学和高考备考提出了新的要求,教材中有关能垒、快(慢)反应、决速步骤等概念、知识虽然未明确表示,但活化能、催化剂、碰撞理论等知识点的考查绕不开这些概念和知识,新课教学时教师应以碰撞理论为突破口,引导、促成学生建构起相关的知识网络,在备考中做必要的针对性练习。
2018—2020年高考化学试题中的反应历程(机理)题的分析与本题相似,笔者在这里就不再赘述。
六、反应历程(机理)题的解题模型
1.切入点:先从设问开始,再回已知和历程中读题、审题。
2.重点:物质(微粒)的变化。物质观、微粒观、变化观是串起历程的主线,抓住这条线,解决问题就会很容易。
3.难点:循环图。闭合的环让学生懵“圈”,解决方法是可记住反应物就是起点,最终产物就是终点,失而复得的是催化剂,自生自灭的是中间产物。
4、易失分点:叙述理由。教师可在教学中向学生归纳、总结学科化的表述。
七、反应历程(机理)题的迁移应用
以2021年高考全国甲卷第13题为例:
乙醛酸是一种重要的化工中间体,可采用如图2所示的电化学装置合成。图中的双极膜中间层中的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法正确的是( )

图2
A.KBr在上述电化学合成过程中只起电解质的作用
C.制得2 mol乙醛酸,理论上外电路中迁移了1 mol电子
D.双极膜中间层中的H+在外电场作用下向铅电极方向迁移
高考中这类题很多,如2020年全国卷Ⅱ第9题二氧化碳过量排放可对海洋生物的生存环境造成很大影响……再往前追溯,如2016年全国卷Ⅰ第11题电解池中电解后浓Na2SO4溶液变为稀Na2SO4溶液。这类题学科特点非常明显,情境都是研究物质组成、结构、变化规律、用途,这类题被统称为“物质(微粒)变化题”。这类题很像反应历程(机理)题,反应历程(机理)题研究基元反应,而物质(微粒)变化题研究的是任意反应。它们有两个共同点:一是常用图来表示物质(微粒)的变化;二是串起反应过程的主线是物质观、微粒观、变化观。这两类题解决问题的思维和方法是相同的,不同的仅仅是必备知识。两类题型相互借鉴、融会贯通,能大大提高学生解决问题的能力。笔者在这里用反应历程(机理)题的解题模型验证一下。
【答案】D

解题模型是一种“套路”,2021年高考后有一种说法是高考题要反“套路”,教师与学生要辩证地看待这种说法。若学生只会生搬硬套,遇到新情境“套路”肯定就毫无用处。若学生在套路的基础上会举一反三,遇到新情境时运用“套路”就能快速有效地解题。物质(微粒)变化题出现的时间比反应历程(机理)题早得多,如果学生建构起物质(微粒)变化题的解题模型,当反应历程(机理)题出现时就能很容易解决。教师不能把学生教“死板”,不能只是教学生简单地记忆和套用解题模型,要让学生去发现、领悟、完善这个解题模型。一个解题模型用于新情境,虽然是“旧瓶装新酒”,却能“日久弥香”。
