表面活性剂对甲基红离解常数的影响研究
2022-05-18张元勤
张元勤
(乐山师范学院 新能源材料与化学学院,四川 乐山 614004)
0 引言
酸碱指示剂在分析测试中应用十分广泛,其变色点和变色范围受介质的影响,因此研究介质对酸碱指示剂变色点和变色范围的影响对测试结果的准确性有重要意义。表面活性剂水溶液作为一类特殊的介质,以其笼效应、微粘度效应、局部浓度效应、定位效应、静电效应和极性效应[1-3]影响调节着许多化学反应的进行,已有文献报道不同类型表面活性剂对指示剂离解常数及变色范围的影响[4-5]。本文研究了阳离子表面活性剂CTAB、阴离子表面活性剂磺化琥珀酸二辛脂钠盐和两性离子Brij35 三种表面活性剂对甲基红离解常数、变色点和变色范围的影响,实验发现,不同类型表面活性剂对甲基红的离解常数、变色点和变色范围的影响不同,其中CTAB 影响较大,磺化琥珀酸二辛脂钠盐和Brij35 影响较小。因此,可以选择不同的表面活性剂形成的胶束溶液作为滴定介质提高酸碱滴定的灵敏度,减小测量误差,扩大酸碱指示剂的应用范围。
在酸碱滴定的等当点附近具有一定的pH 突跃时,指示剂从一种颜色突变为另一种颜色,常根据GB/T604—2002 酸碱指示剂在不同的pH 缓冲溶液中而引起颜色变化的特性来测定酸碱指示剂的变色范围,由于人的视觉对指示剂颜色变化的敏锐程度不一样,即在确定指示剂的变色点及变色范围会有所差异,本文尝试一种用分光光度计观测指示剂在变色点附近的吸光度发生突变来确定指示剂变色范围的方法。结果表明:用分光光度发测定的甲基红的变色范围与GB/T604—2002 测定出的变色范围有一定的不同,但差距不大。我们认为仪器测定的变色范围更准确,这为测定酸碱指示剂的变色范围提供了一种新的方法,也为利用分光光度法进行酸碱滴定提供了可能性。
1 实验部分
1.1 仪器与试剂
V-630 紫外分光光度计(日本分光珠式会社),PHS-3E pH 计(上海雷磁公司),超级恒温器(上海实验仪器厂有限公司)。
甲基红、95%乙醇、无水乙醇、磷酸二氢钾、聚氧乙烯月桂醚(Brij35)、十六烷基三甲基溴化铵(CTAB)、磺化琥珀酸二辛脂钠盐、盐酸、磷苯二甲酸氢钾、乙酸钠、氢氧化钠、乙酸均为分析纯,实验用水为超纯水。
甲基红储备液溶液:准确称取0.5000 g 甲基红溶解于300 mL 95%乙醇中,溶解后移入500 mL 容量瓶中,用水稀释至刻度。
甲基红标准溶液的配制:移取8 mL 甲基红储备液于100 mL容量瓶中,加入50 mL乙醇溶液,用水稀释至刻度。
HMR 溶液和MR-溶液的配制:分别移取10 mL 甲基红标准溶液于100 mL 容量瓶中,分别加入10 mL 0.1 mol.L-1HCl 和35 mL 0.2mol.L-1NaAc,再加水稀释至刻度。
1.2 实验方法
1.2.1 最大吸收波长的测定
HMR 溶液的最大吸收波长:取两个1 cm 比色皿,分别装入水和HMR 溶液,以水为参比,测最大吸收波长。MR-溶液的最大吸收波长测法类似。图1 和2 分别为HMR 和MR-的吸光度随吸收波长的变化关系。由图1 和2 可见,HMR 和MR-的最大吸收波长λA、λB分别为521 nm、431 nm,以下实验均在其对应的最大吸收波长下测定其相应的吸光度。

图1 HMR 的最大吸收波长
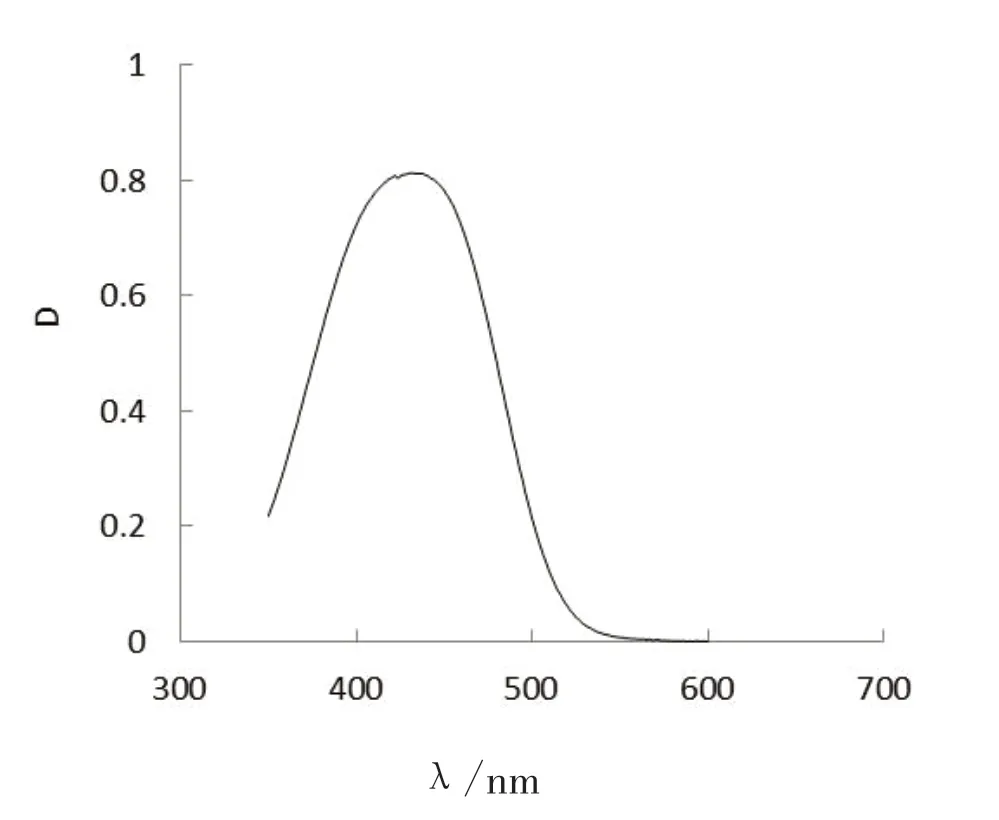
图2 MR-的最大吸收波长
1.2.2 指示剂离解常数的测定
取HMR 和MR-溶液,分别用0.01 mol.L-1的HCl 和CH3COONa 稀释至原溶液的一系列倍数,为一系列待测溶液,测定溶液的吸光度。用吸光度对溶液浓度作图,分别计算甲基红HMR和MR-在两波长下的摩尔吸光系数。
另在25 mL 容量瓶中加入0.875 mL 甲基红标准溶液和5 mL 0.1 mol.L-1的CH3COONa 溶液,并分别加入10.00 mL、8.00 mL、5.00 mL、3.00 mL、1.00 mL的0.1 mol.L-1的CH3COOH,用水定容,测定最大吸收波长下各溶液的吸光度及pH。由公式(2)可计算出指示剂离解平衡常数的pK。
1.2.3 指示剂变色范围的测定
根据GB/T604—2002,在25 mL 比色管中加入不同pH 值的缓冲溶液24 mL 和0.2 mL 待测指示剂,摇匀,在25 ℃下恒温20 分钟,测定两波长下各溶液的吸光度和pH 值以确定指示剂的变色点和变色范围。
2 结果与讨论
2.1 表面活性剂对酸碱指示剂离解常数的影响
2.1.1 摩尔吸光系数的计算
按文献[6]进行测定。
2.1.2 酸碱指示剂离解常数的计算
酸碱指示剂的离解平衡反应为:


根据上式和比尔定律可化为:

式(2)中,DA、分别为在HMR 和MR-在最大吸收波长处溶液的吸光度。αA,HMR、αA,MR-、和αB,HMR、BMR,分别为在波长521 nm、431 nm 下的摩尔吸光系数。λA、λB分别为αA,MR-与αA,HMR和αB,MR-与αB,HMR的比值。

图4 MR 在波长521 nm、431 nm 下吸光度随MR-浓度变化关系
根据图3 和4,拟合甲基红的酸式和碱式吸光度随浓度变化的曲线,可得HMR、MR-在酸式波长下的摩尔吸光系数分别为63 390 L.mol-1.cm-1、2 340 L.mol-1.cm-1,在碱式波长下的摩尔吸光系数分别为6 200 L.mol-1.cm-1、27 420 L.mol-1.cm-1。

图3 HMR 在波长521 nm、431 nm 下吸光度随HMR浓度变化关系
2.1.3 水溶液中指示剂离解常数的测定
在不同pH 下,甲基红的MR-与HMR 相对含量不同,根据公式(1),用pH 对l g([MR-]/[HMR])作图,如图5 所示,直线与纵轴的交点即甲基红的pK 值为4.94,与文献值4.95±0.05相符,表明用该方法测定甲基红的离解常数可行。

图5 pH 与lg[MR-]/[HMR]关系
2.1.4 表面活性剂对甲基红离解常数的影响
在25 mL 容量瓶中分别加入0.875 mL 标准甲基红溶液、5 mL 0.2 mol.L-1的CH3COONa 溶液、5 mL 0.1 mol.L-1CH3COOH 和不同体积的表面活性剂溶液,然后用水定容至刻度,测定溶液在两波长下的吸光度及pH 值。由式(2)可计算出指示剂在不同表面活性剂下的pK,图6—图8 分别为磺化琥珀酸二辛酯钠、CTAB 和Brij35 对离解常数的影响关系图。
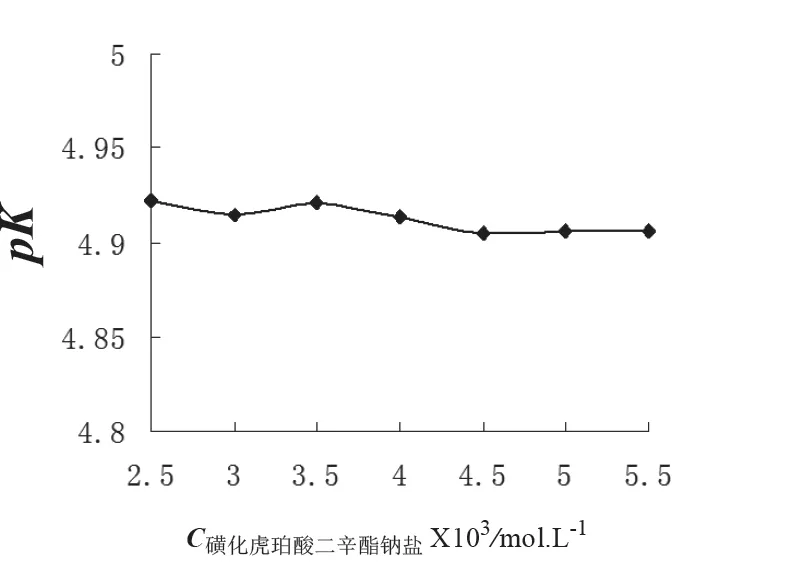
图6 pK 随磺化琥珀酸二辛酯钠盐浓度变化关系

图7 CTAB 对pK 的影响

图8 随Brij35 对pK 的影响
由图6 可见,随着磺化琥珀酸二辛酯钠盐浓度的增大,甲基红的pK 变化较小,这可能是阴离子磺化琥珀酸二辛酯钠盐形成的胶束对H+的静电效应远远强于局部浓度效应和胶束对MR-的排斥作用,使得甲基红的pK 刚开始有减小的趋势,磺化琥珀酸二辛酯钠盐浓度增大到一定值后,MR-和HMR 达到饱和,pK 值也趋于稳定。
由图7 可见,甲基红的pK 先随CTAB 浓度的增大而减小,这可能是CTAB 与甲基红碱式MR-通过静电相互作用,使MR-的局部浓度增大,使得离解平衡不断向右移动,pK 逐渐减小。当CTAB 浓度增大到一定值后,pK 达到最小值,这可能是MR-在CTAB 阳离子表面活性剂胶束中的吸附达到饱和。当CTAB 浓度进一步增大时,pK逐渐增大,这可能是CTAB 浓度进一步增大时只起到稀释的作用,pK 值随之增大。
由图8 可见,甲基红的pK 随Brij35 浓度的增大而增大,当Brij35 浓度增大到一定值后,pK的变化变得平缓,并趋于一定值,这可能是随着非离子表面活性剂Brij35 浓度的增大,由于局部浓度效应使得HMR 的浓度增大,pK 值逐渐增大,当Brij35 浓度增大到一定值后,吸附达到饱和状态,pK 趋于一定值。
2.2 表面活性剂对酸碱指示剂变色点及变色范围的影响
根据GB/T604—2002,测得一系列不同pH水溶液中甲基红吸光度随pH 的变化如图9 所示。

图9 甲基红水溶液吸光度与pH 关系
利用指示剂在变色点附近发生颜色突变时其吸光度也会发生突变的特点可以确定指示剂的变色点和变色范围。由图9 可见,由甲基红吸光度随pH 变化趋势可确定其变色范围为3.97-5.94,与GB604—2002 比色法测出的甲基红的变色范围4.4-6.2 比较而言,变色范围有所变宽,甲基红在pH 为3.97 就开始发生颜色的变化,出现微弱的橙色,5.94 时红色就完全变为橙色,这表明采用比色法所测定的变色范围有一定的误差,采用分光光度法更能准确测定甲基红的变色范围。
根据GB/T604—2002,在25 mL 比色管中加入不同pH 值的缓冲溶20 mL 和0.2 mL 待测指示剂,4 mL 一定浓度的表面活性剂摇匀,在25 ℃下恒温20 分钟,测两波长下各溶液的吸光度和pH 值,作吸光度与pH 关系图,如图10、图11、图12 所示。

图10 磺化琥珀酸二辛脂钠盐下甲基红吸光度与pH 关系

图11 CTAB 下甲基红吸光度与pH 关系

图12 Brij35 下甲基红吸光度与pH 关系
由图10 可见,磺化琥珀酸二辛脂钠盐下甲基红吸光度随pH 变化趋势可测定其变色范围为3.94-5.87,与分光光度法测出的甲基红的变色范围3.97-5.94 比较而言,变色点和变色范围有一定的减小,这表明加入磺化琥珀酸二辛脂钠盐形成的胶束溶液对指示剂的变色点和变色范围有一定的影响,但效果不明显。
由图11 可见,CTAB 下甲基红吸光度随pH变化趋势可确定其变色范围为3.84-5.67,与分光光度法测出的甲基红的变色范围3.97-5.94 比较而言,变色范围有一定的减小,这表明加入CTAB 形成的胶束溶液对酸碱滴定的准确度有一定的提高,可以加入CTAB 来控制指示剂的变色点,从而满足较佳的滴定条件,减小滴定误差以及扩大酸碱指示剂的应用范围。
由图12 可见,Brij35 下甲基红吸光度随pH变化趋势可确定其变色范围为4.19-5.96,与分光光度法测出的甲基红的变色范围3.97-5.94 比较而言,变色点增大,变色范围减小,这表明加入Brij35 形成的胶束溶液对酸碱滴定准确度有一定的提高,可以加入Brij35 来控制指示剂的变色点,从而满足较佳的滴定条件,减小滴定误差。
3 结论
不同类型的表面活性剂对酸碱指示剂的平衡常数、变色点和变色范围均有不同程度的影响,其中以阳离子表面活性剂的影响最大。利用光度法测定指示剂的变色点和变色范围有一定的可行性,利用光度法进行酸碱滴定是值得探索的新方法。
