1-肉桂酰基吡咯烷-2.5-二酮类物质的制备及应用
2022-05-16李江红石克金贾东豪
李江红 石克金 张 滢 贾东豪 陈 林
(1.成都大学药学院四川抗菌素工业研究所,四川成都,610106;2.成都中医药大学临床医学院,四川成都,611137)
1-肉桂酰基吡咯烷-2.5-二酮(1a,图1)为α,β-不饱和酰亚胺物质,可作为迈克尔受体参与迈克尔加成的串联环化反应(Michael-Initiated Ring Closing reaction)构建含有羰基的杂环结构。杜大明教授课题组以1-肉桂酰基吡咯烷-2.5-二酮类物质为受体,1.3-二酮类物质为供体,发生(3+3)的串联环化反应,成功构建了二氢吡喃酮骨架,收率高达97%[1]。之后,他们又以3-羟基吲哚酮为供体,与1-肉桂酰基吡咯烷-2.5-二酮发生迈克尔加成的串联环化反应,构建了吲哚螺γ-丁内酯结构,实现了(2+3)的环化反应[2]。根据文献报道,1-肉桂酰基吡咯烷-2.5-二酮的制备方法有:(1)用吡啶为碱[1],反应时间长达50小时,但实际收率比较低。(2)用正丁基锂拔去丁二酰亚胺氮原子上的氢,形成锂盐,再与肉桂酰氯反应[3]。由于使用正丁基锂,对反应条件要求比较严苛,需要严格无水无氧,且需要低温至-78℃。(3)用离子对试剂为介质[4],效果虽好,但成本较高。本文通过研究,直接用氢氧化钠或碳酸氢钠,将丁二酰亚胺在水相转化成钠盐,结晶析出,然后,于室温条件与肉桂酰氯反应制备得到产物(如图1)。本方法条件简单,温和可控,试剂使用方便,产品收率高。

图1 1-肉桂酰基吡咯烷-2.5-二酮的合成
1 实验部分
1.1 试剂与仪器
试剂:肉桂酸(上海麦克林生化科技有限公司);二氯甲烷(DCM)、N,N-二甲基甲酰胺(DMF)、草酰氯、氢氧化钠、丙酮等均为分析纯,购自成都市科隆化学品有限公司。
仪器:85-2型恒温磁力搅拌器(上海司乐仪器有限公司);FA1604N电子天平(上海菁海仪器有限公司);Agilent AV-400(600 MHz)核磁共振仪(安捷伦科技有限公司);ZF-Ⅰ型三用紫外分光仪(上海市安亭电子仪器厂)。
1.2 1-肉桂酰基吡咯烷-2.5-二酮(1a)的合成
步骤1:将肉桂酸(10.0 mmol,1.48 g)加入三口瓶中,再加入DCM(20 mL),搅拌。滴加入(COCl)2(58.0 mmol,4.6 mL),并滴加2滴DMF。油浴锅加热,反应物料搅拌回流2 h。之后,减压浓缩混合物,得淡黄色油状物,冷藏后固化,得肉桂酰氯(1.60 g,收率96%)。
步骤2:将丁二酰亚胺(11.1 mmol,1.10 g),NaOH(10.0 mmol,0.44 g),加入H2O(10 mL)中,搅拌,得淡黄色溶液,然后加入丙酮(30 mL),析出固体,过滤,减压烘干得丁二酰亚胺钠盐(1.22 g,收率90%)。
步骤3:将丁二酰亚胺钠盐(10.0 mmol,1.22 g),溶于DMF(5 mL)中,于室温搅拌,然后,肉桂酰氯(1.83 g,11.0 mmol)的THF(10 mL)溶液慢慢滴加入反应液。TLC监控至反应完全。加入EA(10 ml),H2O(4 mL),分离有机相,碳酸氢钠(5%)水溶液4 mL洗涤有机相,分相后,再加入0.5克无水硫酸镁干燥有机层,过滤除去硫酸镁,减压浓缩有机相至无液体流出,残留物硅胶柱层析(二氯甲烷洗脱),蒸干得产品1-肉桂酰基吡咯烷-2.5-二酮(1a,1.83 g,收率80%)。1H NMR(600 MHz,CDCl3)δ(ppm):7.93(d,J=15.6 Hz,1H),7.59-7.62(m,2H),7.39-7.45(m,3H),7.03(d,J=15.6 Hz,1H),2.87 (s,4H).13C NMR(151 MHz,CDCl3)δ(ppm):174.5,164.2,148.7,133.9,131.5,129.0,128.9,119.1,28.7。
根据上述类似的合成方法,我们还制备了以下几个衍生物(见图2)。
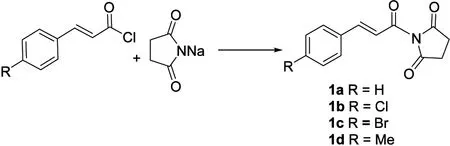
图2 1-肉桂酰基吡咯烷-2.5-二酮的底物的扩展
(1)(E)-1-(3-(4-氯苯基)丙烯酰基)吡咯烷-2,5-二酮(1b),收率83%。1H NMR(600 MHz,CDCl3)δ (ppm):7.85 (d,J=15.1 Hz,1H),7.53 (d,J=8.3 Hz,2H),7.38(d,J=9.0 Hz,2H),7.01(d,J=15.8 Hz,1H),2.87 (s,4H)。13C NMR(151 MHz,CDCl3)δ(ppm):174.5,164.0,147.0,137.4,132.3,130.0,129.3,119.6,28.5。
(2)(E)-1-(3-(4-溴苯基)丙烯酰基)吡咯烷-2,5-二酮(1c),收率79%。1H NMR (600 MHz,CDCl3)δ (ppm):7.86-7.77 (1H),7.59-7.48 (2H),7.47-7.39 (2H),7.05-6.97 (1H),2.88-2.80 (4H).13C NMR (151 MHz,CDCl3)δ(ppm):174.4,164.0,147.1,132.8,132.3,130.2,125.9,119.7,28.7。
(3)(E)-1-(3-(p-甲基苯基)丙烯酰基)吡咯烷-2,5-二酮(1d),收率85%。1H NMR (600 MHz,CDCl3)δ (ppm):7.88 (d,J=15.0 Hz,1H),7.49 (d,J=8.4 Hz,2H),7.21 (d,J=7.8 Hz,2H),6.97 (d,J=15.0 Hz,1H),2.87 (q,J=15.0 Hz,4H),2.38 (d,J=14.4 Hz,3H).13C NMR (151 MHz,CDCl3)δ(ppm):174.5,164.4,148.8,142.2,131.2,129.7,129.0,118.2,28.7,21.6。
1.3 1-肉桂酰基吡咯烷-2.5-二酮的应用
为了拓展1-肉桂酰基吡咯烷-2.5-二酮类物质的用途,我们以1-肉桂酰基吡咯烷-2.5-二酮类物质为受体,分别与吲哚啉-2-亚胺(3)和吡唑酮(4)反应。在碱的催化作用下,实现了(3+3)的串联环化反应,分别构建了咔啉酮和吡唑并δ-内酯结构(见图3)。
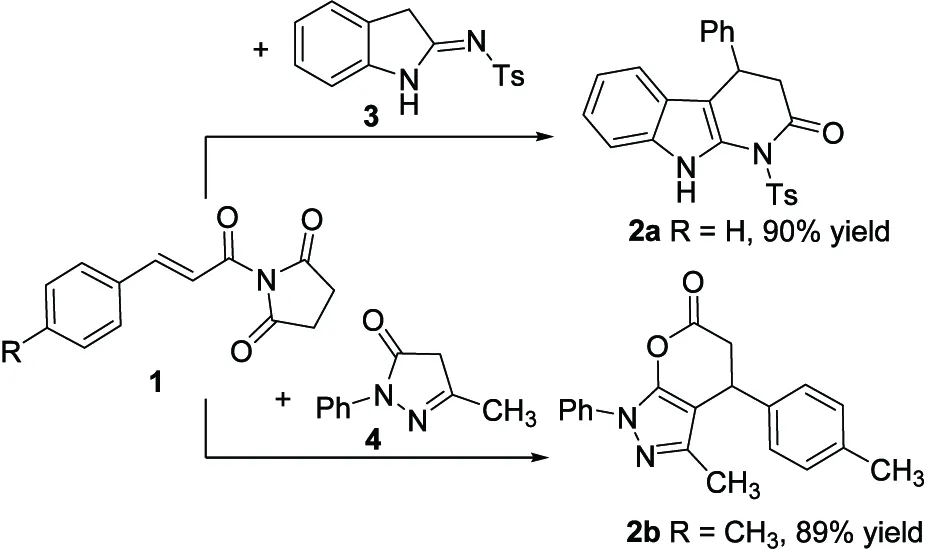
图3 1-肉桂酰基吡咯烷-2.5-二酮在合成中的应用
4-苯基-1-对甲苯磺酰基-1,3,4,9-四氢-2H-吡啶并[2,3-b]吲哚-2-酮(2a)的合成:将1a(27.5 mg,1.2 mmol)与N-(吲哚啉-2-基亚乙烯)-4-甲基苯磺酰胺(28.6 mg,1.0 mmol)加入试管中,再加入乙腈(1.0 mL),加入1,8-二氮杂双环[5.4.0]十一碳-7-烯(1.51 mg,0.1 mmol),于40 ℃搅拌,反应1 h。反应完成之后,硅胶柱层析(PE/EA=6:1),得产品2a (37.53mg,收率90%)。Rf=0.5 (PE/EA=4:1).1H NMR (600 MHz,CDCl3)δ (ppm):9.60 (s,1H),7.87 (d,J=6.6 Hz,2H),7.42 (d,J=7.2 Hz,1H),7.27 (d,J=8.4 Hz,2H),7.21 (t,J=7.8 Hz,1H),7.13 (d,J=6.0 Hz,2H),7.05 (m,3H),6.89 (d,J=7.8 Hz,2H),4.33 (dd,J=6.6,6.0 Hz,1H),3.14 (dd,J=15.0,6.6 Hz,1H),2.93 (dd,J=14.4,4.8 Hz,1H),2.43 (s,3H).13C NMR (151 MHz,CDCl3)δ (ppm):169.2,145.8,141.3,134.4,133.5,131.0,129.6,128.61,128.55,126.91,126.87,124.5,122.0,120.6,118.3,111.4,101.1,43.0,35.0,21.7.HRMS (ESI):m/z calculated for C24H20N2O3S+H+:417.1267,found:417.1265。
3-甲基-1-苯基-4-对甲基苯基-4,5-二氢吡喃并[2,3-c]吡唑-6 (1H)-酮(2b)的合成:将1d(27.5 mg,1.2 mmol)与5-甲基-2-苯基-2,4-二氢-3H-吡唑-3-酮(17.4 mg,1.0 mmol)加入试管中,再加入甲苯(1.0 mL),加入碳酸铯(3.26 mg,0.1 mmol),于50 ℃搅拌,反应1 h,反应完成之后,硅胶柱层析(PE/EA=6:1),得产品2b(27.05 mg,收率89%)。Rf=0.5(PE/EA=6:1).1H NMR (600 MHz,CDCl3)δ (ppm):7.75-7.77 (m,2n),7.45-7.48 (m,2n),7.29-7.31 (m,1n),7.17 (d,J=8.4 Hz,2n),7.11 (d,J=8.4 Hz,2n),4.23 (t,J=6.6 Hz,1n),3.18 (q,J=7.8 Hz,1n),2.98 (dd,J=15.8,6.2 Hz,1n),2.35 (s,3n),1.98 (s,3n)。13C NMR (151 MHz,CDCl3)δ (ppm):165.7,146.9,145.9,137.9,137.6,137.4,129.8,129.2,126.9,126.5,120.9,99.6,38.2,34.3,21.0,13.0。HRMS (ESI):m/z calculated for C20H18N2O2+H+:319.1441,found:319.1441。
2 结论
根据本方法,用氢氧化钠预先将丁二酰亚胺制成其钠盐,再与肉桂酰氯反应,条件相当温和,成功制备得到1-肉桂酰基吡咯烷-2.5-二酮。苯环上进行取代后,也成功制备了另外几个衍生物,收率较高(79%-85%)。本工艺条件简单、方便易行。同时,将该类物质用于新的杂环骨架结构的构建,制备了咔啉酮(2a)和吡唑并δ-内酯(2b)两个新结构物质,且收率较高,进一步体现了该类物质的有用性。
