雌二醇偶联碱性磷酸酶工艺改进
2022-05-16王一恺
王一恺
(上海科华生物工程股份有限公司,上海 200233)
雌二醇(Estradiol,E2)属于甾醇类性激素,是反映人体健康的重要指标。目前,酶联免疫检测是应用较为广泛的雌二醇含量测定方法,具有便捷、快速、成本低廉的优势。天然雌二醇分子本身不含有可直接用于偶联的官能团,目前雌二醇免疫原及酶标抗原的制备均是将雌二醇衍生物与相应的载体蛋白进行偶联,再采用竞争法测得样本中雌二醇含量[1-2]。雌二醇化学发光法检测诊断试剂盒用原料雌二醇偶联碱性磷酸酶(E2-AP)的普遍制备工艺是混合酸酐法[3],该工艺是用氯甲酸乙酯与三乙基胺活化E2衍生物使其形成酸酐,而后与碱性磷酸酶反应形成酶结合产物。但是,其成酐副产物较多,并且随着反应时间延长而增多。而且偶联物在化学发光检测中的稳定性与检测值的相关性较差,制备过程中涉及到的化学试剂毒性较大。因此本文采用碳二亚胺法的偶联工艺制备E2-AP,以期能解决上述问题。
1 实验原理
1.1 混合酸酐法
混合酸酐法是利用氯甲酸乙酯与三乙基胺活化E2衍生物使其形成酸酐,而后与碱性磷酸酶的游离氨基反应形成酶结合产物,反应原理如图1所示。但是,其偶联物的稳定性与检测值的相关性较差,并且制备过程中涉及的化学试剂毒性较大。
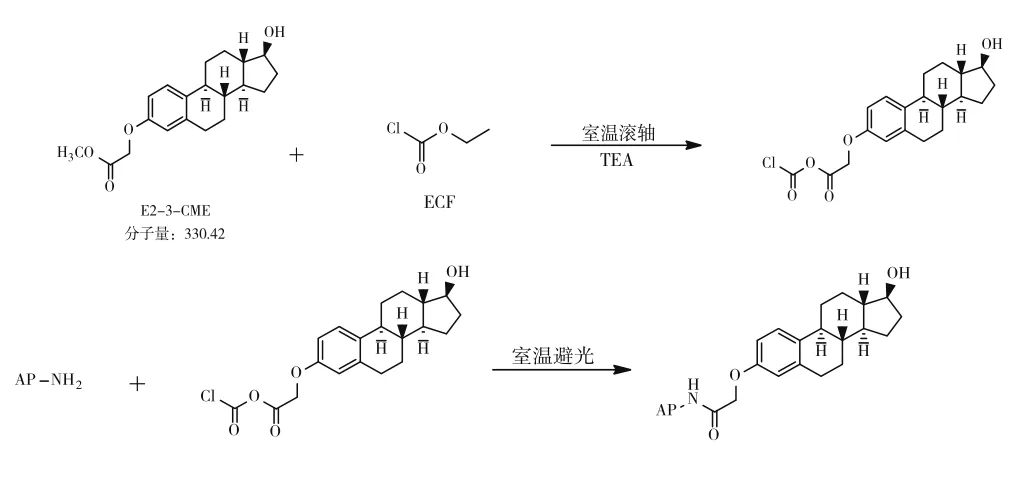
图1 混合酸酐法反应原理
1.2 碳二亚胺法(不加NHS)
碳二亚胺法(不加NHS)是利用碳二亚胺试剂EDC活化E2-3-CME的羧基端,再与碱性磷酸酶上的游离氨基反应生成酶结合产物[4-5],反应过程如图2所示。

图2 碳二亚胺法(不加NHS)反应原理
1.3 碳二亚胺法(加NHS)
碳二亚胺法(加NHS)是利用碳二亚胺试剂EDC活化E2-3-CME的羧基端,然后加入NHS加速活化效率,再与碱性磷酸酶上的游离氨基反应生成酶结合产物。反应过程如图3所示。
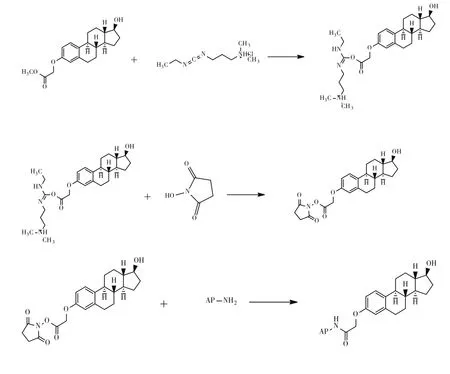
图3 碳二亚胺法(加NHS)反应原理
2 材料与方法
2.1 材料与试剂
氯甲酸乙酯(ECF),纯度≥96%,国药集团;三乙基胺(TEA),纯度≥99%,Sigma;无水二氧六环(DIO),纯度≥99%,Sigma;Estradiol 3-CME(E2-3-CME),纯度≥99%,Fitzgerald;碱性磷酸酶(少糖基)(AP),纯度≥95%,Roche;1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC),纯度≥99%,Sigma;二环己基碳二亚胺(DCC),纯度≥99%,Sigma;N-羟基琥珀酰亚胺(NHS),纯度≥99%,赛默飞;二甲基甲酰胺(DMF),纯度≥99.8%,Sigma;氯化钠,纯度≥99%,太仓美达试剂;磷酸氢二钠,纯度≥99%,太仓美达试剂;磷酸二氢钠,纯度≥99%,太仓美达试剂;硼酸钠,纯度≥99%,国药集团;三(羟甲基)氨基甲烷(Tris),纯度≥99%,Amresco。
2.2 仪器与设备
SRT-202滚轴,海门其林贝尔仪器制造有限公司;GL-88B旋涡混合器,海门其林贝尔仪器制造有限公司;Finnptpette移液器,赛默飞;BioLogic LP纯化仪,BIO-RAD;G25脱盐柱,GE Healthcare;卓越C1800化学发光仪,上海科华生物工程股份有限公司。
2.3 实验设计
2.3.1 混合酸酐法制备酶结合物
2.3.1.1 制备流程
(1)称取E2-3-CME 3 mg,用DIO 50 μL溶解,配制成60 mg/mL的样品溶液。(2)量取138 μL TEA,加入872 μL DIO,混合均匀,配制成1 mol/L的溶液。(3)量取87 μL ECF,加入872 μL DIO,混合均匀,配制成1 mol/L的溶液。(4)活化。从(1)中取出50 μL,再从(2)和(3)中各取出10 μL加入其中。(5)室温滚轴反应30 min。(6)偶联。取AP脱盐至硼酸缓冲液(pH=9.0)中,按照E2∶AP =10∶1(摩尔比)加入活化E2,室温避光反应2 h。(7)将偶联物脱盐至Tris缓冲液(pH=7.4)中,加入等体积甘油-20 ℃保存。
2.3.1.2 在37 ℃的稳定性实验
配制E2-AP稀释液至0.5 μg/mL,取一半于37 ℃放置7 d,另一半于4 ℃放置。配制校准品浓度为0 pg/mL、50 pg/mL、250 pg/mL、500 pg/mL、1 000 pg/mL和4 500 pg/mL,依次编号为S1~S6,抗雌二醇单抗-磁微粒包被稀释液至0.5 mg/mL。按照顺序放置试剂及样品至全自动化学发光仪中检测实验数据。
2.3.1.3 与罗氏对比相关性实验
配制E2-AP稀释液至0.5 μg/mL,取一半于37 ℃放置7 d,另一半4 ℃放置。配制48个样品液及抗雌二醇单抗-磁微粒包被稀释液至0.5 mg/mL。按照顺序放置试剂及样品至全自动化学发光仪中检测实验数据。
2.3.2 碳二亚胺法制备酶结合物
2.3.2.1 制备流程
(1)称取E2-3-CME 2 mg,用DMF 200 μL溶解,配制成10 mg/mL的样品溶液。(2)称取EDC 10 mg,用DMF 0.5 mL溶解,配制成20 mg/mL。(3)活化。向样品溶液中加入EDC溶液58 μL,反应摩尔比为1∶1。(4)室温滚轴反应30 min。(5)催化。再向E2活化液中加入16 μL的NHS溶液(10 mg/mL),使之反应终浓度为5 mmol/L。碳二亚胺法(不加NHS)处理没有此步骤。(6)室温滚轴再反应30 min。(7)偶联。取AP脱盐至磷酸缓冲液(pH=7.4)中,按照E2∶AP =10∶1(摩尔比)加入活化E2,室温避光反应2 h。(8)将偶联物脱盐至pH=7.4的Tris缓冲液中,加入等体积甘油于-20 ℃保存。
2.3.2.2 灵敏度实验
配制加NHS与不加NHS的E2-AP稀释液至0.5 μg/mL。配制校准品浓度为0 pg/mL、50 pg/mL、250 pg/mL、500 pg/mL、1 000 pg/mL 和 4 500 pg/mL,抗雌二醇单抗-磁微粒包被稀释液至0.5 mg/mL。按照顺序放置试剂及样品至全自动化学发光仪中检测实验数据。
2.3.2.3 稳定性实验
配制E2-AP(加NHS)稀释液至0.5 μg/mL,取一半于37 ℃放置7 d,另一半于4℃放置。配制校准品浓度为0 pg/mL、50 pg/mL、250 pg/mL、500 pg/mL、1 000 pg/mL和4 500 pg/mL,抗雌二醇单抗-磁微粒包被稀释液至0.5 mg/mL。按照顺序放置试剂及样品至全自动化学发光仪中检测实验数据。
2.3.2.4 相关性实验
配制E2-AP(加NHS与不加NHS)稀释液各至0.5 μg/mL。配制48个样品液及抗雌二醇单抗-磁微粒包被稀释液至0.5 mg/mL。按照顺序放置试剂及样品至全自动化学发光仪中检测实验数据。
3 结果与分析
3.1 混合酸酐法制备酶结合物在37 ℃的稳定性实验
从表1可以看出,运用混合酸酐法制备的酶结合物在37 ℃时,稳定性快速下降,7 d后只有原来发光值的50%以下。这可能是因为混合酸酐的反应不仅会使3位上的羧基形成酸酐,还会使17位的羟基形成酸酐,或者酯化反应等产生的副产物与AP也能形成偶联物,但成酯后的偶联物稳定性较差,容易水解导致偶联物断裂失活。
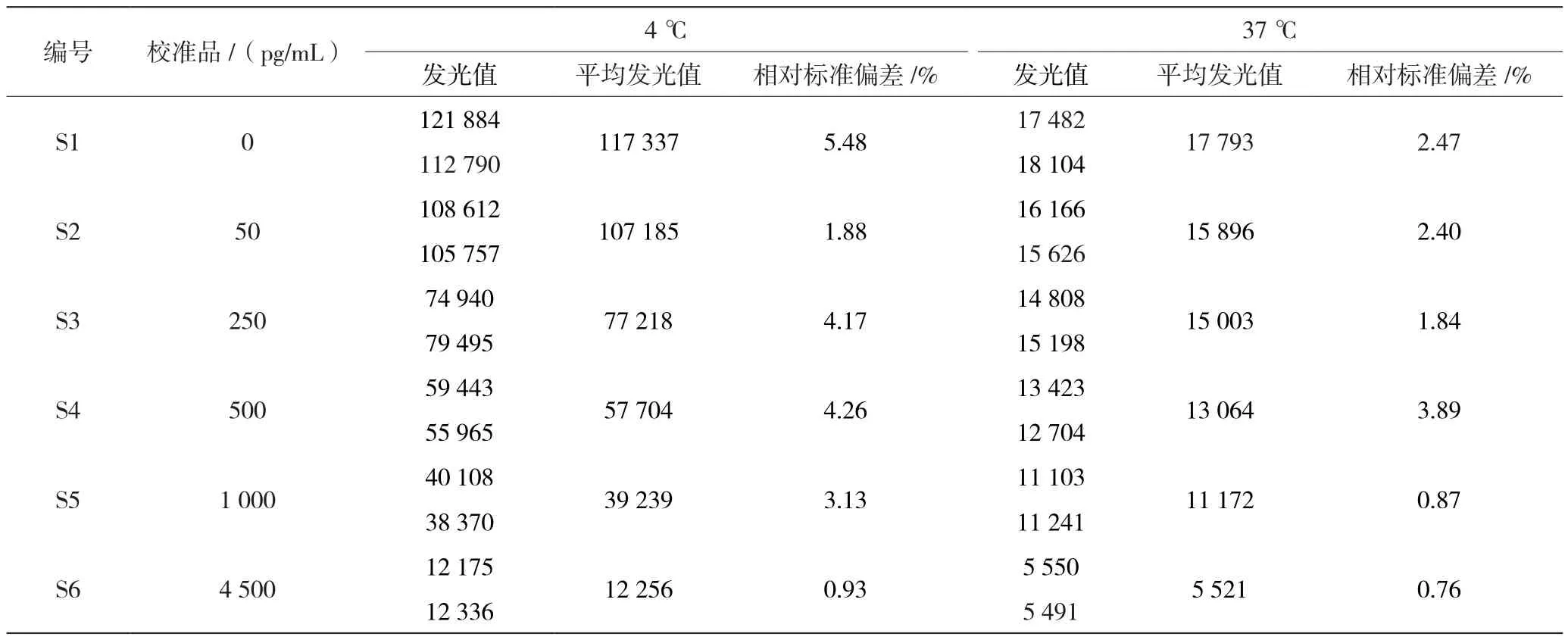
表1 不同温度下E2-AP(0.5 μg/mL)发光值对比
3.2 混合酸酐法制备的酶结合物与罗氏对比相关性实验
以48组罗氏测值浓度的样本所测得酶结合物在4 ℃与37 ℃的发光值见表2,图4、图5、图6、图7分别为表2中4 ℃下罗氏样本浓度、罗氏样本浓度归类的组别与发光值的相关性散点图和37 ℃下罗氏样本浓度、罗氏样本浓度归类的组别与发光值的相关性散点图。从图4和图6可以看到,不论是4 ℃还是37 ℃,图中的点较为零散,说明此法得出的结果波动大,与罗氏的相关性相差较大。从图5和图7中可以看到,不同组别中的发光值有交叉,由于理论上在低浓度组别中的发光值较高,而高浓度组别中发光值应该依次递减,不应该看到不同组别的发光值有大量交叉的情况,所以此法的相关性较差。
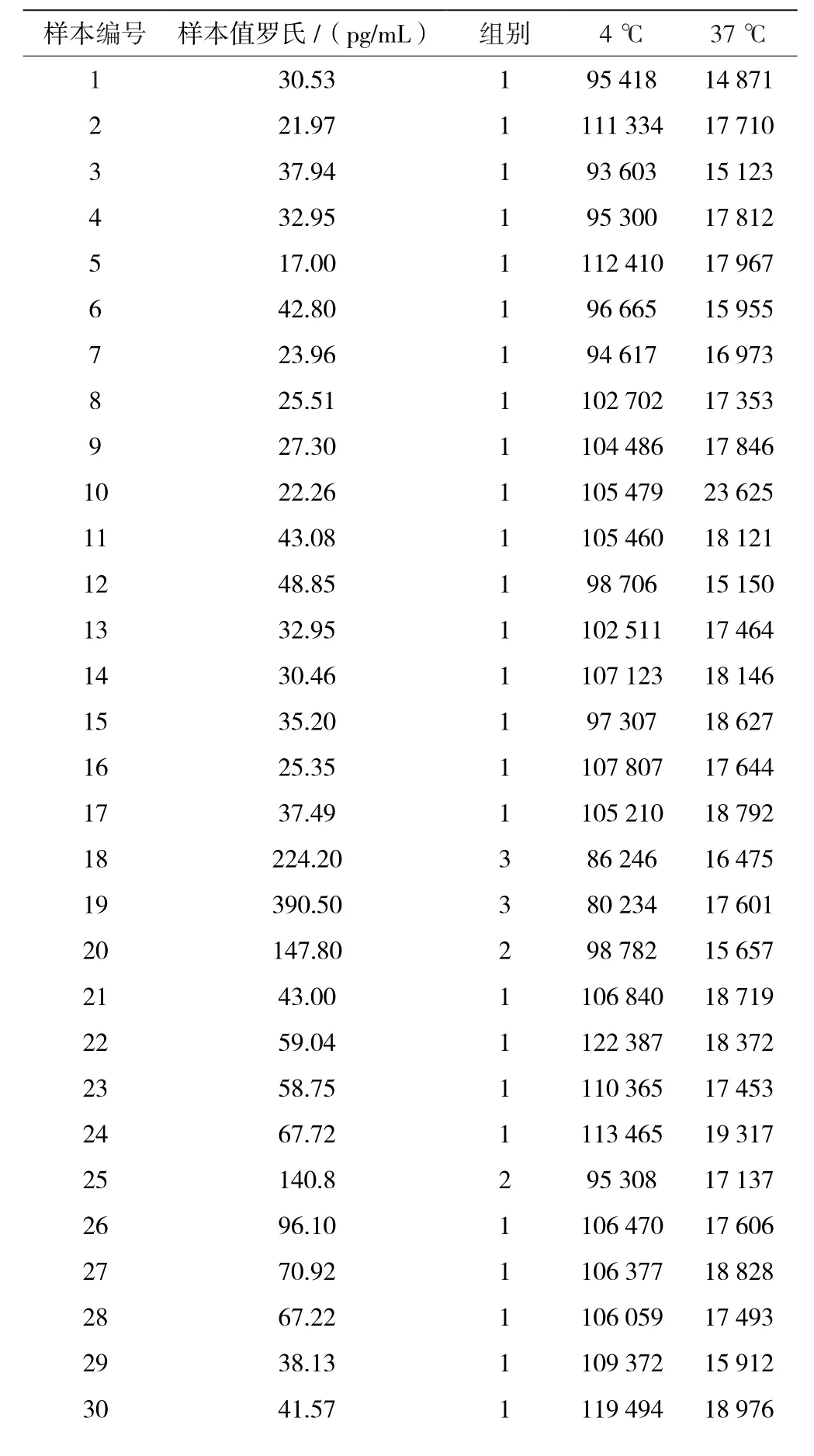
表2 以48组罗氏测值浓度的样本所测得酶结合物在4 ℃与37 ℃的发光值
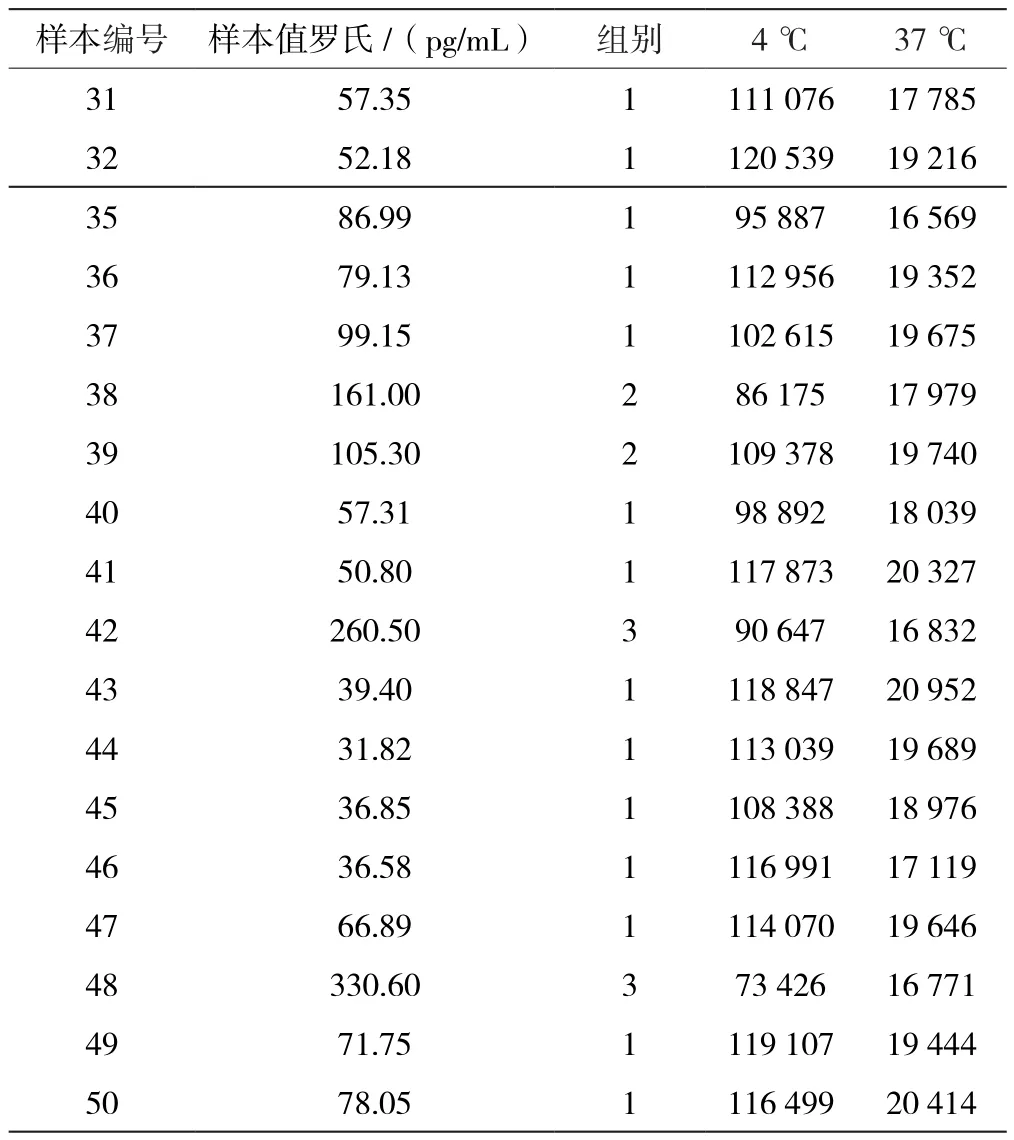
续表2

图4 4 ℃下表2中罗氏样本浓度与发光值相关性散点图

图5 4 ℃下表2中罗氏样本组别与发光值相关性散点图
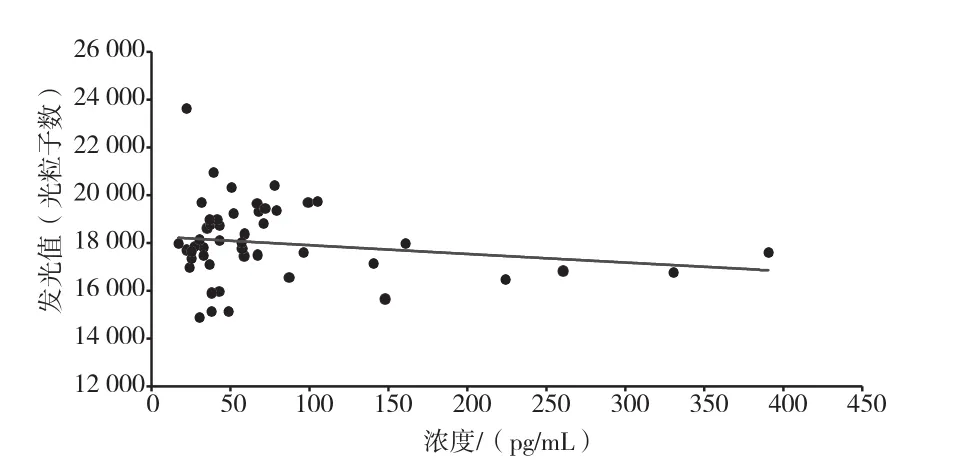
图6 37 ℃下表2中罗氏样本浓度与发光值相关性散点图
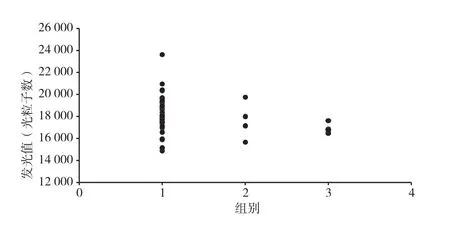
图7 37 ℃下表2中罗氏样本组别与发光值相关性散点图
3.3 碳二亚胺法制备酶结合物的灵敏度实验
从表3可以看到,使用碳二亚胺法制备E2-AP的活化过程中加NHS催化的偶联效率是不加NHS的20倍,并且也高出使用混合酸酐法偶联物活性的2倍以上。
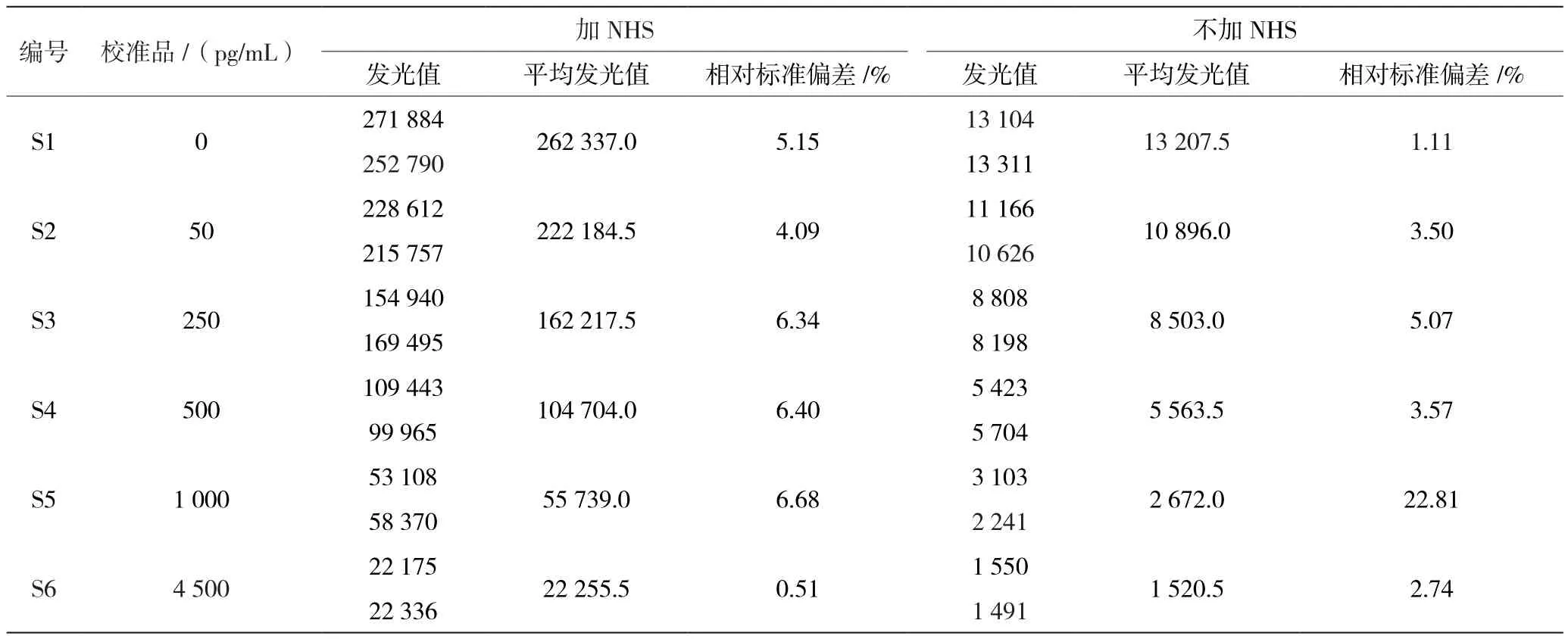
表3 酶结合物相同工作浓度下加NHS催化与不加NHS的发光值梯度对比
3.4 碳二亚胺法制备酶结合物的稳定性实验
从表4可以看到,碳二亚胺法偶联的E2-AP相对较稳定,37 ℃下加速破坏实验后的活性灵敏度只下降了不到15%。碳二亚胺法反应的专一性较强,一般只发生羧基与氨基的酰胺反应,不需要产生酸酐作为中间体。而Estradiol 3-CME的羧基只有在3号位有,所以产物的一致性较高。
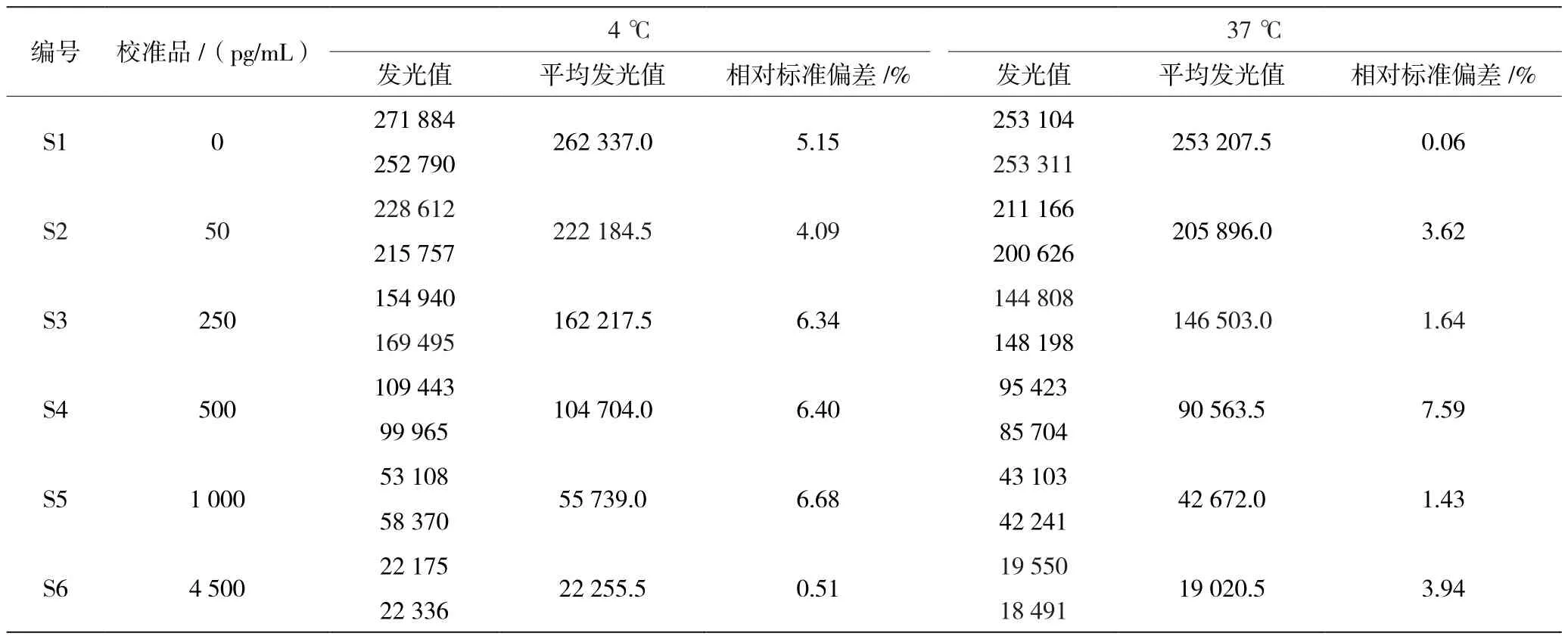
表4 酶结合物相同工作浓度下NHS催化的E2-AP在37 ℃加速破坏试验中稳定性情况
3.5 碳二亚胺法制备酶结合物的相关性实验
以罗氏测值浓度的样本所测得加NHS与不加NHS的发光值见表5,图8、图9、图10及图11分别为表5中加NHS下罗氏样本浓度、罗氏样本浓度归类的组别与发光值的相关性散点图和不加NHS下罗氏样本浓度、罗氏样本浓度归类的组别与发光值的相关性散点图。
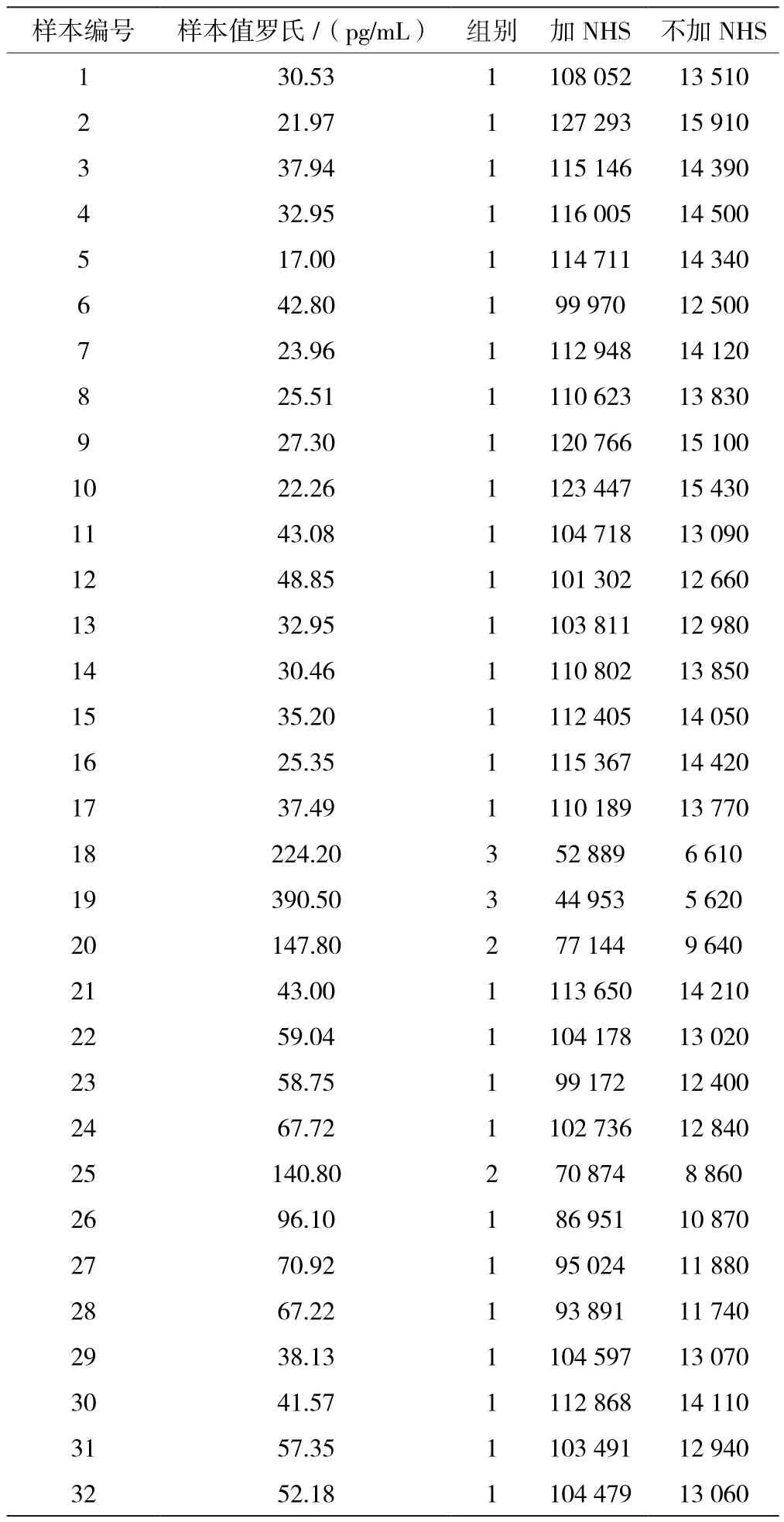
表5 以罗氏测值浓度的样本所测得加NHS与不加NHS的发光值
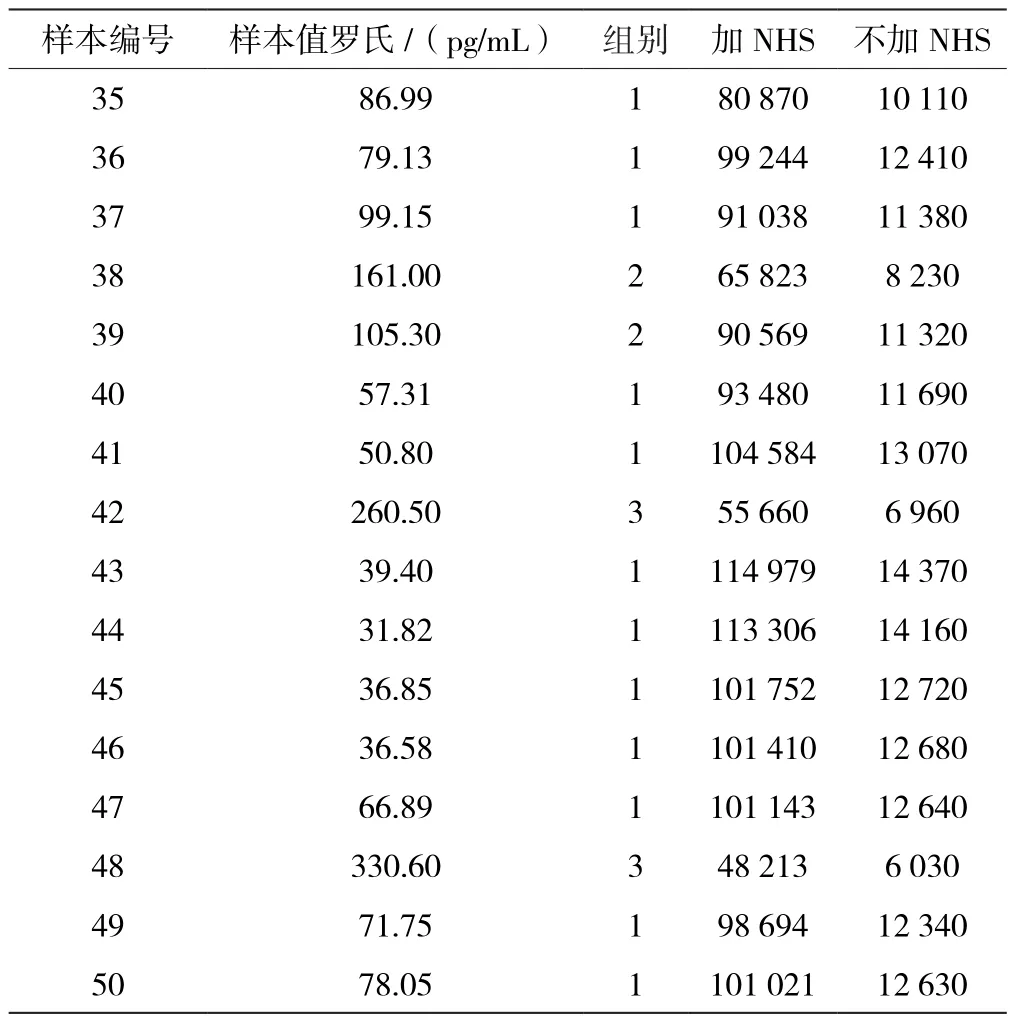
续表5
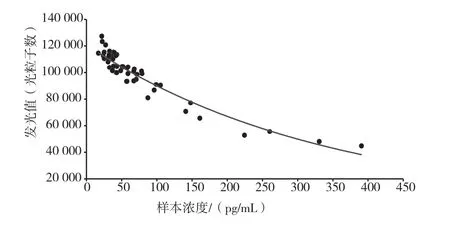
图8 加NHS下表5中罗氏样本浓度与发光值相关性散点图
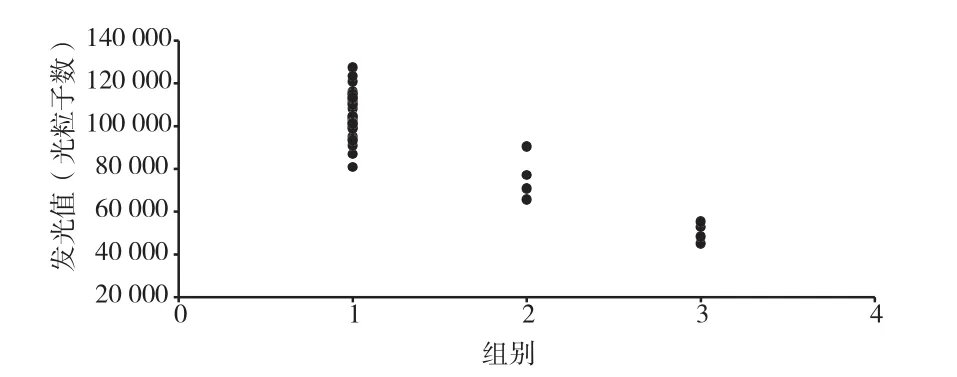
图9 加NHS下表5中罗氏样本组别与发光值相关性散点图
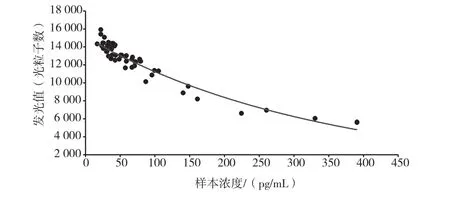
图10 不加NHS下罗氏样本浓度与发光值相关性散点图
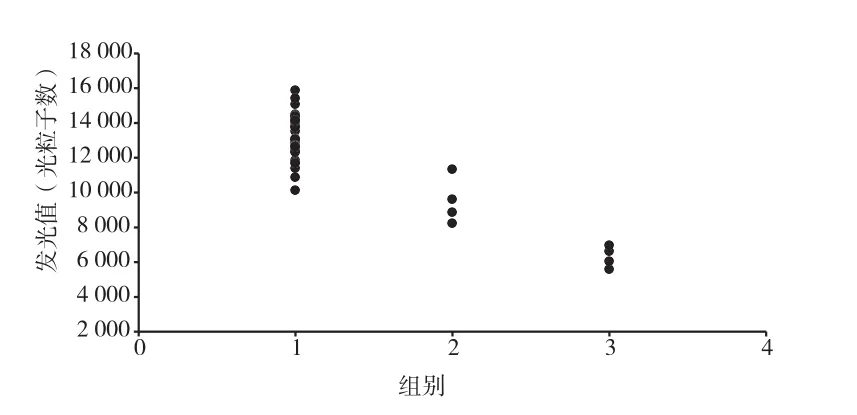
图11 不加NHS下表5中罗氏样本组别与发光值相关性散点图
从图8和图10散点图中可以看到,不论是加NHS或者不加,图中的点都较为密集,说明此法得出的结果波动小,与罗氏的一致性较高。图9和图11中一样可以看到,不同组别中的散点的发光值交叉少,基本能够分段,说明与罗氏的一致性较高。使用碳二亚胺法来偶联雌二醇与碱性磷酸酶(不论是否使用NHS来催化反应)实验结果与罗氏的相关性都非常高,并且比混合酸酐法好很多。
4 结论
雌二醇衍生物Estradiol 3-CME与碱性磷酸酶AP的偶联反应实质上就是羧基与氨基反应形成肽键。本文中只探讨了碳二亚胺类试剂EDC,诸如碳二亚胺中DCC、DIC等其他试剂及多肽合成中常用的试剂HBTO、HOBT等未进行详细探讨。此外,本文中偶联实验均采用E2∶AP=10∶1(摩尔比)偶联,还可以尝试选择其他偶联比、缓冲液体系或雌二醇溶剂等反应条件优化反应产物。
使用混合酸酐法偶联雌二醇与碱性磷酸酶所得的酶结合产物副产物较多,稳定性较差,化学发光法检测得到的相关性也不太理想,最关键的是其制备过程中使用的氯甲酸乙酯等氯甲酸酯类化合物都带有剧毒,对实验人员人身安全十分不利。根据本文实验结果可以看出,使用碳二亚胺试剂EDC,再加入微量的NHS作为催化剂不仅可以大幅提高检测灵敏度,还可以有效增强酶结合物的稳定性、大幅改善相关性。并且,实验过程中涉及的反应试剂毒性相对较低,实验人员人身安全可以得到保障,因此碳二亚胺法可以替代混合酸酐法。
