TACE联合超声引导下微波消融治疗特殊部位原发性肝癌患者疗效研究*
2022-05-16薛红红
邱 云,杨 玫,薛红红
据统计,原发性肝癌(PLC)在我国恶性肿瘤发病谱中居第4位,位列恶性肿瘤死因的第2位。尽管近年来治疗领域取得了一定的进展,但PLC患者5 a总体生存率仅为12.1%[1,2]。虽然越来越多的研究证实了符合经导管肝动脉化疗栓塞术(transcatheter arterial chemoembolization,TACE)治疗指征的PLC患者生存获益显著,但仍有肿瘤细胞残留情况,也是肿瘤复发和转移的重要原因[3,4]。文献报道,在超声引导下微波消融(microwave ablation,MWA)联合TACE治疗非特殊部位肝癌患者疗效肯定,但关于这种联合治疗邻近(最短距离小于0.5 cm)膈顶、胆囊、胃肠道、大血管、肾脏、心脏等重要组织器官等特殊部位的肝癌患者的近远期疗效,仍缺乏高质量的研究证实[5]。本研究采取TACE联合超声引导下MWA治疗特殊部位的PLC患者,观察了疗效及血清甲胎蛋白(alpha-fetoprotein,AFP)、甲胎蛋白异质体L3(alpha-fetoprotein heterogeneity L3,AFP-L3)、血管内皮生长因子(vascular endothelial growth factor,VEGF)和S100钙结合蛋白A4(S100 calcium-binding protein A4,S100A4)水平变化,现报道如下。
1 资料与方法
1.1 一般资料 2017年11月~2019年11月我院收治的特殊部位PLC患者72例,男56例,女16例;年龄为32~78岁,平均年龄为(56.0±10.6)岁。诊断参照《原发性肝癌诊疗规范(2017年版)》的标准[6],经血清肿瘤标志物、影像学或穿刺活检细胞学或组织病理学检查诊断,病灶邻近重要组织器官且最短距离小于0.5 cm,其中病灶邻近膈顶14例,胆囊18例,胃肠道11例,门静脉7例,肝静脉3例,下腔静脉3例,右肾8例,心脏8例。入选对象单个肿瘤病灶最大径不超过5 cm,多发肿瘤肝内病灶不超过3个,且最大径不超过3 cm(至少一个病灶位于特殊部位),Child-Pugh A级48例,B级24例;巴塞罗那分期A期58例,B期14例;骨髓、肺、脑、肾、心脏和凝血功能正常,存在合适的经皮穿刺通路,预计生存期超过3个月。排除标准:严重的肝肾肺脑功能不全或存在血液系统疾病或认知障碍、远处脏器转移或其它部位原发肿瘤、腹水、黄疸或门脉癌栓,存在上消化道出血、Child-Pugh C级等终末期疾病,入组前已行MWA、放化疗等治疗。将特殊部位肝癌患者作为观察组,另选择同期收治的普通部位PLC患者60例作为对照组,两组一般资料和病情比较,无统计学差异(P>0.05)。患者及其家属签署知情同意书,本研究获得我院医学伦理委员会批准。
1.2 TACE治疗 使用美国通用公司提供的数字减影设备,穿刺右侧股动脉,以改良Seldinger技术穿刺插管,置入动脉鞘、导管和导丝,进入腹腔干、肝动脉或肠系膜上动脉、膈动脉,造影,了解肿瘤位置、大小、数量和供血等情况。将微导管超选择插入肿瘤供血动脉,将吡柔比星(国药准字H20045982,浙江海正药业)20 mg/m2、奥沙利铂(国药准字H20123183,南京臣功制药)50 mg/m2和碘化油(国药准字H31021603,上海旭东海普药业)5~10 mL混合成乳剂,经导管注入,并用明胶海绵颗粒(粒径150~350 μm,杭州艾力康医药科技)作进一步补充栓塞,直至血流被完全中断、供血动脉被完全栓塞为止。
1.3 超声引导下MWA治疗 在TACE治疗后1 w,行腹部CT或MRI复查,观察肝内碘油沉积情况,并了解特殊部位肝癌病灶最大径及其与重要组织器官的最短距离,制定消融计划。使用超声扫描仪和宝兴WB-3100A Ⅲ型微波治疗仪。患者仰卧位,局部麻醉。根据肿瘤位置,于超声引导下选择适宜的进针路线,并参考肿瘤直径、邻近血管和脏器情况明确消融方式、功率和时间等参数。对于普通部位肿瘤,消融功率选择在60~80 w,消融时间维持5~15 min,确保肿瘤及其周围0.5~1.0 cm肝组织被完全消融;对于特殊部位的肿瘤,保持消融功率在40~50 w,消融时间维持5~8 min,尽量保证肿瘤及其边缘被完全消融。完成消融后20 min,行超声造影。对残留肿瘤,追加消融。
1.4 疗效判定标准 治疗后1 m,行影像学检查。参考实体瘤治疗应答评价标准[7]评估疗效。目标病灶无动脉期增强表现视为完全缓解;目标病灶直径减少不低于30%视为部分缓解;病灶增大未达疾病进展或缩小未达到部分缓解视为疾病稳定;目标病灶直径增加大于20%或有新病灶发现视为疾病进展。疾病控制率=完全缓解、部分缓解和疾病稳定病例数之和/总病例数×100%
1.5 血清指标检测 采用化学发光法检测AFP(北京科卫临床诊断试剂有限公司);采用ELISA法检测血清AFP-L3、VEGF和S100A4(上海邦景实业有限公司)。

2 结果
2.1 两组临床疗效比较 在治疗后1 m末,观察组疾病控制率与对照组比,无统计学差异(P>0.05,表1、图1)。

表1 两组临床疗效[n(%)]比较

图1 特殊部位PLC患者超声造影表现A~C:57岁男性。治疗前,超声造影检查见肝内造影剂充填弥漫性不均匀,符合肝硬化表现。右后叶近膈顶和第二肝门处一结节大小为3.4 cm×3.0 cm,数处结节呈“快进快退”现象;D~F:同一患者治疗后,超声造影见肝内低回声区,消融区域数处结节无造影剂填充,右后叶近膈顶和第二肝门处见3.9 cm×3.3 cm结节,边界欠清,形态不规则,内部回声不均匀
2.2 两组血清指标比较 在治疗后1 m末,两组血清AFP、AFP-L3、VEGF和S100A4水平比较,无统计学差异(P>0.05,表2)。
2.3 两组不良反应发生率比较 在治疗后,两组不良反应发生率比较,无统计学差异(P>0.05)。

表2 两组血清指标比较
2.4 两组生存率比较 随访24 m,两组累积生存率比较,无统计学差异(不同时间比较,Log-rankx2=2.535、x2=0.176、x2=0.018、x2=0.078,P=0.111、P=0.675、P=0.892、P=0.780,表3、图2)。

表3 两组生存率[n(%)]比较
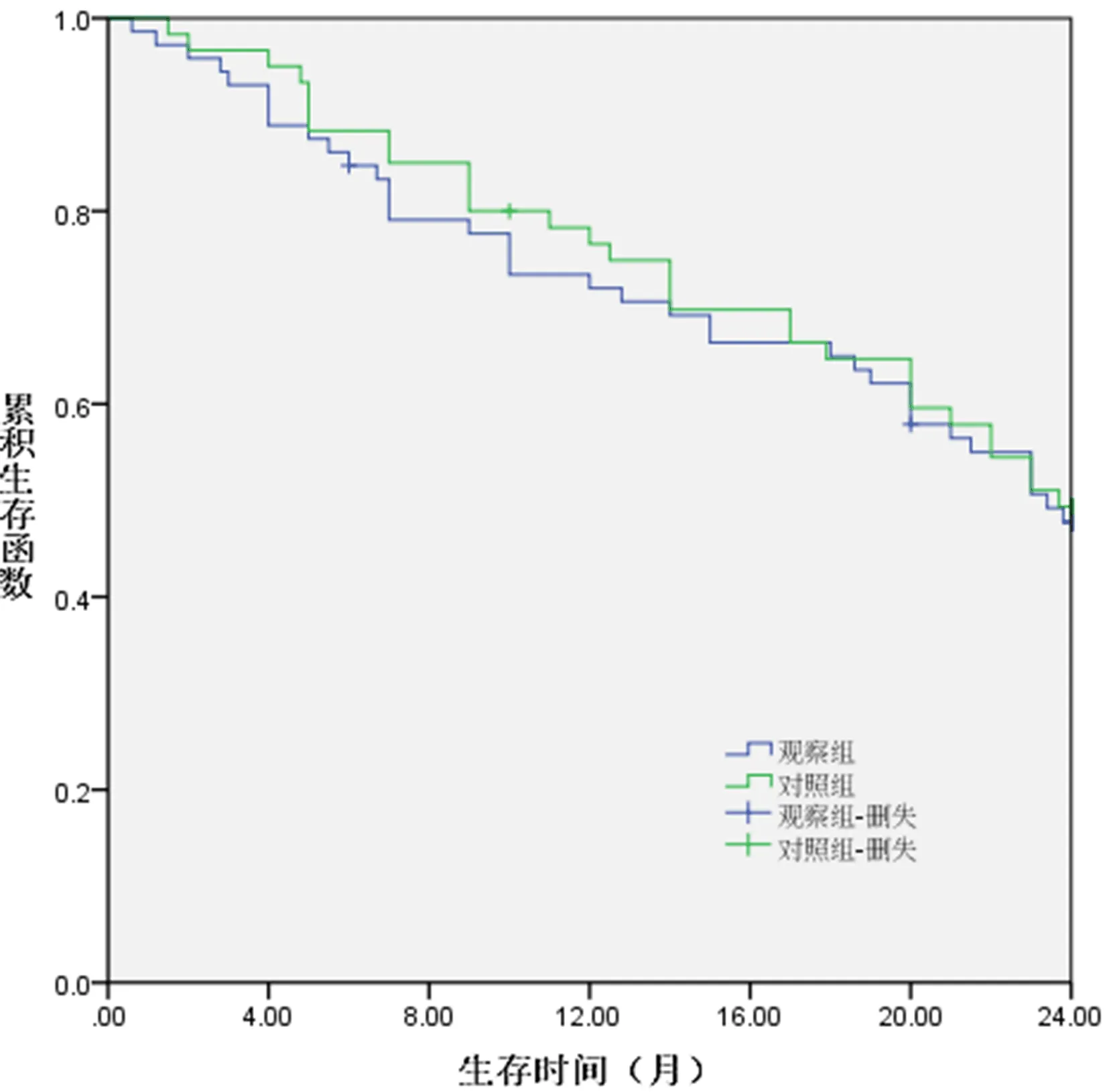
图2 两组Kaplan-Meier生存曲线
3 讨论
据流行病学统计,约23.4%~34.7%肝癌病灶位于特殊部位。尽管单纯TACE治疗能取得一定的效果,但肿瘤病灶完全坏死率偏低,局部复发风险高,不良反应和肝功能损伤也较为严重[8-10]。越来越多的研究表明,超声引导下微波消融治疗特殊部位的肝癌疗效接近手术切除,但也存在肿瘤细胞残留的问题[11,12]。目前,关于TACE术后联合超声引导下MWA治疗特殊部位肝癌的国内外文献报道较少,故本研究对此进行了初步观察。
本研究中,在治疗后1 m末两组疾病控制率并无显著性差异,与既往报道[13]相似。在TACE术后联合超声引导下MWA治疗具有协同效应,首先,肝癌动脉血供被TACE阻断后在很大程度上能提高MWA治疗的热沉降效应,扩大消融范围。其次,病灶血供被TACE阻断后肿瘤体积明显缩小,肿瘤部分坏死或缺血,为微波消融提供了治疗便利,促使肿瘤组织被彻底消融;再者,TACE治疗后病灶呈缺氧、缺血、水肿状态,可提高后续治疗肿瘤细胞对热的敏感性,即便相对较低的温度亦可将肿瘤细胞杀死。微波消融可降低TACE治疗次数,更好地保护肝功能。
本研究中,在治疗后两组血清AFP、AFP-L3、VEGF和S100A4水平降低,但两组并无显著性差异,提示TACE治疗后进行微波消融治疗常见部位肝癌和特殊部位肝癌血清肿瘤标志物均明显降低。肝癌患者血清AFP和AFP-L3水平升高,能有效反映肝脏肿瘤负荷,在肝细胞癌分期和预后评估方面意义重大[14,15]。VEGF属于血管生长相关肽,可结合血管内皮细胞生长因子受体2作用于血管内皮细胞,调控细胞增殖、迁移和新生血管的形成,参与肿瘤发生及细胞迁移过程[16]。S100A4参与肝癌的发生和发展,调控肝癌细胞转移、侵入和瘤区血管生成,在肝癌预后评估方面尤为重要[17,18]。
研究表明,TACE联合超声引导下MWA治疗特殊部位的肝癌患者,其安全性与治疗常见部位肝癌相近[19]。本研究两组2 a累积生存率并无显著性差异,与既往报道[20]相似。
