药物性肝损伤外周血清免疫学特点的初步探析
2022-05-14沈晓萍陶艳艳刘成海
王 宇, 罗 琼, 李 书, 沈晓萍, 李 爽, 陶艳艳, 刘成海,3
1 上海市宝山中西医结合医院 消化科, 上海 201999; 2 上海中医药大学附属曙光医院 a.肝病二科,b.肝病研究所, 上海 201203; 3 上海中医健康服务协同创新中心, 上海 201203
药物性肝损伤(DILI)是指由各类处方或非处方的化学药物、生物制剂、传统中药、天然药、保健品、膳食补充剂[1]及其代谢产物乃至辅料等所诱发的肝损伤,其是最常见和最严重的药物不良反应之一,重者可致急性肝衰竭(ALF)甚至死亡[2]。DILI的发病机制目前分为固有型和特异质型,其中特异质型主要取决于宿主的遗传、免疫和代谢因素。目前关于DILI中涉及的细胞和分子机制报道甚少。DILI免疫机制中,损伤相关分子模式刺激免疫反应,炎性体在其中发挥的关键作用,特定人类白细胞抗原分子上的新抗原递呈触发适应性免疫反应,以及氧化剂和抗氧化剂防御系统之间的失衡均参与了肝损伤发生[3]。本文回顾性分析DILI患者病例资料,就其临床特征、生化以及免疫学特点进行分析,为以后阐明DILI发生的确切机制及临床诊断提供参考。
1 资料与方法
1.1 研究对象 选取2019年1月—2021年8月于曙光医院及宝山分院出院诊断为“药物性肝损伤”“药物性肝炎”的患者。依据病史、患者预后情况、2015版《药物性肝损伤诊治指南》[2]和2021版亚太肝病学会DILI共识指南[4]中DILI诊断标准再次评估,确认存在肝损伤,其次排除其他肝病,再通过因果关系评估来确定肝损伤与可疑药物的相关程度即RUCAM量表,极可能:>8分;很可能:6~8分;可能:3~5分;不太可能:1~2分;可排除:≤0分。收集DILI患者病历资料,包括人口学数据、临床特征、生化以及免疫学指标。从肝功能正常(无肿瘤性疾病、无自身免疫性疾病、无脂肪肝、无感染性疾病、外周血清学检验正常)且做过细胞因子及细胞免疫的胃肠镜全身健康体检者中选取29例作为肝功能正常组,从DILI病例中复核确认42例急性起病治疗前1周内做过细胞因子及细胞免疫评价的作为DILI对照组。

2 结果
2.1 DILI患者的基本特征 共纳入219例DILI患者,其中女122例,男97例。由传统中药、天然药、保健品、膳食补充剂导致损伤89例,由非甾体类抗炎药、抗肿瘤药物等西药导致损伤130例。临床分型肝细胞损伤型82例,胆汁淤积型17例,混合损伤型120例。发病与首次用药间隔时间最长为180 d,最短为1 d,中位数为15 d,其中传统中药、保健品等潜伏期20.50(7.75~30.00)d,非甾体类抗炎药等西药潜伏期为14(7~30)d。
2.2 DILI患者的临床症状分布 纳入病例按照中草药、中成药制剂或保健品和西药类两组分类,症状比例分布:乏力108(41∶67)例,纳差59(24∶35)例,恶心35(19∶16)例,小便色黄者31(14∶17)例,腹胀22(15∶7)例,腹痛16(2∶14)例,皮肤瘙痒或皮疹8(2∶6)例,胁痛4(0∶4)例。大部分患者伴有两种或两种以上的症状(表1)。
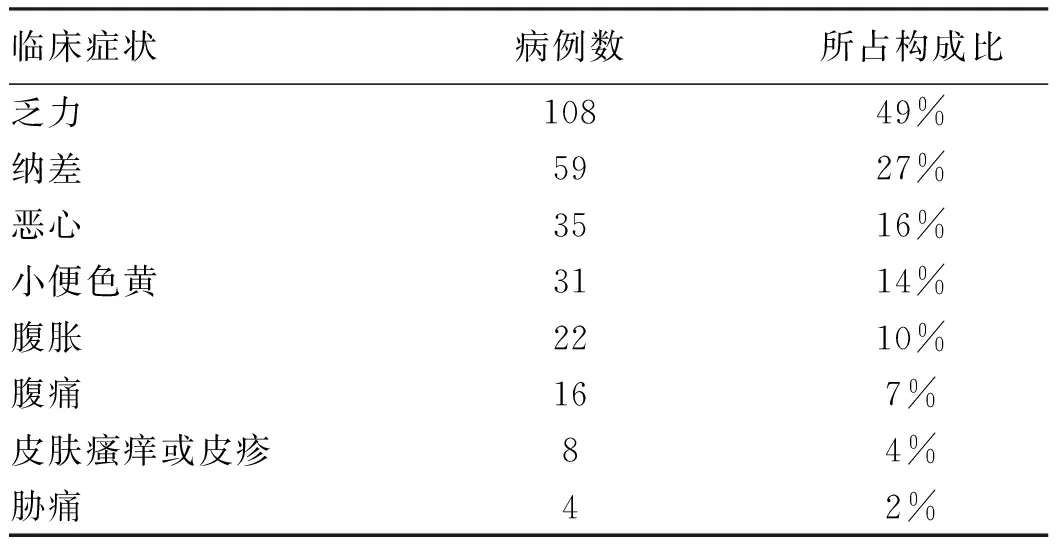
表1 所有DILI患者临床症状分布
2.3 中草药、中成药制剂或保健品和西药两组的外周血指标差异及损伤程度比较 两组间在急性起病1周内的生化以及免疫学指标分析结果显示:细胞毒性T淋巴细胞(%)和CD4/CD8比值比较差异均具有统计学意义(P值分别为0.011、0.002)(表2)。两组在肝损伤程度分级上的分布特征比较,差异无统计学意义(P=0.13)(表3)。
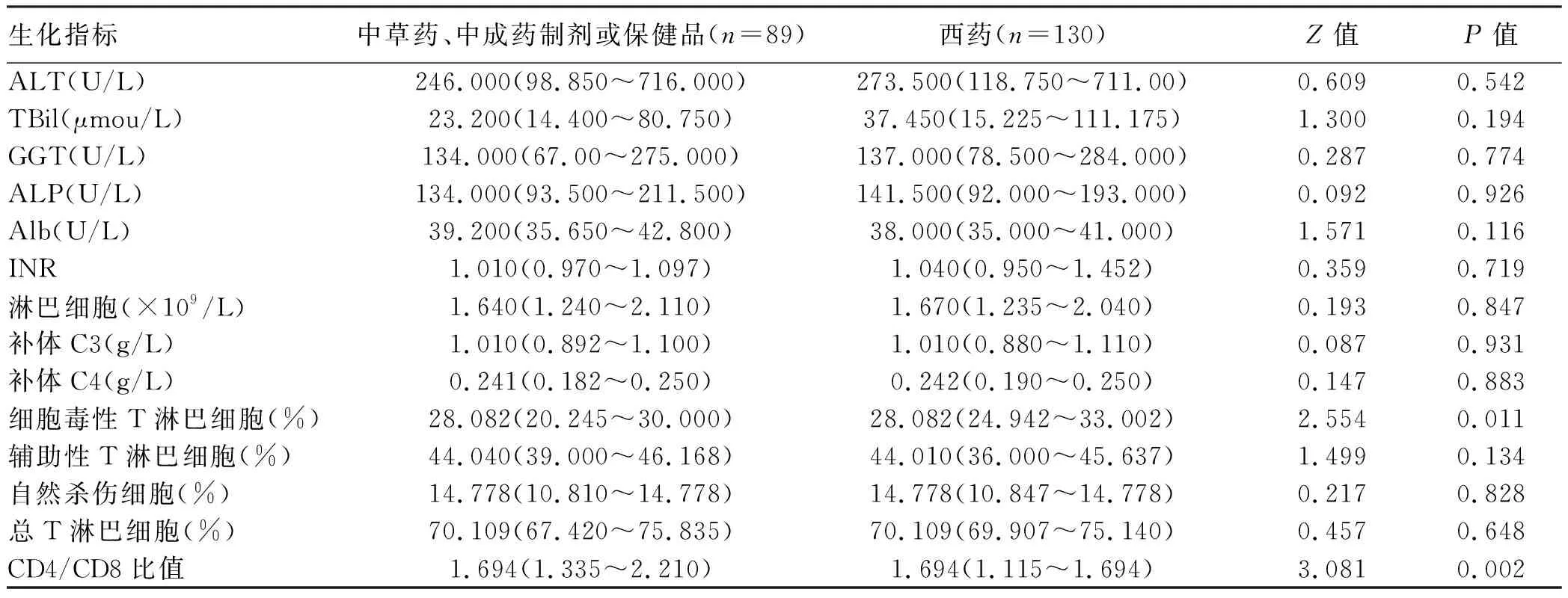
表2 中草药、中成药制剂或保健品和西药两组的外周血指标比较
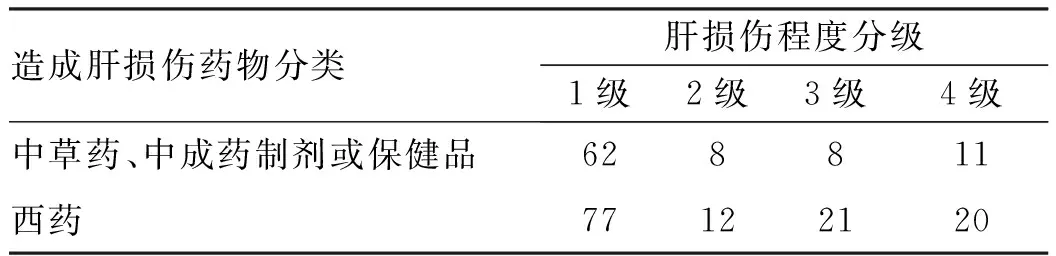
表3 中草药、中成药制剂或保健品和西药DILI患者肝损伤程度分级
2.4 肝功能正常组与DILI对照组之间的外周血指标细胞免疫及细胞因子的差异比较 结果显示IL-6、IL-10在组间差异均具有统计学意义(Z值分别为3.828、2.695,P值分别为<0.001、0.007)。TNFα、自然杀伤细胞(%)、细胞毒性T淋巴细胞(%)、辅助性T淋巴细胞(%)、总T淋巴细胞(%)、CD4/CD8比值,两组间差异均无统计学意义(P值均>0.05)(表4)。
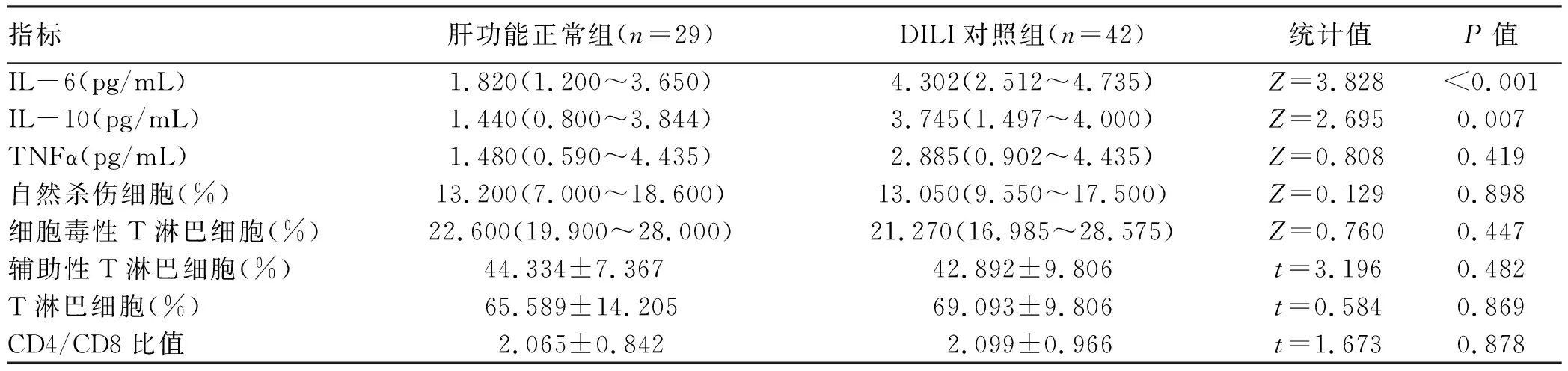
表4 肝功能正常组与DILI组的细胞免疫及细胞因子比较
3 讨论
在DILI发病人群特征中,女性通常被认为是发生DILI的危险因素[5]。中国DILI的年发生率为23.80/10万;其中半数以上DILI患者为肝细胞损伤型,28.3%为混合型,20.31%为胆汁淤积型;引起DILI的药物中,中草药和膳食补充剂占比26.81%[6]。本研究中由中药或者中成药导致损伤89例,由抗结核、抗肿瘤等西药导致损伤130例。其中临床分型肝细胞损伤型82例,胆汁淤积型17例,混合损伤型120例。DILI潜伏期差异很大,可短至数日,长达数月。本研究观察到DILI发病与首次用药间隔时间最长为180 d,最短为1 d,中位天数为15 d。DILI患者多数无明显症状,仅表现为血清ALT、AST及ALP、GGT等肝生化指标不同程度的升高,经统计,乏力症状在本次研究中占比较高。
DILI的细胞死亡模式取决于损伤药物,它也在很大程度上决定了损伤的机制和DILI严重程度[7]。相关特异性T淋巴细胞的激活取决于可溶性药物的直接激活以及相关的半抗原机制反应。但是,本研究未发现外周免疫血清学在DILI的3种典型损伤模式(肝细胞损伤型、胆汁淤积型和混合型)中具有差异,可能与胆汁淤积型样本量偏少有关,也可能由于外周免疫检测指标未能直接反映DILI发生过程中早期肝组织学内部的免疫微环境特点。
DILI的发病机制仍然分为药物及其代谢产物的直接肝毒性和特异质性肝毒性两大类,亦有学者将其概括为药物及其代谢产物所致的上游事件以及肝脏靶细胞损伤通路和保护通路失衡构成的下游事件,目前观点倾向于认为适应性免疫攻击是最后的共同事件[8]。在适应性免疫方面,DILI发生机制中源自蛋白质加合物的受损肽可导致CD4+辅助性T淋巴细胞活化,并被CD8+细胞毒性T淋巴细胞识别,从而通过免疫反应破坏肝细胞[9]。此前,关于抗肿瘤DILI的临床研究[10]显示,肝组织免疫染色显示大量CD8+T淋巴细胞和较少的CD4+T淋巴细胞或CD20+B淋巴细胞。肝脏组织炎症浸润及外周血免疫的特征可以提高对DILI潜在发病机制的理解,并探寻不同药物种类导致肝损伤的特征性效应淋巴细胞。在本研究中作者发现细胞毒性T淋巴细胞(%)以及CD4/CD8在中草药、中成药制剂或保健品和西药类两组之间具有显著差异(P值分别为0.011、0.002),这提示中草药及中成药等多成分药物导致的DILI可能更多为宿主相关性。不同于成分明确的西药暴露于某种药物特性或剂量,因此两者可能在适应性免疫紊乱及先天性免疫耐受突破中具有不同的致病特点。中草药及中成药与成分明确的西药在肝损伤程度分级上并未显示出统计学差异,这或许与样本量偏小有关,也可能与外周血免疫指标纳入较少未能体现其真实免疫病理微环境水平有关。此外,急性肝损伤发生时,宿主几乎没有时间触发有效的适应性免疫反应。从该角度来看,先天免疫系统可能比适应性免疫系统在早期具有更多的作用,因此这也是在外周血中适应性免疫指标没有显著差异的原因之一。
炎症应激假说认为某些DILI是药物暴露与急性炎症相互作用所致,炎症应激可能既是DILI的独立易感因素,又是DILI的促进因素[11]。由药物或反应性代谢物引起的直接肝细胞功能障碍和死亡导致DILI的发生,肝细胞损伤会刺激先天和适应性免疫反应的激活,进而分泌促炎细胞因子和趋化因子,产生组织肝毒性介质并释放信号,进一步招募炎症反应细胞到肝脏。DILI可能与免疫耐受的突破和肝脏炎症的加剧有关[12]。既往临床单药肝损伤研究[13]显示,肝组织的免疫组织化学特征为T淋巴细胞在肝细胞损伤区域浸润,表明适应性免疫系统可能参与了发病机制。药物与TNFα等细胞因子的相互作用可能导致会特异质性DILI[14]。适应性免疫和先天免疫的一个共同点是细胞因子的产生,包括各种细胞因子启动细胞信号通路,最终导致细胞死亡或增殖修复受到抑制。在此次临床回顾性观察中发现,IL-6与IL-10在肝功能正常组与DILI组中具有显著差异,IL-6可能在肝脏炎症反应、氧化应激、内质网应激和细胞凋亡中发挥病理作用,但样本量偏小,仍需进一步验证。单核巨噬细胞在各种内源性和外源性介质的作用下激活后分泌IL-10,IL-10通过影响免疫介质释放及抗原提呈发挥免疫抑制效应。对DILI发病中IL-10的进一步探索可能对其在DILI中起作用的具体分子机制以及治疗靶点的潜在应用具有重要意义。本次观察性研究,作者发现IL-10在肝功能正常组与DILI组中具有显著性差异,提示其或在DILI发生机制中的损伤自限性方面发挥了作用,其可能被相关药物-蛋白复合物激活,对肝脏炎症反应及过度免疫激活产生抑制效应。但同样基于样本量的限制及免疫细胞因子指标纳入较少,仍需要进一步验证其特征性意义,为后续DILI损伤标志物及治疗靶点做充分临床研究。
通过此次回顾性临床观察,作者对DILI发病的潜伏期、性别比、临床表现、损伤类型作了验证,对关于DILI发病的细胞免疫及体液免疫的特点作了探索,发现了中药及中成药与西药在外周免疫血清学分布上的差异,而且发现了炎症因子IL-6以及免疫炎症抑制因子IL-10在DILI发病血清学中的特征性表现。但本次回顾性研究,样本量偏少,所纳入的细胞免疫及细胞因子指标不足,仍需在前瞻性研究中进一步扩大样本及研究项目,以便为DILI的防治诊断提供更好的参考依据。
伦理学声明:本研究方案于2018年3月7日经由上海中医药大学附属曙光医院伦理委员会审核批准,批号:2017-560-43。
利益冲突声明:本研究不存在研究者、伦理委员会成员、受试者监护人以及与公开研究成果有关的利益冲突。
作者贡献声明:王宇负责课题设计,资料分析,撰写论文;沈晓萍、罗琼参与收集数据,修改论文;李书、李爽、陶艳艳、刘成海负责拟定写作思路,指导撰写文章并最后定稿。
