光谱法研究氯喹与人血清蛋白的相互作用*
2022-05-09岑建芳王慧晓周志强杨立云
岑建芳,王慧晓,周志强,杨立云
(南宁师范大学 广西天然高分子化学与物理重点实验室,广西 南宁 530001)
0 引言
人血清白蛋白(Human serum albumin,HSA)是人血清中含量最丰富的载体蛋白质[1],占人体血浆总蛋白的50%~60%,其在维持渗透压的平衡和转运药物小分子中扮演着重要的角色。当不同结构的药物分子进入人体后,血清蛋白会和这些物质发生相互作用[1-3],进而影响药物的释放和代谢。因此,研究人血清白蛋白与药物分子的相互作用,对了解药物在人体内的吸收、运输、储存及代谢进程,具有重要意义。
氯喹(Chloroquine,CQ)是一种应用广泛的自噬抑制剂,能抑制溶酶体的活性,进而破坏自噬体与溶酶体的融合,因此对多种癌细胞具有较好的抑制效果。将CQ与化疗、光热治疗等方法相结合,可明显提高抗肿瘤效果。例如,Chen等[4]通过联合紫檀芪和氯喹来治疗胰腺导管腺癌;Xu等[5]设计了一个功能化的二硫化钼纳米片递送阿霉素和氯喹,可有效地杀死Hela-R细胞。最新的研究结果表明CQ有望用于新型冠状病毒的治疗[6]。
通过模拟人体生理环境,采用荧光光谱、圆二色光谱等方法,在分子水平探讨了CQ和HSA的作用机制,获取此过程中的结合常数及结合模式,同时探究了CQ对HSA蛋白结构的影响。研究结果有望为CQ的临床应用提供一定的理论依据。
1 实验部分
1.1 仪器与试剂
LS-55荧光分光光度计(英国Perkin Elmer公司);QM-8075型高灵敏度稳瞬态荧光光谱仪 (日本HORIBA公司);圆二色光谱仪(英国Applied Photophysics);人血清白蛋白(>96%,美国Sigma-aldrich公司);氯喹(>98%,美国Sigma-aldrich公司);磷酸二氢钾、磷酸氢二钠、氯化钾、氯化钠(AR,国药集团化学试剂有限公司)。
1.2 实验方法
1.2.1 荧光光谱
荧光猝灭光谱:在pH =7.4的PBS溶液中,利用LS-55荧光分光光度计测量不同温度 (298K,304K,310 K)下,CQ与HSA相互作用的荧光光谱。其中,C(HSA)= 2.0×10-6mol/L,C(CQ)= 9.693×10-4mol/L,CQ以3 μL的体积累计加入HSA溶液。激发波长设为280 nm,激发狭缝和发射狭缝分别为:15 nm和10 nm,记录波长范围:280 ~480 nm。
同步荧光光谱:在298 K时,设置仪器激发波长和发射波长的波长差(Δλ)分别为15 nm和60 nm,分别得到酪氨酸残基和色氨酸残基的特征谱图。
1.2.2 荧光寿命
激发波长设为278 nm、发射波长设为350 nm、激发狭缝和发射狭缝分别设为15 nm和10 nm,用QM-8075型高灵敏度稳瞬态荧光光谱仪测量HSA及HSA-CQ体系的荧光寿命。
1.2.3 圆二色光谱
常温下,扫描范围为200~260 nm,响应时间为0.5 s,仪器由Chirascan控制。HSA和CQ的摩尔比为:1∶0,1∶4,1∶10,1∶20,1∶40,平行测定3次。利用SELCON3软件计算HSA中各二级结构的含量。
2 结果与讨论
2.1 荧光猝灭机制和结合常数
HSA在350 nm附近呈现较强的荧光发射峰,而CQ几乎不具有内源荧光(曲线I表示)。随着CQ的不断加入,HSA的荧光强度逐渐减小,且最大荧光发射峰出现明显红移,表明CQ能有效猝灭HSA的内源荧光。不同浓度的CQ与HSA相互作用时,HSA的荧光光谱图(T= 298 K,C(HSA)= 2.0×10-6mol/L,C(CQ)/(×10-4mol/L),A~H: 0, 0.06,0.11,0.17,0.23,0.29,0.35,0.41),CQ猝灭HSA的荧光光谱(图1)。
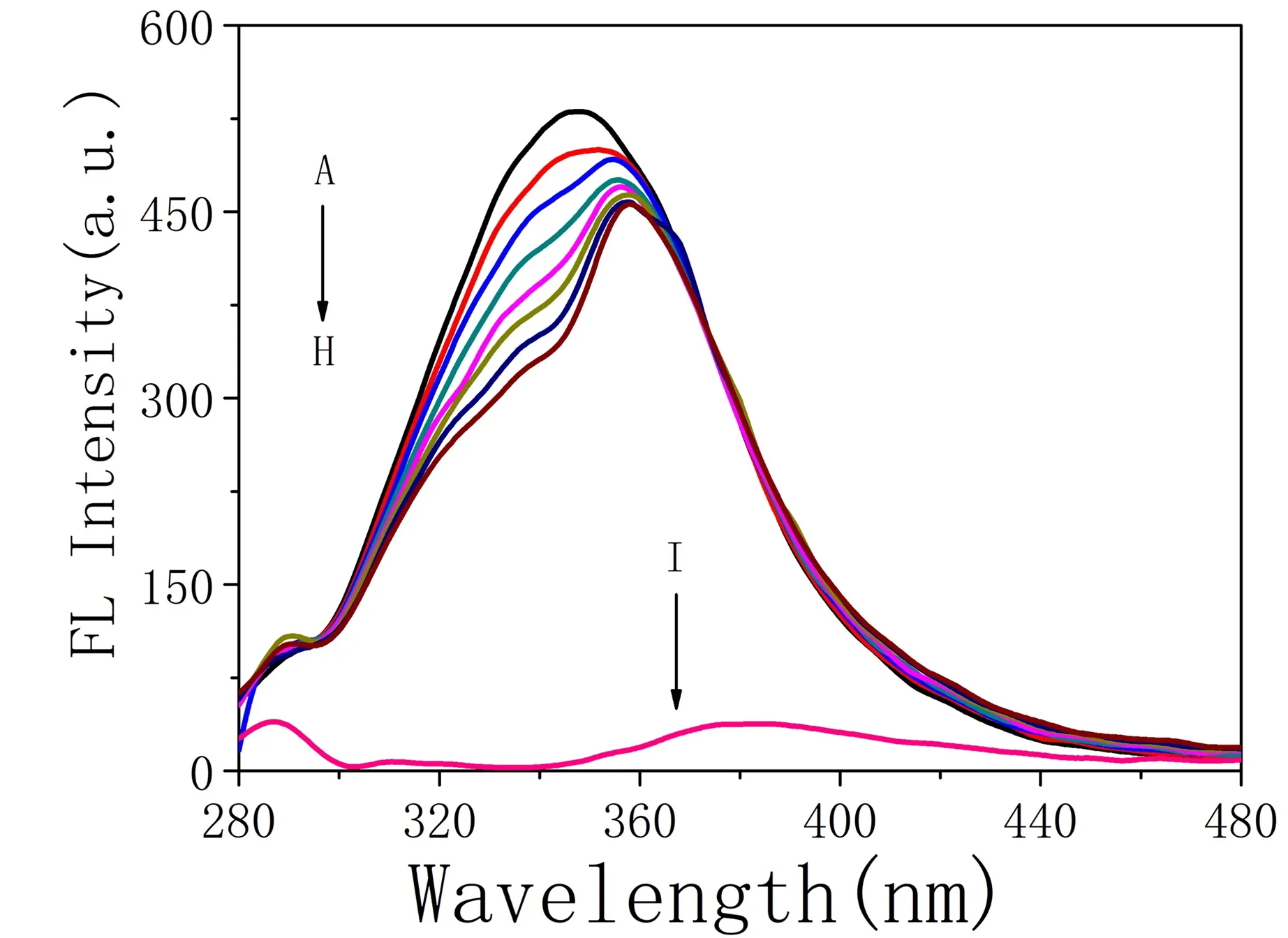
图1 HSA的荧光光谱:曲线I:CQ的荧光光谱图
荧光猝灭类型分为2种:动态猝灭和静态猝灭。对动态猝灭,猝灭剂与荧光体分子之间发生有效碰撞,不会导致蛋白质本身的结构和生理活性发生变化,因此其猝灭常数Ksv随着温度上升而增大;静态猝灭与动态猝灭不同,因其生成了静态复合物,因此猝灭常数Ksv随着温度上升而减小[7,8]。这种猝灭类型不仅在微观方面影响蛋白质的二级构象,且在宏观层面上也会影响蛋白质的生理活性。为了研究CQ猝灭HSA的作用机制,用Stern-Volmer方程处理不同温度下(298、304和310 K)的荧光猝灭数据:
F0/F=1+Ksv[Q]
(1)
式中,F0为HSA单独存在时的荧光强度;F为加入CQ后HSA的荧光强度。[Q]为CQ的浓度,Ksv为猝灭常数。以F0/F对[Q]作图,拟合得直线,如图2所示,计算Ksv的结果(表1)。显然,随着温度上升,荧光猝灭常数Ksv减小,说明CQ与HSA的作用模式是静态猝灭。
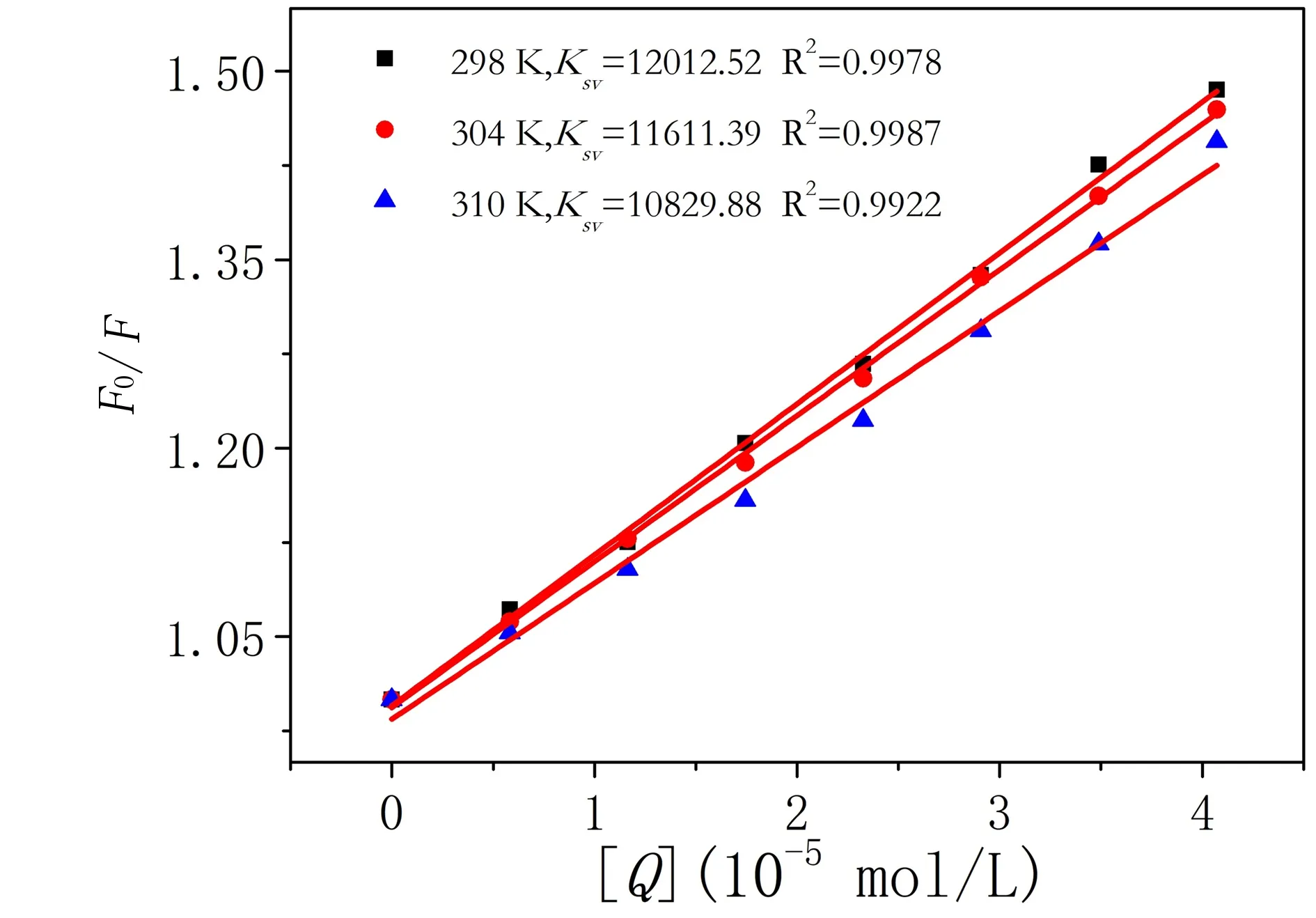
图2 三个不同温度下时的Stern-Volmer关系图
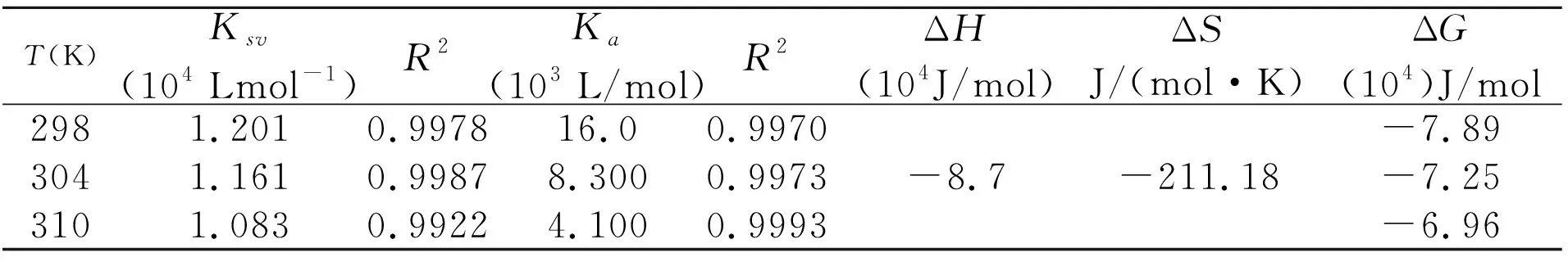
表1 CQ和HSA相互作用的猝灭常数、结合常数以及热力学常数
为了进一步验证CQ与HSA作用是形成复合物的静态猝灭,利用时间分辨荧光光谱法测定CQ作用前后HSA的荧光寿命。动态猝灭会使HSA的荧光寿命改变,而静态猝灭的荧光寿命则基本保持不变[9,10],如图3所示。HSA的荧光寿命是6.03±0.05 ns,HSA-CQ体系的荧光寿命为5.87±0.10 ns。可见,CQ加入HSA前后,HSA的荧光寿命并没有很明显的改变,进一步证明了CQ和HSA之间是有静态复合物生成的静态猝灭。
对静态猝灭,猝灭数据可以用修正的Stern-Volmer方程来进一步处理[11,12],修正方程为:
F0/ΔF=1/(Kafa[Q])+1/fa
(2)
式中: ΔF为CQ作用前后HSA的荧光强度的差值(F0-F),fa为荧光团可接近猝灭剂的部分,Ka为CQ与HSA相互作用体系中的有效猝灭常数,其值与结合常数接近。以F0/ΔF对1/[Q]作图,如图4所示,所得热力学参数见表1。由表1知,结合常数Ka随着温度的升高而减小,与Ksv随温度的变化趋势一致,说明CQ确实与HSA结合生成静态复合物。
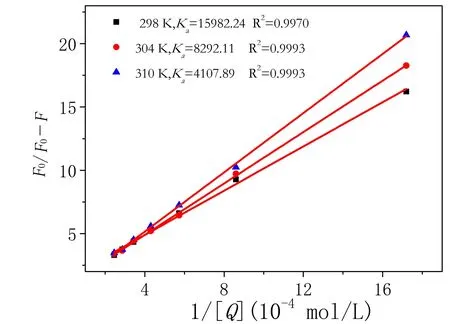
图4 不同温度下修正的Stern-Volmer关系图
2.2 CQ和HSA之间的结合模式
一般情况下,小分子与生物大分子之间主要通过疏水作用力、静电引力、氢键和范德华力等发生相互作用[13]。为了判断CQ与HSA之间的主要作用力类型,可以通过Van’t Hoff方程计算二者之间相互作用过程中的焓变(ΔH)、熵变(ΔS):
lnKa=-ΔH/RT+ΔS/R
(3)
式中:Ka为相应温度下的结合常数,R为标准气体常数,T为热力学温度。以lnKa对1/T作图,如图5所示。由斜率可求出焓变(ΔH),由截距可以求出熵变(ΔS),反应的吉布斯自由能(ΔG)可由式(4)计算。

图5 CQ与HSA相互作用的Van’t Hoff曲线
ΔG=ΔH-TΔS
(4)
热力学参数列于表1。可见,CQ与HSA相互作用的吉布斯自由能变ΔG<0,表明CQ与HSA相互作用是自发反应;ΔH<0,说明两者之间的反应为放热反应;ΔH<0、ΔS<0,说明两者之间的结合力主要是氢键和范德华力[14,15]。
2.3 CQ对HSA二级结构的影响
2.3.1 同步荧光光谱
CQ与HSA作用前后的同步荧光光谱图(图6)。当Δλ = 15 nm时,提供酪氨酸残基特征谱图,当Δλ=60 nm时,提供色氨酸残基特征谱图[16]。从图6a可知,随着CQ不断加入,酪氨酸残基的最大荧光发射波长基本保持不变,说明酪氨酸残基周围环境没有变化。而色氨酸残基的最大荧光发射波长发生了明显的红移现象,说明色氨酸残基周围环境的亲水性增大(图6b)[17]。不同浓度的CQ与HSA相互作用时,HSA的同步荧光光谱图(图T= 298 K,C(HSA)= 2.0×10-6mol/L,C(CQ)/ (×10-4mol/L),A~H: 0,0.06,0.11,0.17,0.23,0.29,0.35,0.41),如图6所示。
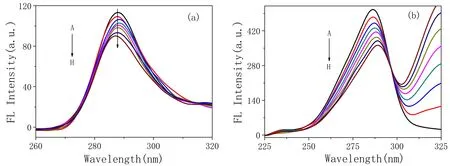
图6 不同浓度的CQ与HSA相互作用时,HSA的同步荧光光谱图
2.3.2 圆二色光谱
圆二色光谱可以反映蛋白质的二级结构变化。如图7所示,HSA的CD光谱有两个负的吸收峰,分别在208 nm和222 nm。在208 nm处的吸收峰反映了HSA的α-螺旋结构的特征吸收[18,19]。从图7中可以看出,随着CQ浓度的增加,两个吸收峰的强度都有所降低,且208 nm处的吸收峰降低更为显著。

图7 pH=7.4时的HSA-CQ体系的CD光谱图
为了定量分析HSA二级结构的改变,使用SELCON3解析CD数据,结果列于表2,可以看出α-螺旋含量由原来的62.6%下降到44.6%,说明HSA的α-螺旋结构有所伸展,原因是CQ与蛋白质的多肽链的氨基酸残基结合,破坏了蛋白质的氢键结构,导致肽链变得疏松[20]。
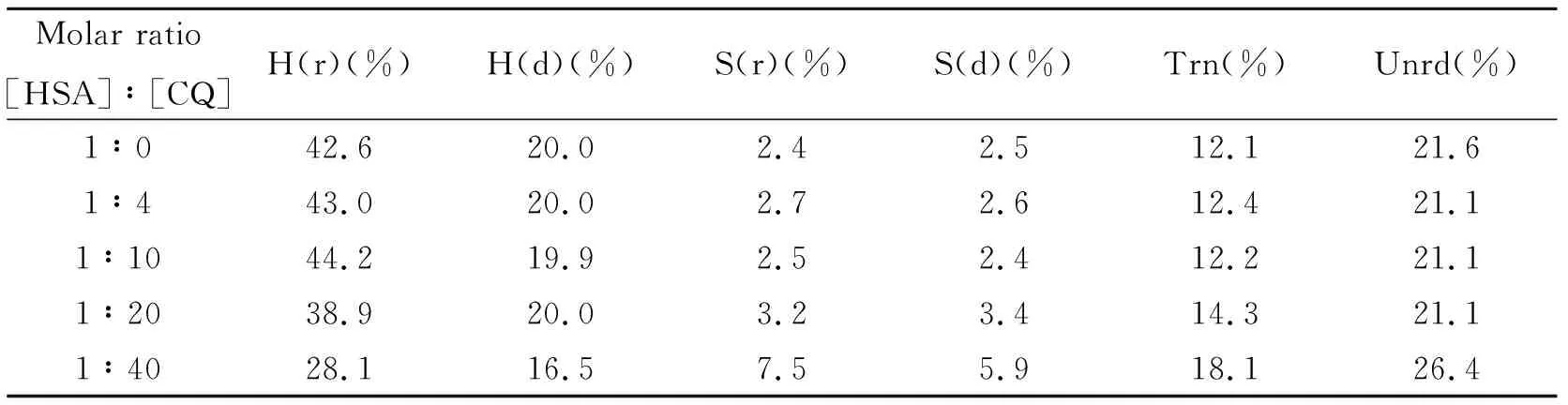
表2 SELCON3 解析得到不同二级结构的分数
3 结论
综合利用荧光光谱、圆二色光谱等方法,探究了CQ和HSA的相互作用。结果表明,CQ能通过静态猝灭的模式有效猝灭HSA的内源荧光,且结合常数Ka随着温度T的上升而减小,与荧光猝灭常数Ksv随温度的变化趋势一致。通过作用过程中的热力学参数,可以得到两者的主要结合力为氢键和范德华力,且为自发反应。同步荧光光谱结果表明,CQ与HSA相互作用后,蛋白质中的酪氨酸残基周围环境不变,色氨酸残基周围环境的亲水性增大。圆二色光谱表明,CQ与HSA的相互作用改变了HSA的二级结构。
