2种氟苯尼考注射液在鸡体内的药动学和生物等效性研究
2022-05-09孙政杨彦平曹博邱康毕冠华刘艳宋延平
孙政 杨彦平 曹博 邱康 毕冠华 刘艳 宋延平




摘要 [目的]比较先灵葆雅动物保健公司生产的氟苯尼考注射剂(参比制剂)和国内某厂家生产的氟苯尼考注射剂(受试制剂)在鸡体内的药代动力学特征,并评价2种制剂间的生物等效性。[方法]选用24只快大型白羽肉鸡,分为2組,按0.067 mL/kg的剂量分别给予受试制剂和参比制剂。采用液质联用法测定血药浓度,使用WinNonlin软件计算2种制剂的药代动力学参数和生物等效性。[结果]受试制剂和参比制剂的峰浓度(Cmax)分别为(4.85±0.57)和(4.83±0.43)μg/mL,达峰时间(Tmax)分别为(39.58±23.68)和(41.67±16.06)min,曲线下面积(AUC0-24 h)分别为(1 561.32±497.38)和(1 529.25±444.88)(μg·min)/mL。双单侧t检验法和置信区间法结果均表明2种制剂生物等效。[结论]国产氟苯尼考注射液与先灵葆雅动物保健公司生产的氟苯尼考注射液生物等效。
关键词 氟苯尼考注射液;药代动力学;生物等效性;液质联用
中图分类号 S 859.79 文献标识码 A
文章编号 0517-6611(2022)08-0081-04
doi:10.3969/j.issn.0517-6611.2022.08.022
开放科学(资源服务)标识码(OSID):
Study on the Pharmacokinetics and Bioequivalence of Two Kinds of Florfenicol Injection in Chicken
SUN Zheng,YANG Yan-ping,CAO Bo et al (Xi’an United Nations Quality Detection Technology Co.,Ltd.,Xi’an,Shaanxi 710086)
Abstract [Objective] To compare the pharmacokinetic characteristics and evaluate the bioequivalence of two kinds of florfenicol injections produced by Schering plough animal health company (reference preparation) and a domestic manufacturer (test preparation).[Method]24 fast large white-feathered broilers were randomly divided into two groups.The reference preparation and test preparation were administrated by the dose of 0.067 mL/kg.LC-MS/MS method was used to determine the plasma concentration,and pharmacokinetic parameters and bioequivalence result of the two preparations were calculated by WinNonlin.[Result]The peak concentrations(Cmax) of test preparation and reference preparation were (4.85±0.57) and (4.83±0.43) μg/mL respectively,Tmax were (39.58±23.68) and (41.67±16.06) min respectively,AUC0-24 h were (1 561.32±497.38) and (1 529.25±444.88) (μg·min)/mL.Analysis of double one-sided t-test and confidence interval showed that the two preparations were bioequivalent.[Conclusion]Two kinds of florfenicol injections from Schering-Plough animal health company and domestic market were bioequivalent.
Key words Florfenicol injection;Pharmacokinetic;Bioequivalence;LC-MS/MS
氟苯尼考是一种醇胺类的广谱抗菌药,由美国先灵葆雅公司于1988年研制成功。它对多种革兰氏阳性菌、革兰氏阴性菌和支原体等有较强的抗菌活性,主要用于治疗由敏感菌引起的猪、鸡和鱼类细菌性疾病 [1],在英、美、日、韩等国家均有广泛应用 [2]。我国于1999年批准氟苯尼考为国家二类新兽药,此后大量高校和企业对氟苯尼考开展研究。目前我国已批准上市多种氟苯尼考制剂,如氟苯尼考粉、氟苯尼考可溶性粉、氟苯尼考预混剂、氟苯尼考注射剂等,可通过混饲、混饮、肌肉注射、静脉注射等方式给药。同时,氟苯尼考也常与其他药物组合制成复方制剂,比如主要用于治疗猪胸膜肺炎放线菌导致的呼吸道感染的氟苯尼考-氟尼辛葡甲胺注射液 [3]。
氟苯尼考的毒性试验结果表明,虽然氟苯尼考的副作用比氯霉素小,但当氟苯尼考的使用剂量较高时,对动物的消化、免疫、生殖系统和器官均有毒性。当氟苯尼考被大量应用于水产养殖时,对生态环境也有污染 [4-7]。因此,氟苯尼考在畜牧业中的应用应加以控制。药品使用量与其疗效密切相关。为保证药物疗效,控制仿制兽药质量,我国于2015年发布的《兽药产品批准文号管理办法》 [8]规定:申请非新兽药的兽药产品批准文号的厂家需要根据农业农村部制定的比对试验要求和目录开展比对试验。农业农村部发布的第一批比对目录中要求氟苯尼考注射液的仿制药申请批准文号时需要与原研厂家药品进行比对,并提供生物等效性试验结果 [9]。笔者根据《兽用化学药品生物等效性试验指导原则》 [10],建立了一种液质联用法测定鸡血浆中氟苯尼考含量的方法,采用血药法计算2种制剂在鸡体内的药动学参数,并评价2种制剂间的生物等效性。
1 材料与方法
1.1 材料
1.1.1 试验动物。选择35日龄左右(体重3 kg左右)健康公鸡24只,品种为快大型白羽肉鸡AA+。自由采食饮水,饲料为不含抗菌药物的全價日粮。试验前,适应性饲养7 d。
1.1.2 药品。
参比制剂(R):氟苯尼考注射液,由先灵葆雅动物保健公司法国厂生产,批号RKPB072002。
受试制剂(T):氟苯尼考注射液,市售国产产品。
1.1.3 试剂。
氟苯尼考标准品由中国兽医药品监察所生产,批号K0301703;乙腈为色谱纯;甲醇为色谱纯;屈臣氏品牌的蒸馏水;EDTA-K2抗凝管。
1.1.4 仪器与设备。液质联用仪(LC-20AD/API 4000)、离心机(5810R)、电子天平(十万分之一)、涡旋振荡仪、移液器。
1.2 方法
1.2.1 动物分组、给药与采血。试验采用随机、单次给药、2×2自身交叉设计。
24只受试鸡按体重大小采用蛇形分组法分成2组。2组受试鸡按表1注射药品,给药剂量0.067 mg/kg,清洗期10 d。
受试鸡于给药前(0 min)和给药后10、15、20、30、60、120、240、360、480、1 440 min分别采集外周血0.5 mL,置于EDTA-K2抗凝管中,并立即来回倒置,混匀;3 500 r/min离心10 min。离心后,吸取上清血浆分装于准备好的冻存管中,一式2份(测试管和备份管),及时将分装的血浆样品置于冻存盒中,-20 ℃下冷冻暂存;待1个周期全部血样采集完后,将血样保存在-80 ℃冰箱中,待测。
1.2.2 血液样品分析。
1.2.2.1 液质联用色谱条件。
流动相为超纯水(A)、乙腈(B);色谱柱为Kinetex C18(50 mm×4.6 mm,2.6 μm);流速1.0 mL/min;柱温40 ℃;进样量1 μL。洗脱梯度如下:0~0.7 min,从10%B升高到95%B;0.7~1.5 min,95%B;1.5~1.6 min,从95%B降至10%B;1.6~2.5 min,10%B。质谱条件如下:ESI-源,MRM模式,离子对356.05/185.02。
1.2.2.2 样品前处理。取待测血浆样品50 μL置于1.5 mL离心管中,加入250 μL甲醇溶液沉淀蛋白质,4 ℃、3 500 r/min离心10 min,取上清液进样分析。
1.2.3 血液样品分析方法验证。
1.2.3.1 标准溶液的配制。
标准品储备液:准确称取1 mg氟苯尼考,用甲醇溶解,配制成1 mg/mL的标准品储备液。梯度稀释标准品储备液,配制成浓度0.5~100.0 μg/mL的标准品储备液以及浓度分别为1.5、40.0和80.0 μg/mL的标准品储备液。
1.2.3.2 定量限测定。
将空白鸡血浆45 μL置于1.5 mL离心管中,取5 μL浓度0.5 μg/mL的标准品储备液,配制成血浆浓度50 ng/mL的模拟血浆溶液;加入250 μL甲醇溶液沉淀蛋白质,4 ℃、3 500 r/min离心10 min,取上清液进样分析。
1.2.3.3 标准曲线绘制。取0.5~100.0 μg/mL的标准品储备液各5 μL,分别与45 μL空白鸡血浆混匀,配制成血浆浓度50~10 000 ng/mL的模拟血浆溶液;加入250 μL甲醇溶液沉淀蛋白质,4 ℃ 3 500 r/min离心10 min,取上清液进样分析。配制3批样品,分3 d测定。
1.2.3.4 准确度与精密度测定。取1.5、40.0和80.0 μg/mL的标准品储备液各5 μL,分别与45 μL空白鸡血浆混匀,配制成血浆浓度分别为150、4 000和8 000 ng/mL的模拟血浆溶液;加入250 μL甲醇溶液沉淀蛋白质,4 ℃ 3 500 r/min下离心10 min,取上清液进样分析,各浓度平行配制6份。配制3批样品,分3 d测定氟苯尼考标准品的准确度和精密度。
1.2.3.5 回收率测定。提取回收率样品:配制方法同准确度与精密度测定所用样品。
回收率参比样品:取空白血浆100 μL,加入500 μL甲醇作为沉淀剂,4 ℃、3 500 r/min离心10 min;取295 μL上清液,往上清液中加入5 μL 1.5、40.0和80.0 μg/mL的标准品储备液,混匀,配制成含150、4 000和8 000 ng/mL氟苯尼考的回收率参比溶液,进样分析。按照以下公式计算回收率:回收率=提取回收率样品峰面积/参比回收率样品峰面积×100%。
1.2.3.6 基质效应的测定。
分别使用空白血浆加入甲醇沉淀蛋白质后的上清液和甲醇,配制成相同浓度的氟苯尼考溶液,各稀释剂均平行配制6份,进样分析。按照以下公式计算基质效应:基质效应=上清液配制的氟苯尼考溶液峰面积/甲醇配制的氟苯尼考溶液峰面积×100%。
1.2.3.7 稳定性试验。按“1.2.3.4”方法配制模拟血浆溶液2组,每组3个浓度水平,每个浓度平行配制6份。一组在室温下放置9 h,用250 μL甲醇溶液沉淀蛋白质,4 ℃、3 500 r/min离心10 min,取上清液进样分析,考察样品在室温条件下的稳定性;另一组在-90~-70 ℃冰箱中保存24 h后,室温下融化,融化后重新保存在-90~-70 ℃冰箱中,冻融3次循环后加入250 μL甲醇溶液沉淀蛋白质,4 ℃、3 500 r/min离心10 min,取上清液进样分析。
1.2.4 数据处理。
采用非房室模型法计算药动学参数,包括半衰期(T1/2)、达峰时间(Tmax)、峰浓度(Cmax)和曲线下面积(AUC0-24 h),结果均以平均值±标准差表示。
将AUC0-24 h和Cmax经对数转换后,进行方差分析。方差分析模型中将给药顺序、药物、周期作为固定效应,将受试鸡个体作为随机效应,计算AUC0-24 h和Cmax的几何均值比率(受试制剂/参比制剂)的90%置信区间。
2 结果与分析
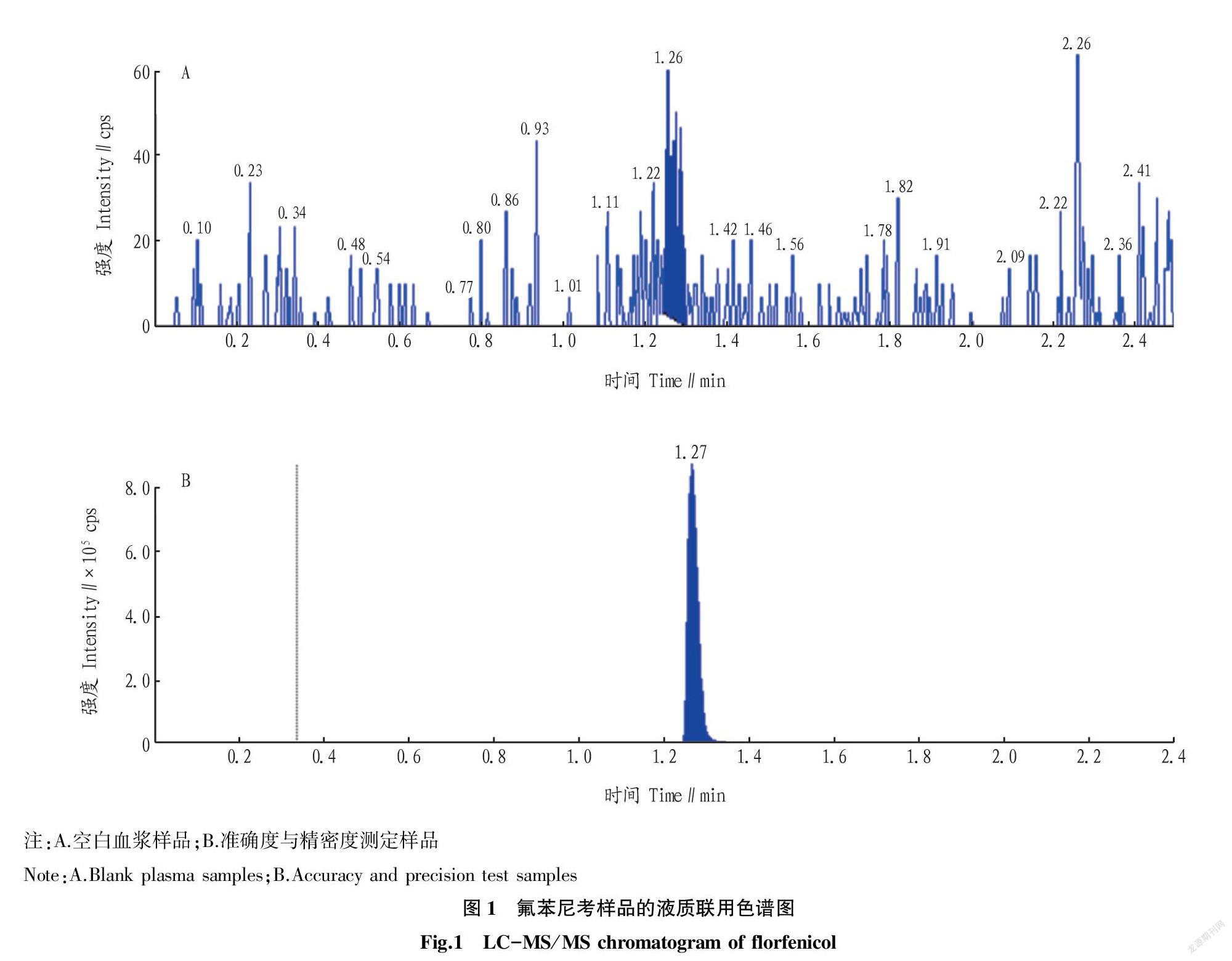
2.1 分析方法验证结果 根据《兽用化学药品生物等效性试验指导原则》(农业部公告第1247号),评价分析方法验证结果,具体见表2。氟苯尼考样品的液质联用色谱图见图1。
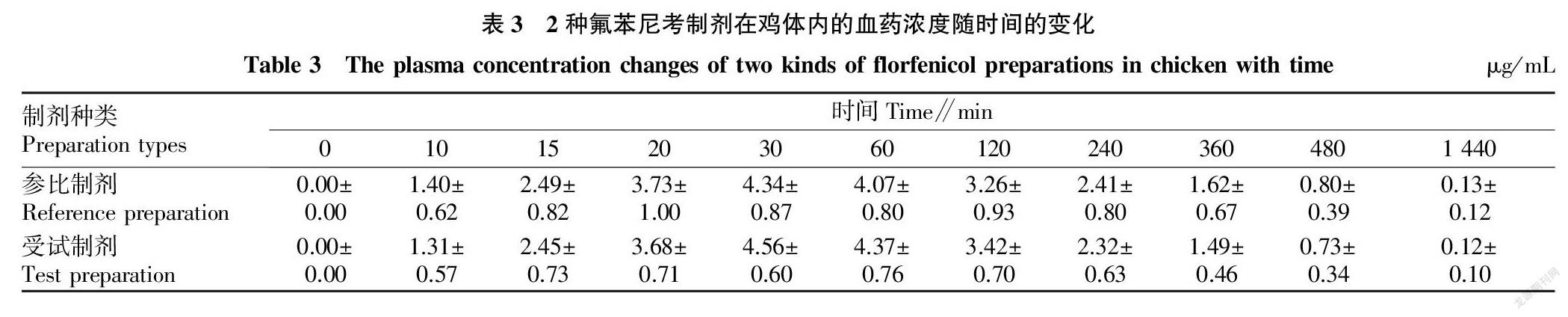
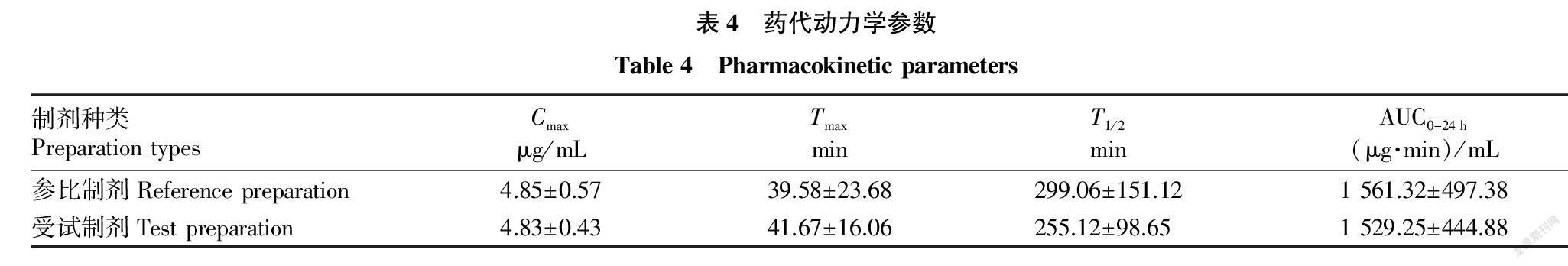
2.2 血药浓度和药动学参数 受试鸡肌肉注射2种制剂后,血药浓度-时间数据见表3。使用非房室模型计算药代动力学参数,结果见表4。由表4可知,参比制剂的Cmax为(4.85±0.57)μg/mL,Tmax为(39.58±23.68)min,T1/2为(299.06±151.12)min,AUC0-24 h为(1 561.32±497.38)(μg·min)/mL。受试制剂的Cmax为(4.83±0.43)μg/mL,Tmax为(41.67±16.06)min,T1/2为(255.12±98.65)min,AUC0-24 h为(1 529.25±444.88)(μg·min)/mL。
2.3 生物等效性
《兽用化学药品生物等效性试验指导原则》 [10]规定需先将AUC0-24 h和Cmax进行对数转换,再采用方差分析法进行显著性检验,使用双单侧t检验法和90%置信区间法评价2种制剂的生物等效性。
方差分析结果表明,AUC0-24 h经对数转换后,不同给药顺序、制剂和周期间均无显著差异,但不同动物个体间存在显著差异(P<0.01);Cmax经对数转换后,不同给药顺序、制剂、周期和动物个体之间均无显著差异(P>0.05)。
双单侧t检验结果(表5)表明,AUC0-24 h和Cmax经对数转换后,t1和t2的P值(Prob_80_00和Prob_125_00)均小于0.05,说明2种制剂间生物等效。
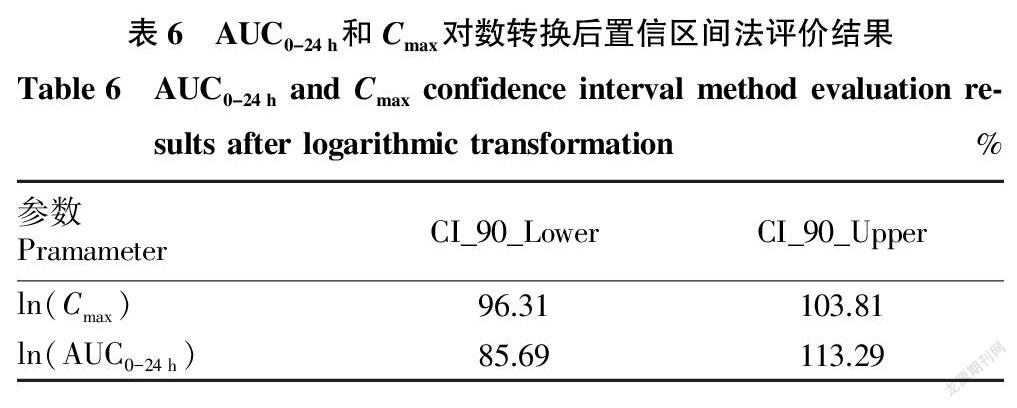
AUC0-24 h和Cmax对数转换后置信区间法评价结果(表6)表明,AUC0-24 h和Cmax几何均值比经对数转换后90%置信区间分别为96.31%~103.81%和85.69%~113.29%,均在80%~125%内,说明2种制剂间生物等效。
2.4 安全性评价
24只受试鸡在试验过程中均未发生不良事件,全部完成2周期采血试验。试验结束后24只受试鸡的身体状况均良好,因此按0.067 mg/kg的剂量给药时2种制剂对鸡的生长发育没有不良影响。
3 讨论
该研究采用液质联用法测定鸡血浆中氟苯尼考的含量,与其他文献报道采用的气相色谱法 [11]和液相色谱法 [12-13]相比灵敏度高、样品前处理简单、分析时间短,且方法验证结果表明采用该方法可以准确检测鸡血浆中氟苯尼考的含量。
药动学参数分析表明参比制剂和受试制剂均在1 h内达到吸收峰值,5 h左右达到半衰期,比沈建忠等 [14]报道的氟苯尼考肌注半衰期长2 h左右。这可能是由于动物品种、体重、合成工艺和制剂中辅料的不同造成的。从氟苯尼考的药动学参数来看,该研究中2种氟苯尼考制剂在鸡体内的持续时间更长。
2种生物等效性评价方法均证明2种氟苯尼考注射液制剂具有生物等效性,且给药期间受试鸡未发生不良事件,因此这2种制剂在兽药临床上可以替代使用。
参考文献
[1]
孙继超,董朕,张继瑜,等.氟苯尼考毒性的研究进展[J].湖北农业科学,2020,59(12):9-12.
[2] 刘芳.两种氟苯尼考粉剂在鸡体内的药动学比较研究[D].扬州:扬州大学,2016.
[3] 冯全利.氟苯尼考注射液、氟尼辛葡甲胺注射液及氟苯尼考—氟尼辛葡甲胺注射液在猪的药动学比较研究[D].扬州:扬州大学,2014.
[4] 张莺脐,张羡宇,郭庆芳,等.氟苯尼考对太平洋牡蛎(Crassostrea gigas)早期发育的影响[J].海洋科学,2021,45(1):100-109.
[5] WANG X,HAN C,CUI Y Q,et al.Florfenicol induces renal toxicity in chicks by promoting oxidative stress and apoptosis[J].Environmental science and pollution research international,2021,28(1):936-946.
[6] 沈強兵.山羊氟苯尼考中毒病的诊疗体会[J].中国动物保健,2020,22(8):82,84.
[7] ZHANG Y Q,ZHANG X Y,GUO R,et al.Effects of florfenicol on growth,photosynthesis and antioxidant system of the non-target organism Isochrysis galbana[J/OL].Comparative biochemistry and physiology,part C:Toxicology & pharmacology,2020,233[2021-03-17].https://doi.org/10.1016/j.cbpc.2020.108764.
[8] 《兽药产品批准文号管理办法》中华人民共和国农业部令 2015年第4号[A].2015.
[9] 农业部办公厅.农业部办公室关于印发《兽药比对试验要求》和《兽药比对试验目录(第一批)》的通知:农办医〔2016〕32号[A].2016-05-05.
[10] 中华人民共和国农业部.中华人民共和国农业部公告 第1247号:兽用化学药品生物等效性试验指导原则[A].2009-08-20.
[11] 董静.氟苯尼考给猪肌注的药动学—药效学研究[D].武汉:华中农业大学,2008.
[12] 刘芳,韩孝欣,王东亮,等.两种氟苯尼考粉剂在肉鸡体内的药动学比较[J].畜牧与兽医,2016,48(4):101-103.
[13] 李朋朋,张珍,李林育,等.3种氟苯尼考产品在猪体内的药代动力学及相对生物利用度研究[J].安徽农业科学,2019,47(24):125-127,142.
[14] 沈建忠,胡顶飞,吴先爱.氟苯尼考在鸡体内的药代动力学研究[C]//第四届中国畜牧兽医青年科技工作者学术研讨会论文集.北京:中国畜牧兽医学会,2001:255-258.
