LiFePO4锂离子电池的低温性能改进
2022-05-07苏林华高春辉陈明国张炜鑫
苏林华,高春辉,陈明国,张炜鑫
(1.国网内蒙古东部电力有限公司,内蒙古 呼和浩特 010000;2.国网电力科学研究院武汉南瑞有限责任公司,湖北 武汉 430074)
与其他正极材料锂离子电池相比,磷酸铁锂(LiFePO4)正极锂离子电池的1 C循环寿命可达2 000次,还具有穿刺不爆炸、过充时不容易燃烧和爆炸等优点,大规模的应用日益增加[1-2]。LiFePO4锂离子电池在低温环境下的使用受到限制,除了放电容量会严重衰减外,还因为低温下不能对电池进行充电[3]。
研究电极材料的热/动力学界面稳定性,可降低界面阻抗,获得耐低温的纳微结构转化规律,从根本上解决电池低温下性能劣化的问题。在制备LiFePO4的过程中进行碳包覆,是降低界面阻抗的重要手段,在设计碳基LiFePO4正极材料时,关键问题是控制碳的添加量。现有的碳包覆主要是将LiFePO4粉末与蔗糖混合,再进行热处理,或采用熔盐铸造法,这些方法包覆的碳都不均匀。多巴胺单体具有自聚合特征,可形成聚多巴胺(PD)层,PD层不仅可以附着在有机材料表面,还能对各种无机材料表面进行修饰[4]。采用多巴胺包覆LiFePO4粉末,还可解决LiFePO4粉末分散性差的问题。高温碳化后,PD层可转变为一种氮掺杂的无定型碳层,为LiFePO4的电子转移提供电子隧道,弱化极化效应,提高相应的电化学性能。阻止锂离子电池在低温条件下性能衰减的另一个关键,是开发具有较高Li+电导率的低温电解液。氟代溶剂是目前研究较多的一类材料,在开发具有特殊功能的锂离子电池电解液时应用广泛。氟化会使溶剂的凝固点降低、闪点升高、抗氧化性提高,有助于提升电解液和电极之间的接触性能,生成含有氟化物的固体电解质相界面(SEI)膜和正极-电解质相界面(CEI)膜。
针对低温下LiFePO4锂离子电池性能衰减严重的问题,本文作者利用多巴胺自聚合原理,在LiFePO4晶体上覆盖一层氮掺杂的无定型碳层;同时,在含氟有机溶剂中加入双三氟甲磺酰亚胺锂(LiTFSI)和双(五氟乙基磺酰基)亚胺锂(LiBETI)两种不同性质的锂盐,制备LiFePO4锂离子电池用低温混合锂盐电解液(MLiE)。
1 实验
1.1 LiFePO4/C的制备
利用多巴胺的自聚合原理对LiFePO4进行表面修饰。首先利用Tris缓冲液(三羟甲基氨基甲烷盐酸盐,北京产,98%)配制pH=8.5的碱性溶剂,然后按1.0mg/ml的用量加入多巴胺(Aladdin公司,AR)。待多巴胺完全溶解后,再加入10mg/ml的LiFePO4(Macklin公司,99.5%)固体粉末,搅拌反应5 h,使多巴胺自聚合包覆在LiFePO4表面,形成PD层。产物离心分离并用甲醇(Macklin公司,98%)洗数次后,清理掉LiFePO4孔内及表面没有聚合的多巴胺分子。将干燥后的粉末用碾钵研磨,再置于高温管式炉中,在N2气氛中、300℃下保温3 h,之后升温至750℃,保温10 h,合成碳包覆的LiFePO4(LiFePO4/C)。
1.2 混合锂盐电解液MLiE的制备
所有电解液的调配均在氩气保护的手套箱内完成。所用溶剂氟代碳酸乙烯酯(FEC,Aladdin公司,99%)在使用前用4A分子筛干燥,以保证水分降到0.003%以下;锂盐LiTFSI(Aladdin公司,99%)、LiBETI(Aladdin公司,99%)均在烘箱中120℃下真空(-0.1 MPa,下同)干燥24 h。将FEC加到样品瓶中,依次加入LiTFSI、LiBETI,配制总浓度为1mol/L的电解液,其中 n(LiTFSI) ∶n(LiBETI)=1∶1。
1.3 实验电池和对比电池的组装
将制备的 LiFePO4/C(对比电池为 LiFePO4)、乙炔黑(Macklin公司,99.5%)、聚偏氟乙烯(PVDF,Aladdin公司,99%)按质量比9.0∶0.5∶0.5混合,添加一定量的溶剂N-甲基吡咯烷酮(NMP,国药集团,99%),磁力搅拌24 h,制得浆料。将浆料均匀地涂覆在12μm厚的铝箔(巩义产,99.8%)衬底上,厚度约为150μm,在 120℃下真空干燥12 h,再以16 MPa的压强压实,得到正极片(90 mm×60 mm)。
将人造石墨(Macklin公司,99.5%)、乙炔黑、丁苯橡胶(SBR,Macklin公司,99%)和羧甲基纤维素钠(CMC,Macklin公司,99.5%)按质量比 94.0∶2.0∶2.5∶1.5 混合,添加一定量的蒸馏水,磁力搅拌24 h,制得浆料。将浆料均匀地涂覆在8μm厚的铜箔(巩义产,99.8%)衬底上,厚度约为80μm,在120℃下真空干燥12 h,再以16 MPa的压强压实,得到负极片(90 mm×60 mm)。
以Celgard 2400膜(美国产)为隔膜,注入配制的MLiE电解液,制备软包装LiFePO4锂离子电池(15 mm×78 mm×170 mm),设计容量为20 Ah。对比电池为商用电解液CE[1 mol/L LiPF6/EC(济南产)]。测试前,电池以0.02 C恒流充电至4.20 V,用CT2001A电池测试系统(武汉产)进行活化,以便在负极表面形成均匀的SEI膜。
1.4 材料分析
用S-4700扫描电子显微镜(日本产)观察所购买的LiFePO4和制备的LiFePO4/C的颗粒形貌;用XRD-6000型X射线衍射仪(日本产)分析晶型结构,Cukα,扫描速度为3(°)/min;用JEM-3010透射电子显微镜(TEM,日本产)观察碳包覆层厚度;用Par Stat 2273电化学工作站(美国产)对电极进行EIS测试,频率为10-2~105Hz,振幅为5 mV。
1.5 电池测试
用CT2001A电池测试系统测试电池性能,并使用BE-TH高低温箱(东莞产)控制温度。
在室温(20℃)下,对组装的电池进行不同倍率的放电容量测试:静置5 min后,以不同的倍率放电至3.00 V,并记录放电容量;静置10 min后,以0.50 C恒流充电至4.20 V,转恒压充电至0.05 C。
电池的电化学性能测试:先以0.10 C倍率循环5次,调整倍率为0.20 C循环,以此反复,直至电流增至1.00 C。
在低温条件下测试时,先在常温下对电池进行0.10 C充电,让Li+从LiFePO4的晶格中脱出,完成正极从LiFePO4到FePO4相的转变。电池先以一定倍率恒流充电至3.65 V,转恒压充电至4.20 V,再在相同倍率下恒流放电至2.50 V,如此循环3次。
1.6 黏度测试
采用Brookfiled黏度计(美国产),通过浸入被测液中转子持续旋转形成的扭矩来测定电解液的黏度。
2 结果与讨论
2.1 LiFePO4/C的结构分析
用SEM观察购买的LiFePO4和碳包覆后的LiFePO4/C的颗粒形貌,结果如图1所示。
从图1(a)可知,LiFePO4颗粒是均匀的类球形,颗粒尺寸基本上都在1μm以下。从图1(b)可知,当采用PD包覆LiFePO4,并进行高温碳化后,LiFePO4颗粒的形貌发生了变化,颗粒边缘因包覆碳层的存在而圆形化,碳包覆层抑制了LiFePO4的团聚,得到的LiFePO4/C颗粒形貌尺寸均一。

图1 LiFePO4改性前后的SEM图Fig.1 SEM photographs before and after LiFePO4 modified
LiFePO4及LiFePO4/C的XRD图见图2。

图2 LiFePO4及LiFePO4/C的XRD图Fig.2 XRD patterns of LiFePO4 and LiFePO4/C
从图2可知,LiFePO4与LiFePO4/C的峰值相同,且峰形尖锐,峰值出现的位置也相同,晶型结构完整,都体现出了LiFePO4典型的橄榄石结构(JCPDS-83-2092),属于正交晶系的Pmnb空间群。这是由于碳是以无定形态或非晶态存在,同时也说明,少量的包覆碳没有改变材料的晶型。
图3为LiFePO4/C的TEM图。

图3 LiFePO4/C的TEM图Fig.3 Transmission electronic microscope(TEM)photograph of LiFePO4/C
从图3可知,LiFePO4颗粒外表面被碳层均匀包覆,包覆厚度约为100 nm。碳包覆层加速了电子迁移过程中的速度,且粒子与粒子之间通过无定形碳层连接,形成了独特的三维网络导电结构。
2.2 MLiE测试
电解液黏度对电池低温条件下性能的影响很大。图4为混合电解液MLiE和商用电解液CE不同温度下的黏度测试结果。
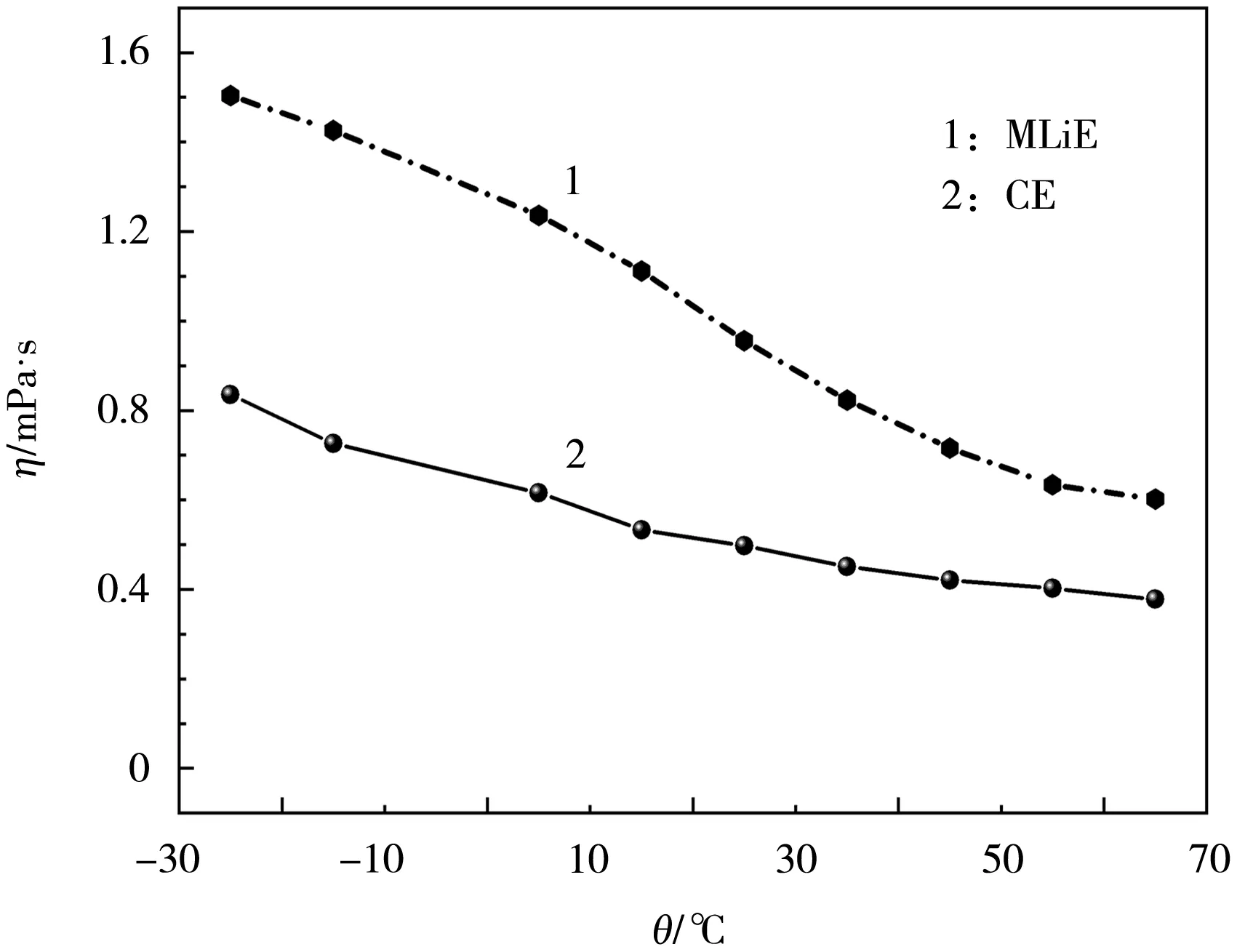
图4 MLiE和CE在不同温度下的黏度Fig.4 Viscosities of MLiE and commercial electrolyte(CE)at different temperatures
从图4可知,随着温度的降低,MLiE和CE的黏度均呈现增加的趋势,其中在温度为65~-25℃时,CE的黏度增加了0.902 mPa·s,而MLiE只增加了0.457 mPa·s。黏度越小,斜率越小,意味着溶剂的黏度越低,低温性能也就越好。
图5为低温条件下LiFePO4电极的EIS。

图5 不同电解液中LiFePO4电极的EISFig.5 Electrical impedance spectroscopy(EIS)of LiFePO4 electrodes in different electrolytes
图5中的曲线由高频、中频半圆区和低频区的斜线组成。高频区半圆对应通过电极、电解液界面SEI膜的Li+扩散,中频区半圆对应电荷转移过程,低频区的斜线对应Li+在活性物质内的Warburg扩散阻抗。当温度为-20℃和60℃时,在商用电解液CE中,LiFePO4电极的SEI膜阻抗(Rf)分别是MLiE电极的3.21倍和1.12倍。较低的Rf代表着较低的Li+扩散阻抗和较快的Li+传递速度。这表明,在高温或低温条件下,使用混合锂盐电解液降低了Li+扩散阻抗,加快了Li+的传递,提高了电池的容量。
2.3 电池电化学性能测试
图6为室温下实验电池和对比电池不同倍率的放电容量测试结果。

图6 室温(20℃)下不同LiFePO4电池不同倍率的放电容量Fig.6 Discharge capacities of different LiFePO4 batteries at room temperature(20℃)at different rates
从图6可知,在室温下,以0.1 C、0.2 C、0.5 C和1.0 C倍率放电,实验电池的放电容量分别为19.7 Ah、19.6 Ah、19.5 Ah和19.3 Ah;对比电池的放电容量分别为19.1 Ah、19.0 Ah、18.8 Ah和18.5 Ah;两种电池的放电容量差分别为0.6 Ah、0.6 Ah、0.7 Ah和0.8 Ah。 实验结果表明,使用LiFePO4/C和MLiE制备的实验电池,室温放电容量高于由商用电解液CE和普通LiFePO4制备的对比电池,在0.1 C、0.2 C、0.5 C和1.0 C倍率下的放电容量分别提高了3.1%、3.2%、3.7%和4.3%。这表明,在室温下,使用LiFePO4/C和MLiE制备的LiFePO4锂离子电池具有更好的倍率性能。这主要是由于使用LiFePO4/C作为正极,碳包覆层具有更高的电导率,界面阻抗较低,同时混合锂盐电解液在LiFePO4锂离子电池石墨负极表面形成的SEI膜降低电池内部界面阻抗的效果更好,可以减小电荷传递之间的电阻,提高电池在室温条件下的放电容量。
2.4 低温倍率性能测试
图7为低温下实验电池和对比电池不同倍率的放电容量测试结果。
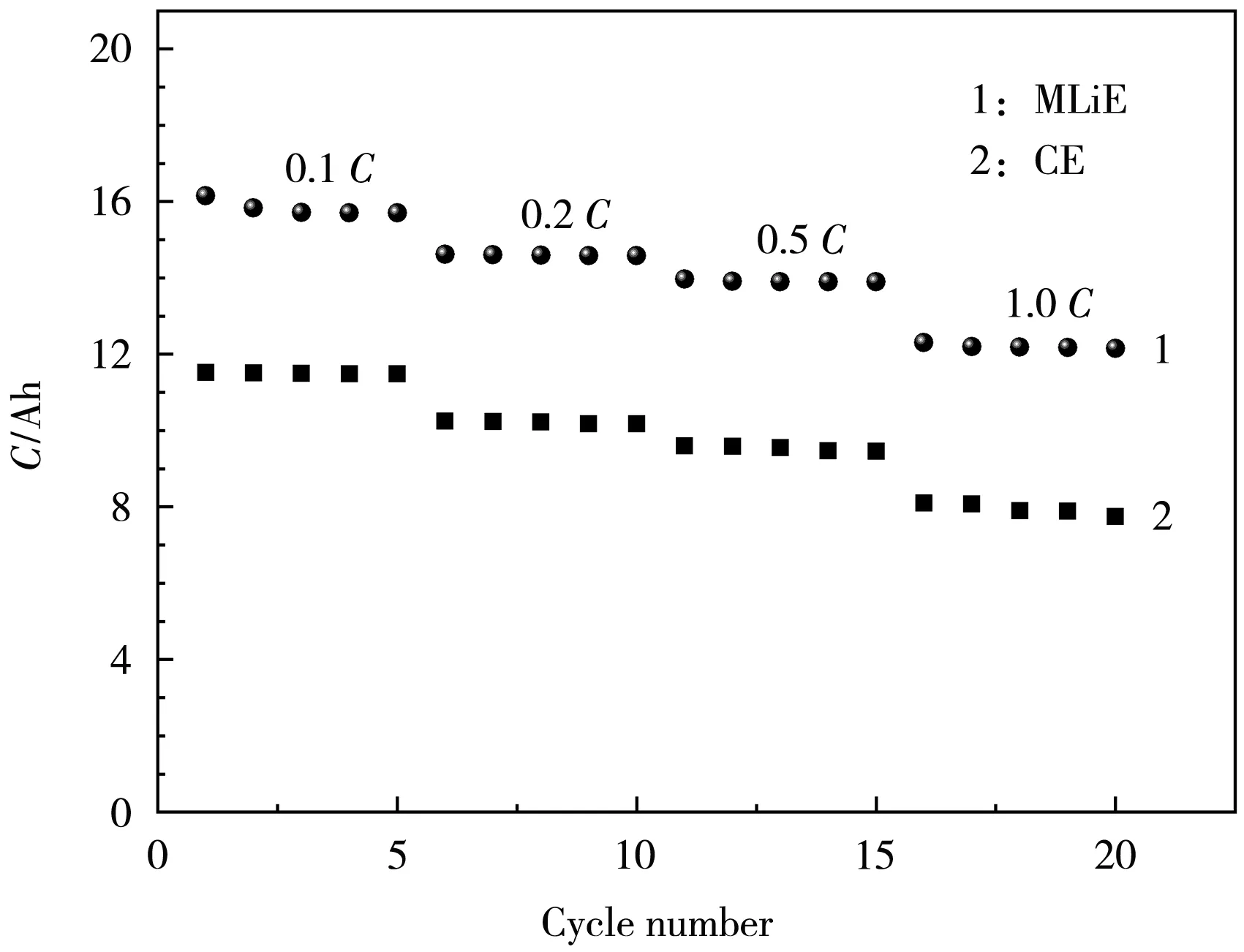
图7 低温(-20℃)下不同LiFePO4电池不同倍率的放电容量Fig.7 Discharge capacity of different LiFePO4 batteries at low temperature(-20℃)at different rates
从图7可知,在低温(-20℃)下,以0.1 C、0.2 C、0.5 C和1.0 C倍率放电,实验电池的放电容量分别为15.8 Ah、14.6 Ah、13.9 Ah和12.4 Ah;而对比电池的放电容量分别为11.5 Ah、10.1 Ah、9.2 Ah和7.5 Ah;两种电池的放电容量差分别为4.3 Ah、4.5 Ah、4.7 Ah和4.9 Ah。 由此可见,在低温环境下,实验电池的放电容量均高于对比电池,0.1 C、0.2 C、0.5 C和1.0 C倍率的放电容量分别提高了37.4%、44.6%、51.1%和65.3%。
3 结论
为解决LiFePO4锂离子电池在低温环境下性能衰减较快的问题,本文作者对现有的LiFePO4正极进行碳包覆改性,采用多巴胺自聚合原理,在LiFePO4材料表面形成一层均匀的无定型碳层;同时,选取一种含氟的有机溶剂FEC,添加到混合锂盐(LiTFSI+LiBETI)溶液中,制备混合锂盐电解液(MLiE)。
以LiFePO4/C为正极,石墨为负极,组装20 Ah LiFePO4锂离子电池。测试结果发现,与商用LiFePO4和商用电解液CE相比,基于LiFePO4/C和MLiE电解液的LiFePO4锂离子电池的放电容量更高。在低温-20℃下,0.1 C、0.2 C、0.5 C和1.0 C放电容量分别增加了 37.4%、44.6%、51.1%和65.3%。这主要是由于:一方面LiFePO4/C作为正极,碳包覆层降低了界面阻抗;另一方面采用由含氟有机锂盐和含氟有机溶剂组成的全氟有机电解液,在充放电过程中形成了富含LiF的SEI膜,提高了锂离子电池正负极的可逆性,从而提高了放电容量。
本文为锂离子电池低温环境下大规模应用所遇到的问题提供了借鉴思路和解决办法。
