层状镍钴锰酸锂三元正极材料的研究进展
2022-05-07吴彩云冯传启张朝峰梁葛萌郭再萍
吴彩云,冯传启,张朝峰,梁葛萌,郭再萍
(1.湖北大学化学化工学院,湖北 武汉 430062; 2.安徽大学物质科学与信息技术研究院,安徽 合肥 230601;3.阿德莱德大学化工及先进材料系,南澳大利亚 阿德莱德 5005,澳大利亚)
尽管太阳能、风能等可再生能源在一定程度上可以满足目前的需求,但这些能源的获取取决于气候和地理变化,且难以储存,因此储能系统日益受到人们的关注。目前应用广泛的储能装置是锂离子电池。正极材料在锂离子电池的容量、工作电压、循环稳定性和热稳定性等方面起着重要的作用,设计合成高性能正极材料是发展锂离子电池技术的关键。层状镍钴锰酸锂(LiNi1-x-yCoxMnyO2,NCM)是近年来研究广泛的正极材料之一[1-3]。
在NCM三元正极材料中,Ni参与氧化还原反应,决定材料容量;Co可增加离子导电性,提升倍率性能,还可在一定程度上降低Li/Ni混排程度;Mn不参与氧化还原反应,但可提高结构稳定性。NCM三元正极材料综合了LiCoO2的稳定性、LiNiO2的高容量和LiMnO2的低成本等特性,通过控制3种金属元素的比例,利用协同作用获得具有良好综合性能的材料。
NCM三元正极材料存在因阳离子混排、岩盐相生成与氧损失、表面残余锂、电极/电解液界面副反应、颗粒裂纹等造成的循环稳定性与倍率性能较差的问题。本文作者针对上述问题的形成原因及应对策略,进行了讨论、总结与展望。
1 层状三元正极材料NCM及合成
Z.L.Liu等[4]结合 LiCoO2、LiNiO2和 LiMnO2三者的优势,合成了NCM三元正极材料,晶体结构与LiCoO2基本一致,同时循环稳定性要好于 LiNiO2和 LiCoO2。T.Ohzuku等[5]合成了LiNi1/3Co1/3Mn1/3O2并应用于锂离子电池正极材料,在 2.5~4.6 V时,放电比容量高达200 mAh/g。 此后,三元材料NCM的研究逐渐增加。NCM与LiCoO2类似,具有α-NaFeO2型层状结构,属于 R-3m空间群,结构中O2-占据R-3m 6c位置,形成立方致密堆积的框架,Ni、Co和Mn混合占据3b八面体间隙位置,Li+占据3a八面体间隙位置。在该结构中,Li层与过渡金属(TM)层在c轴方向上堆垛,形成二维Li+扩散路径,使Li+可在层间进行可逆嵌脱[6]。
NCM的合成方法主要有高温固相法、溶剂热法、溶胶-凝胶法和共沉淀法等,目前较适用的方法是共沉淀法。该方法可解决高温固相法中材料难以按化学计量比达到分子级、原子级混合的难题,且操作较简单,制备的产品形貌均匀、振实密度高[7]。共沉淀法的基本操作是将钴盐、镍盐和锰盐配成混合过渡金属盐溶液,再加入络合剂、共沉淀剂等,通过控制反应温度、pH值及搅拌速率等条件,得到前驱体,将前驱体与锂盐混合均匀,高温烧结后得到三元NCM材料[7]。
2 NCM的缺点与改性
与传统的一元层状正极材料LiCoO2、LiNiO2和LiMnO2相比,NCM三元正极材料具有容量高、毒性小和价格低等优势,目前已广泛应用于商业锂离子电池中,但仍存在一系列问题,如Li/Ni混排、岩盐相的形成与氧损失、表面残余锂、电极/电解液界面副反应和存在颗粒裂纹等[8-9]。
2.1 锂/镍(Li/Ni)混排
2.1.1 概述
NCM层状材料为R-3m结构,是O-Li-O-TM-O-Li-O-TMO沿立方相[111]方向的重复O3结构,如图1(a)所示[10]。根据晶体场理论,e轨道的非配对电子自旋导致Ni3+的不稳定性,因此,Ni在面心立方八面体位置倾向于形成与Li+半径相似的Ni2+,Ni2+在迁移至锂层与TM层之间的四面体间隙位点后,会进一步迁移至相邻的八面体锂位点,并且不可逆地永久占据,此时,空间群由R-3m转变为Fm-3m结构[见图1(b)][10]。此外,在深度充电状态下,由于锂位点空出,材料结构极不稳定,Ni2+也会从TM层迁移到锂层,以维持电荷平衡[见图1(c)、(d)][10]。一方面,占据锂位点的Ni2+会在充电过程中被氧化成半径更小的Ni3+/Ni4+,导致晶体结构中锂层间距减小,Li+迁移能垒增加;另一方面,占据锂层位置的Ni2+也阻碍了Li+扩散。Li/Ni混排导致正极材料容锂能力下降,在循环中表现出电极容量不可逆地下降,循环性能与倍率性能变差。
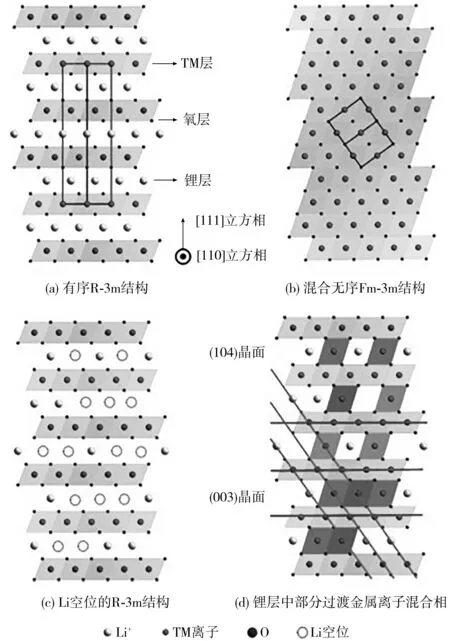
图1 层状NCM的有序-无序相及结构转变[10]Fig.1 Ordered-disordered phase in layered NCM and structural transformation[10]
2.1.2 改性手段
有研究表明,金属阳离子掺杂是抑制Li/Ni混排的一种手段[8-9]。掺入锂位点的阳离子,可通过优先占据锂位点来抑制Ni2+的迁移;掺入TM位点的高价阳离子,可以平衡由Ni2+带来的反位缺陷,从而通过抑制Ni2+迁移来抑制Li/Ni混排。此外,锂位点的掺杂元素由于不参与氧化还原反应,可作为“支柱”来稳定锂层板结构;TM位点的掺杂元素可形成强力金属-氧键,来稳定晶体结构。M.H.Chu等[11]合成了Nb掺杂的LiNi0.8Co0.1Mn0.1O2正极材料,因为 Nb5+与 Li+、TM离子的半径均较为相近,所以能进行双位点掺杂。Nb掺杂后的LiNi0.8Co0.1Mn0.1O2在充电过程中,晶胞参数c的变化范围小于掺杂前,说明Nb5+在锂位点掺杂可以缓解严重的晶格收缩,防止局部坍塌,稳定晶体结构,提高材料稳定性。电化学性能测试结果表明:以2 C的电流在2.7~4.5 V充放电,1%(质量分数)Nb掺杂的材料第200次循环时的容量保持率为81%,高于原始NCM的55%。在TM位点上掺杂,可以抑制Li/Ni混排、提高Li+迁移系数,改善Li+的扩散性能。这种高价态阳离子双位点掺杂,既能稳定晶体结构,又能抑制Li/Ni混排。
掺杂的阳离子不参与充放电过程的氧化还原反应,会造成部分容量下降,因此要严格控制用量,以便在抑制Li/Ni混排与维持电极容量之间达到平衡。梯度掺杂策略是一种应对方法,高浓度表面使材料和电解液界面更稳定,可以减少副反应的发生,内部的低浓度元素掺杂几乎不会影响材料容量,使材料可以兼顾稳定性和高容量[12]。H.F.Yu等[13]合成了Al梯度掺杂及同步LiAlO2包覆的LiNi0.9Co0.1O2,以1 C的电流在2.7~4.3 V充放电,第100次循环的容量保持率高达97.4%。Al梯度掺杂可将惰性元素掺杂造成的容量损失最小化,表面富集的Al元素和LiAlO2涂层可同时稳定晶体结构,防止电解液穿透边界,并减少副反应。
2.2 岩盐相的形成以及氧损失
2.2.1 概述
在NCM重复嵌脱锂的过程中,脱出的锂通常通过O2-氧化为O2来补偿电荷,导致晶格氧的释放。一旦空位的氧原子被释放并与电解质反应,高价态Ni4+会被还原为低价态Ni2+,并从TM层的八面体位置扩散到锂层的八面体位置,Li缺陷的阳离子空位逐渐被TM离子所取代,从而发生层状结构到表面类尖晶石相和岩盐相组合的不可逆相变[14-16]。S.Lee等[14]对充放电前后的LiNi0.89Mn0.055Co0.055O2进行了环形暗场扫描透射电子显微镜(ADF-STEM)分析,并给出了相应的(100)晶面的原子模型(见图2)。
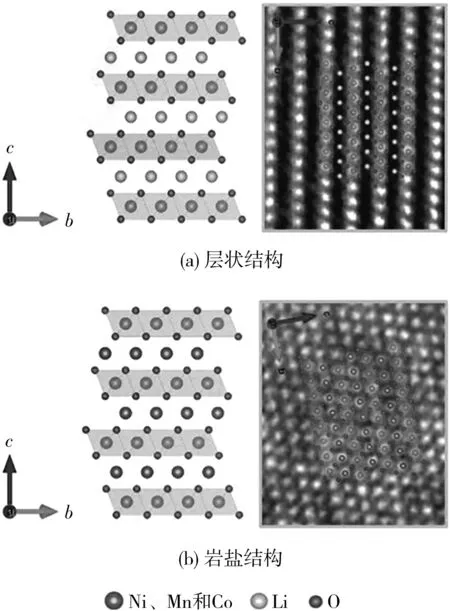
图2 层状结构和岩盐结构在(100)晶面的原子结构及ADFSTEM投影[14]Fig.2 Atomic structure and annular dark-field scanning transmission electron microscopy(ADF-STEM)photographs of layered structure and rock-salt structure in the(100)plane[14]
从图2可知,LiNi0.89Mn0.055Co0.055O2存在由层状向岩盐状的转变。随着充放电时间的延长,这种不可逆相变会进一步由表层粒子深入到内部,消耗活性锂位点,并产生绝缘表层,阻碍锂扩散到内部。
2.2.2 改性手段
通过高价阳离子掺杂,形成强力金属-氧键,从而抑制金属溶解和氧空位形成,是缓解岩盐相形成以及氧损失的一种策略[14-16]。Q.X.Ma等[17]在 Li1.2Mn0.7Ni0.2Co0.1O2中掺入Se6+,发现掺杂后的正极材料具有更好的倍率性能和循环性能。这是因为Se6+掺杂可形成强力的Se—O键,从而减少Ni和O原子的杂化,提高结构稳定性,进而抑制O2的产生。
表面包覆对抑制岩盐相的形成和氧损失也有着重要的作用。Q.M.Gan等[18]在LiNi0.8Co0.1Mn0.1O2的表面包覆一层Li3PO4,高分辨透射电子显微镜(HRTEM)和原位XRD分析结果表明:Li3PO4层可抑制层状结构向岩盐样结构的转变。原位X射线吸收光谱和原位拉曼光谱分析发现:金属-氧化物抑制了相变键的强度,从而可抑制表面氧的释放。
2.3 表面残余锂
2.3.1 概述
材料在高温煅烧过程中会有部分锂挥发损失,因此在合成NCM的过程中,通常会加入稍微过量的锂源,导致部分残余锂沉积在NCM表面。这些残余锂与环境中的H2O、CO2和O2反应,会产生LiOH、Li2CO3,聚集在NCM表面。这不仅会阻碍Li+的输运,还会促进NCM与电解质、黏结剂和导电添加剂的副反应,导致气体的生成[19]。
2.3.2 改性手段
解决NCM表面残余锂的方法是包覆一层能与残余锂反应的化合物,如Al2O3、金属磷酸盐等。这类化合物可以与残余锂反应生成高Li+迁移率的Li+主体化合物涂层,一方面抑制电极与电解液界面的副反应;另一方面促进Li+的传输。D.Becker等[20]以钨酸铵为原料对LiNi0.8Co0.1Mn0.1O2进行包覆。在高温条件下,钨酸铵一部分分解为WO3,另一部分与表面残留的LiOH反应,生成Li2WO4。此方法可消除表面残余锂,生成的WO3和Li2WO4作为涂层包覆在NCM811表面,既阻止了NCM与电解液的接触,又通过Li2WO4增强了材料的Li+电导率。
2.4 电极/电解液界面副反应
2.4.1 概述
在高电压时,电解质会快速分解产生HF等酸性物质,进一步诱发TM溶解;另外,还会在NCM表面生成不稳定的固体电解质相界面(SEI)膜,降低NCM的循环稳定性[8-9]。
2.4.2 改性手段
一般来讲,只需在NCM表面涂覆一层不参与氧化还原反应的非活性物质(如氧化物、氟化物和磷酸盐等),即可阻止正极材料与电解液直接接触,从而抑制电解质的腐蚀和活性物质的分解。实际上,这类惰性物质的电子和离子电导率较低,会导致可逆能力和倍率性能降低,因此,使用Li+/电子导体涂层效果更好。Li+导体具有较高的Li+电导率,可为Li+的运输提供通道;电子导体涂层可提供电子来抵消阳离子插入诱导的电荷不平衡,允许Li+的快速渗入。M.K.Azar等[21]在LiNi0.8Co0.1Mn0.1O2的表面负载一层还原氧化石墨烯(RGO)-ZrO2复合物,进行双功能包覆。ZrO2涂层可以抑制LiNi0.8Co0.1Mn0.1O2颗粒和电解液的直接接触,免受有害的副反应和HF攻击,提升循环性能和热稳定性;RGO涂层可弥补ZrO2涂层的低导电性,在正极材料的表面提供导电网络,以提高电极的离子/电子电导率。
2.5 颗粒裂纹
2.5.1 概述
传统的NCM正极材料是纳米级别的一级粒子聚集成微米级别的二次颗粒。这种二级结构在反复充放电时,存在内部应变引起的初级粒子的各向异性收缩和膨胀,最终形成颗粒裂纹,导致电极材料阻抗快速增加和容量快速衰减。
颗粒裂纹是高镍NCM降解的主要因素,因为裂纹会减少颗粒之间的连接,导致充电状态不均匀,加剧颗粒的粉化和碎裂;还会暴露颗粒内部更多的活性位点与电解液反应,加速材料的降解。目前普遍认为,高镍NCM材料颗粒间裂纹产生的内在原因,是高截止电压(≥4.2 V)下的 H2→H3相变所带来的c轴方向晶胞骤然收缩。c轴方向晶胞骤然收缩会引起不均匀的机械应力,从而导致颗粒破裂、容量衰减[22-23]。S.Y.Zheng等[22]采用原位XRD、固体原位核磁共振光谱(NMR)对LiNi0.8Co0.1Mn0.1O2高镍材料在充放电过程中的相变进行分析,通过6Li自旋回波原位NMR中Li峰位置在-0.1%~0.2%的变化,判断H1→H2→H3的相变。H2相的形成是由Mn位点附近的Li+(LiMn)脱出引起的。固体原位NMR显示,Li0.91与Li0.80之间有显著的峰位移,说明Li+从LiMn位点脱出。继续充电,最终形成一个没有LiMn的相,即H2相。H3相有两种类型,即H3-1和H3-2。从Li0.22到Li0.15,峰值逐渐增加,表明Li+从Ni位点(LiNi)脱出,说明H3-1相的形成主要是由于在Ni位点附近的Li+脱出伴随的晶胞参数c的降低引起的。当充电即将结束时,在化学位移为0附近观察到一个新形成的峰,表明Li+重新出现在LiNi附近,形成了H3-2相。对于H3-1,Li+有逃逸LiNi的倾向;而对于H3-2,Li+可以重新排序,并形成锂无序材料。此外,原位XRD分析显示,随着充电时Li+脱出数量的增加,(003)衍射峰的位置逐渐变化,对应于H1→H2→H3相变,而且在一次充放电后,峰值不能完全恢复到原来的位置,表明存在不可逆相变。这种不可逆相变的持续积累,会导致裂纹随着循环的深入而恶化。
2.5.2 改性手段
对于颗粒裂纹问题,目前解决的办法主要有掺杂、表面包覆及单晶结构设计[24-25]等。掺杂和包覆通过提高化学稳定性来抑制裂纹的产生。Ni位点的高价态阳离子掺杂可通过强力的M—O键来稳定晶体结构,减少氧空位的产生,进而延缓H2→H3相变,缓解裂纹产生。Li位点的阳离子掺杂,可以抑制Li/Ni混排,从而减少Ni2+的产生和迁移。较少的氧空位和较轻的Li/Ni混排,能够使NCM在充放电过程中保持更稳定的带电状态,从而避免因Li+嵌脱不均匀所导致的内部应变。包覆可以通过保护性涂层来阻止电解液渗透到粒子中,从而抑制电解液在颗粒内部发生副反应,进而抑制裂纹的产生。H.Yang等[26]同步合成了Ti掺杂La4NiLiO8包覆LiNi0.8Co0.1Mn0.1O2正极材料。这种双优化策略提升了LiNi0.8Co0.1Mn0.1O2的倍率和循环性能,原因是:①La4NiLiO8包覆层能抑制电解液侵蚀,提高LiNi0.8Co0.1Mn0.1O2表面的导电性;②Ti4+掺杂能抑制阳离子混排和有害的相变;③Ti和La4NiLiO8双重改性抑制了LiNi0.8Co0.1Mn0.1O2的晶间裂纹。
此外,单晶正极由于没有电解液渗透的晶界,可抑制因电解液渗透副反应而加剧的裂纹扩散;单晶正极具有高压实密度,能够在循环过程中承受更高应力而不会开裂[27-28]。G.N.Qian等[28]合成了单晶与多晶LiNi0.6Co0.2Mn0.2O2,对比发现:单晶LiNi0.6Co0.2Mn0.2O2可通过消除内部晶界和晶间断裂来提高NCM的循环性能。
3 结论与展望
进一步提高NCM材料的电化学性能,需要解决Li/Ni混排、岩盐相的形成与氧损失、表面残余锂、电极/电解液界面副反应及颗粒裂纹等问题。目前较好的解决手段,包括元素掺杂、表面包覆及单晶结构设计。掺杂可通过调节化学成分来稳定材料的内部结构,从而抑制Li/Ni混排、岩盐相的形成与氧损失,但也存在一些缺点,如引入杂质相、降低容量等,因此,合理选择掺杂元素及掺杂量尤为重要。后续的掺杂研究方向,应着眼于NCM中掺杂元素的作用机理,并构建完备的材料结构/功能之间的联系,为性能改进提供科学高效的指导。表面包覆从界面角度来提高NCM的稳定性,可消除表面残余锂和抑制电极/电解液界面副反应,但整体性能受限于涂层本身的Li+迁移率与电导率。单晶NCM材料由于内部无晶界,可抑制裂纹产生,提高材料循环稳定性。单晶材料通常晶粒尺寸较大,Li+传输路径较长,导致倍率性能不理想,因此尺寸调节尤为重要。元素掺杂及表面包覆等策略,也可用于单晶材料中,以弥补劣势。
实现完美的产业化,高容量、高稳定性、高倍率性能、安全性与低成本缺一不可。本文作者综述的优化策略,主要是针对稳定性、倍率性能及安全性等,而提高电极容量需要发展高镍与富锂NCM材料。高镍NCM材料由于较高的Ni含量导致颗粒表面稳定性较差,同时循环过程中的表面致密化,也会导致性能快速衰减;富锂NCM材料由于首次不可逆阴离子氧化还原反应的存在,使得首次库仑效率较低,同时阴离子氧化还原反应还会使材料结构衰退和工作电压降低。未来的研究,可将掺杂、包覆、单晶优化策略运用于高镍与富锂NCM材料中,针对性地解决材料中出现的问题,以兼具高容量、高稳定性与高倍率性能,并在此基础上,进一步优化合成方式,提高安全性。
