超声图像血管分割的研究进展
2022-05-06孙国栋石蕴玉刘翔宋家琳赵静文浦秀丽尹玲
孙国栋,石蕴玉,刘翔,宋家琳,赵静文,浦秀丽,尹玲
1.上海工程技术大学电子电气工程学院,上海201620;2.第二军医大学附属长征医院超声科,上海200003
前言
超声影像作为最普及的医学成像方式,近年来在疾病分析诊断中得到广泛应用。超声具有实时、无辐射、操作简便和经济安全等优势,现已成为疾病早期筛查和诊断的首选方式,广泛应用于临床诊断[1-2]。2020年,超声成像技术在新冠肺炎筛查诊断中发挥了重要的作用。血管分割作为其中的一项关键技术,在诊断中有着重要的研究价值。颈动脉超声图像中,血管壁表现为亮区域,血液则为暗区域,对其内中膜进行研究,能够对血管疾病发生的风险进行评估,从而进行有效预防和治疗,这在临床上具有重要的研究意义,但同一部位由不同机器所得图像的分辨率和清晰度都存在明显差异,故图像的分辨率或清晰度是影响临床精准诊疗的一个关键。
血管本身具有形状小和图像亮度不均匀等问题,需要和医学先验知识相结合才能得到比较好的分割结果,这导致超声图像分割相比自然图像更困难和复杂。血管分割在超声诊断中发挥重要作用的同时也面临以下挑战:(1)血管中包含噪声等大量复杂信息;(2)血管周围环绕着其它不相关的组织结构。目前还没有一种普遍适用的超声图像血管分割方法,也还没有一种准确评估分割算法的客观标准。
1 超声图像血管分割方法
在超声图像的血管分割中,血管的定位和提取是极其关键的。实际分割过程中血管只占整个图像的小部分区域,影像的其余部分会对分割的精度和速度产生干扰[3]。故分割前要先对图像进行滤波和感兴趣区域提取,这是血管分割的关键,对后续分割算法评估和血管形态描述等研究有重要的意义(图1)。
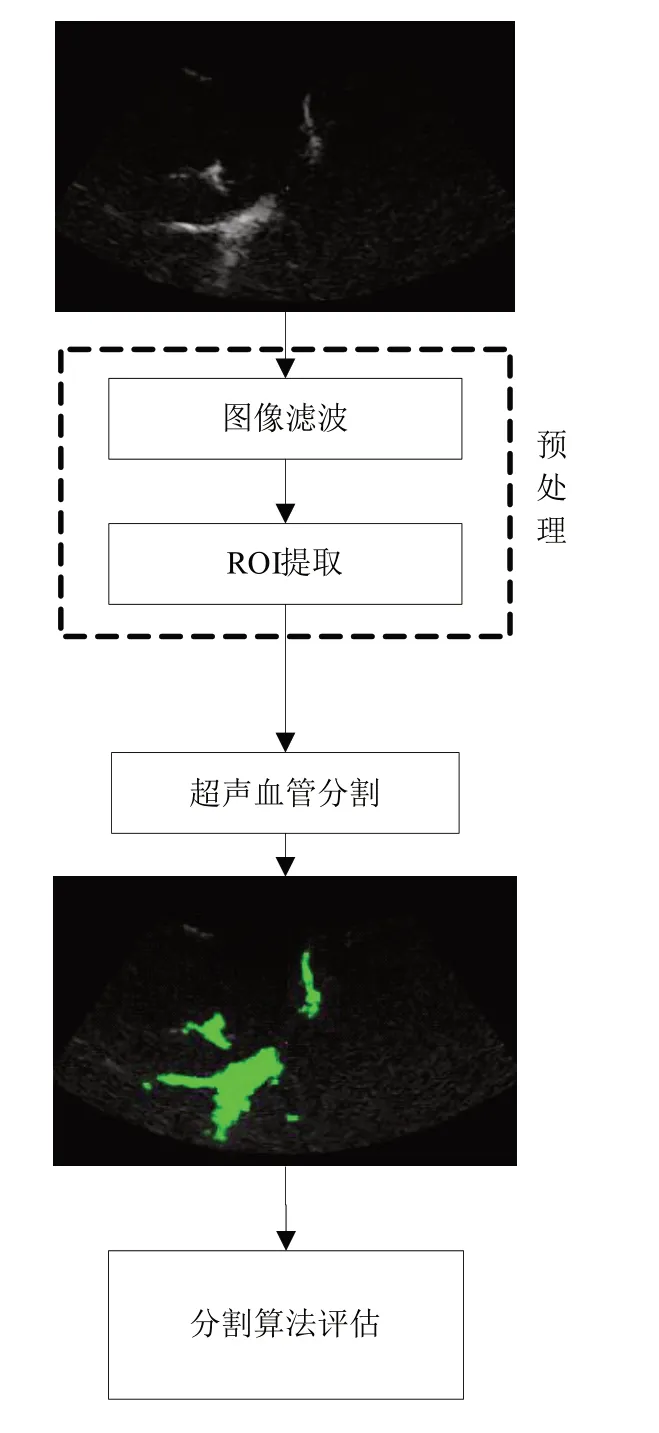
图1 超声图像血管分割Figure 1 Blood vessel segmentation in ultrasound image
1.1 超声图像预处理
预处理可去除图像斑点噪声、改善超声图像的质量。抑制斑点噪声、保留并增强超声图像细节是预处理的重要环节[4]。超声图像中的斑点是一种服从Gamma分布的乘性噪声,可采用中值滤波、高斯平滑滤波和小波变换等非线性滤波算法对其进行研究[5]。其中,基于各向异性扩散的方法能在平滑噪声的同时较好地保留超声图像的细节[6-7],实验证明滤波后的血管分割结果明显好于滤波前。李锵等[8]和王力等[9]提出一种基于高斯滤波的双边滤波模型对图像进行预处理,可以通过对邻域内各相邻像素点空间上的亮度相似性信息进行非线性组合来实现滤波。Zhang等[10]采用基于匹配滤波的算法,使用滤波器和图像卷积来提取目标,利用局部图像块和滤波核之间的相关性,在提取血管边缘时利用图像灰度在血管横截面呈现出的高斯分布特性,对高斯滤波器与血管进行匹配,从而对超声图进行有效的预处理。
1.2 基于特征提取的分割方法
超声图像血管的分布一般呈树状结构,这就决定了其分割方法的特殊性。传统的基于超声图像特征提取的血管分割方法可分为基于区域、基于边界和基于特定理论的分割(图2)。
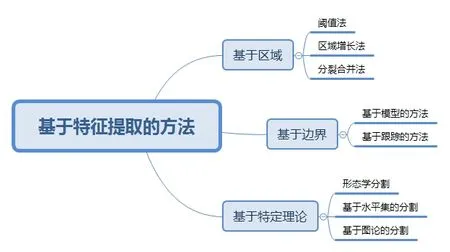
图2 基于特征提取的分割方法Figure 2 Segmentation methods based on feature extraction
(1)基于区域的方法是指利用区域内部的相似性,直接将感兴趣区域提取出来[11],具体包括阈值法、区域增长法[12-13]与分裂合并法等。该方法能有效克服其它分割算法存在分割不连续的缺点,但对噪声敏感,不太直接适用于超声图像的分割。
(2)基于边界的方法是根据图像局部的不连续性进行检测。实现过程简单,但该方法获得的边缘通常不能形成闭合曲线,一般还需结合追踪方法来形成封闭轮廓。Snake 主动轮廓模型能使初始轮廓线慢慢接近于目标的实际边缘,通过寻找能量函数上局部最小值,并用动态优化来逼近分割目标的真实轮廓[14-18]。Snake模型确保了检测到的边缘的连续性和闭合性,其局限性主要是对初始曲线的位置较敏感、不能收敛到图像的凹陷处。
(3)基于特定理论的分割方法主要有基于形态学、水平集和图论的分割。形态学的优点是速度快、抗噪性好。利用形态学对图像进行处理面临的主要问题是如何寻找合适的元素结构[19-20];基于水平集的分割是将移动界面作为零水平集嵌入到一个较高维度的水平集函数中,根据曲面演化方程来确定界面的演化结果;基于图论的算法[21-22]能充分利用图的数据结构特征,其鲁棒性好,但存在计算量大的缺点。
1.3 基于机器学习的分割方法
传统方法不能摆脱对人工的依赖,削弱了分割算法的泛化能力。机器学习算法消除了人工处理带来的随机偏差,改善了传统方法的短板,提高了临床医生诊断的客观性和准确性[23-25]。深度学习通过逐层的特征变换提取来完成血管自动分割,面临以下问题[26-28]:①深度学习模型的好坏依赖于大数据的驱动,但影像数据及金标准的数据难以收集;②深度网络模型缺乏可解释性。虽然经典图像处理算法中所采用的一些血管特征提取和分类模型都比较传统且不够新颖,但在对于缺乏大样本数据的医学图像的研究背景之下,充分利用传统且成熟的图像分割处理技术却是当下一种务实可行的研究方法。
1.3.1 基于多分类器的分割 对超声图像进行血管的分割可转为分类问题。聚类作为一种无监督的分割方法,能对分类样本的实际情况进行客观反映,已成功用于超声图像分割[29-30]。Ricci等[31]和Naik等[32]提出一种基于支持向量机的颈动脉内外膜分割方法。首先,采用K-means算法对像素点进行聚类并提取感兴趣区域,然后通过构建用于分类的特征向量来得到二值图像,最后进行边界的提取。这一思想理论上也可用于超声血管的提取。为解决三维肝脏超声血管分割的问题,甘露等[33]提出一种三维空间中多尺度旋转不变的血管连通性特征,充分利用血管组织是一种管状的树型连通结构,能有效地分离出噪声和目标区域(图3)。

图3 兔子肝脏门静脉血管Figure 3 Rabbit liver portal vessels
1.3.2 基于神经网络的分割 卷积神经网络(Convolutional Neural Network, CNN)具有很好的数据迁移能力、鲁棒性强,能自适应学习分割目标特性有差异的网络模型[34-35]。CNN 由卷积层、池化层和全连接层组成(图4)。对血管进行分割实际上就是对血管区域进行分类和标记的过程。较浅的卷积层具有分辨率高、感受野小的特点,有利于特征图和原图的对齐,可以提供更多的位置信息;反之,高层具有分辨率低、感受野大的特点,有利于对像素进行精确的分类。
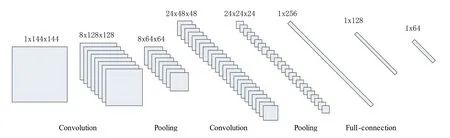
图4 卷积神经网络基本结构Figure 4 Basic structure of convolutional neural network
在U-Net网络中,编码器和解码器之间的跳跃连接可改善其分割的性能,使其网络能更好地学习到较粗粒度信息位置和全局信息之间的关系[36-37]。U-Net最大的特点是它的特征融合方式,通过收缩路径进行卷积和最大池化,使得感受野增强、每一层级的输入尺寸减小、输出的特征图数量增多。扩张路径通过上采样后接卷积操作逐渐恢复图像原尺寸,利用跨越连接将同一层级和空间位置关联性较强的浅层特征进行拼接融合来实现分割[38]。为解决网络在层数过深时产生梯度消失或爆炸的问题,Alom 等[39]在上下采样中引入R2U-Net(Recurrent Residual U-Net)来改善由于网络层数增加导致的分割结果退化问题,并使用批量归一化和Prelu 激活函数对网络进行优化,从而提高模型的拟合程度和网络性能[40],更准确地分割出CT 图像的肝脏,后续对算法改进有望可用来提取超声图像血管(图5)。

图5 R2U-Net网络结构Figure 5 R2U-Net network structure
2 血管分割评价指标
超声图像血管分割结果将直接影响后续血管形态参数的描述与分析。对分割算法的评价不仅能提高现有算法的性能,还对分割算法具有评估意义。医学图像分割评价具有一般性、客观性和定量性[41]。针对不同的超声血管分割方法,评价方法也存在较大的差异(图6)。
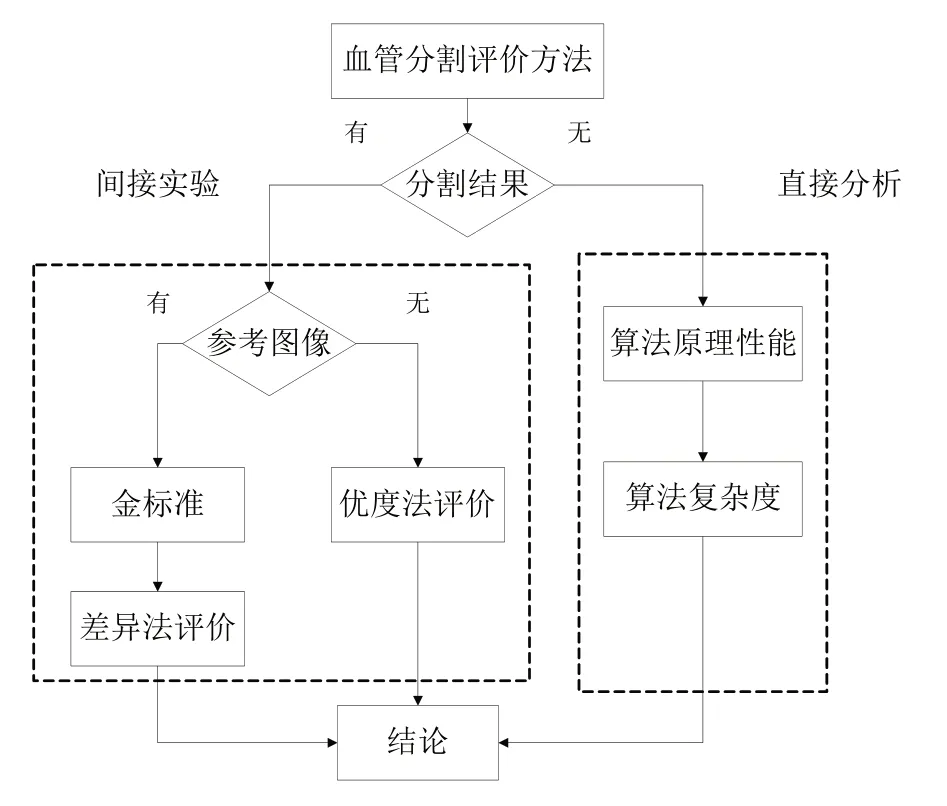
图6 超声图像血管分割评价方法分类Figure 6 Classification of methods for evaluating blood vessel segmentation in ultrasound image
(1)直接分析法:直接对算法本身进行分析,主要涉及算法的原理、性能和复杂度等方面,并不会直接涉及分割流程,结果主观性较强。
(2)间接实验法:根据分割结果间接地对算法进行评估。优度法指在没有理想分割结果的情况下,根据结果中相关特性来定量评估算法的优劣;差异法需要理想的分割结果作为金标准,通过对比算法的分割结果与金标准来评估算法的好坏。
对于超声图像血管分割算法的评价,评价指标的选取是至关重要的。结合其图像的本身特点和需求,差异法相对更加有效和客观。差异法中两个重要的评价指标是分类相似性和距离相似性,能定量评价分割算法的好坏。当分割结果与标准参考图像越接近,其相似性测度值越大。表1列出几种常用的评价指标。

表1 评价指标Table 1 Evaluation indexes
(1)面积交叠度(DICE)。待评价算法的分割结果为A,参考图像为B,相似性测度SI定义如下:

(2)Jaccard 系数。预测结果为A,理论分割结果为B。JAC定义如下:

(3)曲线距离测量。豪斯多夫距离(MSSD)用来测量两条曲线的最大差异,定义如下:
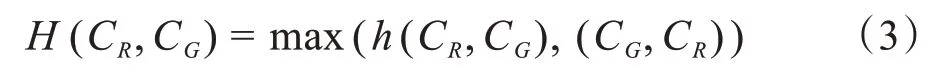
其中,CR和CG分别表示分割结果和标准参考图的边界曲线。H(CR,CG)的值越小,代表分割算法性能越好。MSSD对分割出的边界比较敏感,通常会与其它测量标准一起使用,如平均最小距离,定义如下:
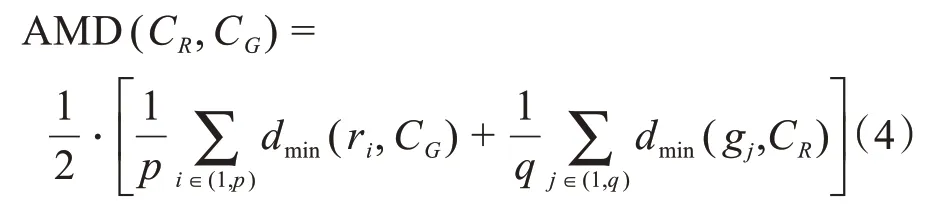
其中,i取值介于(1,p)之间;j取值介于(1,q)之间;r代表分割结果;g代表图像标注的金标准;ri和gj分别表示图像分割结果与标记图像的离散曲线;dmin表示求两曲线间最小距离;p和q分别代表CR和CG的离散值。AMD表示分割结果与标准参考图的边界曲线的平均偏离度,其值越小,表示结果越接近标准的参考图,进一步说明分割算法越优。
(4)基于像素统计的测量。将图像中每一个像素标记为目标或背景,通过与标准参考图像的标记做比较,可归结为真阳性TP、假阳性FP、真阴性TN和 假阴性FN[42]。 准确度(accuracy)、精确率(precision)和召回率(recall)可用来描述一个算法的性能:

3 总结与展望
本研究主要介绍了超声图像的血管分割方法及其评价指标,目的是辅助医生能更好地做出临床诊断。目前,虽然各大医院拥有先进的超声成像设备,但在疾病的诊断过程中医生仅凭借临床经验来衡量病灶特点做出的诊疗报告具有较强的主观性。随着病人增多且个别疾病难以诊断,医疗影像数据量越来越大;另一方面,随着研究不断深入,超声图像分割呈现出多学科交叉的特点,并趋向于高效实时的自动分割。如何在保证分割质量的同时提高分割效率是极其关键的。对于超声图像血管分割的结果,大多采用主观性评价,依赖医生经验易产生差异性和非实时性。图像分割质量的评价是整个图像处理过程中不可或缺的一步,近年来研究人员对此做了大量的工作,但目前还没有一种准确评估血管分割算法成功与否的客观标准。因而,研究适合超声图像血管分割的客观评价方法在医学图像分割领域是迫切需要的。
计算机视觉等人工智能技术在辅助临床医生的诊断过程中发挥了至关重要的作用[43],但也面临着诸多挑战:(1)影像数据标注是严重制约深度学习广泛应用的一个普遍问题,数据标注费时费力且不同任务需要不同形式的标注,金标准的建立也是个悬而未决的问题。可以考虑采用迁移学习来提高算法精度。(2)医学图像各异不均,正负样本比例极度不均衡。例如,肿瘤的像素数量比正常组织通常少一个甚至多个数量级[44]。(3)可解释性是极其重要的,临床决策在很大程度上取决于解释。深度学习是不可解释的黑盒子,分类器训练过程缺乏理论支持等质疑也从未停息。缺乏证据和解释会让医生很难相信机器学习模型的预测[45-46]。
在未来,将医学先验知识和图像分割算法进行紧密结合是极其重要的,这将会成为提高临床诊断有效性的核心问题。超声图像血管分割结果的定量化分析对医生来说是相当有用的,如分析血管长度和弯曲度等形态参数可作为未来的研究方向。总之,超声图像血管分割对于临床工作而言具有重要的应用价值。