甘草碱溶性多糖超声提取法的研究
2022-05-06唐世明
唐世明

摘 要:以NaOH浓度、料液比、提取时间、提取温度为考察因素,通过单因素试验确定各因素最佳水平。试验结果表明,单因素试验确定各因素最佳水平为NaOH浓度40 mg/mL、料液比1∶20(vol)、提取时间25 min、提取温度45 ℃。
关键词:甘草;碱溶性多糖;提取法
文章编号:1005-2690(2022)04-0025-03 中国图书分类号:O657.5 文献标志码:B
甘草为多年生草本植物,其根茎具有药用价值,有缓解咳嗽、清热解毒、祛痰止咳、消炎等作用,有效成分是甘草酸、多糖和黄酮类化合物[1]。甘草多糖(GPS)具有毒性小、抵抗毒素、提高机体免疫力等优点[2],提取方法涉及化学、物理、生物、医药等技术手段,包括传统提取法、复合酶法、微波提取法、超声提取法等。超声提取法是在超声场中极大的压强下,使整个细胞壁破裂而释放胞内物质,整个过程属于物理变化,可保障胞内物质在一定时间内不发生任何变化,并且使用成本低、自动化率较高,可用于大规模的工业生产,同时避免了对环境和产品的污染[3]。目前,药理活性研究主要集中在甘草黄酮、三萜类化合物(甘草酸)及甘草水溶性多糖上,而在甘草碱溶性多糖方面的研究报道比较少。本研究以超声法提取甘草碱溶性多糖工艺参数,主要考察NaOH浓度(mg/mL)、料液比、提取时间(min)、提取温度(℃)这4个因素对多糖提取率的影响,为确定超声法提取甘草碱溶性多糖提供理论依据。
1 材料与方法
1.1 材料
1.1.1 试材
甘草购于和田市欣明维吾尔医药材交易市场,烘干粉碎。
1.1.2 试剂
石油醚(分析纯)、无水乙醇(分析纯)、正丁醇(分析纯)、三氯甲烷(分析纯)、丙酮(分析纯)、浓硫酸(分析纯)、苯酚(分析纯)、NaOH(分析纯)、葡萄糖(分析纯)。
1.1.3 仪器
可见分光光度计722S(上海精密科学仪器有限公司制造),台式离心机TDL—40B9(上海安亭科学仪器厂制造),数显恒温水浴锅HH—Z(国华电器有限公司),超声波清洗仪KQ-250DB(昆山市超声波仪器有限责任公司)。
1.2 提取过程
对甘草进行清洗、烘干、粉碎处理。圆底烧瓶中称取30 g粉末(加入180 mL石油醚)放入水浴锅中(60~90 ℃)脱脂2 h,用180 mL 80%乙醇浸泡残渣3 h,水浴(80 ℃)加热1 h,过滤。提取液离心5 min(2 000 rpm),取上清,加入0.1%活性炭,水浴锅(60 ℃)脱色20 min,离心5 min(2 000 rpm),取上清加入1.5倍体积的氯仿-正丁醇摇匀,静置25 min后吸取上清液,加入95%乙醇静置12 h,离心5 min(2 000 rpm)。去除上清,沉淀依次用无水乙醇、丙酮多次洗涤,60 ℃干燥。
1.3 甘草碱溶性多糖含量测定
量取甘草碱溶性多糖提取液1 mL于50 mL的容量瓶中,加水至刻度,摇匀;再精确量取此稀释液溶液1 mL于10 mL的容量瓶中,加水至刻度,摇匀,将提取液稀释500倍。精确量取稀释后的溶液2 mL于试管中,滴加6%苯酚溶液1.0 mL、浓硫酸5.0 mL,摇匀,静置20 min,于490 nm处测定吸光度A值。利用葡萄糖作标准曲线[4],再代入吸光度计算得到甘草碱溶性多糖含量。根据标准线的回归方程计算样液中多糖浓度(C),据式(1)、式(2)和式(3)计算出甘草碱溶性多糖的提取率及粗糖得率。
甘草碱溶性多糖的提取率=M2/M1×100% (1)
M2=C×V×10-3=(A-b)/a×n×V (2)
甘草碱溶性多糖粗糖得率=M3/M1×100% (3)
式中:M1为甘草干粉的质量(g);M2为提取出的粗多糖质量(g);M3为醇沉所得的粗多糖质量(g);C为提取液的浓度(mg/L);V为提取液体积(L);A为吸光度;a为标准曲线的斜率;b为标准曲线在纵坐标上的截距;n为提取液的稀释倍数。
2 试验设计
分别对NaOH浓度、料液比、提取时间、提取温度4个因素进行单因素试验,以确定各因素的影响程度及适用范围。
2.1 NaOH浓度对甘草碱溶性多糖提取的影响
称取脱脂后甘草粉末2.0 g共4份,分别加入20 mg/mL、30 mg/mL、40 mg/mL、50 mg/mL NaOH溶液40 mL,在45 ℃下超声提取25 min,提取1次,提取液处理后测定各滤液的总糖,并计算出多糖的提取率和多糖粗糖得率。
2.2 料液比对甘草碱溶性多糖提取的影响
称取脱脂后甘草粉末2.0 g共4份,分别加入40 mg/mL NaOH溶液,其料液比分别为1∶15、1∶20、1∶25、1∶30,在45 ℃下超声提取25 min,提取1次,提取液处理后测定各滤液的总糖,并计算出多糖的提取率和多糖粗糖得率。
2.3 提取时间对甘草碱溶性多糖提取的影响
称取脱脂后甘草粉末2.0 g共4份,分别加入40 mg/mL NaOH溶液40 mL,在45 ℃下分别超声提取15 min、20 min、25 min、30min,提取1次,提取液處理后测定各滤液的总糖,并计算出多糖的提取率和多糖粗糖得率。749DCE71-6172-4D11-81F1-586C28A1D95A
2.4 提取温度对甘草碱溶性多糖提取的影响
称取脱脂后甘草粉末2.0 g共4份,分别加入40 mg/mL NaOH溶液40 mL,分别在40 ℃、45 ℃、50 ℃、55 ℃下超声提取25 min,提取1次,提取液处理后测定各滤液的总糖,并计算出多糖的提取率和多糖粗糖得率。
3 结果与分析
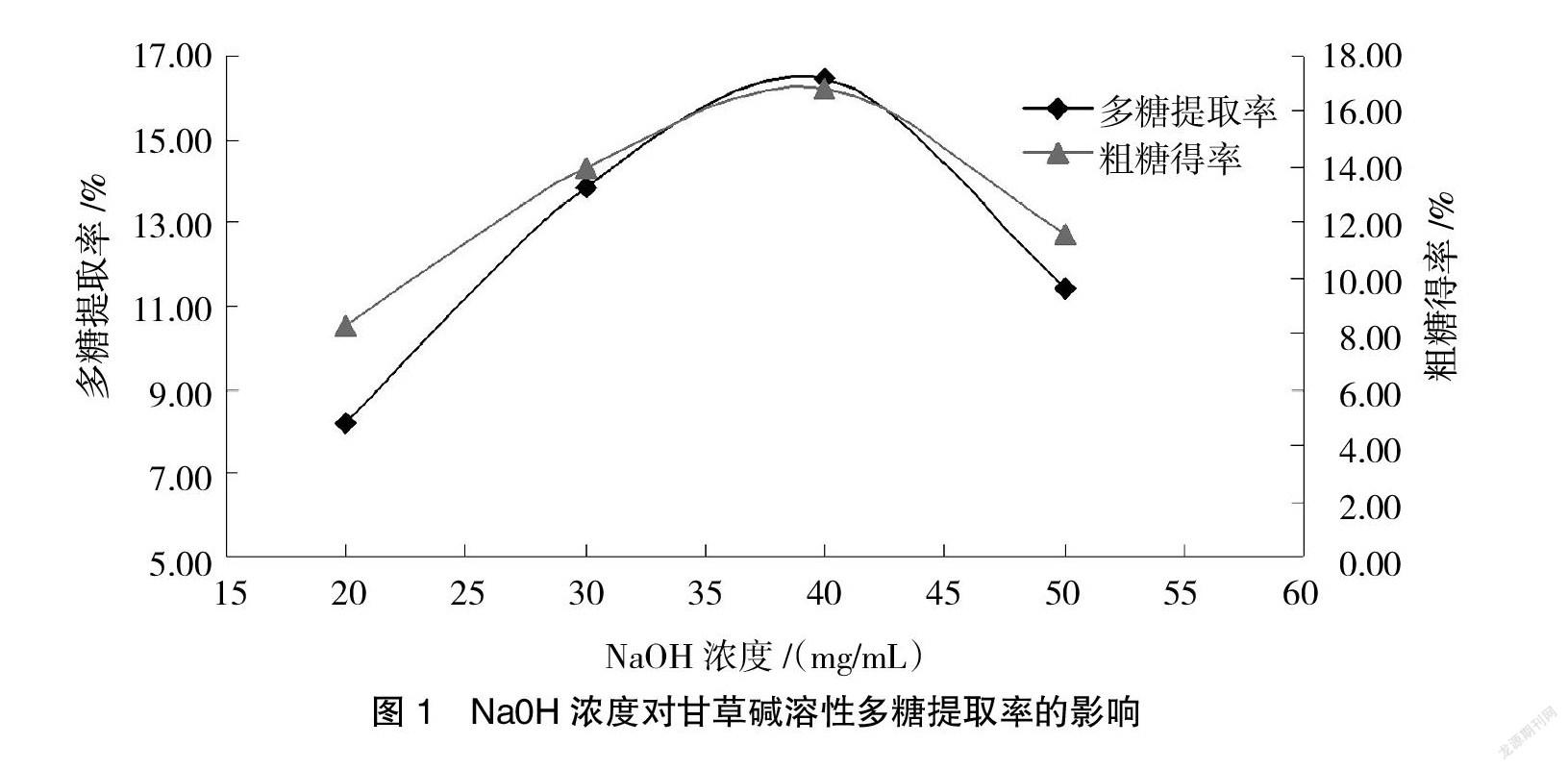
3.1 NaOH浓度对甘草碱溶性多糖提取的影响
由图1可知,NaOH浓度对甘草碱溶性多糖提取率、粗糖得率有一定影响,随着NaOH浓度升高,甘草碱溶性多糖的提取率及粗糖得率也不断升高,在水平3(40 mg/mL)时达到最大值,此后随着NaOH浓度的升高,多糖提取率及粗糖得率反而下降。这可能是因为NaOH浓度的升高使pH值发生了变化,导致部分多糖的支链结构受到破坏,溶于碱的特性消失,目标产物的提取率及得率降低。因此,将NaOH浓度最佳水平确定为40 mg/mL。
3.2 料液比对甘草碱溶性多糖提取的影响
由图2可知,料液比对甘草碱溶性多糖提取率、粗糖得率有一定影响,料液比达到水平2(1∶20)时,甘草碱溶性多糖提取率及粗糖得率均基本达到最大值,此后料液比重和多糖提取率及粗糖得率呈反比。
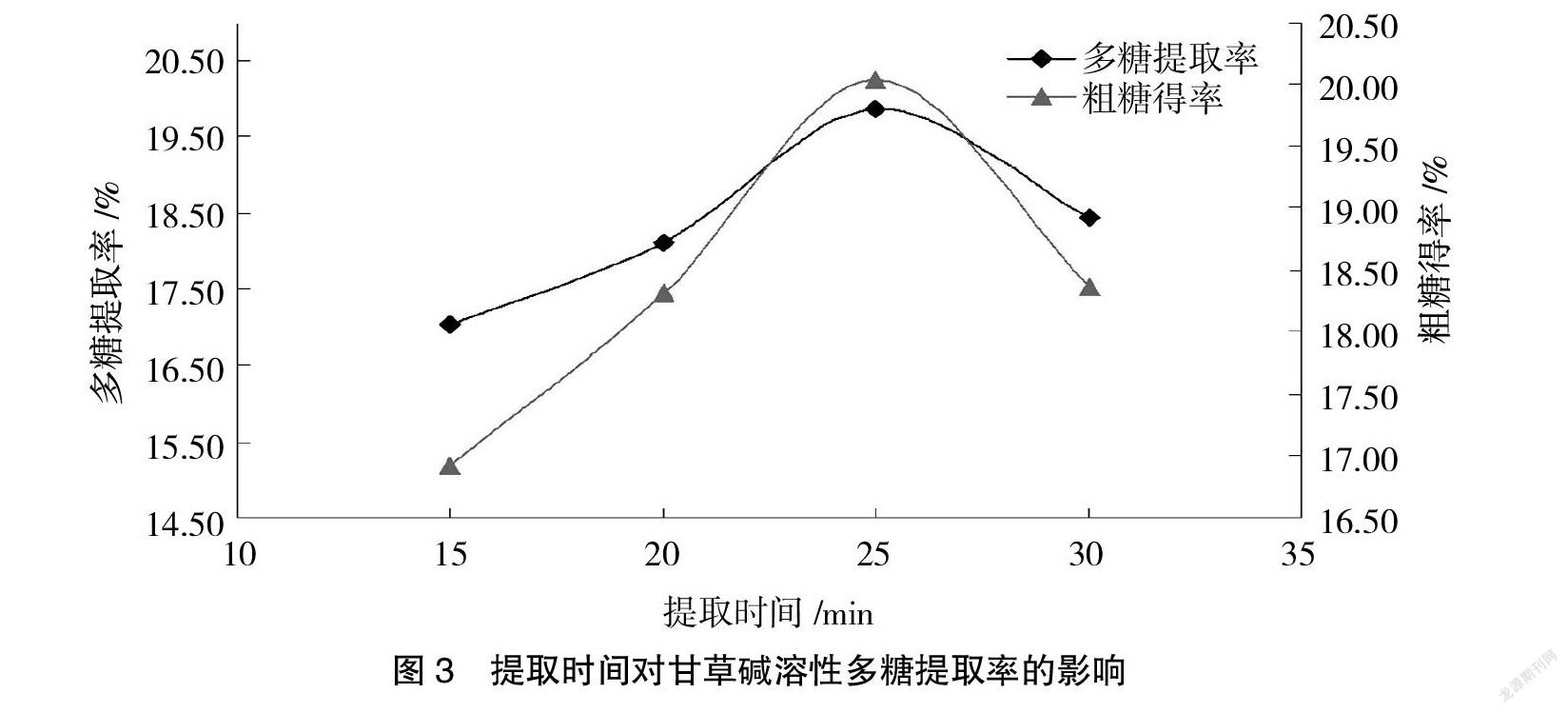
3.3 提取时间对甘草碱溶性多糖提取的影响
由图3可知,提取时间对甘草碱溶性多糖提取率、粗糖得率有一定影响,提取时间在水平3(25 min)时多糖提取率、粗糖得率达到最大值,此后随着时间延长,多糖提取率及粗糖得率反而下降。这与超声波长时间的机械作用会破坏多糖结构有关。
3.4 提取温度对甘草碱溶性多糖提取的影响
由图4可知,随着提取温度升高,甘草碱溶性多糖的提取率及粗糖得率也不断升高,在水平3(45 ℃)时达到最大值,此后随着温度升高,多糖提取率及其得率反而下降。这与多糖的热不稳定性有关。
4 讨论与结论
超声波提取试验中呈现了过程简易、耗时短、提取率高的特点,达到了以尽量少的试验达到较好结果的目的。
本试验研究了超声法提取甘草碱溶性多糖的主要条件,即NaOH浓度、料液比、提取时间、提取温度。通过单因素试验确定了甘草碱溶性多糖的最佳提取条件为NaOH浓度40 mg/mL、料液比1∶20(vol)、提取时间25 min、提取温度45℃。然而,本试验并未考虑到4个因素之间的交互作用,需要重新设计试验。考虑到4个因素的2阶以及所有的交互作用,应该选取更多因素水平设计试验,选出试验因素的最优理论值,再通过试验验证,检验优化条件下甘草碱溶性多糖的提取率及其粗糖得率是否与理论预测值接近。若与理论预测值接近,则说明所得到的回归模型就是最终模型。若与理论预测值相差较大,则说明所得到的回归模型并非最终模型,还需要重新设计试验进一步研究。
参考文献:
[1]王学宏.中药多糖的免疫及抗肿瘤作用研究进展[J].齐鲁医学杂志,2000,15(3):230-233.
[2]惠寿年,童阿玲.国内对甘草化学成分的研究进展[J].中药学,1999,30(4):313-315.
[3]刘霞,谢建新,李艳.甘草多糖的超声提取及含量分析[J].西北药学杂志,2004,19(2):60-61.
[4]高麗娟,田晓燕.甘草残渣中多糖的分光光度法测定[J].宁夏大学学报(自然科学版),2002,23(2):182.749DCE71-6172-4D11-81F1-586C28A1D95A
