APRI评分对HELLP综合征预测价值
2022-04-29王美蓉徐琳高林
王美蓉,徐琳,高林
(1 青岛大学附属医院产科,山东 青岛 266003; 2 高密市人民医院产科)
HELLP综合征是一种罕见、严重的妊娠期高血压疾病并发症,以溶血、肝酶升高、血小板减少为特点,可导致母体多器官功能障碍综合征、弥散性血管内凝血(DIC)、肝梗死或出血、肺水肿、肾衰竭等,对围生儿的影响主要表现为胎儿窘迫、胎儿生长受限、早产等。国外文献报道,HELLP综合征在妊娠期女性发病率为0.17%~0.85%,孕妇和胎儿病死率高达23.1%~56.9%[1]。国内文献报道HELLP综合征发病率明显低于国外,仅占重度妊娠期高血压疾病的2.7%[2]。HELLP综合征通常发生在孕28~36周,约85%的病人伴有高血压和蛋白尿[3]。HELLP综合征临床表现缺乏特异性,确诊主要依靠血小板降低和肝酶升高等实验室检查结果。天冬氨酸氨基转移酶与血小板比值指数(APRI)是指天冬氨酸氨基转移酶(AST)和血小板计数(PLT)的比值指数。APRI评分整合了AST和PLT两个变化趋势相反的临床指标,目前主要用于慢性乙型肝炎或乙醇性肝病病人肝硬化的评估[4]。HELLP综合征同样存在AST的升高和PLT的降低,APRI评分能否用于HELLP综合征的预测,国内尚无相关研究。本研究旨在评估APRI评分对HELLP综合征的预测价值。
1 资料与方法
1.1 研究对象
选取青岛大学附属医院2016年12月—2018年12月收治的50例HELLP综合征病人作为试验组,入组病人均产前发病,平均发病孕周为(30.14±5.29)周;选取年龄相似(与试验组病人的年龄相同或者上下浮动1岁)并且孕周相同的健康孕妇50例作为对照组。纳入标准:①HELLP综合征病人符合2020年我国《妊娠期高血压疾病诊治指南》的诊断标准[5];②病历资料完整。排除标准:妊娠合并慢性高血压、妊娠期糖尿病、妊娠合并乙型肝炎、妊娠期肝内胆汁淤积症及其他合并疾病。本研究经青岛大学附属医院伦理委员会批准。
1.2 观察指标
观察两组孕妇的年龄以及部分实验室检查指标:血红蛋白(HGB)、PLT、AST、丙氨酸氨基转移酶(ALT)、肌酐(Cr)、血浆凝血酶原时间(PT)和D-二聚体、活化的部分凝血活酶时间(APTT)。通过AST和PLT计算APRI评分。
1.3 统计学方法
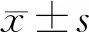
2 结 果
2.1 两组孕妇各观察指标比较
试验组PLT、ALT、AST、Cr、APTT、D-二聚体和APRI评分与对照组比较,差异均具有统计学意义(t=-7.903~16.022,P<0.05);两组年龄、HGB、PT比较差异无显著性(P>0.05)。见表1。
2.2 HELLP综合征危险因素的Logistic回归分析
单因素Logistic回归分析显示,ALT、AST、Cr、APRI评分、APTT、D-二聚体是HELLP综合征的危险因素。在多因素Logistic回归分析中建立APRI模型和AST模型,分别将HGB、ALT、Cr、APTT纳入两个模型中进行多因素回归分析,结果显示,APRI评分、AST分别是APRI模型和AST模型的独立危险因素。且APRI评分的OR值大于AST,提示与AST相比,APRI评分异常时病人发生HELLP综合征的风险更高。见表2。
2.3 ROC曲线分析
APRI评分的ROC曲线下面积(AUC)为0.947,95%CI为0.904~0.990;AST的AUC为0.853,95%CI为0.773~0.934,APRI评分的预测价值较AST更加显著(Z=2.02,P=0.043)。当AST取值为45 U/L时,其预测HELLP综合征的灵敏度为72.0%,特异度为90.0%。APRI评分预测HELLP综合征的界值为0.561 9分,此时其诊断灵敏度为88.0%,特异度为90.0%。见图1。
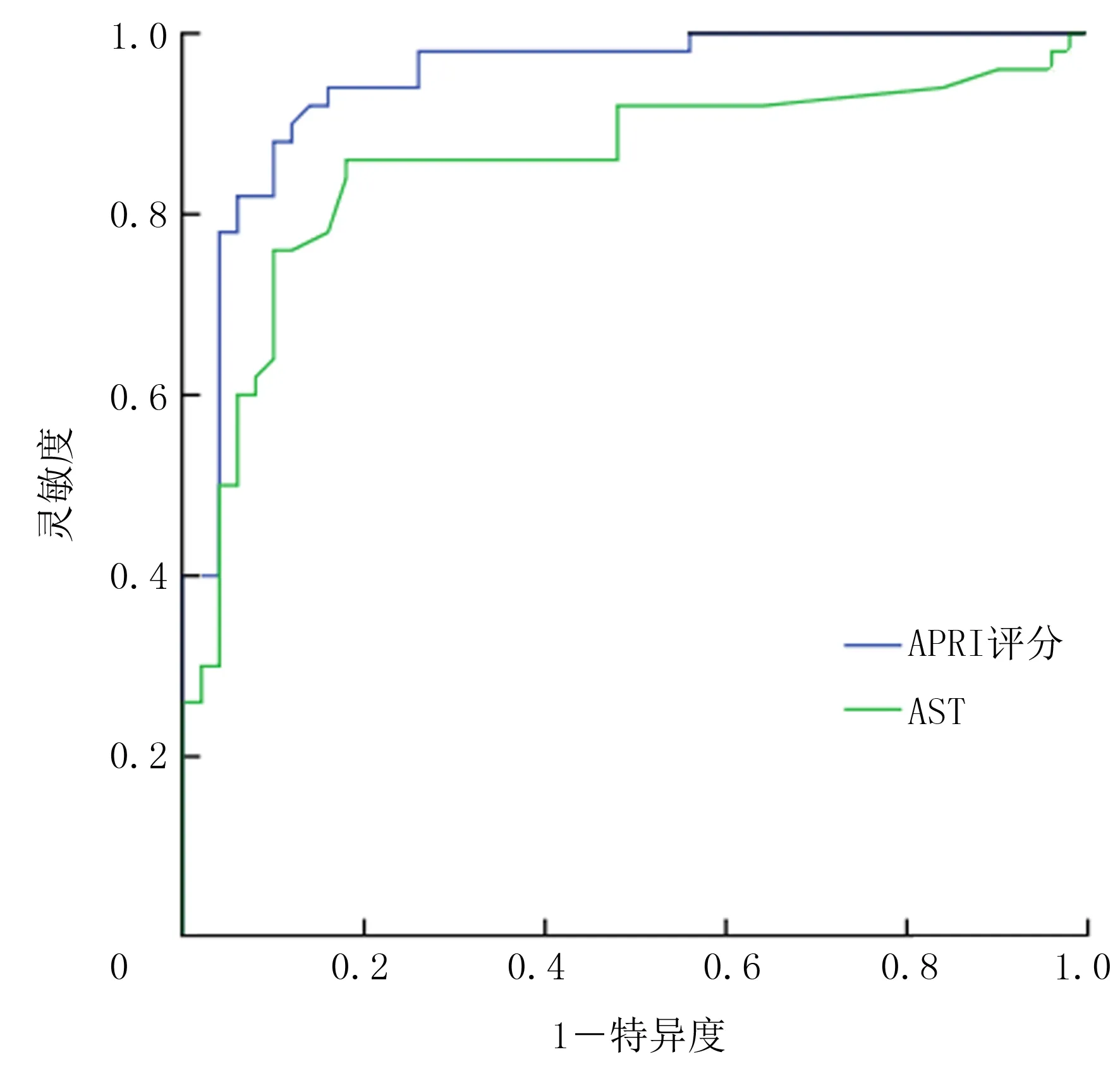
图1 APRI评分和AST预测HELLP综合征的ROC曲线
3 讨 论
HELLP综合征的发病机制目前尚不完全清楚,临床表现缺乏特异性,难以根据症状预测疾病的进展。基于实验室指标、影像学检查的早期预测和预警是HELLP综合征临床研究的方向之一。常见的血清学预测指标主要有AST、ALT和PLT等。

表1 两组孕妇各观察指标比较
李霞等[6]研究发现,炎症因子如白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)等与HELLP综合征存在相关性,可作为临床监测的指标。
肝酶升高是HELLP综合征的主要表现之一。AST、ALT都是反映肝细胞受损指标,而AST还可反映红细胞溶血情况。目前研究发现,HELLP综合征病人肝损伤启动于功能失调胎盘分泌的各种因子[7]。过度分泌的胎盘因子可引起肝窦毛细血管化和肝窦内皮细胞肿胀、凋亡,导致肝窦血流受阻、肝小叶缺血坏死,从而使肝功能受损。本研究中,试验组病人AST、ALT水平较对照组均明显升高,单因素Logistic回归分析显示AST、ALT皆为HELLP综合征的危险因素。AST模型多因素Logistic回归分析显示,AST为HELLP综合征的独立危险因素;ROC曲线分析显示,当取值为45 U/L时,AST预测HELLP综合征的灵敏度为72.0%,特异度为90.0%。
PLT下降是诊断HELLP综合征的必要条件。有研究表明,子痫前期病人存在血小板的过度消耗,推测原因可能为活化血小板黏附、聚集于受损血管内皮,导致血小板周转率增加、寿命缩短,使PLT下降[8]。妊娠期胎盘分泌的半乳糖凝集素(Gal-1)可触发多种血小板的激活反应,如诱导P选择素和GPⅢa表达,触发血小板GPⅡb/Ⅲa构象改变和F-肌动蛋白聚合。JESCHKE等[9]发现,HELLP综合征病人胎盘Gal-1存在过度表达,早发性HELLP综合征病人全身Gal-1水平与PLT存在显著负相关性[9-10]。
APRI评分是由WAI等[11]基于慢性丙型肝炎病毒(HCV)感染者常规实验室数据设计的用于预测HCV相关肝纤维化和肝硬化的新指标。近年来研究发现,APRI评分作为一种无创筛查指标,还可用于慢性乙型肝炎、儿童肝移植和非乙醇性脂肪肝病人肝纤维化的预测[12-15]。目前国外将APRI评分用于HELLP综合征预测的研究尚较少,AMAZ等[16]研究表明,APRI评分可以作为HELLP综合征的预测指标(AUC=0.927,95%CI=0.879~0.960),预测HELLP综合征的界值为0.339分(灵敏度为82.6%,特异度为87.6%)。国内尚无该方面的研究。在本研究中,试验组APRI评分明显高于对照组,APRI模型多因素Logistic回归分析显示,APRI评分为HELLP综合征的独立危险因素。与AST相比,APRI评分异常时病人发生HELLP综合征的风险更高。ROC曲线分析显示,APRI评分预测效果优于AST(AUC分别为0.947和0.853),APRI评分预测HELLP综合征的界值为0.561 9分(灵敏度为88.0%,特异度为90.0%)。
D-二聚体是纤维蛋白的降解产物,反映体内凝血和纤维蛋白溶解的水平。正常妊娠会改变孕妇体内凝血-纤溶系统平衡,导致D-二聚体水平升高[17]。
GUTIÉRREZ等[18]通过研究重新界定了孕期D-二聚体的正常参考值:孕早期为0.169~1.202 mg/L,孕中期为0.393~3.258 mg/L,孕晚期为0.551~3.333 mg/L。本研究中健康孕妇孕晚期D-二聚体的水平为(1.98±1.13)mg/L,在上述正常参考值范围内,而试验组病人D-二聚体水平高于上述参考值范围。KUCUKGOZ GULEC等[19]认为,子痫前期病人D-二聚体的升高可反映器官内皮细胞功能的障碍。MARCQ等[20]研究表明,HELLP综合征病人D-二聚体水平明显高于单纯子痫前期病人,但D-二聚体不能用于HELLP综合征的预测。本研究中试验组D-二聚体水平明显高于对照组,差异有统计学意义;单因素Logistic回归分析显示,D-二聚体是HELLP综合征的危险因素。但纳入多因素回归分析表明,D-二聚体不是HELLP综合征的独立危险因素。虽然本研究中未显示D-二聚体对HELLP综合征的预测价值,但它仍可作为HELLP综合征发生风险的监测指标。
综上,APRI评分对HELLP综合征有一定预测价值,且其预测价值优于AST。但本研究为单中心研究,病例数相对较少,结果可能存在局限性。后续研究将纳入多中心、大样本病例进行分析,以进一步明确APRI评分对HELLP综合征的预测价值。
