益肾祛痰活血法治疗血管性痴呆的有效性与安全性评价*
2022-04-28董新刚芦锰赵云李伟峰
董新刚,芦锰,赵云,李伟峰,3
1.河南中医药大学第一附属医院,河南 郑州 450000;2.河南中医药大学,河南 郑州 450046;3.河南中医药大学第三附属医院,河南 郑州 450008
作为痴呆的第二大类型疾病,血管性痴呆极有可能伴随人口老龄化进程不断加剧和脑血管病发病率持续攀升,逐步取代阿尔茨海默病成为老年性痴呆的最大发病因素和严重威胁中老年人身心健康的重大疾病之一[1]。目前,西医治疗血管性痴呆以干预危险因素,改善脑组织代谢循环和影响胆碱能系统的药物为主,但价格昂贵、针对性不强、不良反应多、服用周期长、治疗效果欠佳等问题却普遍存在。中医药在延缓痴呆发展进程,提高生存质量方面独具特色和优势。第五批全国名老中医药专家学术经验继承工作指导老师黎少尊针对本病提出了“三元络脑”学说[2],认为本病发生发展与肾虚、痰浊、瘀血密切相关[3]。
本研究以文献研究为基础,运用Cochrance系统评价方法,对益肾祛痰活血法治疗血管性痴呆开展系统评价,为中医药防治血管性痴呆提供循证依据。
1 资料与方法
1.1 纳入标准临床试验设计:临床随机对照试验或虽未说明具体方法但有随机字样的临床试验。诊断标准:中医参照《血管性痴呆的诊断、辨证及疗效判定标准》[4]、《中药西药临床研究指导原则》中呆病的诊断标准;西医参照中华医学会神经分会制定的《血管性痴呆诊断标准》等,符合以上中西医标准之一者。干预措施:对照组为西药常规治疗、空白对照组或相类似者。试验组给予益肾祛痰活血类方药或联合西药治疗,剂型不限;益肾祛痰活血法界限:文献中明确提出以益肾祛痰活血为主要治疗方法,处方按照益肾祛痰活血法组成。结局指标:临床疗效判定、简易精神状态评价量表(simplified mental state assessment scale,MMSE)、日常生活能力量表(activities of daily living,ADL)、长谷川痴呆量表(Hasegawa dementia scale,HDS)、Blessed行为量表(Blessed behavior scale,BBS)及安全性指标。研究对象不受种族、国籍、性别、年龄限制。
1.2 排除标准研究对象不明确、其他痴呆类型及认知功能障碍者;动物实验、系统评价等非临床试验和临床设计非随机对照者;临床试验设计存在明显缺陷/错误及无法提取数据者;重复发表及一稿多投者。
1.3 检索策略通过计算机检索数据库,中文医学数据库:中国知网、万方数据库、中国生物医学文献数据库和维普中文科技期刊全文数据库;外文医学数据库:Embase、Cochrance Library及PubMed,检索日期均从建库之日起至2020年6月30日。中文检索词为“益肾/益肾/温肾/滋肾”“祛瘀/化瘀/活血/逐淤/消瘀/通瘀”“化痰/祛痰/逐痰/涤痰/理痰” “血管性痴呆”“卒中后痴呆”“多发梗死性痴呆”“小血管性痴呆”和“出血性痴呆”等,英文检索词为“Tonifying Kidney,Removing Phlegm and Blood Stasis”“vascular dementia”“post-stroke dementia”“multi-infarct dementia” “small-vessel dementia” “hemorrhagic dementia”等,检索词包含但不仅限于以上词语。根据不同数据库需求,使用主题词检索与自由词检索结合策略完成检索。
1.4 筛选评价NoteExpress(3.4.0.8879版)完成文献查重。依据纳排标准,在文献评价人员各自独立完成文献初筛和交叉核对后,将分歧文献交由高级评价人员研判决定。根据Cochrance协作网系统评价手册(5.3)推荐的偏倚风险评估工具实施评价。GRADE(3.2版)软件完成结局指标证据等级评估。
1.5 统计学方法应用Cochrance协作官方网站提供的RevMan 5.3软件进行数据处理。计量资料采用WMD/SMD表示,计数资料采用RR/OR表示,各效应均数CI值控制在95%以内;采用χ2检验和I2统计评价纳入文献异质性,异质性小,利用固定效应模型分析;异质性大,根据异质性产生原因,确定是否采用随机效应模型进行分析。漏斗图型分析偏倚性。
2 结果
2.1 文献检索查重后剔除重复文献2 365篇,初步获取文献1 546篇;通过阅读篇名、题录及摘要进行筛选,初步纳入文献93篇;根据纳入、排除标准,通过阅读全文最终纳入文献15篇。
2.2 基本特征本研究共纳入益肾祛痰活血法治疗血管性痴呆15项研究,共纳入患者1 345例,其中治疗组623例,对照组722例。各研究在性别、年龄、疗程等方面比较,差异无统计学意义(P>0.05),基线平稳,具有可比性,见表1。两项研究报道脱落情况[7-8]。

表1 纳入研究文献的基本特征
2.3 文献质量评价纳入15项研究,8项研究[6-9,11-14]描述了随机分配序列,其中7项采用了随机数字表法,1项采用了随机抽样法[6],质量评价为低偏倚风险;其余7项未明确描述随机分配方法,偏倚风险不清楚。有两项研究报告实施双盲[8,13],且使用模拟安慰剂;1项研究采用分配隐藏[8],其余研究对分配方案隐藏描述不清楚;1项研究[13]提及安全性指标,但缺失数据结果,完整性存在高偏倚风险;所有研究均具体描述干预措施。文献方法学质量评价具体描述见表2,偏倚风险评估见图1。

表2 纳入研究文献方法学评价表

图1 文献偏倚风险图
2.4 Meta分析
2.4.1 MMSE量表14项研究[5-15,17-19]观察了临床疗效指标,共涉及1 252例患者。异质性检验显示,P<0.000 01,I2=91%,研究间统计学异质性大,故应用随机效应模型,Meta分析显示,与对照组比较,治疗组能够提高MMSE量表,差异具有统计学意义[MD= 2.76,95%CI(1.56,3.97),P<0.000 01],详见图2。
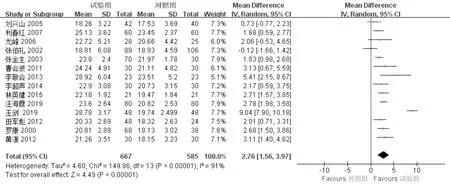
图2 MMSE量表的Meta分析
应用敏感性分析探寻异质性来源,删除文献[5]后,其余文献异质性降到I2=48%,提示此文献可能为异质性主要来源。分析该文献发现,治疗组中使用自拟益气活血化痰法中药联合健脑益智颗粒,干预药物不同是其产生异质性来源。敏感性分析见图3。漏斗图不对称,提示本次结果可能有发表偏倚,见图4。
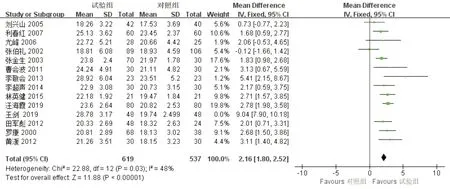
图3 MMSE量表敏感性分析
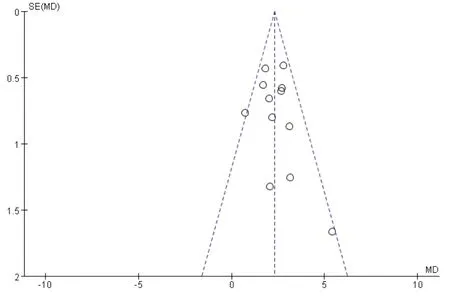
图4 MMSE量表的Meta分析漏斗图
2.4.2 ADL量表10项研究[5-6,7,9-12,14,16,19]报道了ADL量表指标,其中7项研究[4-5,7,9-11,19]采用同一标准评价,涉及575例患者。异质性检验显示,各个研究之间异质性大(P<0.000 01,I2=98%),运用随机效应模型合并Meta分析显示,在降低ADL评分方面,试验组明显优于对照组,两组差异具有统计学意义[MD=-6.53,95%CI(-10.41,-2.66),P<0.000 01],见图5。
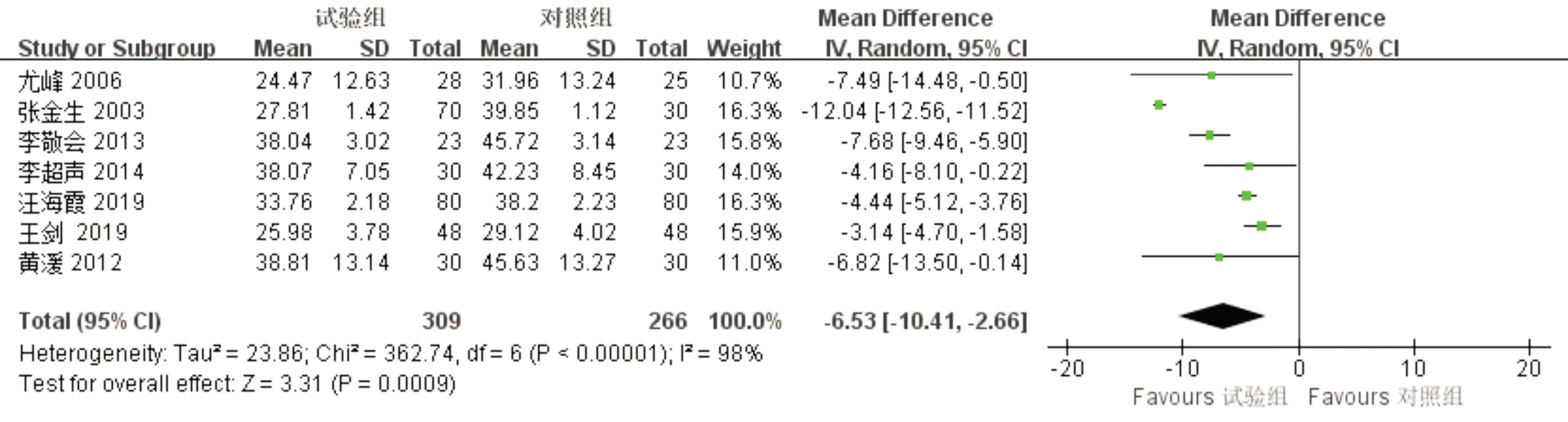
图5 ADL量表的Meta分析
按照不同疗程分亚组,比较各研究间质异性:①疗程≥60 d组,共纳入研究5项,各研究之间异质性无明显差异(P=0.46,I2=0%),Meta分析表明,在降低ADL评分方面,治疗组优于对照组,两组差异有统计学意义[MD=-4.28,95%CI(-4.89,-3.66),P<0.000 01];②疗程<60 d组,共纳入研究两项,两项研究异质性差别较大(P<0.000 01,I2=95%),对随机效应模型进行Meta分析显示,在降低ADL评分方面,试验组与对照组比较,差异具有统计学意义[MD=-9.95,95%CI(-14.22,-5.68),P<0.000 01],见图6。
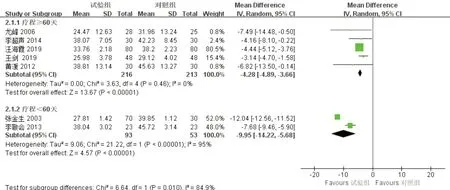
图6 ADL量表亚组分析
2.4.3 临床疗效8项研究[5,7-8,10,12-13,16,18]报道了临床疗效,异质性检验显示I2=12%,运用固定效应模式合并分析:在临床疗效的有效率方面,试验组优于对照组,差异具有统计学意义[RR=1.22,95%CI(1.12,1.34),P<0.000 01],见图7。
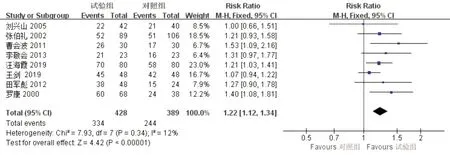
图7 临床疗效的Meta分析
2.4.4 HDS量表4项研究[6,12,14,19]报道了HDS量表指标,经异质性检验,各研究间异质性明显(P<0.000 01,I2=89%),采用随机效应模型合并分析,Meta分析结果显示,试验组可提高HDS量表评分[MD=3.04,95%CI(1.50,4.58),P=0.000 01],见图8。

图8 HDS评分的Meta分析
按照药物疗程不同,分亚组比较各研究间质异性:疗程≥60 d组,纳入研究两项,各研究之间异质性无明显差异(P=0.64,I2=0%),Meta分析表明,在提高HDS评分方面,试验组优于对照组,两组差异具有统计学意义[MD= 4.83,95%CI(3.85,5.80),P<0.000 01];疗程<60 d组纳入研究两项,两项研究异质性差异较大(P<0.000 01,I2=83%),对随机效应模型进行Meta分析显示,在提高HDS评分方面,试验组与对照组比较,差异具有统计学意义[MD= 1.86,95%CI(0.39,3.34),P=0.01],见图9。

图9 HDS评分亚组分析
2.4.5 BBS量表两项研究[8,13]报道了BBS量表指标。异质性检验显示,I2=75%,运用随机效应模式合并分析:在改善BBS方面,试验组与对照组比较,差异无统计学意义[MD=-0.19,95%CI(-2.34,1.96),P=0.0.86],见图10。

图10 BBS量表的Meta分析
2.4.6 安全性指标所有研究中,共有8项研究[7-8,11-13,16-18]报道了安全性指标,两项研究[7-8]报道了治疗后安全性指标无异常改变,其他6项[11-13,16-18]未报道治疗后安全性指标。两项研究[12,16]提到各组均有恶心、眩晕、头痛等不良事件发生,但不影响试验研究进程,且组间比较,差异无统计学意义(P>0.05),这提示临床应用安全性较好,见表3。

表3 不良反应发生情况
2.4.7 证据评价应用GRADE(3.2)对纳入本研究结局指标实施证据评价,主要依据研究局限性、结果不一致性、间接证据、结果不确定性、报告偏倚等5个方面进行评价,评价结果显示:结局指标的证据质量评级多为低级或极低级,见表4。

表4 GRADE证据评价
3 讨论
血管性痴呆属中医学“健忘”“呆病”“痴呆”等疾病的范畴。中医对其早有认识。如《灵枢·海论》提出:“髓海不足,则脑转耳鸣,胫酸眩冒,目无所见,懈怠安卧。”认为痴呆与肾精亏虚,髓海不足有关。《血证论》又载:“又凡心有瘀血,亦令健忘……凡失血家猝得健忘者,每有瘀血。”“若血瘀于内,而善忘如狂……”明确了瘀血与健忘、善忘有关。清代《辨证录·呆病门》《石室秘录·呆病治法》等书中则重点阐述痰与痴呆的关系,并记载了转呆丹、洗心方、还神至圣汤等方剂。黎少尊教授认为,血管性痴呆病位在脑,为本虚标实之证,即以肾精亏虚为主,以痰、瘀为标,肾虚、痰浊、瘀血互结,阻络损髓贯穿疾病始终,肾虚、痰浊、瘀血为本病的基本病机,这与部分学者观点相近[20-21]。故本研究对以益肾活血祛痰法治疗血管性痴呆的疗效及安全性开展系统性评价。
本次评价结果显示,从干预效果方面看,本次纳入的15项研究,MMSE评分在剔除王剑等[5]研究后异质性明显降低,能提高量表评分;同时,在降低ADL量表评分,提升HDS量表评分,提高临床疗效等方面,治疗组均优于对照组,说明与单纯西药相比,单独应用益肾活血祛痰中药或联合西药常规治疗,在改善MMSE、ADL、HDS量表评分,提高临床疗效等方面优势明显,可有效改善血管性痴呆患者的临床症状。另外,BBS量表Meta分析显示,差异无统计学意义(P>0.05),考虑可能与本次评价纳入的研究较少有关。从干预时间上看,除MMSE评分和临床疗效外,ADL评分及HDS评分在药物干预疗程上均显示异质性。进行亚组分析,当干预时间≥60 d时,各研究间的异质性不明显;当干预时间<60 d时,各研究间的异质性大,提示疗程与治疗效果密切相关,疗程越长,患者的获益度越高。从安全性指标及不良事件发生方面看,本次评价共有8项研究报告了安全性指标,两项研究[7-8]报告了最终结果,即安全性指标无变化;两项研究报告了不良事件,其中田军彪等[12]的研究为对照组发生不良事件,曹会波等[16]的研究虽然治疗组也发生了不良事件,但其发生率明显低于对照组,且两项研究均不影响研究实施,提示应用益肾活血祛痰法治疗血管性痴呆安全可靠,不良事件发生率低。
本次系统评价的局限性:本次评价未能纳入外文文献,可能存在纳入文献遗漏情况。文献质量评价显示,本次纳入的15项研究中,有7项研究未提随机方法,仅有两项研究报告了实施双盲,1项进行分配隐藏,1项存在数据缺失情况;证据质量GRADE评级结果提示,结局指标多被评为低级或极低级,这都在一定程度上影响了本次研究的证据强度。本次研究纳入近几年发表的文献较少,采用当时最新公认的诊断标准不多,疗效评价单一,公信度较高的结局指标采用较少,对安全性指标重视不够。另外,一些研究干预时间短,影响了对中药长期疗效的评判和对患者生存质量的评估。
综上,益肾活血祛痰法能明显改善血管性痴呆患者MMSE、ADL、HDS等量表评分,有效提高临床疗效;该治法安全可靠,不良事件发生率低,如能适当延长中药干预时间,血管性痴呆患者可能获益更佳。同时,在今后的研究中,如能进一步规范试验设计,有效控制偏倚,高质量地开展临床试验并规范研究报告,必将能得出证据等级更高的研究结论。
