三七粉血清药物化学研究*
2022-04-26刘耀晨王德勤张洪兵郭海彪韩彦琪张铁军
刘耀晨,王德勤,张洪兵,郭海彪,韩彦琪,林 娟,张铁军,5**,许 浚,5**
(1.天津医科大学药学院 天津 300070;2.广州白云山和记黄埔中药有限公司 广州 510515;3.天津药物研究院天津市中药质量标志物重点实验室 天津 300301;4.天津药物研究院中药现代制剂与质量控制技术国家地方联合工程实验室 天津 300301;5.天津药物研究院释药技术与药代动力学国家重点实验室 天津 300301)
三七为五加科人参属植物三七Panax notoginseng(Burk.) f.H.Chen 的干燥根和根茎,收载于《中国药典》,传统功效为活血化瘀、消肿止痛[1]。三七中以皂苷类有效成分为主,还含有多种非皂苷类成分,如糖类、氨基酸、黄酮类等[2]。三七粉是将三七药材经粉碎而成,作为中药饮片主要用于外伤出血、胸腹刺痛及跌扑肿痛等[3]。三七粉的质量标准主要参考《中国药典》,但现行《中国药典》质量标准仅规定了三七粉中人参皂苷Rg1、Rb1及三七皂苷R1的含测总量[1],相关研究表明,三七皂苷成分主要与活血、抗炎、免疫调节、神经保护等药理作用相关[4-10]。因此,现行标准不能真正反映三七粉质量与疗效的关系。
为解决我国中药质量标准存在的问题,刘昌孝院士提出中药质量标志物(Q-Marker)的概念,明确了QMarker 的基本条件,Q-Marker 研究应对中药有效成分的传递和转化过程进行研究[11,12]。三七粉以口服用药的形式通过体内传输发挥临床疗效,化学物质基础经过质量传递和代谢转化后体现出其特有的生物效应。入血成分及其代谢产物是三七粉最终的“效应成分”。从质量传递与溯源的角度,血中的效应成分是质量传递体系的最终环节,也是中药质量标志物确定的重要依据[13]。因此,必须明确三七粉体外化学成分组-体内血行成分组的传递-转化过程,为三七粉药效物质基础的传递过程提供清晰的路径。目前三七皂苷成分表征及单体皂苷的代谢转化研究已有报道[14-20],但缺乏三七粉化学物质组及其体内血行成分组的表征。
本研究建立三七粉的化学指纹谱,运用液质联用技术对所含化学成分进行了全面分析;随后结合血清药物化学方法建立给药血浆的血行成分指纹谱,分析血中移行的原型药物成分及代谢物,明确体外化学成分组-体内血行成分组的药效物质基础传递-转化过程,为三七粉的质量标志物确定与全面质量控制提供依据。同时为课题组后期深入三七粉分子作用机制,从成分的“有效性”方面框定其质量标志物奠定基础。
1 仪器与试剂
1.1 主要仪器
Acquity UPLC 超液相色谱仪(美国Waters 公司);Xevo G2 Q-Tof 高分辨质谱(美国Waters 公司),配备ESI 离 子 源;Acquity UPLC BEH C18(2.1×100 mm, 1.7 μm)色谱柱(美国Waters 公司);HAC-Ⅰ自动浓缩氮吹仪(天津市恒奥科技有限公司);3K15高速冷冻离心机(德国Sigma公司)
1.2 试药
对照品人参皂苷Re(批号110754-201827)、人参皂苷Rd(批号111818-201603)、人参皂苷Rg1(批号110704-201827)、三七皂苷R1(批号10745-201820)均购于中国食品药品检定研究院,人参皂苷Rc(批号M29F11S109055)购自上海源叶生物科技有限公司,所有对照品质量分数均大于98%;色谱纯乙腈、甲醇和甲酸购自天津市康科德科技有限公司;纯净水购自杭州娃哈哈饮用水有限公司;三七粉购自广州白云山和记黄埔中药有限公司(批号YPA8L0006)。
2 方法
2.1 三七粉样品溶液制备
取三七粉1 g,精密称定,置具塞锥形瓶中,加入70%甲醇10 mL,超声提取20 min,重复2 次合并提取液,以70%甲醇稀释至25 mL,0.22 μm微孔滤膜滤过,即得三七粉样品溶液供检测分析。
2.2 三七粉大鼠灌胃溶液制备
取三七粉适量,加入羧甲基纤维素钠溶液制成混悬液,并稀释至浓度为0.3 g·mL-1,即得。
2.3 对照品溶液制备
精密称取适量人参皂苷Re、Rd、Rg1、Rc 和三七皂苷R1,置于量瓶中,加入甲醇,制备成0.1 mg·mL-1各对照品储备液;分别量取上述储备液适量,稀释,制备成均为10 μg·mL-1的混合对照品溶液。4℃下保存,进样前经0.22 μm微孔滤膜滤过。
2.4 含药血清制备与处理
2.4.1 给药与采血
雄性SD 大鼠(200±20 g),饲养1 周后,随机分为两组并称定体重,按1 mL/100 g的灌胃剂量,空白组给予羧甲基纤维素钠溶液,给药组灌以三七粉混悬液。
实验大鼠给药4 h 后以10%水合氯醛麻醉,肝门静脉取血置肝素化试管中,于4℃条件下3500 rpm 离心10 min分离血浆,置-20℃冰箱中保存备用。
2.4.2 血浆样品的处理
取大鼠血浆样品500 μL,加入甲醇,混匀,于4℃条件下13000 rpm 离心10 min,上清液使用N2吹干,残渣以甲醇复溶,离心吸取上清液供检测分析。
2.5 LC-MS分析
色谱分析采用Waters Acquity UPLC 液相色谱系统,色谱柱为Waters Acquity UPLC® BEH C18(2.1×100 mm,1.7 μm)柱,流动相系统由A(0.1%甲酸乙腈)和B(0.1%甲酸水溶液)组成,流速0.4 mL·min-1,柱温45℃,进样量5 μL。运用梯度洗脱,梯度程序设置如下:0-3 min,8%-20% A;3-6 min,20%-25% A;6-16 min,25%-40%A;16-22 min,40%-65%A;22-26 min,65%-75%A;26-27 min,75%-95%A。
质谱分析采用Waters Xevo G2 Q-Tof 高分辨质谱,配备电喷雾离子源(ESI),毛细管电压正离子模式3.0 kV,负离子模式2kV。离子源温度110℃,样品锥孔电压30V,锥孔气流速50 L·h-1,氮气脱气温度350℃,脱气流速800 L·h-1,扫描范围50-2000m/z,内参校准液亮氨酸脑啡肽用于分子量实时校正。
2.6 数据处理
2.6.1 三七粉化学成分鉴定
通过标准品参照、文献检索和数据库检索,对比分析正负模式下的MS、MS/MS 数据信息,结合保留时间、峰强度等对各色谱峰进行结构鉴定与确证,明确三七粉中所含的化学成分。
2.6.2 入血原型成分及代谢产物鉴定
通过比对三七粉样品、大鼠给药血浆及空白血浆样品的色谱图,结合标准品色谱图和文献检索,对比各色谱峰的MS、MS/MS 数据信息,对三七粉吸收入血的原型成分进行结构鉴定;进一步分析原型成分的裂解规律,结合碎片离子的特征中性丢失,比对相关代谢产物的MS、MS/MS质谱信息,对其结构进行鉴定,明确体内代谢途径。
3 结果与分析
3.1 三七粉样品分析
采用“2.5”项下优化的条件,对三七粉样品溶液进行检测分析,正、负离子模式下,三七粉样品及混合对照品的BPI 色谱图(图1-图2)。按照“2.6.1”项下数据处理方法确定化学成分结构,对三七粉主要化学成分进行表征,共鉴定得到54个化合物(表1),其中原人参二醇皂苷类36 个,原人参三醇皂苷类14 个,黄酮类1个,糖类1 个,氨基酸类1 个和酯类化合物1 个。

图1 三七粉BPI色谱图

图2 混合对照品负离子模式BPI色谱图

表1 三七粉化学成分LC-MS数据
3.1.1 皂苷类
三七粉中皂苷类化合物,结构中含有葡萄糖、鼠李糖等多个糖基取代,在质谱中容易逐级丢失产生一系列特征碎片离子,进一步断裂C-17 支链取代烷基,形成84 Da的特征中性丢失[16]。
原人参二醇型皂苷类化合物,以人参皂苷Rb1为例,其C-3 位和C-20 位羟基均有二糖取代,分别由两分子葡萄糖2→1 位相连和两分子葡萄糖6→1 位相连。在质谱中分子离子[M-H]-m/z1107连续丢失四分子葡萄糖,形成m/z945、m/z783、m/z621 的碎片离子及m/z459 的原人参二醇型皂苷元离子,进一步失去C-17 支链产生m/z375 的碎片离子,所得碎片信息与文献数据一致,MS/MS谱图见图3。
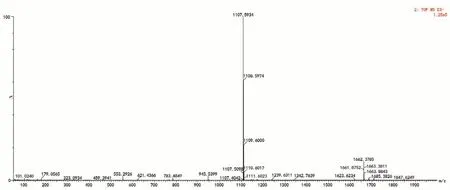
图3 人参皂苷Rb1的MS/MS谱图

续表
原人参三醇型皂苷类化合物,以三七皂苷R1为例,C-6 位羟基由一分子葡萄糖与一分子木糖2→1 位相连取代,C-20位羟基被一分子葡萄糖取代。在质谱中,[M-H]-m/z931的分子离子连续丢失一分子木糖和两分子葡萄糖,形成m/z799、m/z637 的碎片离子及m/z475 的原人参三醇型皂苷元离子,进一步断裂C-17烷基支链失去84 Da,产生m/z391的碎片离子所得,碎片信息与文献数据一致,MS/MS谱图见图4。

图4 三七皂苷R1的MS/MS谱图
3.1.2 氨基酸类
正离子模式下检测到三七素[M+H]+m/z177 的分子离子,丢失一分子NH3和H2O 产生m/z160 和159 碎片离子,m/z159 碎片离子丢失一分子CO 产生m/z131碎片离子,m/z160碎片离子可发生重排并丢失一分子CO2产生m/z116 关键碎片离子,所得碎片信息与文献数据一致[21],MS/MS谱图见图5。

图5 三七素的MS/MS谱图
3.1.3 黄酮类
正离子模式下检测到槲皮素[M+H]+m/z303 的分子离子,可丢失一分子H2O 形成碎片m/z285 碎片离子,继续丢失一个CO产生m/z257 碎片离子[22],所得碎片信息与文献数据一致,MS/MS谱图见图6。
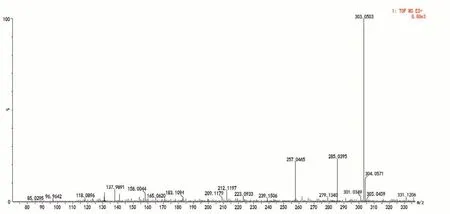
图6 槲皮素的MS/MS谱图
3.2 三七粉血浆样品分析
采用“2.5”项下优化的条件,对三七粉、大鼠空白血浆及给药血浆样品进行检测分析,负、正离子模式下,三七粉、大鼠空白血浆和给药血浆样品的BPI色谱图如图7、图8 所示。按照“2.6”项下数据处理方法确定化学成分结构,在给予三七粉的大鼠血浆中共鉴定得到14 个吸收原型药物成分和4 个代谢物(表2-表3)。

图7 负离子模式BPI色谱图

图8 正离子模式BPI色谱图

表2 三七粉吸收入血原型成分LC-MS数据

表3 三七粉大鼠血浆代谢物LC-MS数据
3.2.1 三七粉血浆样品代谢物鉴定
吸收入血的原型药物成分在体内不同药物代谢酶的作用下,经过Ⅰ相和Ⅱ相代谢反应,原型成分的化学结构和精确质量数都会被改变。然而,绝大多数代谢物仍然保留了其原型的结构特征,通过分析裂解规律来进行代谢物的鉴定。
M1在负离子模式下产生[M-H]-m/z475的分子离子及m/z391 的碎片离子,形成84 Da 的特征中性丢失,被鉴定为原人参三醇。M2 的在质谱图中具有与M1 一致的裂解行为,但其分子离子[M-H]-m/z473 比M1小2 Da,推测为脱氢原人参三醇。
M3在负离子模式下显示[M-H]-m/z459的分子离子,失去84 Da 产生了m/z375 的碎片离子,质谱裂解行为与原人参二醇一致,因此被鉴定为原人参二醇。
M4 在质谱图中显示[M+Na]+m/z645 的分子离子,正离子模式下丢失一分子葡糖糖和一分子水,产生[M+Na-glc-H2O]+m/z465 和[glc+H2O+Na]+m/z203 的碎片离子,经与文献比对鉴定为人参皂苷C-K[23]。
4 讨论
本研究中,采用UPLC-ESI-Q-TOF-MS/MS 的技术方法,优化液相色谱、质谱分离检测条件,建立三七粉指纹谱分析所含化学成分,经与标准品和文献数据比对,分析其质谱裂解规律,结果在三七粉样品中共鉴定得到54 个化学成分,以皂苷类化合物为主,包括原人参二醇皂苷类36 个,原人参三醇皂苷类14 个,黄酮类1个,糖类1个,氨基酸类1个和酯类化合物1个。
在三七粉化学成分研究的基础上,进一步建立给药血浆的血行指纹谱,通过比对三七粉、大鼠给药血浆及空白血浆样品的色谱图,筛选分析血中移行的原型药物成分及代谢物,结果在大鼠血浆中共鉴定得到18个三七粉相关的外源性化合物,包括14个吸收原型药物成分和4个代谢物。吸收原型药物成分中原人参三醇皂苷类有6 个分别为三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rh1、人参皂苷Rg2、人参皂苷F1;原人参二醇皂苷类有6 个,分别为人参皂苷Rb1、人参皂苷Rd、人参皂苷F2、人参皂苷Rg3、人参皂苷Rk1、三七皂苷Fa;氨基酸类成分有1个为三七素;黄酮类成分有1 个,为槲皮素。代谢物中原人参二醇和人参皂苷C-K 来源于原人参二醇型皂苷;原人参三醇和脱氢原人参三醇来源于原人参三醇型皂苷[24]。在给药大鼠血浆中检测到的吸收原型成分及其代谢产物可能是三七粉潜在真正的活性成分,并与三七粉的药理作用直接相关,为后期课题组进行三七粉传统功效的作用机制研究奠定基础,它们作为三七粉最终的“效应成分”可作为其质量标志物的候选。
