肝素钠对白蛋白检测的干扰实验分析
2022-04-23田国亮李有杰
田国亮,李有杰
(1.滨州医学院基础医学院,山东 烟台 264003;2.淄博市第一医院检验科,山东 淄博 255200)
目前检验科主要使用血清或者血浆标本来定量检测白蛋白浓度,如罗氏公司《白蛋白检测试剂盒说明书》中提到可以使用血清或者肝素锂、K2-EDTA血浆检测白蛋白;而贝克曼库尔特公司《白蛋白测定试剂盒(溴甲酚绿法)使用说明书》中提到仅可使用血清标本检测此项目。既往有报道显示[1-3],血浆标本与血清标本检测白蛋白的结果有差异。本研究根据中华人民共和国卫生行业标准WS/T 416-2013《干扰实验指南》文件,评价肝素钠对溴甲酚绿法检测人血清白蛋白的干扰效应,现将结果报道如下。
1 材料和方法
1.1 样本来源 收集淄博市第一医院2020 年12 月临床未使用肝素钠药物的患者的混合血清作为样本来源,根据《干扰实验指南》附录B:常见被测量的建议实验浓度和ALB的医学决定水平[4],共收集3 个浓度,分别为25、35 和50 g/L。
1.2 仪器和试剂 全自动生化分析仪(美国贝克曼库尔特有限公司,型号:AU5800);白蛋白测定试剂盒(美国贝克曼库尔特有限公司,批号AUZ8181)与配套校准物(批号1121M)。检测前仪器功能正常,质控在控。
1.3 干扰物储存液配制 取用肝素钠注射液(江苏万邦生化医药股份有限公司,规格:2 ml∶12 500 U),加去离子水8 ml 至溶液总容积为10 ml,使肝素钠浓度稀释为1250 U/ml[5]。
1.4 干扰物筛查实验(配对差异实验)
1.4.1 样本制备 ①基础样本:取ALB 浓度分别为25、35 和50 g/L的血清作为基础样本液;②测试样本:实验样本与对照样本制备方法见表1。实验样本中基础样本与干扰物储存液的比例为19∶1,其中肝素钠浓度为62.5 U/ml;对照样本中基础样本与生理盐水的比例为19∶1,其中肝素钠浓度为0 U/ml。

表1 实验样本与对照样本的制备(μl)
1.4.2 确定干扰判断标准 本实验基于ALB 总误差6%[6]的1/3,即2%偏倚作为最大允许干扰值dmax。
1.4.3 测定重复次数 依据《干扰实验指南》,计算出最大允许干扰值dmax与批内重复性标准差s的比值,其中s由基础样本重复检测20 次计算而得[7]。通过查表得出ALB 不同浓度水平的重复测定次数。
1.4.4 检测要求 为避免携带污染,将实验样本T和对照样本C 按交互顺序检测,中间插入额外检测的对照样本CX,标本按如下顺序检测:C1T1CXCXC2T2CXCX……CnTn。
1.4.5 数据处理与分析 ①干扰效果dobs的计算:干扰效果dobs=实验样本测定均值(xtest)-对照样本测定均值(xcontrol)[8];②计算临界值,式中dnull为无效假设的值,通常为0;s 为批内标准差,Z(1-α/2)为相对于双边检验100(1-α)%可信区间时正态分布的百分位点,n为重复测定次数。
1.5 干扰物剂量效应评价实验
1.5.1 样本制备 ①基础样本:取ALB 浓度分别为25、35 和50 g/L的血清作为基础样本液;②含不同剂量干扰物的测试样本:干扰物高实验浓度样本制备方法参见1.4.1 中实验样本的制备,其肝素钠终浓度为62.5 U/ml。干扰物低实验浓度样本的制备参见1.4.1中对照样本的制备,其肝素钠终浓度为0 U/ml;③将肝素钠终浓度为62.5 U/ml的测试样本与肝素钠终浓度为0 U/ml的测试样本,按照0∶4、1∶3、1∶1、3∶1、4∶0的比例进行配制,可得到肝素钠浓度依次递升的5 个浓度水平实验样本,具体制备方法见表2。

表2 肝素钠不同浓度水平样本的制备
1.5.2 测试重复次数 共测定5 次,排除方法精密度对结果的影响。
1.5.3 剂量效应分析 计算样本中肝素钠浓度为0 U/ml的实验样本的测定均值,用肝素钠浓度依次递升的5 个浓度水平实验样本的每个测定值减去此均值,得出不同肝素钠浓度水平下的干扰效果。以干扰效果为Y 值,肝素钠浓度为X 值,利用SPSS 24.0 软件描绘散点图。如果散点图上数据成近似直线走向,则用线性回归进行分析,计算回归方程;如果散点图上数据显示非线性,则使用非线性回归来评估干扰物的剂量效应。
2 结果与分析
2.1 干扰物筛查实验(配对差异实验)
2.1.1 重复次数的确定 3 个浓度基础样本20 次测定的ALB 均值分别为24.69、34.49、49.59 g/L,dmax分别为0.49、0.69、0.99 g/L,s分别为0.14、0.23、0.33;3 个浓度ALB的dmax/s 均≥3,确定测定次数均为3 次。
2.1.2 干扰效应分析 3 个浓度ALB的dobs分别为-1.1、-1.03、-0.77,dc分别为0.16、0.26、0.37,∣dobs∣>dc,表明3 个浓度下,62.5 U/ml的肝素钠对ALB 测定均存在干扰。
2.2 剂量效应实验 将干扰效果(Y)、干扰物浓度(X)等数据输入SPSS 24.0 软件中,绘制出干扰物剂量相关曲线。由曲线可知,肝素钠对3 个浓度下ALB 测定产生线性负干扰,见图1~图3;低、中、高3 个浓度ALB的线性回归方程结果显示,肝素钠在3 个ALB 浓度下均与干扰效果存在线性回归关系(t=7.100、12.280、4.130,P<0.001);代入线性公式计算得,在肝素钠浓度<3.19 U/ml 时不会对低浓度ALB 测定产生干扰;在肝素钠浓度<17.42 U/ml 时不会对中浓度ALB 测定产生干扰;在肝素钠浓度<30.86 U/ml 时不会对高浓度ALB 测定产生干扰。
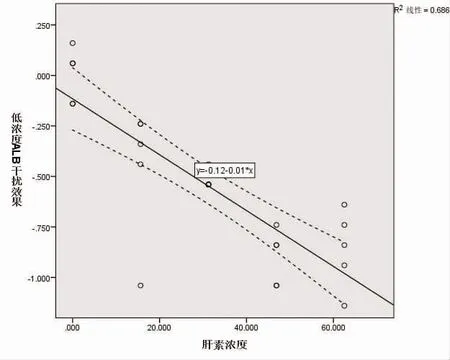
图1 肝素钠对低浓度ALB 干扰的剂量效应曲线
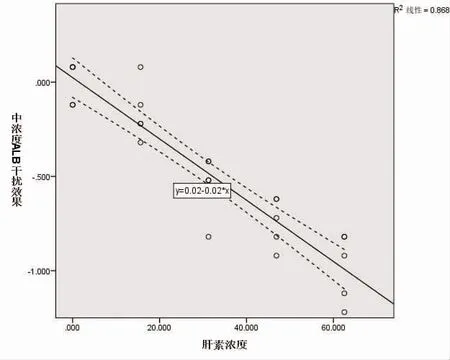
图2 肝素钠对中浓度ALB 干扰的剂量效应曲线
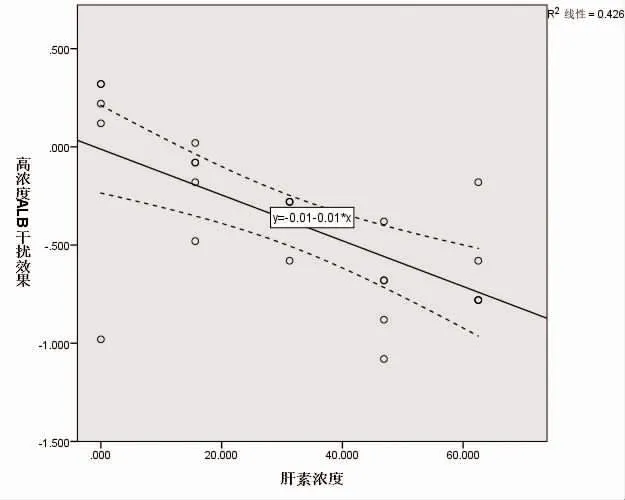
图3 肝素钠对高浓度ALB 干扰的剂量效应曲线
3 讨论
ALB 是人体血浆中含量最为丰富的蛋白质,占总蛋白的57%~68%。其为人体重要的营养蛋白,并参与维持酸碱平衡、维持血浆胶体渗透压,能保持人体内环境的稳定,还能转运血浆中多种物质[9]。在肾病患者中,白蛋白检测可以评估患者的预后情况,而且是透析患者护理质量的一项评价指标。白蛋白还可作为健康老年人预测死亡率的因素[10]。人血清白蛋白浓度也被用来通过佩恩公式估计校正后的钙水平,从而减少对钙浓度的错误估计[11]。目前,人体内白蛋白的检测方法主要有蛋白电泳法、染料结合法(包括溴甲酚绿法和溴甲酚紫法) 和免疫比浊法[12];其中溴甲酚绿法为大多数全自动生化分析仪配套的检测方法,其检测成本低廉,精密度高,线性范围宽,适用于大部分的患者[13]。但由于一些已知或不明原因,溴甲酚绿法ALB 检测会存在其他非白蛋白类物质的非特异干扰,影响检测结果的准确性[14-16]。该项目的测量误差可造成临床医生对患者身体状况的评估失误,甚至影响对患者的治疗。
肝素是一种带有强大负电荷的粘多糖硫酸酯,因首先从肝脏中发现而得名,其平均分子量为15 KDa,呈强酸性。肝素也存在于肺、血管壁、肠粘膜等组织中,是动物体内一种天然抗凝血物质。肝素天然存在于肥大细胞,现在主要从牛肺或猪小肠黏膜提取。其作为一种抗凝剂已有90 多年的历史[17],是由两种多糖交替连接而成的多聚体,在体内外都有抗凝血作用,是世界上使用最广泛的临床抗凝剂。肝素通过与抗凝血酶Ⅲ相互作用来抑制血栓形成。临床上主要用于血栓栓塞性疾病、心肌梗死、心血管手术、心脏导管检查、体外循环、血液透析等。随着药理学及临床医学的进展,肝素的应用不断扩大。在临床中主要用其肝素钠或者肝素钙的水溶液。
检测方法的总误差包括不精密度、方法特异性偏倚和样本特异性偏倚[18]。干扰物既能引起系统误差,也会造成随机误差。对于某些方法,干扰效果的影响超过了不精密度,就成为随机误差的主要来源。从患者个体来说,干扰物引起的检测误差随着患者样本中干扰物浓度的改变而改变。
通过参考《干扰实验指南》,用将潜在干扰物添加到样本中的方式来评价干扰效应,筛选、证实、量化潜在的干扰物质,明确检测方法对干扰物质的敏感性,及时作出风险评估,必要时发布特殊的声明或警示以提醒临床。
由干扰物筛查实验(配对差异实验)、剂量效应实验结果可知,62.5 U/ml 肝素钠会对ALB 低、中、高3 个浓度测定产生负干扰。其原因可能为肝素是一种带有强大负电荷的粘多糖硫酸酯,在到达一定浓度时可能与ALB 测定试剂中带阴离子的溴甲酚绿染料竞争带正电荷的ALB 分子(pH 4.2)的结合位点,使ALB 与染料结合减少,导致ALB 测定结果偏低[19]。
综上所述,肝素钠作为干扰物质,对ALB 测定的影响随着ALB 浓度的增加而减弱。目前临床常规生化分析多采用血清标本进行检测。但是对于临床使用肝素钠药物的患者,尤其对于留置管采血时混入肝素的透析患者,要注意其ALB 结果的准确性,特别是在ALB 浓度偏低时,必要时检验人员应予以说明。
