基于网络药理学探讨血府逐瘀汤中川芎-赤芍药对调节血管新生的分子机制
2022-04-23左春兰刘娜婷蔡晓婷林凡
左春兰 刘娜婷 蔡晓婷 林凡



[摘要] 目的 分析血府逐瘀汤关键药对川芎-赤芍调节血管新生的物质基础和作用机制。方法 从TCMSP数据库及Drug Bank数據库挖掘川芎-赤芍的成分及其对应靶蛋白,从GeneCards数据库获取“血管新生”相关基因;利用Omicshare数据库中的Venn功能获取川芎-赤芍干预血管新生的靶点后,借助Cytoscape(3.8.2)软件构建“活性成分—川芎-赤芍调节血管新生靶蛋白”网络关系图,在String数据库构建“川芎-赤芍调节血管新生靶蛋白--人类蛋白”互作网络,并筛选核心靶点;所得靶点的基因本体论(GO)及京都基因与基因组百科全书(KEGG)通路富集分析在Omicshare网站进行。借助AutoDock vina软件对核心靶点和关键活性成分进行分子对接。结果 获得川芎-赤芍活性成分20种,相关靶蛋白117种,川芎-赤芍调节血管新生靶蛋白72个,其中,关键活性成分为黄芩素、鞣花酸、β-谷甾醇、豆甾醇、杨梅酮、(+)-儿茶素、阿魏酸、川芎嗪等,关键靶蛋白为蛋白激酶Bα(AKT1)、血管内皮生长因子A(VEGFA)、白细胞介素-6(IL-6)、P53肿瘤蛋白(TP53)、肿瘤坏死因子-α(TNF-α)、环加氧酶2(PTGS2)、热休克蛋白90αA1(HSP90AA1)、c-fos原癌基因蛋白(FOS)等。GO结果提示,该药对在细胞增殖、生长、生物粘附、细胞聚集等方面影响血管新生;通路富集结果显示,AGE-RAGE通路、IL-17通路、流体剪应力与动脉粥样硬化信号通路等是药物作用的主要通路。分子对接提示核心靶点与关键化合物具有良好的结合能力。结论 血府逐瘀汤中的川芎-赤芍药对通过多靶点、多途径对血管新生起调节作用,为血府逐瘀汤干预血管新生的进一步研究及临床应用提供一定理论依据。
[关键词] 血府逐瘀汤;川芎-赤芍;血管新生;网络药理学;分子对接
[中图分类号] R285 [文献标识码] A [文章编号] 1673-9701(2022)06-0033-05
[Abstract] Objective To analyze the material basis and mechanism of key components of Xuefu Zhuyu Decoction on Rhizoma Chuanxiong-Radix Paeoniae Rubra regulating angiogenesis. Methods The constituents of Rhizoma Chuanxiong-Radix Paeoniae Rubra and their corresponding target proteins were mined from the TCMSP database and the Drug Bank database, and the angiogenesis-related genes were obtained from the GeneCards database. The target of Rhizoma Chuanxiong-Radix Paeoniae Rubra intervention on angiogenesis was obtained using the Venn function in the Omicshare database. The network relationship map of "active component-Rhizoma Chuanxiong-Radix Paeoniae Rubra regulating angiogenesis target protein" was constructed with the help of Cytoscape(3.8.2) software. The interaction network of "Chuanxiong-Radix Paeoniae regulating Rubra angiogenesis target protein-human protein" was constructed in the String database, and the core target was screened. The gene ontology(GO) and Kyoto Encyclopedia of Genes and Genomes (KEGG) pathway enrichment analysis of the obtained targets were carried out on the Omicshare website. With the help of AutoDock vina software, the core target and key active ingredients were molecularly docked. Results 20 active components of Rhizoma Chuanxiong-Radix Paeoniae Rubra, 117 related target proteins, and 72 angiogenesis-regulating target proteins of Rhizoma Chuanxiong-Radix Paeoniae Rubra were obtained. Among them, the key active ingredients are baicalein, tannic acid, β-sitosterol, stigmasterol, myricetin, (+) -catechin, ferulic acid, and ligustrazine. The key target proteins were protein kinase Bα (AKT1), vascular endothelial growth factor A (VEGFA), interleukin-6 (IL-6), P53 tumor protein (TP53), tumor necrosis factor-α (TNF-α), cyclooxygenase 2 (PTGS2), heat shock protein 90αA1 (HSP90AA1), and c-fos proto-oncogene protein (FOS). GO results suggested that the drug affects angiogenesis in cell proliferation, growth, bioadhesion, and cell aggregation. Pathway enrichment results showed that the AGE-RAGE pathway, IL-17 pathway, fluid shear stress, and atherosclerosis signaling pathways are the main pathway of drug action. Molecular docking suggested that the core target has an excellent binding ability with key compounds. Conclusion The Rhizoma Chuanxiong-Radix Paeoniae Rubra of Xuefu Zhuyu Decoction can regulate angiogenesis through multiple targets and pathways. It provides a certain theoretical basis for the further research and clinical application of Xuefu Zhuyu Decoction on the intervention of angiogenesis.
[Key words] Xuefu Zhuyu Decoction; Rhizoma Chuanxiong-Radix Paeoniae Rubra; Angiogenesis; Network pharmacology; Molecular docking
血管新生是在已有血管基础上形成新血管的过程,其异常可导致缺血性疾病(如心肌缺血、缺血性脑卒中)和血管增生性疾病(如肿瘤、动脉粥样硬化、糖尿病视网膜病变),对人类健康威胁巨大。治疗血管新生已成为相关疾病研究的热点之一[1]。
作为活血化瘀方剂的代表,血府逐瘀汤可活血化瘀、调节血管新生,但具体机制尚不明晰[2]。网络药理学是基于系统生物学和运筹学的网络理论,以整体、系统的观点分析药物与机体之间的相互作用,对揭示疾病机制和药物的研发具有重要意义。
在血府逐瘀汤中,川芎为血中气药,既能活血化瘀,又擅行气化滞,芍药凉血活血、散瘀止痛,二者相互配合而发挥重要作用[3]。因此,本研究选取川芎、赤芍,以网络药理学方法分析其调控血管新生的机制,以期为血府逐瘀汤相关临床应用提供一定理论依据。
1 材料与方法
1.1 获取川芎-赤芍的活性成分和靶蛋白、血管新生相关基因
在TCMSP数据库(http://ibtshk-bu.edu.hk/LSP/tcmsp.php)挖掘,并依据口服利用度(OB)≥30%、类药性(DL)≥0.18筛选川芎、赤芍的潜在有效成分,并检索文献补充。将所得成分的化学结构在PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)中进行验证。
通过TCMSP数据库和Drug Bank(https://www.drugbank.ca/)数据库查找有效成分对应靶点,并在UniProt数据库(http://www.uniprot.org/up-loadlists/)中转换成人类基因名。在GeneCards数据库(https://www.genecards.org/)收集血管新生相关基因。
1.2“川芎-赤芍活性成分—药物调节血管新生靶蛋白”关系网络构建
利用Venn功能(https://www.omicshare.com)对川芎-赤芍活性成分靶蛋白和血管新生相关基因取交集,获取川芎-赤芍干预血管新生的可能靶蛋白。随后将上述数据导入Cytoscape(3.8.2)软件,构建“活性成分—川芎-赤芍干预血管新生靶蛋白”关系网络图,分析网络拓扑结构。其中,Degree值代表成分与靶标之间所对应的关系,BC值表示节点和网络中心点间的距离,两个参数越大说明该节点在网络中作用越重要。
1.3“川芎-赤芍调节血管新生靶蛋白—人类蛋白”相互作用网络(protein protein interaction network,PPI)构建
将川芎-赤芍调节血管新生靶蛋白导入String数据库(https://string-db.org/cgi/input.pl),并指定“Homo sapiens”为限定研究物种,获取蛋白互作信息后,再导入cytoscape中绘制“川芎-赤芍干预血管新生靶蛋白—人类蛋白”PPI,分析网络拓扑结构,筛选核心靶点。
1.4 核心靶点的GO分析和KEGG通路富集分析
应用BioMart数据库(http://www.biomart.org/)转换核心靶点的基因格式,利用Omishare网站进行GO(gene ontology)和KEGG(kyoto encyclopedia of genes and genomes)富集分析,并依据P值大小展示KEGG结果的前20条(P<0.01)。
1.5 关键活性化合物与核心靶点的分子对接
将1.3筛选出的核心靶点在PDB数据库(https://www1.rcsb.org/)和UniProit数据库中转换成PDB格式,再从TCMSP数据库下载关键活性成分的3D结构。将小分子化合物和大分子蛋白质通过AutoDock软件分别进行加氢和脱水-加氢处理,设置对接参数及对接BOX,借助AutoDock vina进行运算,再通过PyMol软件输出结果。
2 结果
2.1 川芎-赤芍的活性成分和靶蛋白、血管新生相关基因的获取
获得310种川芎、赤芍的成分,其中符合方法1.1篩选标准的活性成分37种,经Pubchem数据库验证后,最终得到有效活性成分20种(其中1种为二者重复成分),相应靶基因共117个。GeneCards数据库中获得血管新生相关基因4609个,应用相关性中位数筛选,得到2327个相关基因。
2.2“川芎-赤芍活性成分—药物调节血管新生靶点”关系网络构建
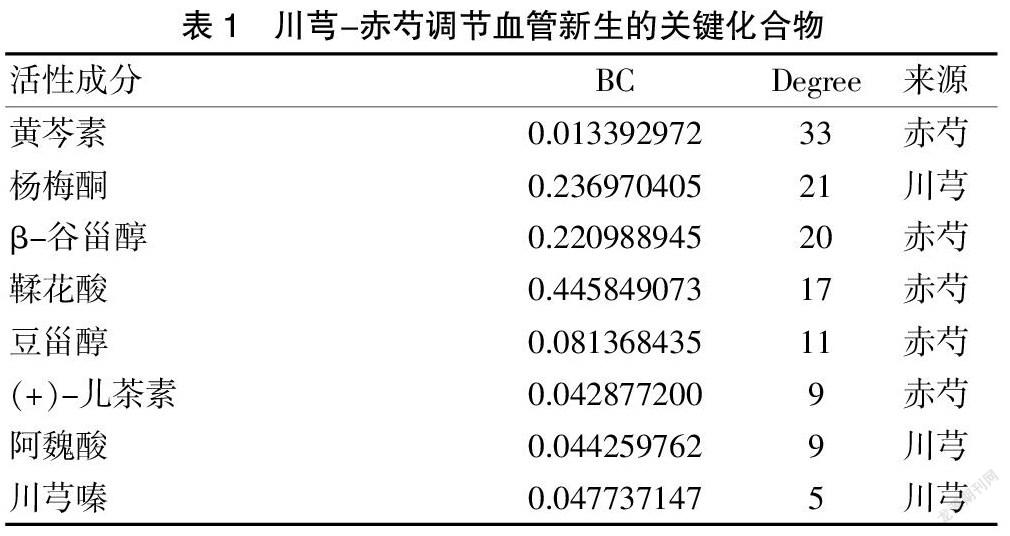
将川芎-赤芍靶蛋白与血管新生相关基因取交集,得到药物调节血管新生的潜在靶点72个。其对应18个有效成分。构建“川芎-赤芍活性成分—药物调节血管新生靶点”PPI,分析结果显示黄芩素(baicalein)、鞣花酸(ellagic acid)、β-谷甾醇(beta-sitosterol)、豆甾醇(stigmasterol)、杨梅酮(myricanone)、(+)-儿茶素[(+)-catechin]、阿魏酸(ferulic acid)、川芎嗪(tetramethylpyrazine)排名位于Degree值和BC值前10位,提示其可能是药物调节血管新生的关键活性成分。上述关键活性成分主要来源于赤芍,提示赤芍作用更重要。见图1、表1。
2.3 “川芎-赤芍调节血管新生靶蛋白—人类蛋白”PPI构建与分析
“川芎-赤芍调节血管新生靶蛋白—人类蛋白”PPI分析表明,Degree值和BC值都位于前10的靶点有8个,分别为蛋白激酶B(protein kinase B,AKT1)、血管内皮生长因子(vascular endothelial growth factor A,VEGFA)、白细胞介素-6(interleukin-6,IL-6)、肿瘤蛋白p53(tumor protein P53,TP53)、肿瘤坏死因子(tumor necrosis factor,TNF)、前列腺素内过氧化物合酶2(prostaglandin-endoperoxide synthase 2,PTGS2)、热休克蛋白90αA1(heat shock protein 90 Alpha family class A member 1,HSP90AA1)、c-fos原癌基因蛋白(proto-oncogene c-Fos,FOS),提示它们可能为药对干预血管新生的关键靶蛋白。见图2。
2.4 GO和KEGG分析及核心靶点的确定
对川芎-赤芍调节血管新生靶蛋白进行GO及KEGG分析,以P<0.01为筛选条件,分别得到5438个相关条目和216条富集通路,其中,富集前20条的通路见图3。
GO分析表明,药对作用涉及生物过程有27个条目,主要为细胞的增殖、生长、粘附和聚集等方面;相关的分子功能条目有8个,涉及活动分子传感器、转录监管机构活动、抗氧化等方面;细胞组成有14个条目,涉及细胞膜、细胞外区域、突触等感受外界信号的结构。
KEGG分析结果显示,相关通路为AGE-RAGE信号通路(AGE-RAGE signaling pathway in diabetic complications)、IL-17信号通路(IL-17 signaling pathway)、流体剪应力与动脉粥样硬化(fluid shear stress and atherosclerosis signaling pathway)信号通路,并且存在多靶点的相互协调作用。
2.5 分子对接
除(+)-catechin因其结构的特殊性,无法进行对接之外,关键活性成分与靶蛋白的结合能信息见表2,部分化合物与靶点分子的具体对接过程见封三图5。结果显示,其中51个对接结果有较优的对接活性(结合能≤-5.0),29个对接结果有强烈的匹配活性(结合能≤-7.0)。以上结果表明,川芎-赤芍关键活性成分与其调节血管新生靶蛋白可有效结合。
3 讨论
本研究分析表明,黄芩素、鞣花酸、β-谷甾醇、豆甾醇、杨梅酮、(+)-儿茶素、川芎嗪和阿魏酸可能为血府逐瘀汤中川芎-赤芍调节血管新生的关键活性化合物。川芎嗪可促进血管内皮生长因子(VEGFA)的表达从而促进血管新生[4]。阿魏酸是肉桂酸的衍生物之一,可通过抑制环氧合酶-2(COX-2)和血管内皮生长因子(VEGFA)表达,从而表现出抗血管生成活性[5]。黄芩素属于黄酮类化合物,其药理作用与抗炎、抗血管生成、抗转移有关,可破坏肿瘤血管系统的发育来抑制肿瘤的转移和进展[6]。鞣花酸是一种多酚二内酯,可下调VEGF基因表达,抑制肿瘤血管生成[7]。β-谷甾醇和豆甾醇属于植物甾醇,其中β-谷甾醇既能促进创伤愈合过程的血管新生,又显著抑制VEGFA的表达,抑制肾肿瘤血管新生[8]。而豆甾醇可通过下调TNF-α抑制小鼠的肿瘤血管生成并抑制胆管癌的生长[9],还可以刺激血管生成从而有益于缺血性疾病的治疗[10]。(+)-儿茶素属于多元酚类的一种,具有明显的抗血管生成作用,从而抑制肿瘤的生长和扩散[11]。杨梅酮具有强大的抗肺癌活性,但其在血管新生方面的作用还有待进一步研究[12]。
本研究分析提示,AKT1、VEGFA、IL-6、TP53、TNF、PTGS2、HSP90AA1、FOS是川芎-赤芍调节血管新生的关键靶点,AGE-RAGE信号通路、IL-17信号通路、流体剪切应力和动脉粥样硬化信号通路等为关键信号通路。
流体剪切应力(fluid shear stress,FSS)是血流与血管壁内皮表面产生的摩擦力,在血管生物学中起重要作用,参与调控血管新生[13]。作用在血管内皮细胞上的FSS会在短时间内引发一系列的反应,包括调节Krüppel样因子2和4(Krüppel-like factor 2/4,KLF2/4)转录、激活血管内皮生长因子受体2(VEGFR2)和酪氨酸激酶(TK),以及一氧化氮(NO)的释放;进而激活MAP激酶、整合素、NF-κB、p21活化激酶和c-Jun N端激酶(JNK);从而这些通路下游表达不同的转录组[14]。
AGE-RAGE信号通路对血管系统的影响主要与炎症及氧化应激有关[16]。关键靶蛋白中的AKT1、IL-6、TNF、VEGFA在该通路中发挥重要作用。AGE-RAGE可降低血管VEGFR2的蛋白质表达,造成血管生成障碍,从而引起一系列糖尿病并发症[17]。白细胞介素-17(IL-17)信号通路同样参与调控血管新生的过程。关键靶蛋白中的IL-6、TNF在该通路中占据重要地位。IL-17可诱导小鼠体内血管内皮细胞迁移及成血管作用,并增強VEGFA表达,参与肿瘤间质中炎症反应和微血管形成[18]。
综上所述,本研究对血府逐瘀汤中的“川芎-赤芍”药对进行了网络药理学分析,定位其调节血管新生的关键成分、靶点与可能的作用通路。但本研究通过数据挖掘,对药物调控血管新生的相关机制进行预测,仍具有一定的局限性,未来还需要在基础实验及临床试验中进行进一步验证。
[参考文献]
[1] Moghiman T,Barghchi B,Esmaeili SA,et al. Therapeutic angiogenesis with exosomal microRNAs:An effectual appr-oach for the treatment of myocardial ischemia[J].Heart Fail Rev,2021,26(1):205-213.
[2] Hao P,Jiang F,Cheng J,et al. Traditional Chinese medicine for cardiovascular disease:Evidence and potential mechanisms[J]. J Am Coll Cardiol,2017,69(24):2952-2966.
[3] 袁蓉,施伟丽,信琪琪,等.川芎-赤芍药对研究进展[J].环球中医药,2019,12(5):808-811.
[4] Qing L,Wu P,Zhou Z,et al. Tetramethylpyrazine improved the survival of multiterritory perforator flaps by inducing angiogenesis and suppressing apoptosis via the Akt/Nrf2 pathway[J]. Drug Des Devel Ther,2019,13:1437-1447.
[5] Ekowati J,Hamid IS,Diyah NW,et al. Ferulic acid prevents angiogenesis through cyclooxygenase-2 and vascular endothelial growth factor in the chick embryo chorioallantoic membrane model[J].Turk J Pharm Sci,2020,17(4):424-431.
[6] Park YG,Choi J,Jung HK,et al. Baicalein inhibits tumor progression by inhibiting tumor cell growth and tumor angiogenesis[J]. Oncol Rep,2017,38(5):3011-3018.
[7] ■etin A,Biltekin B. Combining ellagic acid with temozo- lomide mediates the cadherin switch and angiogenesis in a glioblastoma model[J].World Neurosurg,2019,132:e178-e184.
[8] Sharmila R,Sindhu G. Modulation of angiogenesis,proli ferative response and apoptosis by beta-sitosterol in rat model of renal carcinogenesis[J]. Indian J Clin Biochem,2017,32(2):142-152.
[9] Kangsamaksin T,Chaithongyot S,Wootthichairangsan C,et al. Lupeol and stigmasterol suppress tumor angiogenesis and inhibit cholangiocarcinoma growth in mice via downregulation of tumor necrosis factor-α[J]. PLoS One,2017,12(12):e0189 628.
[10] Liu M,Zhao L,Han L.et al. Discovery and identification of proangiogenic chemical markers from Gastrodiae Rhizoma based on zebrafish model and metabolomics approach[J]. Phytochem Anal,2020,31(6):835-845.
[11] Yee EMH,Brandl MB,Pasquier E,et al. Dextran-Catechin inhibits angiogenesis by disrupting copper homeostasis in endothelial cells[J]. Sci Rep,2017,7(1):7638.
[12] Dai G,Tong Y,Chen X,et al. In vitro anticancer activity of myricanone in human lung adenocarcinoma A549 cells[J]. Chemotherapy,2014,60(2):81-87.
[13] Bai L,Shyy JY PhD. Shear stress regulation of endothe- lium:A double-edged sword[J].J Transl Int Med,2018,6(2):58-61.
[14] Kumar S,Williams D,Sur S,et al. Role of flow-sensitive microRNAs and long noncoding RNAs in vascular dys- function and atherosclerosis[J].Vascul Pharmacol,2019, 114:76-92.
[15] Fan Y,Lu H,Liang W,et al. Krüppel-like factors and vascular wall homeostasis[J].J Mol Cell Biol,2017,9(5):352-363.
[16] Xu J,Chen LJ,Yu J,et al. Involvement of advanced glycation end products in the pathogenesis of diabetic retinopathy[J].Cell Physiol Biochem,2018,48(2):705-717.
[17] Kim JH,Kim KA,Shin YJ,et al. Methylglyoxal induced advanced glycation end products(AGE)/receptor for AGE(RAGE)-mediated angiogenic impairment in bone marrow-derived endothelial progenitor cells[J]. J Toxicol Environ Health A,2018,81(9):266-277.
[18] 周瓊,董杰,沈夏波,等.白介素-17在三阴性乳腺癌中的表达及其与新生血管和预后的相关性[J].肿瘤学杂志,2021,27(1):53-57.
(收稿日期:2021-07-13)
