上皮样血管内皮瘤1例
2022-04-21向彬刘凯利陈思文徐珅杰刘蔚李洁
向彬,刘凯利,陈思文,徐珅杰,刘蔚,李洁*
(苏州大学附属第一医院:1全科医学,2病理科,江苏 苏州 215006)
1 临床资料
患者女,63 岁,因“右侧间断胸痛1年余,加重1个月”于2020年6月1日入住苏州大学附属第一医院。患者1年余前无明显诱因出现右侧胸痛,以胸背部为主,为阵发性疼痛,无咯血,无咳嗽咳痰,无发热畏寒等。患者于2018年10月30日行胸部平扫CT(图1A~B)示右肺上叶磨玻璃影,两肺多发结节影,未予重视。后于2019年8月19日复查胸部平扫CT(图1C~D)示右肺上叶磨玻璃影较前增大;两肺多发结节,较前增多,部分较前增大;肝脏多发低密度灶。2019年9月4日行全腹增强CT(图1E)示肝内多发低密度影。近1个月感胸痛较前加重,于2020年6月1日收住我科。既往体健,个人婚育及家族史均无特殊。
体温36.6 ℃,心率71次/min,呼吸18次/min,血压125/73 mmHg(1 mmHg=0.133 kPa)。神清,皮肤黏膜无皮疹、淤点,浅表淋巴结无肿大。两肺呼吸音清,未闻及明显干湿啰音。心律齐,心音正常,未闻及杂音。腹部及四肢无异常。血常规:白细胞7.25×109/L,血红蛋白94g/L,血小板396×109/L。C反应蛋白 1.29 mg/L。肿瘤全套:铁蛋白3.19 ng/ml,余未见异常。抗核抗体谱:核糖体P蛋白弱阳性,余均为阴性。抗中性粒细胞胞浆抗体(-)。6月2日胸腹部增强CT(图1F~H)示双肺多发结节影,较前增多增大,考虑转移性病变;肝多发低密度影,较前进展,考虑转移。18氟-脱氧葡萄糖(18F-fluorodeoxyglucose,18F-FDG)正电子发射计算机断层成像(positron emission tomography-computed tomography,PET-CT)检查示肝多发稍低密度灶伴葡萄糖代谢增高,标准化摄取值(standardized uptake value,SUV)最大为5.49;双肺多发结节,未见明显葡萄糖代谢增高。于6月4日B超引导下行肝脏穿刺术(肝右前叶穿刺)并送检,病理(图2A~C)示肝组织浅蓝色黏液样的基质内见短索状排列的肿瘤细胞,瘤细胞为多边形、短梭形,胞质嗜伊红色,可见管腔或空泡形成,核仁不明显。中间型血管内皮瘤,考虑上皮样血管内皮瘤(epithelioid hemangioendothelioma,EHE)。免疫病理(图2D~E)示肿瘤细胞CD31(+),CD34(+),F8(+),Vimentin(+),Caldesmon(部分+),Ki-67(+,约7%),SMA(部分+)CK(-),CK7(-),CK18(-),CK19(-),CD99(-),CK5/6(-),S100(-),Desmin(-)。经综合分析,诊断为EHE。行实体瘤全靶点基因检测为阴性。患者不考虑化疗,于7月8日行“帕博丽珠单抗200 mg(静脉滴注,第1天)+安罗替尼12 mg(口服,第1~14天)”治疗。现患者胸痛有所缓解,已行三周期疗程,疾病稳定。
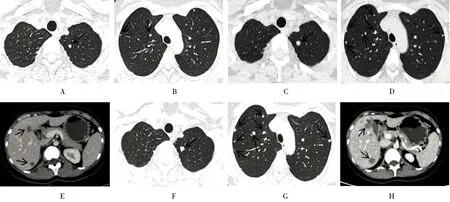
图1 患者影像学检查结果

图2 患者肝穿刺活检病理学资料
2 讨 论
EHE是一种极为罕见的血管肿瘤,患病率<1%[1],由Weiss和Enzinger于1982年命名。EHE通常累及肝、肺及骨骼,亦可见于乳房、皮肤、脾脏等部位。有研究显示,EHE发生在肝脏的概率为21%,发生在肝脏加肺的概率为18%,仅发生在肺或骨骼的概率分别为12%和14%[2]。常见的EHE为肝上皮样血管内皮瘤(hepatic epithelioid hemangioendothe-lioma,HEHE)和肺上皮样血管内皮瘤(pulmonary epithelioid hemangioendothelioma, PEH)。本病例患者有肺、肝的多发结节,为EHE的好发部位。
EHE好发于女性,男女比例为1:4[1]。发病中位年龄为36岁,可累及儿童、中年人及老年人[2]。EHE的发生与基因的异常表达有关,染色体的异常主要表现为染色体12q12-13与12q14-21扩增、11q21缺失、1号及3号染色体易位t(1;3)(p36;q25),形成WWTR1-CAMTA1和YAP1-TFE3融合基因[3]。在2013年更新的世界卫生组织软组织肿瘤分类中,这种融合基因被列为EHE的新基因[4]。
EHE患者多数无症状,通常在体检行胸部X线时发现异常结节。少数在诊断时有症状,如胸痛、咯血或贫血等。EHE在胸部CT上常表现为双侧多发结节影。肺结节直径可达2 cm,但大多数<1 cm,主要位于下肺。对于PEH患者而言,18F-FDG PET-CT检查在评估肺结节葡萄糖代谢状况以及寻找原发病灶或其他转移灶方面具有重要价值[5]。PEH患者的肺结节多数表现为18F-FDG摄取增加,其SUV值会增高[6]。HEHE患者的肝脏在影像上通常表现为偶然发现的两叶多灶性、异质性增强的结节,临床上表现为非特异性腹部症状[7]。本例患者有胸痛的症状,两肺散在多发结节,大小为0.2~0.6 cm,无葡萄糖代谢增高,可能与结节偏小有关。肝脏多发低密度灶,直径为1.7~3.7 cm,有SUV增高,SUV最大为5.49。
EHE的诊断,重点在于组织学、免疫组织化学。EHE的组织特征性特点包括丰富的细胞质,胞质内的空泡、核内包涵体和基质的变性(软骨样、黏液样或透明样变性)[8]。CD31、CD34及Fli-1是血管内皮细胞的标志物。其中,Fli-1和CD31是特异性标志物,CD34特异性虽低,但敏感性高。本病例肝穿刺的病理见肝组织有异型短梭形、多边形细胞、管腔样巢片状生长,可见黏液样的基质、空泡的形成。肿瘤细胞免疫组化CD31、CD34均为阳性,有利于本病的诊断。鉴别诊断包括上皮样血管肉瘤、转移癌和上皮样肉瘤。HEHE主要与肝海绵状血管瘤、肝转移瘤等鉴别。当我们发现肺、肝脏多发结节时,则应考虑EHE。
患者经肝穿刺活检明确为EHE。虽然肺未经穿刺活检,但肺也是EHE的好发部位,根据患者的病史及胸部多发结节短期内增多、增大的特点,从一元论角度,考虑肺亦为EHE的可能。一般累及多个部位的病变,难以确定肿瘤是多中心,还是单一原发性病变转移到其他组织。回顾病史,患者先出现两肺多发结节,随后发现肝多发低密度灶,根据病史及影像学特点,考虑EHE原发于肝和肺。
EHE目前尚无明确的治疗策略。对于无症状的病变,多暂时观察,部分病情可自行缓解。对于局限性病变(病灶较小且数量有限),首先考虑手术切除。若EHE有转移,治疗方法包括化疗、放疗、靶向治疗和免疫治疗。化疗的效果不一,靶向及免疫药物治疗也缺乏大规模的临床研究证明其有效性。Mogler等[9]提出,通过对EHE的肿瘤或血液进行基因检测,明确与疾病相关的基因组改变,可以指导疾病治疗,亦有可能预测靶向治疗的反应。但是EHE的基因检测尚缺乏可靠研究支持。亦有报道称,EHE相关基因中,除了WWTR1-CAMTA1和YAP1-TFE3融合基因,其他基因突变率低,目前并不能有效指导用药[10]。此外,有研究发现HEHE的血管内皮生长因子染色几乎均呈阳性[11]。贝伐珠单抗作为常用的抗肿瘤血管生成药,多篇文献称其联合卡铂、紫杉醇等治疗可以使EHE患者情况得到改善。放疗多用于出现脑、骨骼转移时。程序性死亡受体1是免疫治疗的常规用药。EHE一旦出现转移,如果可以治疗,应该与患者进行商议,确定患者对治疗副作用的接受程度,以最大限度保证患者的生活质量[2]。本例患者为肺、肝多发结节,故不优先考虑手术治疗。虽其基因检测为阴性,但是结合相关文献[10-12],建议行化学治疗联合靶向治疗,由于患者考虑化疗的副作用大,故予靶向治疗联合免疫治疗。
EHE患者预后不同,有些表现为惰性的临床病程,有些则倾向于转移。EHE的预后与肿块的大小和细胞核的分裂象有关,肿瘤越大,细胞核分裂数量越多,5年生存率越低[12]。WWTR1-CAMTA1融合的EHE患者比YAP1-TFE3融合的EHE患者的疗效差,5年总生存率分别为59% 和86%[13]。
在临床的诊治过程中,遇到肺部多发小结节或肝脏多发结节的患者,需排除EHE的可能。虽然是少见病,但是部分恶性程度高,为避免错过最佳治疗时期,应早发现,早诊断,早治疗。
