HPLC法测定钙镁维生素D咀嚼片中维生素D3的含量
2022-04-18张建喜姚玲平陈活林刘剑萍
张建喜,姚玲平,陈活林,刘剑萍
(1.浙江创新生物有限公司,浙江 绍兴 312000;2.浙江医药股份有限公司新昌制药厂,浙江 新昌 312500)
0 引言
维生素D为固醇类衍生物,具抗佝偻病作用,又称抗佝偻病维生素。目前认为维生素D也是一种类固醇激素,维生素D家族成员中最重要的成员是维生素D2(麦角钙化醇)和维生素D3(胆钙化醇)[1]。维生素D均为不同的维生素D原经紫外照射后的衍生物,植物不含维生素D,但维生素D原在动、植物体内都存在。维生素D是一种脂溶性维生素,有五种化合物,对健康关系较密切的是维生素D2和维生素D3。它存在于部分天然食物中;人体皮下储存有从胆固醇生成的7-脱氢胆固醇,受紫外线的照射后,可转变为维生素D3,适当的日光浴足以满足人体对维生素D的需要[2]。钙镁维生素D咀嚼片以碳酸钙、维生素D3、氧化镁为主要成分,每片含标志性成分维生素D34.2 μg,产品规格为1.35 g/片,可补充维生素D,促进钙吸收有助于骨骼和牙齿的健康,有助于骨骼形成[3]。产品中维生素D3含量较低,目前对于保健食品中维生素D3含量测定方法多为食品安全国家标准方法,但测定过程过于繁琐,检测周期长,且测定结果较难重现。参考文献资料中维生素D测定方法研究内容[4-6],本文通过实验研究建立了较为简便的HPLC法测定钙镁维生素D咀嚼片中维生素D3含量的方法。
1 材料与方法
1.1 仪器与材料
Agilent 1260型高效液相色谱仪(安捷伦科技有限公司);METTLER-TOLEDO XS205DU型电子天平(梅特勒-托利多仪器有限公司);DK-S24型电热恒温水浴锅(上海精宏实验设备有限公司);戊醇、正己烷(默克,色谱纯);其余试剂均为分析纯;维生素D3对照品(批号:100061-201809)为中国药品食品检定研究院提供;钙镁维生素D咀嚼片样品为自制(批号为MD200401、MD200402、MD200403)。
1.2 色谱条件
硅胶色谱柱(4.6 mm×250 mm,5 μm);流动相为戊醇:正己烷(3∶997);紫外检测器,检测波长为254 nm;流速为2.0 mL/min;进样量为100 μL;柱温30 ℃。
1.3 溶液配制
样品溶液:取片剂研碎,称取5.0 g,精密称定,置于100 mL带塞子的锥形瓶中,加入二甲亚砜与水的混合溶液(体积比3∶1)25 mL,加入甲醇10 mL,置于50 ℃水浴中加热10 min,不断振摇,冷却后,精密加入正己烷25.0 mL,800 r/min搅拌20 min,静置分层,取上层正己烷层过滤后用于液相测定。
对照贮备溶液:称取维生素D3对照品约20 mg,精密称定,置25 mL棕色容量瓶中,加甲苯不加热溶解,并稀释至刻度。精密吸取上述溶液1.0 mL,置于50 mL棕色容量瓶中,加正己烷稀释至刻度,作为对照贮备溶液。
对照溶液:精密吸取对照贮备溶液1.0 mL,置25 mL棕色容量瓶中,加正己烷稀释至刻度。将溶液转入到100 mL带塞子的锥形瓶中,加入二甲亚砜-水(体积比3∶1)的混合溶液25 mL,加入甲醇10 mL,800 r/min搅拌20 min,静置分层,取上层正己烷层过滤后用于液相测定。
1.4 检测方法
取对照溶液与样品溶液各100 μL,分别注入液相色谱仪,记录色谱图,以峰面积按外标法计算样品中维生素D3的含量。
2 结果与讨论
2.1 提取溶剂筛选
产品配方中维生素D3以维生素D3微粒的形式存在,其微粒以维生素D3与β-环状糊精为原料,经溶解、回流、冷却、离心、干燥等工艺制成。片剂配方中还使用到碳酸钙、氧化镁为主要原料,山梨糖醇、麦芽糊精、乳粉、乳糖、硬脂酸镁、羟丙基甲基纤维素、二氧化硅等为辅料,经制粒、混合、压片、包装等工艺加工制成钙镁维生素D咀嚼片。使用国家标准GB 5009.82检测维生素D3,皂化后萃取过程中乳化严重,无法完成试验。结合产品配方特点,考虑维生素D3的提取尤为关键。
β-环状糊精是淀粉经酸解环化生成的产物,为新型分子包裹材料,溶于水,难溶于甲醇、乙醇、丙酮。维生素D3为脂溶性维生素,在水中不溶,在正己烷、乙醚等非极性溶剂中易溶解。产品配方中其他物料均在正己烷中不溶,部分辅料可在水及二甲亚砜溶剂中溶解,结合产品配方,使用水作为破壁溶剂,50 ℃水浴中加热振摇,冷却后精密加入正己烷25.0 mL,800 r/min搅拌20 min,乳化严重,无法分层。
水中加入甲醇及二甲亚砜,可以减少乳化现象,改用二甲亚砜与水的混合溶液(体积比3∶1)作为破壁溶剂,50 ℃水浴中加热振摇,冷却后精密加入正己烷25.0 mL,800 r/min搅拌20 min,乳化减弱,但分层时间较长。
优化破壁提取过程,改用二甲亚砜与水的混合溶液(体积比3∶1)作为破壁溶剂,加入甲醇,50 ℃水浴中加热振摇,冷却后精密加入正己烷25.0 mL,800 r/min搅拌20 min,乳化减弱,分层时间减少。
2.2 对照溶液及样品溶液浓度确定
称取维生素D3对照品约20 mg,精密称定,置25 mL棕色容量瓶中,加甲苯不加热溶解,并稀释至刻度,作为贮备溶液,精密移取贮备溶液,用正己烷定量稀释。在安捷伦1260液相色谱仪进样,记录色谱图。维生素D3浓度为0.6 μg/mL时,峰面积为80,能满足定量需求。
钙镁维生素D咀嚼片功效成分维生素D3含量为4.2 μg/片,产品规格1.35 g/片,折算后样品量称取5 g溶解破壁后,用25 mL正己烷提取,样品溶液与对照溶液中维生素D3浓度相近。
2.3 二甲基亚砜水混合溶液量的选择
取钙镁维生素D咀嚼片研碎后,称取粉末5.0 g,加入一定量体积的二甲亚砜与水的混合溶液(体积比3∶1),在50 ℃水浴中加热振摇10 min,然后加入甲醇10 mL,加入正己烷25 mL,800 r/min搅拌20 min,静置分层,取上层正己烷层过滤后进样测定,考察溶解破壁溶剂量对维生素D3测定结果的影响,结果如表1所示。
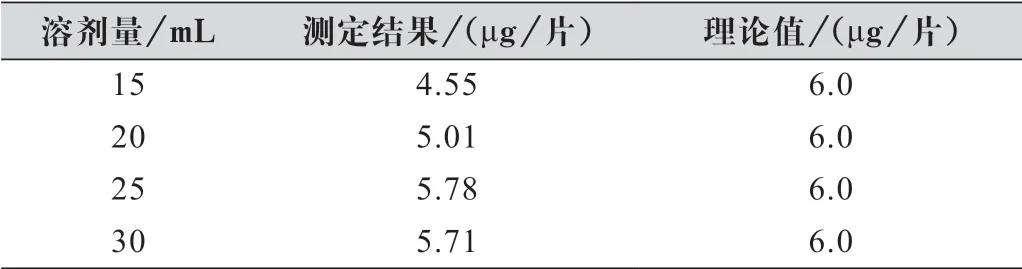
表1 二甲基亚砜水混合溶液量的选择数据表
2.4 溶解破壁温度的选择
取钙镁维生素D咀嚼片研碎后,称取粉末5.0 g,加入25 mL二甲亚砜与水的混合溶液(体积比3∶1),在不同温度水浴中加热振摇10 min,然后加入甲醇10 mL,加入正己烷25 mL,800 r/min搅拌20 min,静置分层,取上层正己烷层过滤后进样测定,考察溶解破壁温度对维生素D3测定结果的影响,结果如表2所示。

表2 溶解破壁温度选择数据表
2.5 加入正己烷后搅拌时间的选择
取钙镁维生素D咀嚼片研碎后,称取粉末5.0 g,加入25 mL二甲亚砜与水的混合溶液(体积比3∶1),在不同温度水浴中加热振摇10 min,然后加入甲醇10 mL,加入正己烷25 mL,800 r/min搅拌不同时间,静置分层,取上层正己烷层过滤后进样测定,考察搅拌时间对维生素D3测定结果的影响,结果如表3所示。

表3 搅拌时间选择数据表
2.6 专属性试验
取不含维生素D3空白辅料5.0 g按照钙镁维生素D咀嚼片处理方法,置于100 mL带塞子的锥形瓶中,加入二甲亚砜与水(体积比3∶1)的混合溶液25 mL,加入甲醇10 mL,置于50 ℃水浴中加热10 min,不断振摇,冷却后,精密加入正己烷25.0 mL,800 r/min搅拌20 min,静置分层,取上层正己烷层制成空白辅料溶液。再取二甲亚砜与水混合溶液(体积比3∶1)25 mL,加入甲醇10 mL,置于50 ℃水浴中加热10 min,不断振摇,冷却后精密加入正己烷25.0 mL,800 r/min搅拌20 min,静置分层,取上层正己烷层制成空白溶液。分别取空白辅料溶液、空白溶液、对照溶液与样品溶液,进样并记录色谱图,空白溶液及空白辅料溶液无干扰,空白溶液图谱如图1所示,空白辅料溶液图谱如图2所示,对照溶液图谱如图3所示,样品溶液图谱如图4所示。
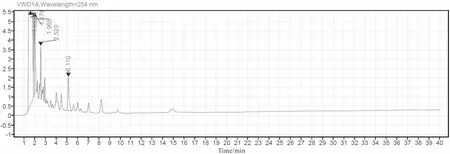
图1 空白溶液图谱
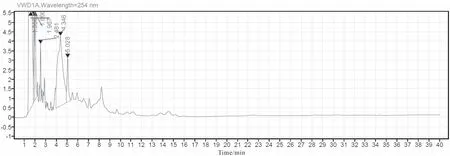
图2 空白辅料溶液图谱

图3 对照溶液图谱

图4 钙镁维生素D咀嚼片样品溶液图谱
2.7 精密度试验
取同一对照品溶液,连续进样6次,记录色谱图,结果维生素D3峰面积为86.14、85.95、86.38、86.40、86.56、87.30,RSD为0.6%,表明仪器精密度良好。取同一批样品,依法平行操作制备6份供试品溶液,分别测定,结果维生素D3含量分别为5.86 μg/片、5.85 μg/片、5.89 μg/片、5.91 μg/片、5.94 μg/片、6.00 μg/片,平均值为5.91 μg/片,RSD为1.0%。不同分析员在不同时间使用不同仪器对同一批样品进行测定,5.54 μg/片、5.61 μg/片、5.59 μg/片、5.62 μg/片、5.37 μg/片、5.62 μg/片,平均值为5.56 μg/片,RSD为1.8%。不同人员及仪器测定结果差值为其平均值的6%,结果一致,表明方法精密度良好。
2.8 标准曲线的绘制和线性关系的考察
精密称取维生素D3对照品约20 mg置于25 mL棕色容量瓶中,用甲苯溶解稀释到刻度,移取1.0 mL该溶液到50 mL棕色容量瓶中,用正己烷稀释到刻度,作为线性贮备溶液。分别移取线性贮备溶液0.5 mL、0.8 mL、1.0 mL、1.5 mL、2.0 mL到25 mL棕色容量瓶中,用正己烷稀释到刻度,将溶液转入到100 mL带塞子的锥形瓶中,精密加入二甲亚砜-水(体积比3∶1)的混合溶液25 mL,加入甲醇10 mL,800 r/min搅拌20 min,静置分层,取上层正己烷层,配制成维生素D3浓度为0.2~0.8 μg/mL的线性溶液,分别进样并记录色谱图,以维生素D3浓度为横坐标,维生素D3峰面积为纵坐标,进行线性回归,计算线性方程和相关系数,得到线性方程为y=135.54x-2.245 6,线性相关系数为0.999 9,结果表明维生素D3在线性范围内呈良好的线性关系,结果如表4所示。

表4 线性数据表
2.9 加样回收率试验
称取5.0 g不含维生素D3的空白辅料,精密称定,置于100 mL带塞子的锥形瓶中,加入二甲亚砜与水(体积比3∶1)的混合溶液25 mL,加入甲醇10 mL,置于50 ℃水浴中加热10 min,不断振摇,冷却,作为本底溶液。精密称取维生素D3对照品约20 mg置于25 mL棕色容量瓶中,用甲苯溶解稀释到刻度,移取1.0 mL该溶液到50 mL棕色容量瓶中,用正己烷稀释到刻度,作为贮备溶液。分别移取贮备溶液0.5 mL、1.0 mL、2.0 mL到25 mL棕色容量瓶中,用正己烷稀释到刻度,配制成50%、100%、200%的标准溶液,分别在本底溶液中加入配制好的系列标准溶液,800 r/min搅拌20 min,静置分层,取上层正己烷层,制成对照溶液浓度水平50%、100%、200%的维生素D3回收率测定溶液,依法处理并测定,计算加样回收率,结果如表5所示。结果表明该方法具有较好的准确度。
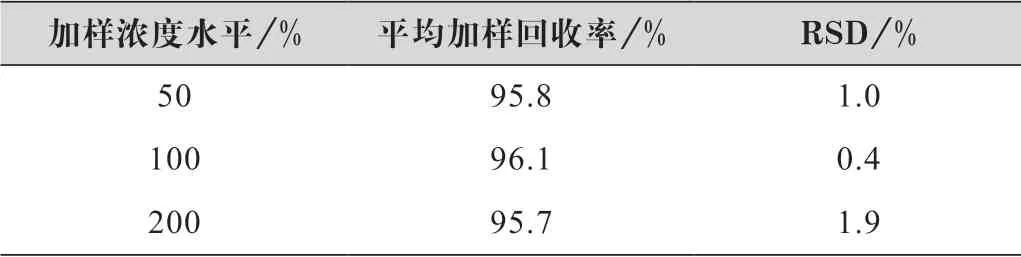
表5 加样回收率数据表(n=3)
2.10 溶液稳定性试验
配制对照品溶液和供试品溶液,分别在避光的条件下室温放置48 h后进样检测,放置后与0 h检测结果相比,对照品溶液峰面积基本一致,供试品溶液测定结果为5.76 μg/片,基本一致,表明溶液在室温避光的条件下48 h内稳定。
2.11 耐用性试验
分别改变测试条件,如改变流动相的比例、柱温、流速及更换仪器色谱柱,依法测定,结果与标准条件下测定结果一致,表明本方法具有良好的耐用性,结果如表6所示。

表6 耐用性数据表
2.12 样品含量测定
取钙镁维生素D咀嚼片样品,分别在本实验、通标标准技术服务(上海)有限公司(SGS)依法测定,结果如表7所示,均符合规定。

表7 钙镁维生素D咀嚼片样品测定维生素D3结果
2.13 讨论
本品中维生素D3以β-环状糊精包埋微粒的形式存在,实验过程中需先用二甲亚砜水溶液(体积比3∶1)在50℃水浴中溶解破壁,使维生素D3游离出来,且需加入甲醇减少乳化,然后用正己烷提取,为消除实验过程中可能产生的系统误差,供试品与对照品的前处理过程完全一致,均为经正己烷溶液提取,HPLC检测,以峰面积,按照外标法计算样品中维生素D3含量,操作简便,由于产品中维生素D3含量较低(约3 μg/g),中国药典对应含量准确度要求80%~115%,精密度要求RSD≤6%,该方法能符合药典要求,结果准确可靠。
3 结语
方法学验证表明,样品研碎后,取粉末用二甲亚砜与水的混合溶液(体积比3∶1)25 mL,加入甲醇10 mL,置于50 ℃水浴中加热10 min,不断振摇,破壁溶解,使其中的维生素D3游离出来,然后用正己烷25.0 mL,800 r/min搅拌20 min,提取溶液中的维生素D3,静置分层后,取上层正己烷层过滤,用于测定钙镁维生素D咀嚼片中维生素D3含量,该方法具有良好的专属性、精密度、线性和准确度,方法较为简便,准确可靠,并经过通标标准技术服务(上海)有限公司(SGS)复核,适用于钙镁维生素D咀嚼片中维生素D3含量检测。
