木质素-聚乙烯共热解生物炭对Cd(II)的吸附性能
2022-04-16秦坤王志康王章鸿杨成刘杰刚沈德魁
秦坤 ,王志康 ,王章鸿 , *,杨成 ,刘杰刚 ,沈德魁
1. 贵州民族大学生态环境工程学院,贵州 贵阳 550025;2. 贵州省工程地质灾害防治工程研究中心(贵州民族大学),贵州 贵阳 550025;3. 贵州民族大学固废污染控制与资源化技术研究中心,贵州 贵阳 550025;4. 东南大学/能源热转换及其过程测控教育部重点实验室,江苏 南京 210000
镉(Cd)是水体中常见的重金属污染物之一,其主要来源于电镀、采矿、炼油和制革等工业,具有较强的迁移性和生物蓄积性,对人类健康和生态系统安全构成严重威胁(蔡佳佩等,2018;张晓峰等,2020)。长期暴露于 Cd环境或者过量的摄入Cd将会对人类的骨骼和肾脏造成严重的损害,导致严重的疾病,例如痛痛病、贫血、骨质疏松等(王丹丹等,2015;陈能场等,2017)。因此,水体中(主要包括地表水和地下水)Cd的存在引起公众和政府组织的高度重视。世界卫生组织指出,饮用水Cd的最大允许质量浓度为0.005 mg·L−1(张长平等,2016;曹健华等,2019;马贵等,2021)。为了达到这一标准,大量的物理、化学或生物技术如纳滤、超滤、反渗透、化学沉淀、离子交换和生物处理等方法被开发用于水体中Cd的处理。然而,这些工艺普遍存在流程复杂、运行成本高、操作难度大等缺陷。相反,吸附法因效率高、成本低、可操作性强等而被认为是一种非常有前景的方法,尤其是利用绿色、可再生的吸附剂。
生物炭是生物质(如秸秆、木屑、有机生活垃圾、动物骨骼、植物残体、动物粪便等)在高温缺氧的环境中热解形成的一类含碳量较高的物质,具有结构疏松、官能团丰富、化学性质稳定、比表面积大、吸附性能强的特点,被成功的应用于固碳缓解全球气候变化、改良土壤性质以及吸附固定污染物(如重金属、染料、农药、抗生素等)(刘岑薇等,2021;姜禹奇等,2021)。共热解生物炭是伴随着共热解技术而新兴出现的一类碳材料,主要来源于同时热处理两种或者多种固体废弃物(例如生物质、塑料、厨余等)(王道涵等,2020;刘群星等,2020;康彩艳等,2021)。不同于单独组分生物质热解,在多组分固体废弃物共热解过程中,各个组分之间由于组分差异、热稳定性差异及热解产物的差异而存在相互作用(协同或者抑制),导致最后所得生物炭在理化特性方面与单独生物质热解生物炭存在明显差别。例如,Liu et al.(2021)发现,将75%的虾壳与25%玉米秸秆进行共热解得到的生物炭比表面积(57.85 m2·g−1)明显高于单独虾壳和玉米秸秆所得的生物炭(分别为42.63 m2·g−1和3.82 m2·g−1),同时该混合生物炭具有更松散的结构和无规则颗粒等特殊形貌。另外,针对共热解生物炭应用性能开发的研究也尚且有限,目前主要尝试应用于作为低廉吸附剂处理污水中染料、重金属、有机物等(Sewu et al.,2017;Fan et al.,2021)。
由此,本研究拟以造纸黑液木质素和聚乙烯共热解生物炭作为典型共热解生物炭的代表,将其应用于溶液中 Cd(II)的吸附,用于初步探索共热解生物炭的潜在应用性能。研究过程中,以单独黑液木质素基生物炭为对比,从吸附影响因素(如溶液初始浓度、吸附时间、反应温度和溶液pH等)、吸附等温线、吸附动力学和吸附热力学等多个方面探索两种生物炭(单独黑液木质素基生物炭和造纸黑液木质素/聚乙烯共混热解生物炭)对水体中Cd(II)的吸附性能,为开发绿色、高效的重金属吸附剂及共热解生物炭的资源化利用提供必要的理论参考。
1 材料与方法
1.1 实验材料
木质素(LG)的来源是提取自湖南省某造纸厂造纸黑液。聚乙烯(PE)和硝酸镉(Cd(NO)3·4H2O)购于Sigma-Aldrich,均为分析纯。
实验前将LG与PE混合物通过称取等质量组分经研磨均匀后得到,命名为LG/PE。
1.2 生物炭的制备
生物炭的制备在立式固定床中进行。称取 1 g样品(LG或LG/PE),以N2为保护气,在开始升温前,连续通入N2排尽空气(20 min)。随后,保持 N2流量为 0.1 m3·h−1,以 10 ℃·min−1的升温速率升温至600 ℃,恒温2 h后,使其自然冷却至室温,收集样品的炭化产物即目标生物质炭。来源于 LG和 LG/PE的生物炭分别命名为 LG-600C和LG/PE-600C。
1.3 生物炭理化性质表征
生物炭的表观形貌利用扫描电镜进行分析(Inspect F50,FEI,USA),即将生物炭样品轻洒在碳胶表面,用气枪吹去固定不牢固部分,随后对该样品进行喷金处理,然后转移至设备中,在放大倍数为2—100 k下进行观察。生物炭的孔隙特性利用N2吸附/脱附分析仪进行测定,生物炭在测试前,需先在350 ℃下脱气5 h,它们的比表面积是根据其在−196 ℃下的 N2吸附/脱附等温线结果基于Brunauer-Emmett-Teller(BET)等式进行计算(Nova 2200e,Quantachrome,USA),对应的相对压力范围为0.05—0.3。生物炭的总孔容是根据氮容量在最高相对压力来计算,而平均孔尺寸则采取Barrett-Joyner-Halenda(BJH)法。利用红外光谱仪(Nicolet 6700,Thermo Fisher Scientific,USA)对生物炭样品表面的官能团进行分析。将样品与高纯度的溴化钾按照质量比例1꞉100进行混合研磨、并压片后,以1 cm−1的步调(分辨率)对样品在400—4000 cm−1波数范围类对红外光吸附振动的变化进行记录和分析。生物炭的无机元素组成(主要包括C、H和S),利用元素分析仪进行测定(EA112,Thermo Finnigan,USA),O的含量通过差值法进行计算。将生物炭与蒸馏水按照1꞉20的比例(质量/体积)进行混合,持续搅拌 2 h后利用 pH计(PHS-3C,雷驰)测定悬浊液的pH,即为对应生物炭的pH。生物炭的灰分含量根据ASTM D 1762-84标准方法进行测定。
1.4 生物炭对Cd(II)的吸附
分别称取0.1 g生物炭粉末,置于100 mL的三角瓶中,并加入50 mL的Cd(II)溶液。随即将三角瓶转移至水平机械摇床中,以120 r·min−1的速度摇晃震荡。当反应结束,利用0.45 μm的滤头对三角瓶中的悬浊液进行过滤,收集滤液,经 1%硝酸稀释后利用原子吸收色谱测定溶液中 Cd(II)浓度(FAAS-M6,Thermo,USA)。其中,Cd(II)的初始质量浓度范围为5—200 mg·L−1;吸附时间为5 min—8 h;环境温度为15—45 ℃;溶液pH为1—5。所有实验设置3组平行,数据采用平均值。
2 结果与讨论
2.1 生物炭理化性质分析
图1为LG-600C和LG/PE-600C的SEM图像。由图可知,LG-600C的表面比较平整、光滑,孔隙以直径大于2 μm的大孔结构为主;而添加PE共热解得到的 LG/PE-600C,其表面相对粗糙,附着大量细碎颗粒,存在丰富的小、微孔隙结构。孔隙分析显示,LG/PE-600C的比表面积和微孔比表面积分别为 213.87 m2·g−1和 108.74 m2·g−1,均约为LG-600C的2.5倍,表明PE的添加能够促进LG孔隙结构的发育(见表1),其原因可能在于PE在共热解过程中作为供氢体提供大量氢/烃基自由基,强化 LG 的分解(Wei et al.,2016)。LG-600C 和LG/PE-600C的平均孔隙直径分别为 40.12 nm和23.85 nm,即 LG/PE-600C的平均孔隙直径小于LG-600C,这与SEM的结果一致。

图1 生物炭的SEM图像Figure 1 SEM images of biochar

表1 生物炭孔隙分析Table 1 Biochar pore analysis
LG-600C和LG/PE-600C的FT-IR图谱见图2。如图所示,LG-600C和LG/PE-600C均具有丰富的表面官能团。其中,波数为3450—3380 cm−1的吸收峰主要归属于−OH的弯曲振动;C-H的伸缩振动吸收峰主要出现在2930、2840、1465、850 cm−1;1640 cm−1和1510 cm−1主要为芳香性C=C的伸缩振动;波数 1120—1020 cm−1的峰主要归属于C−O−C的伸缩振动(Keiluweit et al.,2010)。通过对比分析发现,LG/PE-600C的表面含氧官能团(即−OH和 C−O−C)强度较 LG-600C明显减弱,表明PE的添加导致LG表面含氧官能团的减少。

图2 生物炭的FT-IR图谱Figure 2 FT-IR spectra of biochar
生物炭的元素分析结果见表2。LG-600C的C、H、O含量分别为80.15%、4.12%、14.23%,而PE添加后所得生物炭(LG/PE-600C)的C含量增加,H和O减少。O/C和H/C分析显示,LG-600C的O/C和 H/C分别为 17.75%和 5.14%,均大于LG/PE-600C(分别为5.48%和3.86%)。这一结果表明PE添加共热解促进LG的O的脱除,导致表面含氧官能团减少,芳香化程度增加(Keiluweit et al.,2010;Dewangan et al.,2016)。pH 的结果显示,LG/PE-600C的pH较LG-600C有所增加,其可能与PE添加导致LG的O的脱除和表面含氧官能团减少有关(Chen et al.,2015)。

表2 生物炭的理化特性Table 2 The physical and chemical properties of biochar
2.2 生物炭对Cd(II)的吸附性能
2.2.1 Cd(II)初始浓度的影响
Cd(II)初始浓度对生物炭(LG-600C 和LG/PE-600C)吸附性能的影响见图3。从图中可以看出,LG-600C对Cd(II)的吸附性能相对较弱,在5—200 mg·L−1的初始质量浓度范围内,其最大吸附量仅为5.32 mg·g−1,这一结果与周艳等的报道一致(周艳等,2016)。相比之下,LG/PE-600C对Cd(II)具有较强的吸附性能,最大吸附量高达 39.80 mg·g−1。基于这一结果,下面的研究主要集中在对LG/PE-600C吸附性能的探索。其中,LG/PE-600C在初始质量浓度为 5—100 mg·L−1范围内,随着Cd(II)初始浓度的增加,其吸附量快速增加,由2.44 mg·g−1增加至 35.56 mg·g−1,极差为 33.12 mg·g−1。Cd(II)初始浓度的增加导致吸附量的增加,其原因主要在于较高的初始浓度下,Cd(II)具有较大的移动驱动能,能够有效的克服吸附质和溶液之间的物质移动阻抗(Xu et al.,2014)。当初始质量浓度为100—200 mg·L−1时,LG/PE-600C 的吸附量随着初始浓度的增加变得缓慢,为 35.56—39.80 mg·g−1,极差为 4.24 mg·g−1。这主要因为高浓度下,LG/PE-600C对 Cd(II)的吸附位点逐渐被占据,Cd(II)之间存在较强的竞争吸附和相互排斥作用(Chen et al.,2015)。相比于吸附量,LG/PE-600C对 Cd(II)吸附去除率随着初始浓度的增加呈降低趋势(见图3)。当 Cd(II)初始质量浓度为 5 mg·L−1时,其去除率为97.17%,而Cd(II)初始质量浓度为200 mg·L−1时,其去除率降低至40.04%。这主要因为生物炭提供的吸附位点数一定,随着初始浓度的增大,溶液中未被吸附 Cd(II)的浓度也在增大,去除率因此而降低(Keiluweit et al.,2010)。

图3 初始质量浓度对生物炭吸附性能的影响Figure 3 The effect of initial concentration on the adsorption performance of biochar
2.2.2 吸附时间
如图4所示,LG/PE-600C对Cd(II)的吸附量在0—40 min范围内随着吸附时间的增加而快速增加,由 0 mg·g−1增加至 35.65 mg·g−1。随后,继续增加吸附时间,LG/PE-600C对Cd(II)的吸附量增加较缓慢(吸附量变化范围为 35.65—36.48 mg·g−1,极差为0.83 mg·g−1),逐渐的达到平衡。LG/PE-600C在0—40 min的吸附量占平衡吸附量的 98%,这说明LG/PE-600C对 Cd(II)的吸附主要发生在这一时间段。其原因主要在于,吸附未达到平衡前,LG/PE-600C表面具有大量的吸附位点空位,Cd(II)能够被快速的吸附固定,随着反应的继续,LG/PE-600C表面逐渐被占据,被吸附固定的Cd(II)逐渐减少,导致吸附量增加变缓(Shen,2015)。当吸附到 LG/PE-600C 表面的 Cd(II)与从LG/PE-600C表面脱附下来的Cd(II)相接近时,吸附过程达到动态平衡。
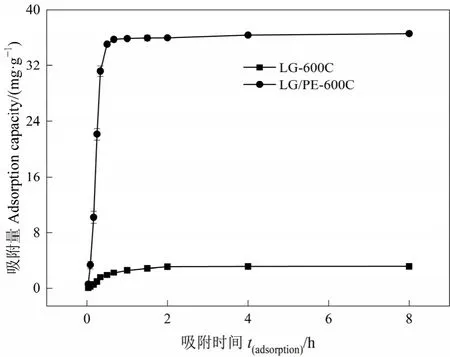
图4 吸附时间对生物炭吸附性能的影响Figure 4 The effect of time on the adsorption performance of biochar
2.2.3 环境温度
环境温度对 LG/PE-600C吸附 Cd(II)的影响见图5。由图可知,当环境温度为15、25、35和45 ℃时,LG/PE-600C对Cd(II)的吸附量分别为24.01、35.56、43.36 和 44.33 mg·g−1,即环境温度的增加有利于生物炭吸附量的提高。这一结果主要归因于较高的环境温度下,溶液中 Cd(II)的热运动加剧,Cd(II)与 LG/PE-600C表面吸附位点的碰撞接触几率增加,从而导致Cd(II)吸附量增加。

图5 环境温度对生物炭吸附性能的影响Figure 5 The influence of ambient temperature on the adsorption performance of biochar
2.2.4 溶液pH
溶液pH对生物炭吸附Cd(II)性能的影响如图6所示。溶液 pH的增加能够促进 LG/PE-600C对Cd(II)的吸附。当溶液pH由1增加至5时,对应的吸附量由 2.78 mg·g−1增加至 35.57 mg·g−1。可能原因在于,较低的溶液pH下,溶液中存在大量的H+,H+的存在将与 Cd(II)形成竞争,导致 LG/PE-600C中大量吸附位点被H+占据,不利于Cd(II)的吸附;而随着溶液pH值的逐渐升高,溶液中H+减少,大量吸附位点暴露,促进 Cd(II)吸附(刘莹莹等,2012)。

图6 溶液pH对生物炭吸附性能的影响Figure 6 The influence of solution pH on the adsorption performance of biochar
2.3 吸附模型及机理分析
2.3.1 吸附等温线模型分析
利用Langmuir和Freundlich吸附等温线模型对LG-600C和LG/PE-600C吸附Cd(II)的过程进行描述(Wang et al.,2016)。其中,Langmuir模型的计算等式为:

式中:
qe——碳材料对 Cd(II)的平衡吸附量(mg·g−1);
ρe——碳材料对 Cd(II)溶液吸附后的平衡质量浓度(mg·L−1);
qm——理论最大吸附量(mg·g−1);
k1——与相互作用能量相关的 Langmuir吸附常数(L·mg−1)。
通过对等式(1)进行变换后,可得到Langmuir模型的线性方程:

Langmuir模型中的参数qm和k1可通过ρe与ρe/qe进行线性拟合后得到。
Freundlich模型的计算等式为:

式中:
qe——碳材料对 Cd(II)的平衡吸附量(mg·g−1);
ρe——碳材料对 Cd(II)溶液吸附后的平衡质量浓度(mg·L−1);
kf——Freundlich 亲和力系数[mg(1−n)Ln·g−1];
n——Freundlich线性常数。
通过对等式(3)进行变换后,可得到Freundlich模型的线性方程:

Freundlich模型中的参数kf和n可通过lnρe和lnqe进行线性拟合后得到。
Langmuir和 Freundlich模型对 LG-600C和LG/PE-600C对Cd(II) 吸附过程的线性拟合结果见表3和图7。由表3可知,LG-600C和LG/PE-600C经Langmuir模型拟合的相关系数(R2)分别为0.998和0.999,而经Freundlich模型拟合得到的R2分别为0.974和0.929,表明LG-600C和LG/PE-600C对Cd(II)的吸附过程更符合于Langmuir模型,即该过程主要为单分子层吸附(Chen et al.,2015)。基于Langmuir模型所得到 LG-600C和 LG/PE-600C对Cd(II)的理论最大吸附量分别为5.54 mg·g−1和40.82 mg·g−1。其中,理论最大吸附量的结果表明,LG/PE-600C对 Cd(II)的吸附性能明显优于部分文献报道中所使用的吸附材料,如活性炭、碳纳米管、牛粪生物炭等(Xu et al.,2014;Fahad et al.,2015;王丹丹等,2015)。

表3 生物炭的吸附等温线参数Table 3 Adsorption isotherm parameters of biochar

图7 生物炭对Cd(II)吸附的吸附等温线拟合Figure 7 Adsorption isotherm fitting of Cd(II) adsorption by biochar
2.3.2 吸附动力学模型分析
利用准一级动力学模型和准二级动力学模型对LG-600C和LG/PE-600C对Cd(II)吸附与吸附时间的关系进行分析(Wang et al.,2016)。其中,准一级动力学模型的计算等式为:

式中:
t——吸附时间(h);
qt——在吸附时间点t时碳材料对Cd(II)的实时吸附量(mg·g−1);
qe——碳材料对 Cd(II)的平衡吸附量(mg·g−1);
k1——吸附速率常数(h−1)。
通过对等式(5)进行积分后,可得到准一级动力学模型的线性方程:
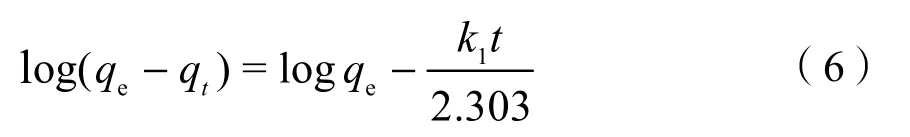
即准一级动力学模型中的参数k1和qe可通过t与log(qe−qt)进行线性拟合后得到。
准二级动力学模型的计算等式为:

式中:
t——吸附时间(h);
qt——在吸附时间点t时碳材料对Cd(II)的实时吸附量(mg·g−1);
qe——碳材料对 Cd(II)的平衡吸附量(mg·g−1);
k2——吸附速率常数[g·(mg·h)−1]。
通过对等式(7)进行积分后,可得到准二级动力学模型的线性方程:

准二级动力学模型中的参数k2和qe可通过t与t/qt进行线性拟合后得到。
准一级动力学模型和准二级动力学模型对LG-600C和LG/PE-600C对Cd(II)吸附过程拟合的结果见图8和表4。由表可知,准二级动力学模型拟合所得到LG-600C和LG/PE-600C对Cd(II)吸附的R2分别为0.936和0.928,明显高于准一级动力学模型(R2分别为0.230和0.459),表明准二级动力学模型可以很好地拟合LG-600C和LG/PE-600C对 Cd(II)的吸附过程。且基于准二级动力学模型所计算得到LG-600C和LG/PE-600C对Cd(II)的理论平衡吸附量为 3.60 mg·g−1和 40.16 mg·g−1,与实际平衡吸附量 3.14 mg·g−1和 36.58 mg·g−1更为接近。另外,吸附过程符合准二级动力学模型说明LG-600C和LG/PE-600C对Cd(II)的吸附主要由化学吸附作用主导(Chen et al.,2015)。
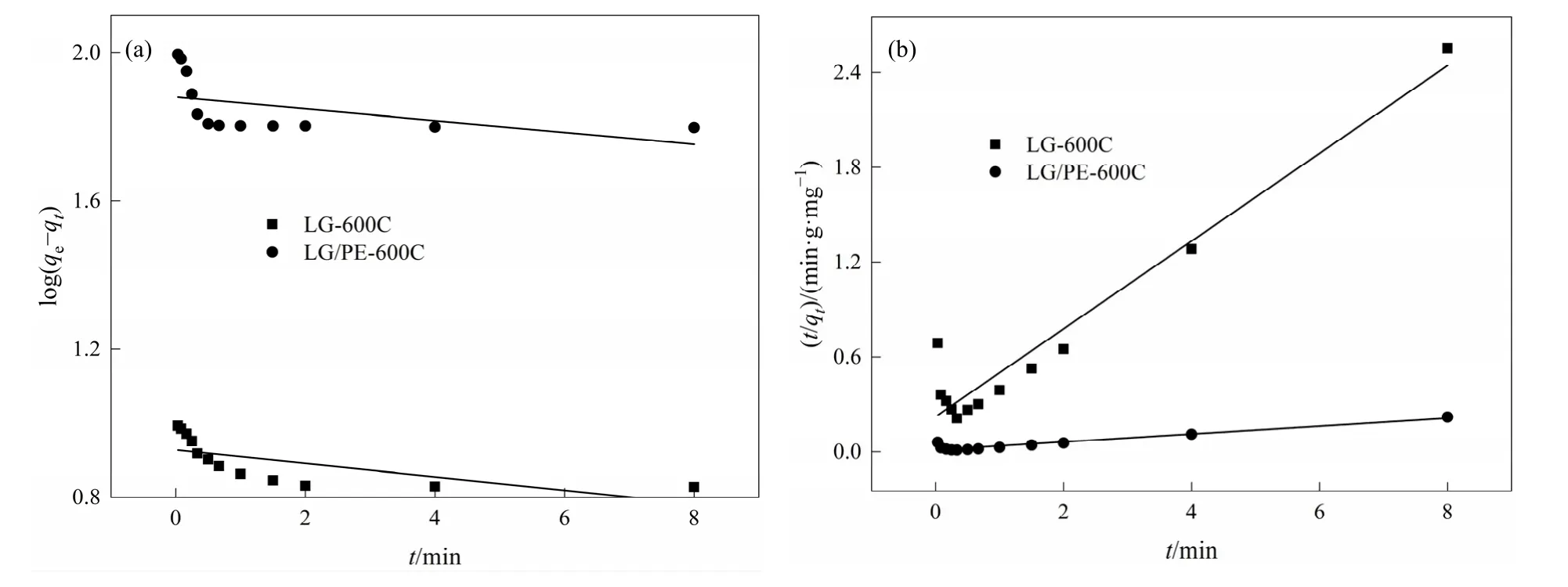
图8 生物炭对Cd(II)吸附的吸附动力学拟合Figure 8 Adsorption kinetics fitting of Cd(II) adsorption by biochar

表4 生物炭吸附动力学参数Table 4 Biochar adsorption kinetic parameters
2.3.3 吸附热力学模型分析
吸附过程受环境温度的影响程度可以通过吉布斯自由能(ΔG0)、焓(ΔH0)和熵(ΔS0)等热动力学参数进行描述。ΔG0用于评判一个反应的自发性,其中,负值的ΔG0表示该反应为自发反应,而正值的ΔG0表示该反应为非自发反应;ΔH0则与系统能量变化有关,其中,ΔH0>0表示该反应为吸热反应,而ΔH0<0表示该反应为放热反应;ΔS0与吸附过程中的无序状态以及吸附剂与吸附质之间的亲和力有关(Murat et al.,2013)。ΔG0、ΔH0和ΔS0通过下面等式计算:

式中:
Ke——无量纲的吸附平衡常数;
R——气体摩尔常数[8.314 J·(mol·K)−1];
T——绝对温度(K)。
Ke通过分配常数(Kw)与溶剂的密度(ρ)进行计算:


式中:
qe——碳材料对 Cd(II)的平衡吸附量(mg·g−1);
ρe——碳材料对 Cd(II)溶液吸附后的平衡质量浓度(mg·L−1);
ρ——水的密度(g·cm−3)。
根据水的密度为1 g·cm−3,所以等式(11)可写成:

反应过程中 ΔG0、ΔH0和 ΔS0三者存在如下等式的关系:

结合等式(13)可得:
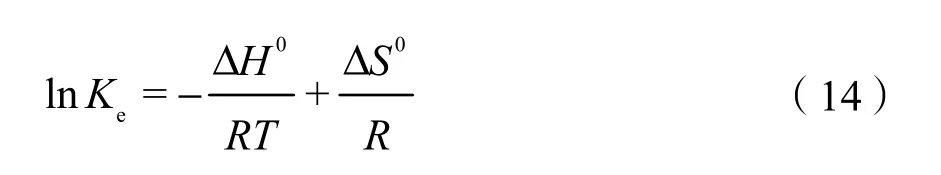
ΔH0和ΔS0可通过1/T和lnKe的线性拟合中的截距和斜率进行计算。
表5为LG-600C和LG/PE-600C对Cd(II)吸附的热力学分析结果。由表可知,LG-600C和LG/PE-600C的 ΔG0均小于 0,表明 LG-600C和LG/PE-600C对 Cd(II)的吸附反应为自发的反应。LG-600C和 LG/PE-600C的 ΔH0分别为 43.84 kJ·mol−1和 55.44 kJ·mol−1,均为正值,表明 LG-600C和 LG/PE-600C吸附 Cd(II)的过程为吸热反应,在一定范围内升高温度有利于反应的进行,这与环境温度对LG-600C和LG/PE-600C吸附Cd(II)影响的结果一致(见图5)。LG-600C和LG/PE-600C的ΔS0均大于0,表示LG-600C和LG/PE-600C吸附Cd(II)过程具有较强无序性,且生物炭和 Cd(II)之间具有较强的亲和力。

表5 生物炭对Cd(II)吸附的热力学参数Table 5 Thermodynamic parameters of Cd(II) adsorption by biochar
2.3.4 潜在吸附机理
孔填塞、表面沉积、配位、离子交换、沉淀等作用被认为是吸附剂吸附固定重金属离子的主要机理(Shen,2015)。其中,孔填塞和表面沉积作用为物理作用,分别与吸附剂孔隙特性和吸附剂表面粗糙程度有关;而配位、离子交换、沉淀为化学作用,分别与表面官能团和吸附剂中矿物质有关(Murat et al.,2013;Wang et al.,2016)。如图1所示,LG-600C和LG/PE-600C具有相对丰富的孔隙结构,N2吸附/脱附分析显示,二者的比表面积分别为 89.12 m2·g−1和 213.87 m2·g−1,由此表明孔填塞作用可能是LG-600C和LG/PE-600C吸附Cd(II)的机理之一。而LG/PE-600C的比表面积较大,表明其表面所能暴露的吸附位点相对较多,其吸附性能较 LG-600C更强,同时,LG/PE-600C具有较LG-600C更小的平均孔隙直径(LG-600C和LG/PE-600C的平均孔隙直径分别为 40.12 nm和23.85 nm),表明LG/PE-600C对Cd(II)具有更强的固定能力(Cd(II)的水合离子半径为 4.26 Å),这与吸附的研究结果一致(Meng et al.,2014;Wang et al.,2017)。从表面粗糙程度来看,LG-600C较平整光滑,而LG/PE-600C表面附着有大量碎屑颗粒(见图1),这表明表面沉积作用也可能是造成LG/PE-600C对Cd(II)吸附量较大的原因(Su et al.,2005)。LG-600C和LG/PE-600C的红外光谱分析显示(见图2),二者表面具有丰富的含氧官能团(包括−OH和C−O−C等)和芳香性的C=C,这些官能团的存在可作为吸附位点通过配位(如C−π阳离子键等)作用吸附固定Cd(II)(见等式 (15)—(16))(Wang et al.,2017)。LG-600C和LG/PE-600C中含有灰分,分别为3.54%和3.87%。据报道,木质素中的灰分主要以钠盐、硅酸盐为主(Marina et al.,2011)。这些灰分组分经过木质素热解后,同样存在于生物炭中,该灰分组分的存在可通过离子交换作用和沉淀作用促进Cd(II)的吸附固定(见等式17)(Chen et al.,2015)。准二级动力学模型的拟合结果表明LG-600C和LG/PE-600C对Cd(II)的吸附主要由化学作用主导,由此推测,LG-600C和LG/PE-600C对Cd(II)的吸附主要通过配位、离子交换、沉淀等作用实现。

3 结论
将 LG与 PE在 600 ℃下共热解得到LG/PE-600C,其表面粗糙,附着大量细碎颗粒,孔隙结构发达,比表面积为213.87 m2·g−1,表面含有丰富的官能团(如−OH,C−H,C=C和C−O−C等)。PE的添加能够促进LG的强化分解和O的脱除,导致所得LG/PE-600C的O含量降低,pH增加。在 Cd(II)初始质量浓度为 5—100 mg·L−1、吸附时间为0—40 min、环境温度为15—45 ℃、溶液pH为1—5的范围内,LG/PE-600C对 Cd(II)的吸附量逐渐增加。Langmuir模型和准二级动力学模型能够很好地拟合该吸附剂过程中,表明 LG/PE-600C对Cd(II)的吸附为化学作用主导的单分子层吸附。基于 Langmuir模型所得到的理论最大吸附量达到40.82 mg·g−1。热力学分析证实,LG/PE-600C 对Cd(II)的吸附为自发的吸热反应。机理分析表明,LG/PE-600C主要通过配位、沉淀、离子交换等作用对Cd(II)进行吸附。
