增强超声对乳腺BI-RADS 4 类肿块的再评估价值*
2022-04-16汪向前吴意赟许华宁蔡婷
汪向前 吴意赟 许华宁 蔡婷
(南京中医药大学附属医院超声医学科,江苏 南京210029)
乳腺影像报告与数据系统 (Breast imaging reporting and data system,BI-RADS)已广泛应用于临床,使乳腺超声报告标准化,促进了医患及医师之间的有效沟通,极大地提高了诊断效率。BI-RADS分类系统在评估3类和5类肿块方面表现良好[1],然而BI-RADS 4类肿块的恶性风险区间为2%~95%,恶性风险跨度较大,部分患者会面临过度诊疗或面对延误诊断而被建议短期随访的风险,给临床决策带来很大困扰。近年来,增强超声(Contrast-enhanced ultrasound,CEUS)在乳腺肿块鉴别诊断方面的价值逐步得到肯定。本研究探讨在常规超声基础上增加CEUS对乳腺BI-RADS 4 类肿块的再评估价值研究,以期进一步提高超声诊断的准确性,给临床决策提供可靠依据。
1 资料与方法
1.1 一般资料 选取2018年9月~2020年3月在我院经手术病理证实的患者174例共180个乳腺肿块,均为女性,年龄19~85岁,平均(48.2±13.5)岁,病灶最大直径0.20~10.40 cm,平均(2.09±1.28)cm。排除妊娠或哺乳期妇女,既往已有明确病理结果或经干预治疗的乳腺肿块者。本研究经我院医学伦理委员会批准,所有患者均签署知情同意书。
1.2 仪器与方法
1.2.1 仪器 使用Philips iU22 彩色多普勒超声诊断仪,常规超声检查采用L12-5 线阵探头,频率5~12 MHz ;CEUS采用L9-3线阵探头,频率3~9 MHz。造影剂采用SonoVue(意大利 Bracco公司)。
1.2.2 CEUS检查 所有患者均由同一位具有5年以上乳腺超声检查经验的超声医师对双侧乳腺进行全面检查,发现可疑肿块后详细记录其位置、最大直径、二维超声特征(形状、边界、纵横比、内部回声、后方回声改变、有无钙化及周围组织改变)及彩色多普勒血流成像特征,规范化对乳腺肿块进行常规超声BI-RADS分类。常规超声检查后行CEUS检查,所选观察切面应避开明显钙化及液化部分,并与周边正常乳腺组织对比观察,聚焦点置定在肿块后方,机械指数0.07。常规制备造影剂悬浮液,经肘静脉团注3.0 mL造影剂,随后用5.0 mL氯化钠溶液冲管,同时开始保存动态影像,记录时间>2 min。
1.2.3 超声造影图像分析 导出声像资料,由2位有两年以上乳腺CEUS检查经验的医师进行读片,2位医师均不参与检查,且对患者的临床资料和最终病理结果均不知情,如果2位医师存在争议,通过讨论达成共识。
1.3 统计学分析 应用SPSS 21.0统计软件,以病理结果为金标准,构建受试者工作特征(Receiver operating characteristic,ROC)曲线,计算 BI-RADS分类经CEUS调整前后的曲线下面积 (Are aunder curve,AUC),采用Z检验对AUC进行比较。P<0.05为差异有统计学意义。
2 结果
2.1 病理结果 174例共180个肿块:良性肿块81个,其中腺病37个,纤维腺瘤15个,导管内乳头状瘤12个,腺病并纤维腺瘤形成和慢性乳腺炎各7个,肉芽肿性乳腺炎3个;恶性肿块99个,其中浸润性乳腺癌82个,导管原位癌8个,乳头状癌4个,黏液癌3个,淋巴瘤和恶性叶状肿瘤各1个。所有乳腺肿块均经常规超声检查诊断为BI-RADS 4类。
2.2 经CEUS BI-RADS分类调整前后与病理诊断结果的对比 本研究180个肿块中,调整前常规超声模式下结果:BI-RADS 4A类 74个,其中良性65个,恶性9个,恶性率12.2%;BI-RADS 4B类 48个,其中良性14个,恶性34个,恶性率70.8%;BI-RADS 4C类 58个,其中良性2个,恶性56个,恶性率96.6%。经CEUS调整后结果:BI-RADS 3类 45个,其中良性43个,恶性2个,恶性率4.4%;BI-RADS 4A类 26个,其中良性24个,恶性2个,恶性率7.7%;BI-RADS 4B类 24个,其中良性11个,恶性13个,恶性率54.2%;BI-RADS 4C类 36个,其中良性4个,恶性32个,恶性率88.9%;BI-RADS 5类 49个,其中良性0个,恶性49个,恶性率100%。见表1。
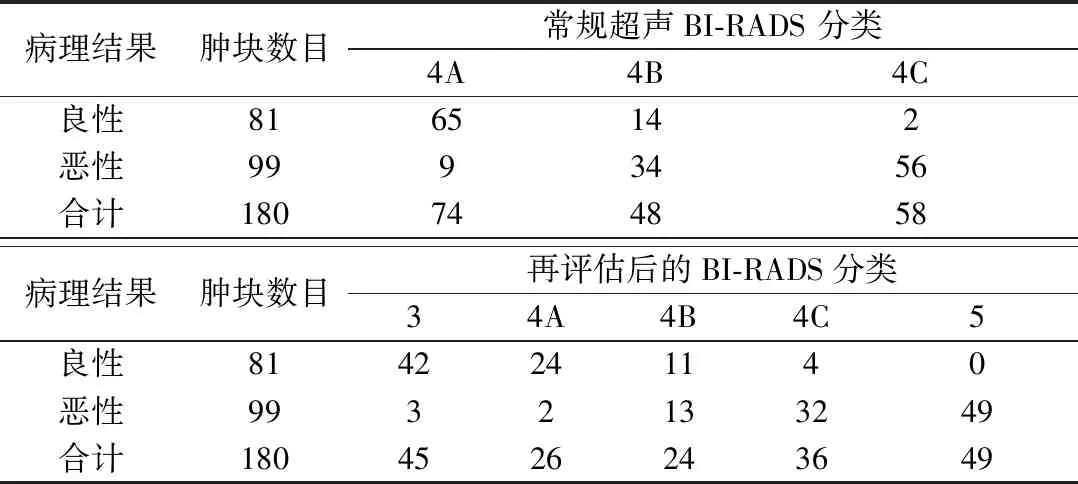
表1 乳腺肿块经CEUS BI-RADS 分类再评估前后与病理诊断对比(个)Table 1 Comparison of breast mass with pathological diagnosis before and after CEUS BI-RADS classification reassessment
2.3 BI-RADS 分类经CEUS调整幅度 对照病理结果,经CEUS检查BI-RADS分类调整后:下调个数为55个,其中,45个BI-RADS 4A类被下调至3类,10个BI-RADS 4B类被下调至4A类;维持不变个数为37个,其中,BI-RADS 4A类16个,BI-RADS 4B类11个,BI-RADS 4C类10个;上调个数为88个,其中13个BI-RADS 4A类被上调至4B类,27个BI-RADS 4B类被上调至4C类,48个BI-RADS 4C类被上调至5类。见图1~3和表2。
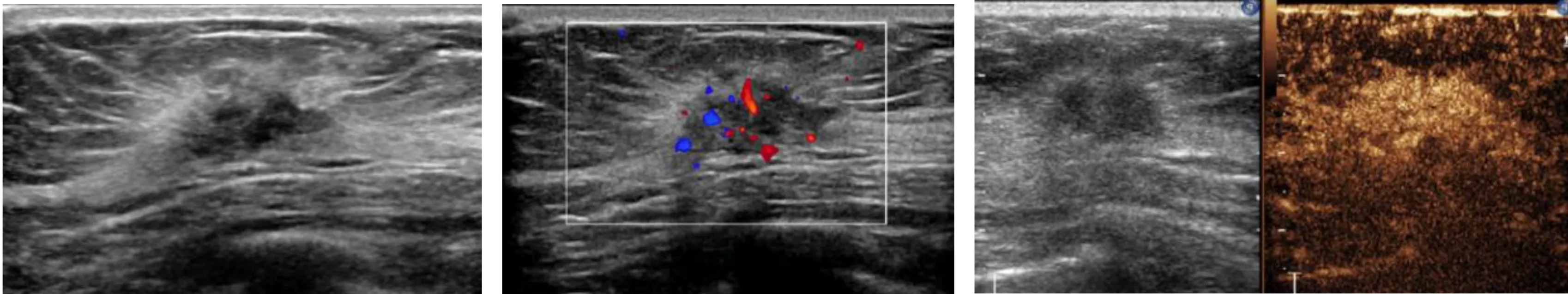
图1 CEUS对常规超声BI-RADS 分类作降类调整Figure 1 Downgrading adjustment of conventional ultrasound BI-RADS classification by CEUS注:常规超声显示实性低回声肿块,边缘不完整、成角,拟BI-RADS 4B类,彩色多普勒显示肿块内部可见点条状血流信号,CEUS显示肿块呈同进均匀性稍高增强,增强后范围未见明显扩大,拟调整降为BI-RADS 4A类。术后病理示:乳腺腺病并导管内乳头状瘤
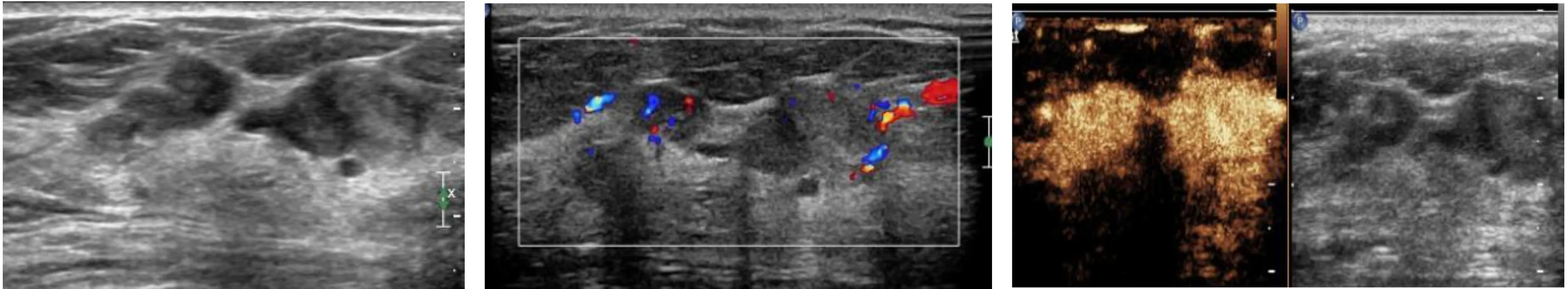
图2 CEUS对常规超声BI-RADS 分类维持不变Figure 2 CEUS maintained the BI-RADS classification in conventional ultrasound注:常规二维超声显示导管走行区见两个类似实性等稍低回声肿块,边缘欠完整,呈浅分叶状,拟BI-RADS 4A类,彩色多普勒显示肿块内部可见少许血流信号,CEUS显示病灶呈快进均匀性高增强,增强后范围未见明显扩大,拟BI-RADS分类维持不变,仍考虑为BI-RADS 4A类。术后病理示:导管内乳头状瘤
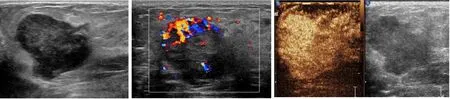
图3 CEUS对常规超声BI-RADS 分类作升类调整Figure 3 Upgrading adjustment of conventional ultrasound BI-RADS classification by CEUS注:常规二维超声显示实性低回声肿块,边缘欠完整,周边似见高回声晕,拟BI-RADS 4B类,彩色多普勒显示肿块近一极边缘可见弥漫丰富血流信号,CEUS显示肿块呈快进不均匀性高增强,增强后形态不规则,且范围明显扩大,拟调整升为BI-RADS 4C类。术后病理示浸润性乳腺癌
2.4 经CEUS BI-RADS分类调整前后诊断效能比较 乳腺肿块经CEUS BI-RADS分类调整前后的诊断效能,见表3。常规BI-RADS分类评估的ROC曲线下面积为0.900,经CEUS调整后BI-RADS分类评估的ROC曲线下面积为0.947,两者比较的差异存在统计学意义(Z=3.007,P<0.05),见图4。这表明CEUS能够提高乳腺BI-RADS 4类病灶良恶性的诊断准确性。

表3 经CEUS BI-RADS分类再评估前后诊断效能比较(×10-2)Table 3 Comparison of diagnostic efficacy before and after CEUS BI-RADS classification reassessment
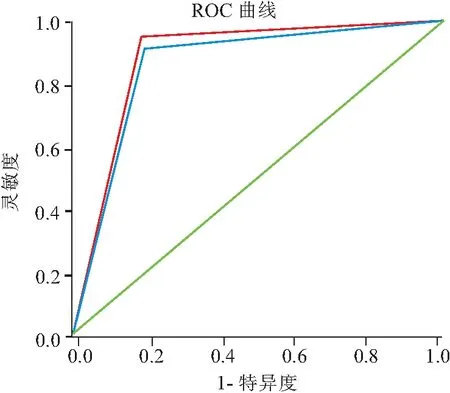
图4 常规超声和CEUS诊断乳腺良恶性肿块的ROC曲线图Figure 4 ROC curves of benign and malignant breast lesions diagnosed by conventional ultrasound and CEUS
3 讨论
美国影像医学会(ACR)在2013年BI-RADS分类(第五版)[2]中指出4类肿块的恶性风险区间为2%~95%,其中4A、4B、4C分别为2%~10%、10%~50%、50%~95%,因其恶性率跨度大,给临床决策带来诸多不便。因此能否找到新的途径优化常规超声BI-RADS分类,降低活检率成为目前亟待解决的问题。既往有大量研究[3-6]显示,CEUS是纯血池显影,能提高常规超声所不能检测到的低速血流的敏感度,能真实反映肿瘤及周边组织的灌注特征,对乳腺肿块良恶性鉴别诊断价值逐步得到认可[7-9],从而有助于提高超声医师对于乳腺良恶性肿块的鉴别诊断能力,可作为常规超声检查的重要补充。
本研究应用常规超声评估病灶的BI-RADS分类:99个恶性肿块中有9个被误诊为良性,均被判为BI-RADS 4A类,分析原因可能与肿块较小,恶性征象不突出,声像图复杂及多样化有关[10-11];81个良性肿块中,有16个被误诊为恶性,其中14个被判为BI-RADS 4B类,2个被判为BI-RADS 4C类,分析原因主要是良性肿块亦可表现出恶性征象,良恶性肿块之间存在部分特征重叠,比如硬化性腺病或肉芽肿性乳腺炎等病变,往往和乳腺恶性肿瘤难以鉴别[12-14]。Takin等[15]对31例硬化性腺病患者进行超声特征分析,主要以内部回声不均质、边缘模糊、形态不规则及非平行生长为主要特点;杨晓云等[16]研究中56例肉芽肿性乳腺炎超声声像图与乳腺癌相似,多表现为低回声肿块、边界不清、形态不规则,而这些特点恰是常规超声BI-RADS分类的评估因素。
大部分乳腺恶性肿块的CEUS表现为高增强[17-18],但因部分肿瘤细胞的增殖速度快于肿瘤内部新生血管的生成速度,无新生血管生成的这部分肿瘤细胞短时间内造影剂灌注不佳,病灶即表现为低增强或充盈缺损[19-21]。CEUS一定程度上可减少假阳性活检肿块数量[22]。本组病例结合CEUS对BI-RADS分类进行调整。下调个数为55个,45个BI-RADS 4A类被下调至3类,10个BI-RADS 4B类被下调至4A类,下调至3类中有 2 个为假阴性,术后病理证实均为导管原位癌,其CEUS表现为同进均匀性低增强的灌注模式。提示经CEUS后有很大一部分降为3类的病例避免了有创穿刺活检,但乳腺癌异质性很强,仅仅依靠增强强度为低增强来判断良恶性往往存在局限性,并不能因为无恶性CEUS征象而不采取临床干预措施。新版BI-RADS分类中,依然要求对此类肿块行组织病理学诊断[23]。上调个数为88个,13个BI-RADS 4A类被上调至4B类,27个BI-RADS 4B类被上调至4C类,48个BI-RADS 4C类被上调至5类。由此可见,在常规超声的基础上结合CEUS可一定程度提高假阴性肿块的检出率,同时还能给部分恶性肿块增加诊断信心。
另外,本组病例中,常规超声BI-RADS分类4A类恶性率12.2%,4B类恶性率70.8%,4C类恶性率96.6%,其中4A、4C类恶性风险与2013年第5版 BI-RADS分类较为一致,4B类恶性风险较其明显增高,分析原因主要是存在同病异像,异病同像,并高估了这部分病灶的恶性风险,与倪暾等[24]研究一致。然而经CEUS再评估后4B类恶性率为54.2%,与2013年第5版 BI-RADS分类中4B类病灶的恶性风险较为一致,说明CEUS可以弥补超声医师在常规超声BI-RADS分类中的不足。
本研究中,经CEUS再评估后的BI-RADS分类诊断敏感度、特异度、准确度、阳性预测值及阴性预测值均优于较调整前,常规BI-RADS分类评估的ROC曲线下面积为0.900,经CEUS调整后的ROC曲线下面积为0.947,说明CEUS在一定程度上提高了诊断效能,实现对乳腺疾病更精准的评估。
4 结论
结合CEUS可对常规超声BI-RADS分类优化再评估,尤其是对BI-RADS 4类肿块的再评估具有一定的应用价值。对于初判为假阴性肿块,可降低患者因漏诊或者延期确诊而导致的延误治疗,对其生存期以及生存质量造成影响;对于初判为假阳性肿块,可以减少不必要的穿刺活检。同时需要注意的是在临床实际工作中,单独靠CEUS评估乳腺肿块的良恶性并不实际,CEUS特征不能作为恶性风险的独立判断指标,良、恶性病灶间存在重叠,必须结合肿块的二维声像图特征以及患者的年龄、肿块的临床特征等进行综合评价,才能给临床提供更为可靠的治疗方案依据。
