1例绝经后子宫内膜非典型息肉样腺肌瘤
2022-04-13邹普润周卫华
邹普润 林 彤 周卫华
1.吉首大学医学院,湖南吉首 416000;2.吉首大学第一附属医院妇二科,湖南吉首 416000
子宫内膜非典型息肉样腺肌瘤(atypical Polypoid Adenomyoma,APA)是一种罕见的子宫内膜病变,最早由Mazur[1]于1981年报道,由不典型的子宫内膜样腺、鳞状上皮和肌纤维瘤间质组成,其组织学形态类似腺癌浸润肌层或恶性混合性苗勒氏肿瘤,可与子宫内膜不典型增生和/或癌并存。多发生于绝经前妇女,患病率逐年增高,且有恶变可能,保守治疗复发率高[2]。目前国内外文献报告绝经后女性APA 病例非常少,临床工作中对该类患者的诊治尚无统一标准,且缺少病例对照与参考,本文探讨为吉首大学第一附属医院(以下简称“本院”)收治的1例绝经后APA 病例,患者出现异常阴道流血症状,患糖尿病,且长期服用非甾体类雌激素类似药物,有子宫内膜肿瘤的典型症状以及高危因素,不易诊断,难以与子宫内膜恶性肿瘤相鉴别,经宫腔镜下病理组织活检确诊为APA,根据患者年龄及已完成生育,予行全子宫加双附件切除术治疗。
1 病例资料
患者,女,67 岁,因“绝经17年,阴道流血1 周”于2021年4月14日入院。患者50 岁左右绝经,绝经后偶有阴道淡黄色分泌物。2021年4月7日无明显诱因出现阴道流血,暗红色,量少,淋漓不尽,4月12日入本院门诊,行妇科B 超示:宫体大小约78 mm×68 mm×64 mm,形态增大。宫内膜厚35 mm,回声强弱不均,可见多发小片状液性暗区,呈“筛孔”样改变,拟“绝经后阴道流血查因”收入院。孕5 产3 存3 人流2,均系平产,35 岁结扎。患者13年前因胆囊结石行腹腔镜行胆囊切除术,7年前因乳腺癌行左乳腺切除术,术后行补充化疗后规律口服“他莫昔分片1片/次,2 次/d”至2021年2月停药,自诉规律复查乳腺彩超均未见明显异常,期间未行妇科B 超及相关激素水平检查。专科检查:宫颈萎缩,无举痛及接触性出血;宫体增大如孕2月大小;余未见明显异常。入院测身高:156 cm;体重:60 kg;体重指数(body mass index,BMI):24.65 kg/m2。急诊肝功能(干化学):血糖24.54 mmol/L(否认糖尿病史);尿沉渣:亚硝酸盐POSITIVE mS/cm,尿葡萄糖3+mS/cm。糖化血红蛋白测定:糖化血红蛋白11.5%。监测空腹血糖波动在:12.5~15.5 mmol/L;三餐后2 h 血糖波动在10.8~22.4 mmol/L。予请本院内分泌科会诊考虑2 型糖尿病,并予指导控制血糖稳定(空腹血糖≤10 mmol/L,餐后血糖≤15 mmol/L)后行宫腔镜下赘生物电切术,术中见宫内膜菲薄、充血,宫腔可见大小约4 cm×4 cm×5 cm肌瘤状结节,表面光滑、充血状、蒂细、突向宫腔。术后病理检测示非典型息肉样腺肌瘤(图1~3),建议临床追观。免疫组化:雌激素受体(estrogen receptor,ER)(+)、孕激素受体(progesterone receptor,PR)(+)、抗平滑肌抗体(anti-smooth muscle antibody,SMA)(血管周围+)、结蛋白(desmin,DES)(间质+)、核抗原Ki-67(腺体40%+);考虑患者现确诊糖尿病、长期服用他莫昔芬药物治疗等高危因素,警惕子宫内膜恶变可能,且患者67 岁,已绝经,建议行全子宫及双附件切除。请本院乳甲外科会诊并查阅患者7年前因乳腺癌行左乳腺切除术相关资料,暂不考虑乳腺癌转移等相关病变,经充分评估及结合患者意愿,予2021年4月28日腹腔镜辅助阴式子宫全切+双侧附件切除术,术后病理检测回示(子宫+双附件):①子宫平滑肌瘤伴玻变;②慢性宫颈炎,小灶呈子宫颈上皮内瘤变(cervical intraepithelial neoplasia,CIN)Ⅰ级;③子宫内膜萎缩,息肉形成伴多灶息肉样增生;④(双侧)输卵管慢性炎;⑤卵巢白体形成,(右)生发上皮包涵囊肿。
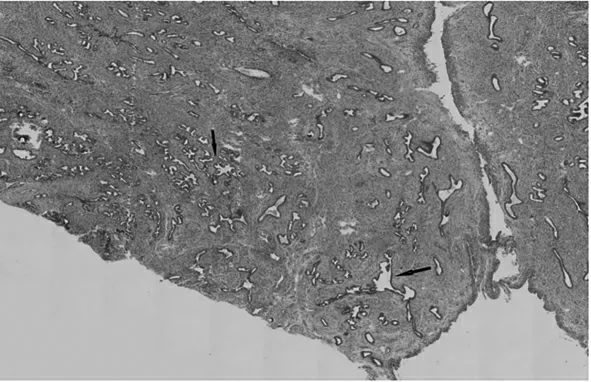
图1 APA 患者低倍镜下病理表现(40×)
随访到2021年8月31日复查均未发现异常情况。
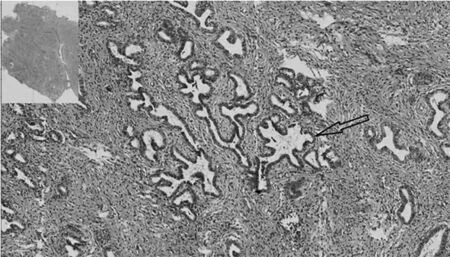
图2 APA 患者高倍镜下病理表现(200×)
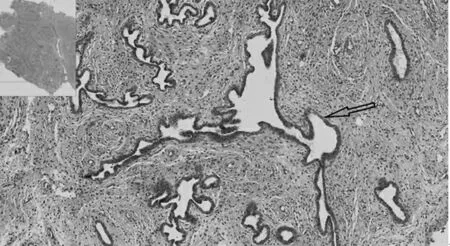
图3 APA 患者高倍镜下病理表现(200×)
2 讨论
APA 是一种具有恶变潜能的良性宫腔病变,常发生于绝经前女性,在绝经后妇女中少见,发病时平均年龄38 岁[3]。但国内有文献报道发病年龄及绝经后发病患者比例均高于国外[4]。临床症状无特异性,常表现为不规则阴道流血、盆腔疼痛或阴道异常分泌物,部分患者有不孕症病史[5],且可无症状,因不孕或体检、超声提示异常进一步宫腔镜检查或诊刮时发现。自APA1981年被报道以来,英文文献报道例数不足500 例,2002年Horn 等[6]报道第1例绝经后妇女的APA 病例,并得出结论高雌激素在APA 的发生中起重要作用。APA 的具体病因及发病机制目前尚不清楚,但Raffone 等[2,6-7]研究均显示与雌激素增加有一定关系,其高危因素与子宫内膜癌相似,包括肥胖、糖尿病、多囊卵巢综合征或长期使用外源性雌激素等;任健等[8]研究结果显示高BMI、血糖升高与APA 的发病可能相关,其报道48 例子宫内膜息肉样腺肌瘤研究中,患者BMI 平均(25.1±4.1)kg/m2。本病例中患者为绝经后妇女,阴道不规则流血,长期口服他莫昔芬(非甾体类雌激素类似物,对子宫内膜有弱雌激素作用)治疗,B 超检查发现宫内膜增厚,且病理检查提示APA,对于该患者而言,乳腺癌病史,长期服用他莫昔芬可能是导致患APA 的关键因素,但患者在口服他莫昔芬期间均未行妇科B 超等相关检查,所以本研究无法得出准确结论,朱一迪[9]研究显示绝经后乳腺癌患者长期口服他莫昔芬可引起子宫内膜病变;且患者入院后诊断2 型糖尿病,有子宫内膜癌高危因素,术前难以与之鉴别。APA 的诊断主要依据病理学诊断,大体上呈息肉样、黏膜下肌瘤样,与周围肌层组织分界清楚,术前、术中亦难以与子宫内膜息肉或子宫黏膜下肌瘤相鉴别[10]。病理学特征一般包括:显微镜下形态学结构表现出复杂,可见到不规则子宫内膜样腺体以及鳞状上皮化生,伴或不伴轻至中度的异型细胞;有研究表明,在免疫组化中,ER 和PR 均阳性,细胞增殖指数Ki-67 表现为低增殖,几乎未超过50%,但在子宫内膜样癌中甚至可能超过90%[11];但这些特征的敏感性及特异性并不高。本病例免疫组化结果完全符合文献中数据范围。
APA 的生物学表现为良性,预后较好,但具有复发性和低度恶变潜能,国外研究显示APA 合并不典型增生占5.5%,合并子宫内膜癌占5.9%。总的复发和进展为癌症的风险分别为28.9%和16.6%[2],因此明确诊断后应积极治疗。对于年龄较大、无生育要求、不能密切随诊或保守治疗无缓解甚至加重的患者,子宫切除术被认为是治疗这种病变的首选方法[2,12],尤其是像本例患者绝经后合并子宫内膜癌高危因素的患者。在年轻的未产妇中,尽管复发率很高,而且即使合并有ⅠA 期子宫内膜癌,也可接受病理指导下的宫腔镜保守手术治疗[10,13]。手术治疗包括刮宫术、经阴道病损切除术、宫腔镜下病损切除术等,其中通过宫腔镜手术进行保守治疗是最佳选择,因为它降低了复发的风险,提高了伴随癌或增生诊断的准确性,并保留了未来怀孕的可能性。一项荟萃分析结果显示接受宫腔镜保守手术治疗的APA 患者的复发率为22%,其他方式复发率为44%[13]。建议采取四步法在宫腔镜直视下手术,即切除病变、切除病变周围内膜、切除病变下浅肌层、子宫内膜多点活检术,并分别做病理检查[10]。
自2002年第1例绝经后妇女的APA 病例被报道以来,近年来国内外均少有文献报道绝经后妇女APA 病例,魏宝宝等[14]报道四川华西第二人民医院7年收治的16 例子宫内膜非典型性息肉样腺肌瘤患者中,仅1例是发生于绝经后。周巧云等[15]报道24 例APA 中,仅1例是发生于绝经后的63 岁妇女,与本病例症状相符,表现为阴道异常出血。其原因:一方面由于该病发病率低、临床医生对该疾病的了解及重视不足;另一方面,该病在临床表现、超声影像等方面缺乏特异性也是重要的原因。且目前尚无统一的治疗方案,本病例参照大多数学者对APA 妇女的治疗建议,经本院行宫腔镜检查病理检查确诊为APA 后,结合患者绝经后妇女,年龄67 岁,予行全子宫+双附件切除。
3 小结
综上所述,对于APA 患者,由于APA 部分症状与子宫内膜恶性肿瘤高度相似,首先需要与子宫恶性肿瘤鉴别,建议先采取腔镜手术切除并多点活检,并分别做病理检查及免疫组化,再根据患者年龄及有无生育要求的原则决定治疗方式。对于绝经后老年APA患者,已无生育要求,一经病理检查确诊,因其复发性和低度恶变潜能,建议首选子宫切除术,术后需要定期随访。尤其是类似于本病例患者的绝经后或无生育要求的妇女,阴道异常流血病史,长期服用雌激素或雌激素类似药物,合并糖尿病,具有子宫内膜肿瘤的典型症状以及高危因素,建议确诊为APA 后直接采取全子宫切除术。
