小金丸联合夏枯草胶囊治疗桥本甲状腺炎伴结节的效果及对炎症因子的影响
2022-04-13张明海
张 微 张明海 胡 君
1.赣南医学院第三附属医院内二科,江西赣州 341000;2.赣南医学院第一附属医院儿科,江西赣州 341000
桥本甲状腺炎是临床常见的自身免疫性甲状腺疾病,多发于中青年人群,早期临床症状不明显,晚期则出现甲状腺功能衰退的表现[1]。桥本甲状腺炎伴结节是临床常见类型,且可增加患者癌变风险[2]。临床中常使用左甲状腺激素改善患者的症状及预防桥本甲状腺炎甲状腺功能减退的趋势,但对于并发甲状腺结节及肿大的甲状腺患者疗效欠佳[3]。中医认为桥本甲状腺炎伴结节按其症状属于“瘿病”的范畴,因情志内伤,外加水土失宜而发[4]。小金丸含有的枫香脂、地龙等多味中药具有散结消肿、化瘀止痛的功效,此外夏枯草可散结消肿、清热解毒,两者联合能够改善患者体内微循环,抑制肿块、瘤体生长。本研究旨在探讨小金丸联合夏枯草胶囊治疗桥本甲状腺炎伴结节的效果及对炎症因子的影响。
1 资料与方法
1.1 一般资料
选取2018年5月至2020年6月赣南医学院第三附属医院收治的60 例桥本甲状腺炎伴结节患者作为研究对象,采用随机数字表法分为对照组(30 例)与研究组(30 例)。对照组中,男6 例,女24 例;年龄23~63 岁,平均(43.41±8.28)岁;病程3~36 个月,平均(9.83±4.16)个月。研究组中,男5 例,女25 例;年龄24~64 岁,平均(44.63±8.16)岁;病程4~37 个月,平均(10.57±4.78)个月。两组患者的一般资料比较,差异无统计学意义(P>0.05),具有可比性。诊断标准:中医诊断参照《中医内科学》[5]中瘿病的诊断标准,西医参照《中国甲状腺疾病诊治指南——甲状腺炎:亚急性甲状腺炎》[6]及《中国甲状腺疾病诊治指南——甲状腺结节》[7]中的相关诊断标准。纳入标准:①符合上述诊断标准者;②经甲状腺超声检查确诊者;③弥漫性甲状腺肿大者等。排除标准:①伴有明显压迫症状者;②伴有严重内科疾病者;③对本研究所用药物过敏者等。所有入选患者及家属均知情同意本研究并签署知情同意书,并经本院医学伦理委员会审核批准。
1.2 方法
对照组患者给予左甲状腺素钠片(德国默克公司,批准文号:H20100524,规格:50μg/片,生产批号:G0065L)口服,25~50 μg/次,1 次/d。研究组患者在对照组的基础上给予小金丸[华润三九(黄石)药业有限公司,国药准字Z42021086,规格:0.6 g/粒,生产批号:201201]及夏枯草胶囊[聚协昌(北京)药业有限公司,国药准字Z19991033,0.35 g/粒,生产批号:210104]口服,小金丸1.2~3.0 g/次,2 次/d;夏枯草胶囊0.7 g/次,2 次/d。12 周为1 个疗程,两组患者均连续治疗2 个疗程。
1.3 观察指标及评价标准
比较两组患者的甲状腺体积及甲状腺结节大小、抗甲状腺过氧化物酶抗体(TPO-Ab)、抗甲状腺球蛋白抗体(thyroid peroxidase antibody,TG-Ab)、促甲状腺激素(thyroid stimulating hormone,TSH)、γ 干扰素(γinterferon,IFN-γ)、白介素-2(interleukin-2,IL-2)、白介素-10(interleukin-10,IL-10)水平与不良反应发生情况。①分别于治疗前及治疗12、24 周采用常规甲状腺彩超测量两组患者的甲状腺体积及甲状腺结节直径大小。②抽取两组患者治疗前及治疗12、24 周5 ml空腹静脉血,用离心机以2500 r/min 的速度离心10 min,离心半径13.5 mm,采用放射免疫法检测血清TPOAb、TG-Ab、TSH 水平。③采用酶联免疫吸附法检测血清IFN-γ、IL-2、IL-10 水平。④观察两组患者治疗期间皮疹、呕吐、脏器损害等不良反应的发生情况。不良反应总发生率=不良反应总发生例数/总例数×100%。
1.4 统计学方法
采用SPSS 22.0 统计学软件进行数据分析,计量资料用均数±标准差(±s>)表示,两组间及组内两两比较采用t检验,组内多时间点整体比较采用方差分析;计数资料用频数或百分率(%)表示,组间比较采用χ2检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者治疗前后甲状腺体积及甲状腺结节大小的比较
两组治疗前的甲状腺体积及甲状腺结节比较,差异无统计学意义(P>0.05);研究组患者治疗12、24 周后的甲状腺体积及甲状腺结节直径均小于对照组,差异有统计学意义(P<0.05);两组患者治疗前后的甲状腺体积及甲状腺结节大小组内整体比较,差异有统计学意义(P<0.05)(表1)。
表1 两组患者治疗前护甲状腺体积及甲状腺结节大小比较(±s>)
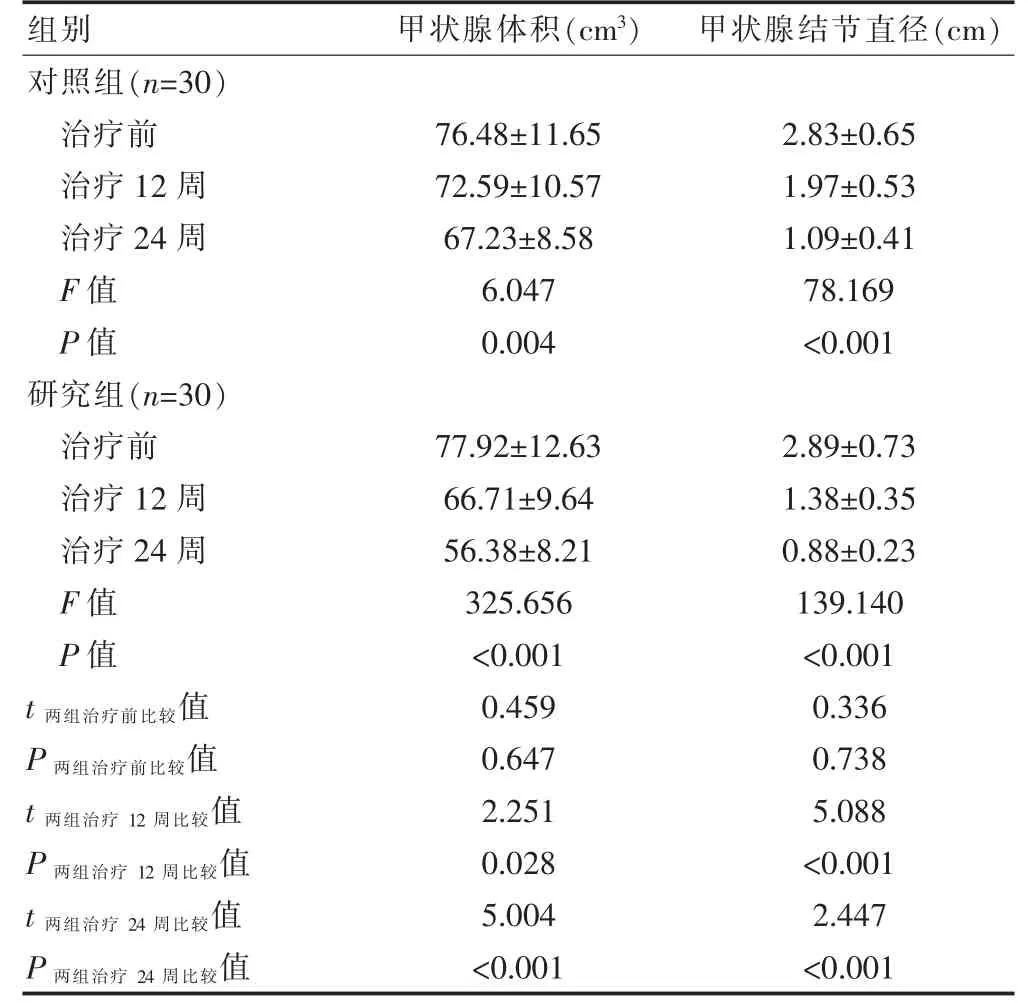
表1 两组患者治疗前护甲状腺体积及甲状腺结节大小比较(±s>)
组别甲状腺体积(cm3)甲状腺结节直径(cm)对照组(n=30)治疗前治疗12 周治疗24 周F 值P 值研究组(n=30)治疗前治疗12 周治疗24 周F 值P 值76.48±11.65 72.59±10.57 67.23±8.58 6.047 0.004 2.83±0.65 1.97±0.53 1.09±0.41 78.169<0.001 t 两组治疗前比较值P 两组治疗前比较值t 两组治疗12 周比较值P 两组治疗12 周比较值t 两组治疗24 周比较值P 两组治疗24 周比较值77.92±12.63 66.71±9.64 56.38±8.21 325.656<0.001 0.459 0.647 2.251 0.028 5.004<0.001 2.89±0.73 1.38±0.35 0.88±0.23 139.140<0.001 0.336 0.738 5.088<0.001 2.447<0.001
2.2 两组患者治疗前后甲状腺功能的比较
两组治疗前的血清TPO-Ab、TG-Ab、TSH 水平比较,差异无统计学意义(P>0.05);研究组患者治疗12、24 周后的血清TPO-Ab、TG-Ab、TSH 水平低于对照组,差异有统计学意义(P<0.05);两组患者治疗前后的血清TPO-Ab、TG-Ab、TSH 水平组内整体比较,差异有统计学意义(P<0.05)(表2)。
表2 两组患者治疗前后甲状腺功能的比较(±s>)
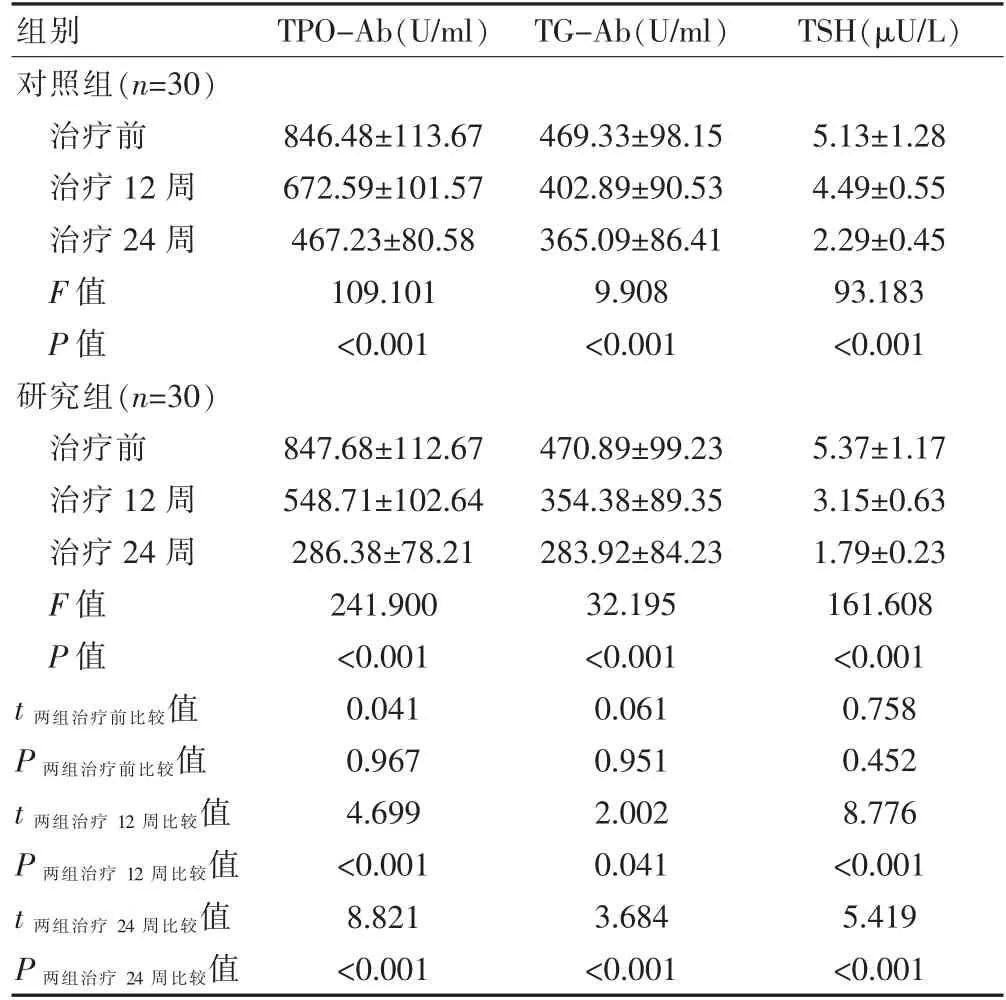
表2 两组患者治疗前后甲状腺功能的比较(±s>)
注 TPO-Ab:抗甲状腺过氧化物酶抗体;TG-Ab:抗甲状腺球蛋白抗体;TSH:促甲状腺激素
组别TPO-Ab(U/ml)TG-Ab(U/ml)TSH(μU/L)对照组(n=30)治疗前治疗12 周治疗24 周F 值P 值研究组(n=30)治疗前治疗12 周治疗24 周F 值P 值846.48±113.67 672.59±101.57 467.23±80.58 109.101<0.001 469.33±98.15 402.89±90.53 365.09±86.41 9.908<0.001 5.13±1.28 4.49±0.55 2.29±0.45 93.183<0.001 t 两组治疗前比较值P 两组治疗前比较值t 两组治疗12 周比较值P 两组治疗12 周比较值t 两组治疗24 周比较值P 两组治疗24 周比较值847.68±112.67 548.71±102.64 286.38±78.21 241.900<0.001 0.041 0.967 4.699<0.001 8.821<0.001 470.89±99.23 354.38±89.35 283.92±84.23 32.195<0.001 0.061 0.951 2.002 0.041 3.684<0.001 5.37±1.17 3.15±0.63 1.79±0.23 161.608<0.001 0.758 0.452 8.776<0.001 5.419<0.001
2.3 两组患者治疗前后炎症因子水平的比较
两组治疗前的血清IFN-γ、IL-2、IL-10 水平比较,差异无统计学意义(P>0.05);研究组患者治疗12、24 周后的血清IFN-γ、IL-2 水平低于对照组,血清IL-10 水平高于对照组,差异有统计学意义(P<0.05);两组患者治疗前后的血清IFN-γ、IL-2、IL-10 水平组内整体比较,差异有统计学意义(P<0.05)(表3)。
表3 两组患者治疗前后炎症因子水平的比较(±s>)
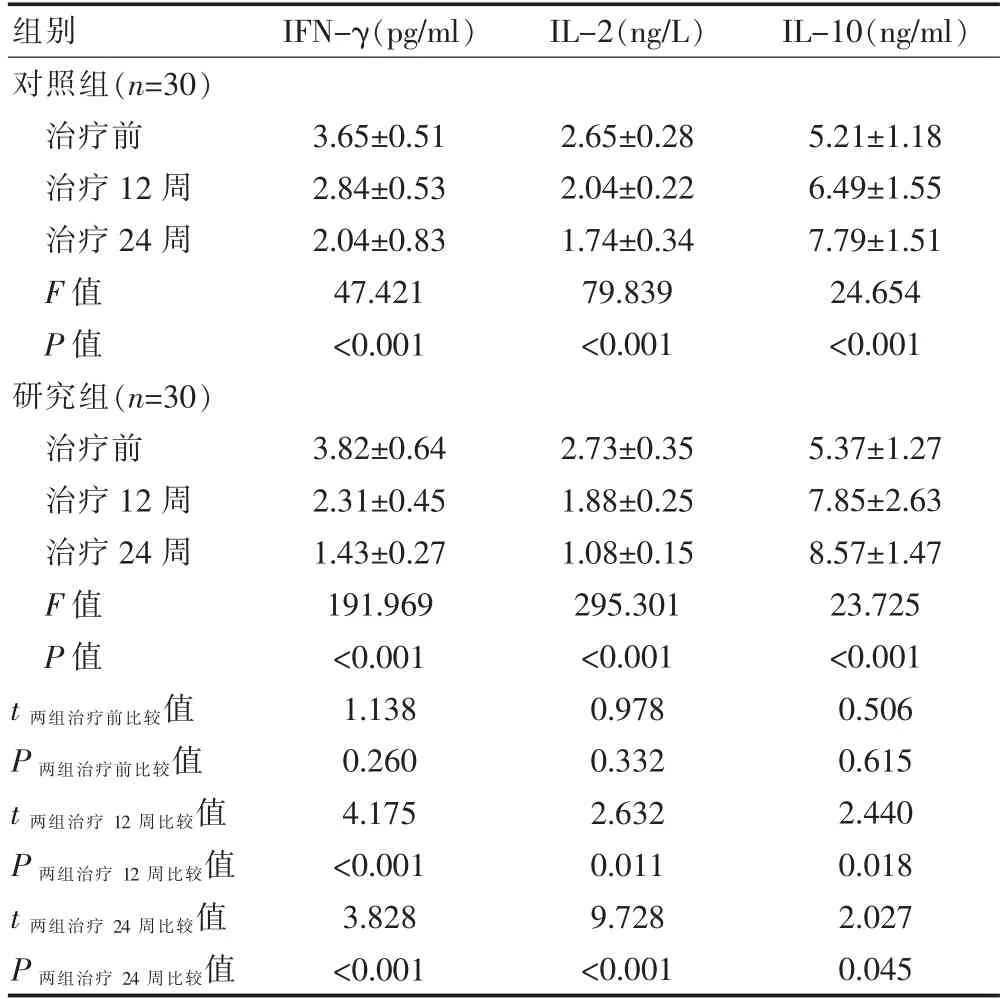
表3 两组患者治疗前后炎症因子水平的比较(±s>)
注 IFN-γ:γ 干扰素;IL-2:白介素-2;IL-10:白介素-10
组别IFN-γ(pg/ml)IL-2(ng/L)IL-10(ng/ml)对照组(n=30)治疗前治疗12 周治疗24 周F 值P 值研究组(n=30)治疗前治疗12 周治疗24 周F 值P 值3.65±0.51 2.84±0.53 2.04±0.83 47.421<0.001 2.65±0.28 2.04±0.22 1.74±0.34 79.839<0.001 5.21±1.18 6.49±1.55 7.79±1.51 24.654<0.001 t 两组治疗前比较值P 两组治疗前比较值t 两组治疗12 周比较值P 两组治疗12 周比较值t 两组治疗24 周比较值P 两组治疗24 周比较值3.82±0.64 2.31±0.45 1.43±0.27 191.969<0.001 1.138 0.260 4.175<0.001 3.828<0.001 2.73±0.35 1.88±0.25 1.08±0.15 295.301<0.001 0.978 0.332 2.632 0.011 9.728<0.001 5.37±1.27 7.85±2.63 8.57±1.47 23.725<0.001 0.506 0.615 2.440 0.018 2.027 0.045
2.4 两组患者不良反应发生情况的比较
治疗期间,对照组患者发生皮疹2 例,呕吐3 例,脏器损害2 例,不良反应总发生率为23.33%;研究组患者发生呕吐1例,不良反应总发生率为3.33%。研究组的不良反应总发生率低于对照组,差异有统计学意义(χ2=5.192,P=0.022)。
3 讨论
桥本甲状腺炎的发病原因与遗传缺陷、过度劳累、精神因素及其他应激反应有关[8];甲状腺结节为甲状腺腺体内局限性增生的肿块,分为甲状腺孤立结节和多发结节;桥本甲状腺炎合并甲状腺结节可增加患者罹患甲状腺癌的风险[9]。目前,对于恶性结节患者一般采取手术治疗,而对良性结节患者常用左甲状腺素钠片治疗。但是随着用药时间的延长,患者可出现心悸、腹泻等不良反应,影响患者的治疗积极性[10]。
中医认为,桥本甲状腺炎伴结节因气血凝滞而致,治疗应遵循理气、散瘀、活血的原则。小金丸中的麝香具有消痛散结的功效,五灵脂、没药、乳香可活血散瘀,枫香脂及木鳖可消肿祛毒,当归活血祛瘀,地龙疏肝理气,香墨理气止痛,草乌祛湿散寒,诸药共奏散结消肿、化瘀止痛的功效。此外,夏枯草胶囊中的夏枯草具有散结消肿、清热解毒的功效。本研究结果显示,研究组患者治疗12、24 周后的甲状腺体积及甲状腺结节直径均小于对照组,研究组患者治疗12、24 周后的血清TPO-Ab、TG-Ab、TSH 水平均低于对照组,且研究组患者治疗期间的不良反应总发生率低于对照组(P<0.05),提示小金丸联合夏枯草胶囊能够缩小桥本甲状腺炎伴结节患者的甲状腺体积及结节大小,改善甲状腺抗体水平,提高甲状腺功能,且不良反应较少。相关研究认为,桥本甲状腺炎的发病机制尚与甲状腺内辅助性T 淋巴细胞介导免疫应答反应有关,辅助性T 细胞1(Th1)/辅助性T 细胞2(Th2)失衡致使炎症因子以及Th1 细胞浸润并破坏甲状腺腺体,T 淋巴细胞浸润及甲状腺纤维化,致使机体免疫系统破坏,导致疾病发生[11-12]。Th1 细胞可产生IFN-γ、IL-2等细胞因子,促使甲状腺滤泡上皮细胞凋亡,破坏甲状腺组织,并参与炎症反应,其水平越高表明病情越严重;IL-10 由Th2 细胞分泌而来,具有抗自身免疫炎症的作用,其水平越高表明病情有所缓解[13]。现代药理学表明,当归中的当归多糖能够抑制在免疫应答和炎症反应中起到关键作用的核因子κB 蛋白的表达,从而抑制机体炎症反应,控制病情发展[14-15];夏枯草胶囊中的夏枯草苷能够抑制炎症因子及趋化因子的分泌,从而促进病情恢复[16-17]。本研究结果显示,研究组患者治疗12、24 周后的血清IFN-γ、IL-2 水平低于对照组,血清IL-10 水平高于对照组,提示小金丸联合夏枯草胶囊能够抑制桥本甲状腺炎伴结节患者炎症反应,从而促进病情恢复,与任意等[18]的研究结果相符。
综上所述,小金丸联合夏枯草胶囊能够缩小桥本甲状腺炎伴结节患者的甲状腺体积及结节大小,改善甲状腺抗体水平,提高甲状腺功能,抑制炎症反应,同时不良反应较少,值得进一步研究和临床推广。
