O/W型乳化液中噻二唑衍生物对铜板的缓蚀效果
2022-04-08谢娟娟金展亨
熊 桑,黄 迪,谢娟娟,金展亨,周 灿
(1.南京工程学院材料与科学工程学院,南京 211167;2.中国石油物资有限公司)
铜板带在粗轧加工阶段以水包油型(O/W)乳化液进行润滑,而暴露在空气中的铜会发生腐蚀变色。该过程涉及化学、电化学和物理作用[1],主要归因于乳化液添加剂中的硫、氯元素与铜反应形成了黑色硫化物。Haseeb等[2]研究了铜和铅青铜在矿物油中的腐蚀特性,发现矿物油中脂肪酸酯含量的增加会加剧铜和铅青铜的腐蚀。因此,铜板带在加工过程中使用的润滑油或乳化液中均需要加入缓蚀剂以抑制其对铜的腐蚀。
针对金属加工液中缓蚀剂的研究,Wiklund等[3]考察了变压器绝缘油中钝化剂Irgamet 39对铜的缓蚀作用,发现Irgamet 39在铜表面能在数小时或数天内形成稳定的抑制膜;Badawy等[4]分析了氨基酸在中性氯化物溶液中对Cu-Ni合金的防腐作用,发现其在Cu-5Ni上的吸附能为-37.81 kJ/mol,说明氨基酸在合金表面有较强的物理吸附;Qiang Yujie等[5]采用电化学方法和量子化学计算研究了银杏叶提取物(GLE)在盐酸中对X70钢的缓蚀效果,结果表明GLE在X70钢表面形成了抑制腐蚀的保护膜;Somers等[6]考察了4种稀土3-(4-甲基苯甲酰)丙酸化合物在NaCl溶液中的缓蚀性能,发现4种化合物的腐蚀抑制作用均以阳极抑制为主;尤龙等[7]基于密度泛函理论(DFT)构建了咪唑啉缓蚀剂与Fe表面的作用模型,讨论了缓蚀剂在溶液中扩散行为,通过计算各组分的Coulomb相互作用能与Vander Waals相互作用能,揭示了咪唑啉缓蚀剂膜抑制溶液中H2O,H3O+,Cl-,HCO3-等腐蚀离子扩散的微观机理。熊桑等[8-9]建立了噻二唑类缓蚀剂(DTA)分子在铜表面稳定吸附的构型,发现DTA可以提供质子并分离出H+,使铜表面的Cu0被氧化成Cu2+,同时DTA分子中的S—S键断裂,与Cu2+结合形成DTA-硫化物混合物;DTA在铜表面的化学吸附过程不可逆,且吸附键键能的大小对缓蚀剂的缓蚀效果起决定性作用。
目前,有关O/W乳化液金属加工液中噻二唑类缓蚀剂抑制铜腐蚀的研究报道仍很少,对其作用效果和作用机理的认识有待进一步提升。因此,本研究基于DFT理论,使用Materials Studio软件的DMol3模块对噻二唑类缓蚀剂分子进行几何结构优化,计算缓蚀剂分子的前线轨道分布及其在Cu表面的吸附能,并测试O/W型乳化液中噻二唑类衍生物对铜腐蚀的抑制性能。
1 实验与计算
1.1 材 料
矿物基础油 D130,生兴行化学上海有限公司天津分公司产品;极压剂亚磷酸二正丁酯,锦州圣大化学品有限公司产品;表面活性剂硬脂酸丁酯,东莞市铂融高分子材料有限公司产品;油性剂油酸,上海九麟实业有限公司产品;乳化剂烷基酚聚氧乙烯醚;德国汉姆公司产品;缓蚀剂甲基苯三唑衍生物(MBD)、2,5-双(正辛基二硫代)噻二唑(EDD)、2,5-双(十二烷基二硫代)噻二唑(BDDT),均为分析纯,南京皇泰医药科技有限公司产品。3种缓蚀剂的结构如图1所示。

图1 3种缓蚀剂分子的结构—C; —H; —N; —S。图2同
1.2 缓蚀剂与金属表面作用能的计算
构建Cu原子层平板模型,模拟单元大小为1.537 4 nm×1.448 4 nm×3.512 5 nm,共有92个Cu原子,厚度为3 nm。基于DFT理论,运用Materials Studio软件的DMol3模块对3种缓蚀剂分子进行几何结构优化,分析前线轨道分布。
1.2.1乳化液的介电常数
混合液中,由于溶剂化作用的存在,溶质离子与溶剂分子形成络合物,并放出大量热。溶剂化作用可以改变溶剂和溶质离子的结构,影响反应速率、反应进程、反应机理及反应产物。在铜板加工过程中,使用的润滑剂类型可能不同(包括水基润滑剂、油基润滑剂、乳化液等),致使缓蚀剂分子在溶剂化作用下的量子化学参数、反应活性存在差异。溶剂化作用下,混合液的介电常数(εtot)采用式(1)计算。
εtot=X×εA+(1-X)×εB
(1)
式中:εA、εB分别为A、B的介电常数,C2/(N·M2);X为A试剂所占A/B混合溶液的质量分数。
1.2.2缓蚀剂与铜表面的吸附能
对铜和缓蚀剂分子的吸附过程进行分子动力学模拟,根据DFT第一性原理,使用DMol3模块计算出缓蚀剂分子吸附在Cu(111)面的吸附能(Eads),其计算如式(2)所示。
Eads=EMe+Mo-EMe-EMo
(2)
式中:EMe+Mo为缓蚀剂分子吸附在金属表面的能量,eV;EMe为金属表面的能量,eV;EMo为单个缓蚀剂分子的能量,eV。吸附能绝对值越大,缓蚀剂分子抑制金属腐蚀的效果越好。
1.3 乳化液的制备
表1为乳化油的组成。按表1中各组分配比,在基础油D130中依次加入极压剂、油性剂、消泡剂和缓蚀剂,搅拌均匀后加入乳化剂,继续搅拌,得到棕黄色、透明乳化油。然后,将去离子水缓慢加入乳化油中,稀释至乳化油质量分数为5%,加热至50 ℃,搅拌20 min,得到乳化液。
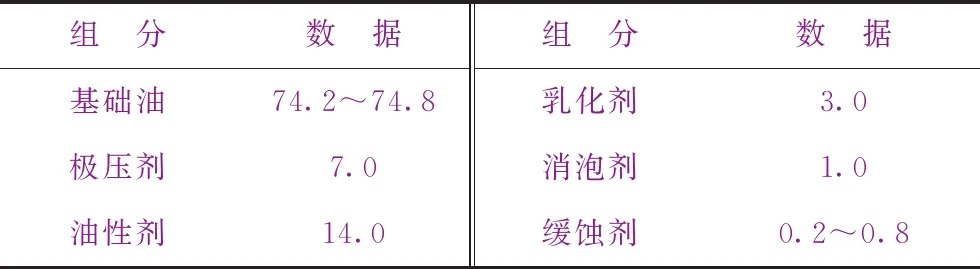
表1 乳化油组成 w,%
1.4 电化学性能测试方法
使用普林斯顿VersaSTAT MC电化学工作站测定铜在乳化液中的动电位极化曲线,其中参比电极为饱和甘汞电极,辅助电极为铂电极,电位范围为-1.5~1.5 V,扫描速率为1 mV/s。采用ZEISS公司生产的Sigma 500型扫描电子显微镜(SEM)对电化学测试后的铜表面形貌进行分析。
采用塔菲尔外推法可从极化曲线中计算相关电化学参数,包括腐蚀电位(Ecorr)、电流密度(icorr)、阴极塔菲尔斜率(βc)、阳极塔菲尔斜率(βa)和缓蚀效率(η)。其中,η的计算如式(3)所示。
(3)
式中,icorr和icorr,0分别为在有、无缓蚀剂的乳化液中铜电极的电流密度,A/cm2。
2 结果与讨论
2.1 缓蚀剂分子前线轨道分布
室温下,水的介电常数为78.54 C2/(N·M2),润滑油的介电常数按正十六烷的介电常数2.06 C2/(N·M2) 计算,乳化液的介电常数由式(1)求得,为74.74 C2/(N·M2)。基于DFT理论,运用DMol3模块计算3种缓蚀剂分子在真空、水溶液、油溶液和乳化液中的前线轨道能,包括最高占据轨道能EHOMO、最低未占据轨道能ELUMO,结果如表2所示。
由分子前线轨道理论分析可知:ELUMO表示缓蚀剂分子得电子的能力,ELUMO的绝对值越小,表明缓蚀剂分子越容易得电子;EHOMO表示缓蚀剂分子失电子的能力,EHOMO的绝对值越大,表明缓蚀剂分子越容易失电子[8]。由表2可以看出:缓蚀剂MBD分子的EHOMO随着体系溶剂变化幅度较小,而其ELUMO随着体系溶剂变化幅度较大;MBD分子在水溶液和乳化液中ELUMO相近,且明显低于其在油溶液和真空中的ELUMO,说明MBD分子在水中的得电子能力受到抑制、而更易失电子。而对缓蚀剂EDD、BDDT分子而言,其在水溶液和乳化液中的EHOMO和ELUMO均相近,且绝对值均大于其在油溶液和真空中的值;虽然其在油溶液中的EHOMO和ELUMO绝对值稍小,但明显大于其在真空中EHOMO和ELUMO的绝对值,说明EDD、BDDT在水溶剂环境中更易得、失电子,缓蚀效果更好[9]。
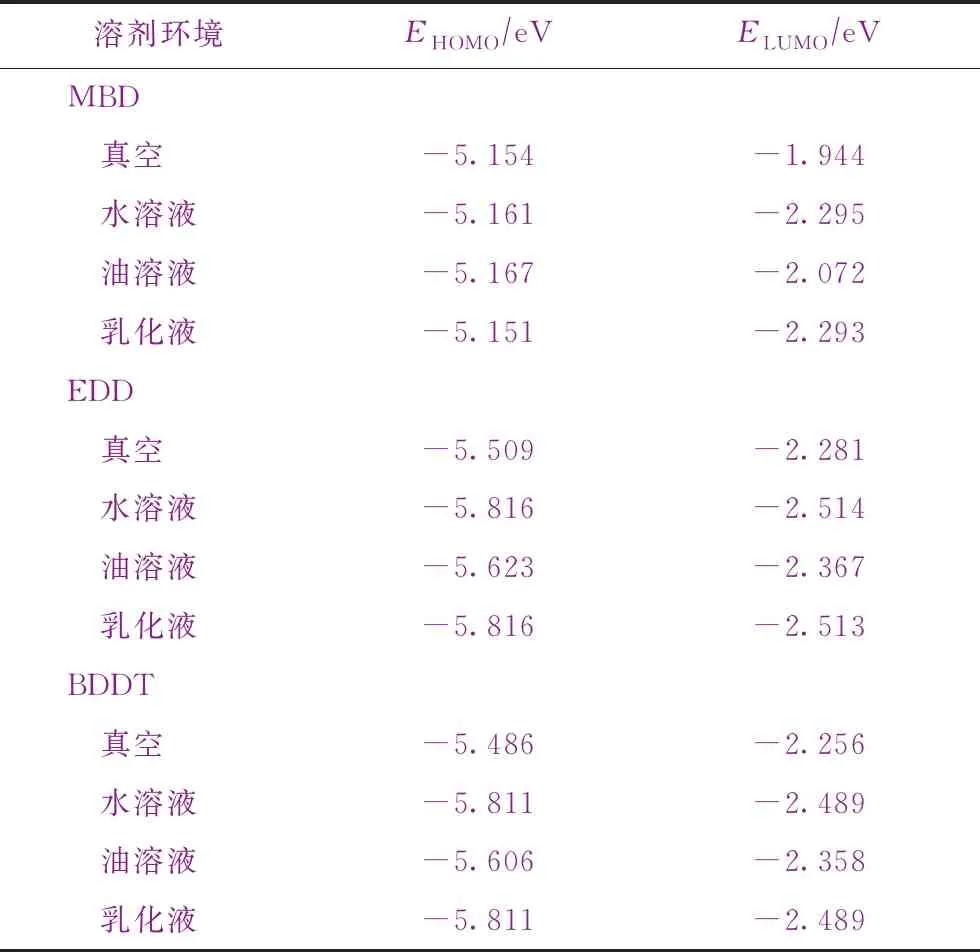
表2 不同溶剂条件下3种缓蚀剂分子的EHOMO和ELUMO变化
2.2 反应活性位点
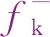
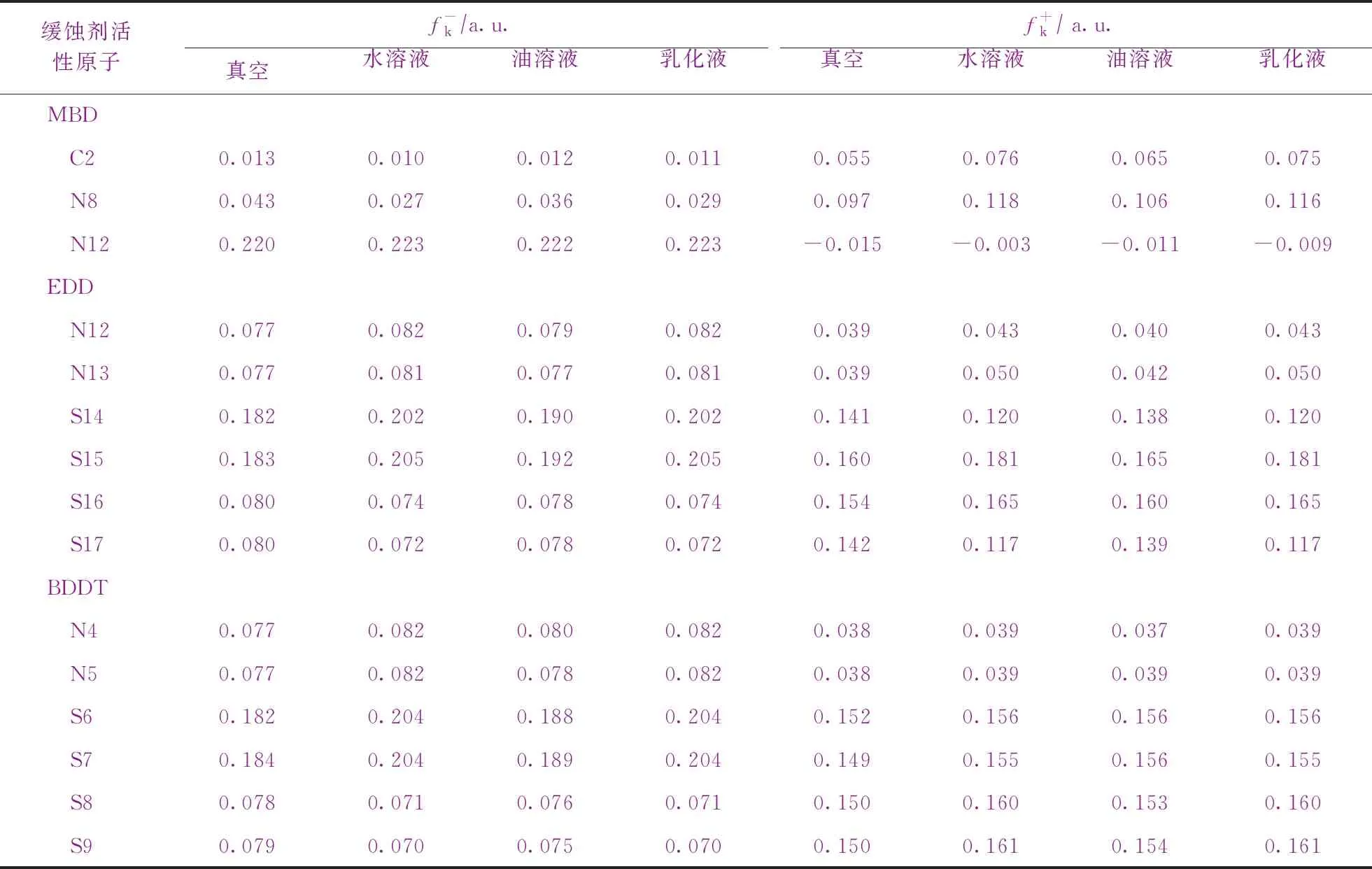
表3 3种缓蚀剂分子中活性原子在不同溶剂条件下的福井指数
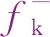
2.3 缓蚀剂分子在铜表面的吸附能
缓蚀剂在Cu(111)晶面吸附的稳定构型如图2所示,Cu(111)晶面上缓蚀剂分子的吸附能和成键键长如表4所示。由图2和表4可知,Cu原子分别与EDD、BDDT分子中的一个S原子形成Cu—S键,其键长分别为0.251 7 nm和0.223 8 nm,但未与MBD分子形成化学键,说明MBD分子在Cu金属表面的吸附属于物理吸附,而EDD、BDDT分子在Cu金属表面的吸附属于化学吸附。
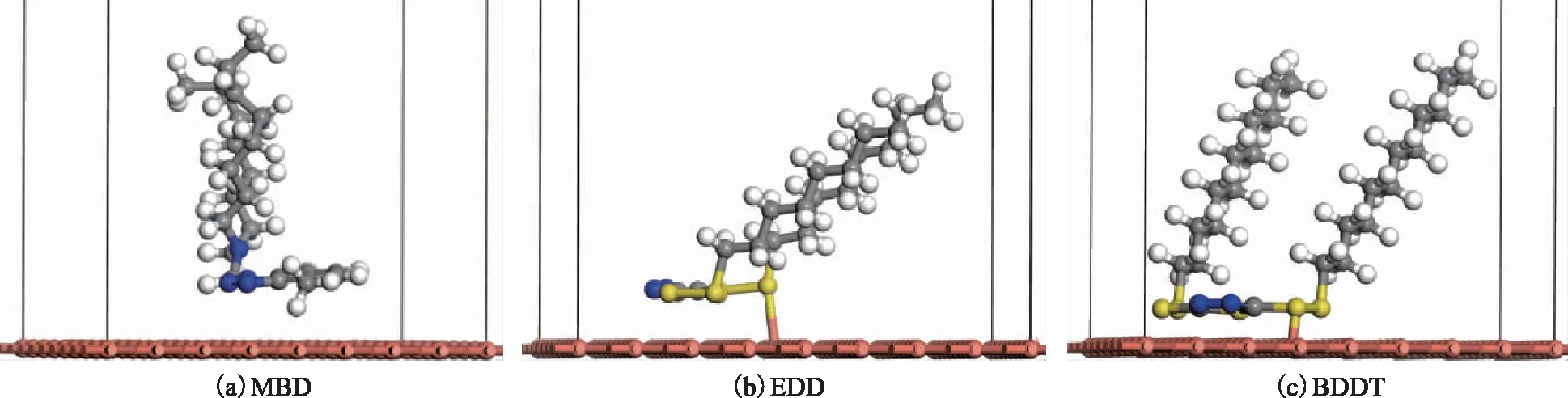
图2 3种缓蚀剂在Cu(111)晶面吸附的稳定构型
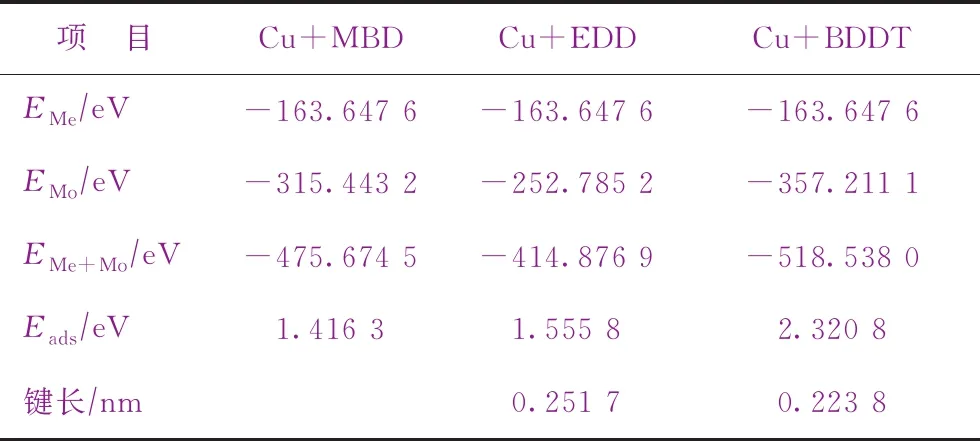
表4 缓蚀剂分子在Cu(111)晶面上的吸附能与成键键长
2.4 动电位极化曲线
图3为铜电极在有、无缓蚀剂的乳化液中的极化曲线。由图3可知,在乳化液中加入缓蚀剂后,铜电极的极化曲线向电流密度较低的方向移动,极化曲线的阴极段和阳极段均减小,腐蚀电位的移动距离减小,且小于0.1 V,说明3种缓蚀剂均属于混合型缓蚀剂[9],吸附在铜表面对阴极和阳极反应均有抑制作用。

图3 铜电极在无缓蚀剂乳化液和添加不同缓蚀剂乳化液中的极化曲线■—无缓蚀剂; ●—MBD; ◆—EDD; ▲—BDDT
由图3计算相关电化学参数,结果如表5所示。由表5可以看出:缓蚀剂的加入,使铜电极极化曲线的电极电位增加,极化曲线的βc、βa均变小,腐蚀电流减小,说明铜电极腐蚀速率减小,这是因为缓蚀剂吸附在铜表面,抑制了乳化液对铜电极的腐蚀;同时,缓蚀剂的加入,使icorr降低,η升高,缓蚀率η由小到大的顺序为MBD 表5 铜在乳化液中极化的相关参数 为了进一步分析缓蚀剂对铜基体的保护作用,对电化学测试后的铜电极表面进行SEM表征,结果如图4所示。由图4可知:铜电极在无缓蚀剂的乳化液中进行电化学测试后,其表面存在明显的点蚀现象;在含有缓蚀剂EDD和MBD的乳化液中进行电化学测试后,铜电极表面腐蚀减缓,但局部仍然有点蚀现象;在含有缓蚀剂BDDT的乳化液中进行电化学测试后,铜电极表面光亮,没有明显的腐蚀。这进一步证实缓蚀剂BDDT在铜金属表面形成完好的钝化保护膜,有效抑制了乳化液对铜表面的腐蚀。这与量子化学计算结果一致。 图4 电化学测试后不同乳化液中铜电极的SEM照片 量子化学参数计算结果表明,MBD在Cu(111)面为物理吸附,EDD和BDDT在Cu(111)面为化学吸附。缓蚀剂MBD分子在水环境中的得电子能力受到抑制,而更易失电子;EDD、BDDT分子在水溶液和乳化液中更易得、失电子,对铜缓蚀效果更好。 缓蚀剂分子中活性原子的福井指数计算结果表明:3种缓蚀剂分子的活性位点主要集中在N原子、S原子以及芳香环上的C原子上;在水溶液和O/W乳化液中,活性原子的福井指数均比其在真空和油溶液中的数值大,说明水的溶剂化效应使缓蚀剂分子具有更强的局部反应活性。 3种缓蚀剂对铜板的缓蚀效率由小到大的顺序为MBD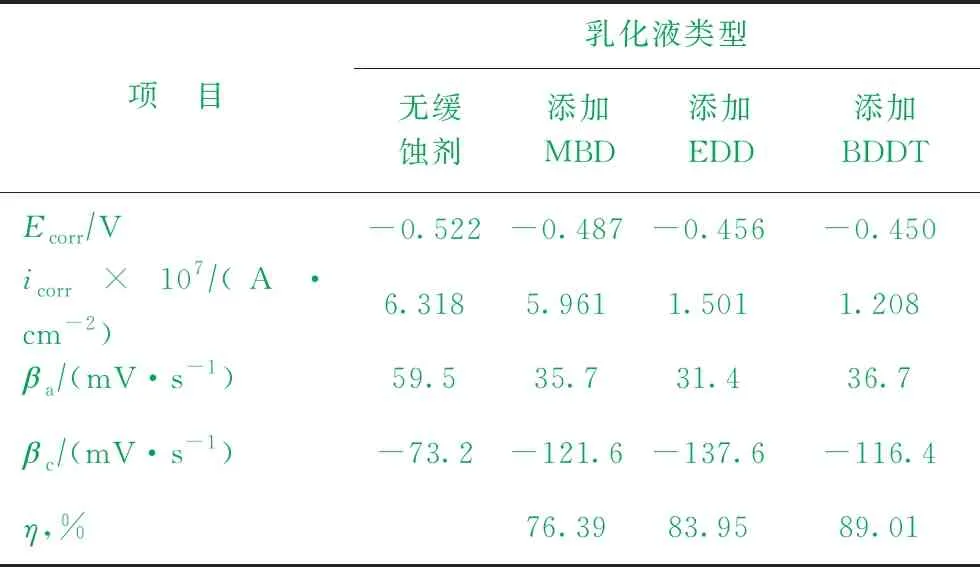
2.5 表面分析

3 结 论
