QuEChERS-超高效液相色谱串联质谱法快速测定婴幼儿奶粉中5种黄曲霉毒素含量
2022-04-07王小乔许晓辉张虹艳吴福祥潘秀丽李晨曦
王小乔,许晓辉,张虹艳,冯 翀, 2,吴福祥,潘秀丽,李 赟,李晨曦
(1.兰州市食品药品检验检测研究院,甘肃 兰州 730050;2.兰州理工大学 生命科学与工程学院,甘肃 兰州 730050)
真菌毒素是真菌的次生代谢产物,是全球食品和饲料中最常见的污染物之一[1].黄曲霉毒素是由黄曲霉和寄生曲霉产生的一类真菌毒素,黄曲霉毒素分为M1、B1、B2、G1、G2等几类,此类物质对人和动物健康有着极强的危害[2].如果人类饮食中含有真菌毒素[3],会严重损害中枢神经系统、肝脏和肾脏,甚至发生脑损伤和死亡.牛奶及其奶制品中黄曲霉毒素来源一般是由于动物摄入被黄曲霉毒素污染的饲料,经体内代谢所产生[4],或者生产加工过程中仪器清洗、包装不当等,暴露在空气中发生有机物霉变[5-6].婴幼儿奶粉质量安全一直是全社会关注的焦点,食用被黄曲霉毒素污染的婴幼儿奶粉对婴幼儿的身体健康会造成危害.因此,开发一种快速、便捷、精确的检测方法来筛查婴幼儿奶粉中黄曲霉毒素是非常有必要的.
黄曲霉毒素的含量测定方法主要有高效液相色谱法[7-8]、酶联免疫法[9]、液相色谱-质谱联用法[10-11]等.因高效液相色谱法和酶联免疫法检出限高,不利于微量复杂样品的检测,特别是在含量极低的条件下难以检测,而采用液相色谱-质谱联用法却能够解决这些问题.黄曲霉毒素的法定限量值很低,复杂样品基质会降低其检测灵敏度,因此需要减小基质效应以增强检测灵敏度.检测黄曲霉毒素时,最常用的去除杂质的方法是免疫亲和法.但是此方法所使用的净化柱价格高、使用程序复杂、费时费力,不利于快速、高效筛查黄曲霉毒素[12-13].常规QuEChERS法(Quick、Easy、Cheap、Effective、Rugged and Safe)是样品萃取后经C18或PSA净化,其在分析脂肪含量高的样品时,不能有效去除脂质,导致检测管路堵塞,出现色谱柱柱压升高、色谱图异常、重复性和精密度差等问题.而增强型脂质去除技术是一种能够选择性去除复杂基质中脂质的独特吸附剂,结合体积排阻和疏水相互作用,可以提升净化效果.
为了监控婴幼儿奶粉中黄曲霉毒素的风险因子,本文采用增强型脂质去除分散式固相萃取管(enhanced matrix removal lipid-dispersed solid phase extraction,EMR-Lipid dSPE)的QuEChERS法净化样品,建立了一种超高效液相色谱串联质谱同时测定婴幼儿奶粉中5种黄曲霉毒素的快速筛查方法.本研究所开发建立的方法前处理简单、方便快捷,能够快速筛查婴幼儿奶粉中黄曲霉毒素的含量,为婴幼儿奶粉的风险因子监控提供技术服务.
1 试验部分
1.1 仪器与试剂
Agilent 6460A三重四极杆液质联用仪(美国安捷伦);分析天平(梅特勒-托利多);涡旋混合器(美国Scientific);5810 R离心机(德国艾本德);SBL-10DT超声清洗器(宁波新芝).
乙腈(HPLC级,德国Merck公司);EMR-Lipid dSPE 净化管(美国安捷伦);甲酸、乙酸铵(HPLC级,东京化成工业株式会社); 硫酸钠、氯化钠、乙二胺四乙酸二钠(Na2EDTA)、柠檬酸、磷酸氢二钠(分析纯,国药集团化学试剂有限公司);水(屈臣氏).
对照品:黄曲霉毒素B1、B2、G1、G2混合对照品溶液,批号SSBG004,纯度:100.0%,来源FERMENTEK;黄曲霉毒素M1对照品溶液,批号18377-004,纯度:100.0%,来源Bepure.
1.2 试验方法
1.2.1 Na2EDTA-Mcllvaine缓冲液
磷酸氢二钠7.1 g、柠檬酸8.4 g、乙二胺四乙酸二钠19.5 g,加水650 mL,溶解,即得.
1.2.2 标准溶液制备
混合标准储备溶液:精密量取质量浓度分别为0.51、0.50、0.51、0.48 μg/mL的黄曲霉毒素B1、B2、G1、G2混合标准溶液 1.00 mL和质量浓度为0.50 μg/mL的黄曲霉毒素M1对照品溶液1.00 mL,置于10.00 mL容量瓶中,使用乙腈定容至刻度,摇匀,得到质量浓度分别为51、50、51、48、50 ng/mL的黄曲霉毒素B1、B2、G1、G2、M1混合标准溶液.分别精密量取上述混合标准溶液2.00 mL至5 mL容量瓶中,用乙腈定容至刻度,摇匀,配制成混合标准使用溶液.
1.2.3 样品溶液制备
提取:准确称取1 g婴幼儿奶粉,于50 mL离心管中,加入1粒陶瓷均质子和 Na2EDTA-Mcllvaine缓冲液3 mL,充分涡旋,精密加入乙腈10.00 mL,涡旋1 min,在300 W功率下超声10 min后,加入萃取盐包(4 g 硫酸钠,1 g 氯化钠),充分涡旋1 min,4 000 r/min速度下离心10 min,取上清液待净化.
净化:精密吸取上述待净化液2.00 mL置于EMR-Lipid dSPE净化管中,涡旋1 min,4 000 r/min速度下离心10 min,取上清液,使用0.22 μm滤膜过滤后上液相色谱质谱联用仪测定.
1.2.4 阴性样品溶液的制备
取空白基质样品,按照“1.2.3”样品溶液制备方法制成空白样品溶液,即为阴性样品溶液.
1.2.5 色谱条件
色谱柱:ACQUITY BEH C18柱(1.7 μm, 2.1 mm×100 mm);流速:0.3 mL/min;柱温:35 ℃;自动进样室温度: 4 ℃;进样量:2 μL;流动相:A为0.1%甲酸-2 mmol/L乙酸铵的水溶液,B为0.1%甲酸的乙腈溶液,梯度洗脱程序如表1所列.
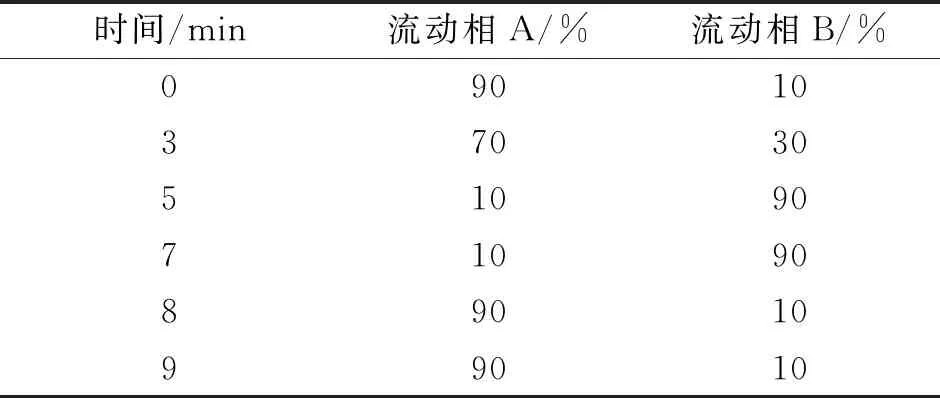
表1 流动相梯度洗脱程序
1.2.6 质谱条件
电喷雾电离模式:正离子模式;气流温度:325 ℃;载气流速:10 L/min;雾化器压力:0.345 MPa;鞘气流速:11 L/min;鞘气温度:350 ℃;毛细管电压: 4 000 V;各个化合物主要质谱参数如表2所列.
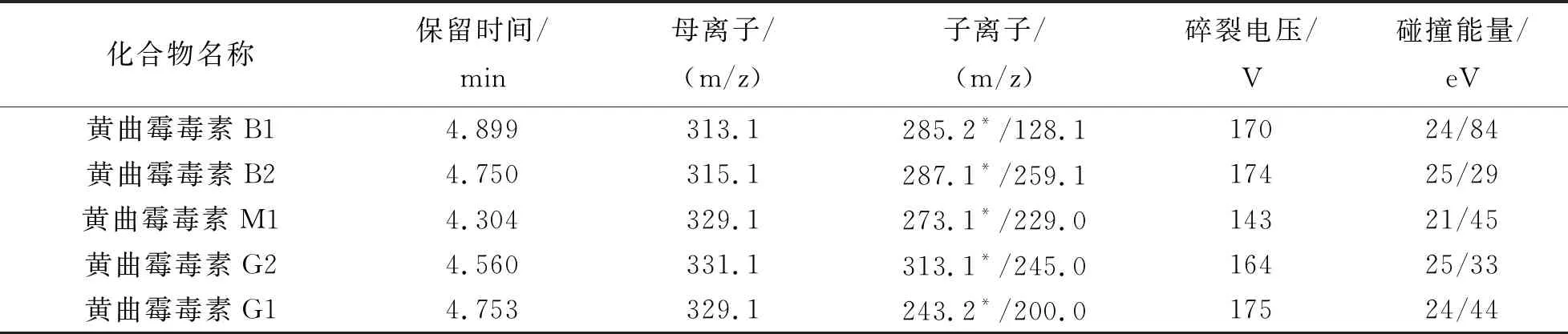
表2 主要质谱参数
1.3 数据处理
采用安捷伦液相色谱质谱联用仪数据处理软件MassHunter进行数据处理和分析.
2 结果与讨论
2.1 前处理条件优化
2.1.1 提取溶剂的选择
常用的提取溶剂有甲醇、乙腈、乙酸乙酯等.考虑到乙腈的盐析效果较好,有利于后续的QuEChERS方式净化样品,且5种黄曲霉毒素在乙腈中的溶解性相比在甲醇和乙酸乙酯中好,因此选择以乙腈为提取溶剂.因奶粉样品为干燥粉末,因此在加入有机提取溶剂前先加入3 mL缓冲盐溶液活化复原,而该缓冲盐溶液能够溶解样品中水溶性杂质,加入萃取盐包后,在低温高速状态下离心使水相溶液和有机相提取液有效分层,杂质被溶解到水相溶液中,去除杂质效果良好.
2.1.2 净化方法的选择
婴幼儿奶粉主要富含蛋白质、脂类和磷脂,传统的免疫亲和柱净化过程步骤繁琐,且价格昂贵,操作费时费力.而增强型脂质去除分散式固相萃取管,能够同时去除脂肪和磷脂等杂质,省去了活化、洗脱等步骤,简化了操作过程,降低了成本,缩短了净化时间.因此,本试验以乙腈为提取溶剂,选择QuEChER盐包盐析沉淀蛋白进行粗提取后,采用增强型脂质去除分散式固相萃取管净化粗提取液.
2.2 色谱质谱条件优化
2.2.1 色谱条件的优化
本试验研究的黄曲霉毒素化合物为中等极性,因此选择了适合大部分化合物分离的通用型色谱柱.由于采取电喷雾正离子模式检测待测组分,在酸性环境下有利于待测组分的离子化,故采用在流动相中加入甲酸酸化.为了防止出现色谱峰拖尾、不对称等现象,选择在流动相的水相中加入适量的乙酸铵.经试验优化,最终选择含0.1%甲酸的乙腈溶液-0.1%甲酸-2 mmol/L乙酸铵的水溶液作为流动相.
2.2.2 质谱条件的优化
分别配制0.5 ng/mL待测物的单标溶液,在正离子模式下,依次进行一级和二级质谱扫描.在一级质谱中找到每个化合物的母离子,在子离子扫描中找出响应值较大的子离子,选择稳定性好、响应值高的子离子为定量离子,同时优化出各待测物的最佳碎裂电压和碰撞能量.由于被分析物种类不多,因此采用MRM采集模式,也能够保证每个峰的采集点数,确保被检测物的灵敏度和选择性达到要求.优化后的MRM图如图1~2所示.
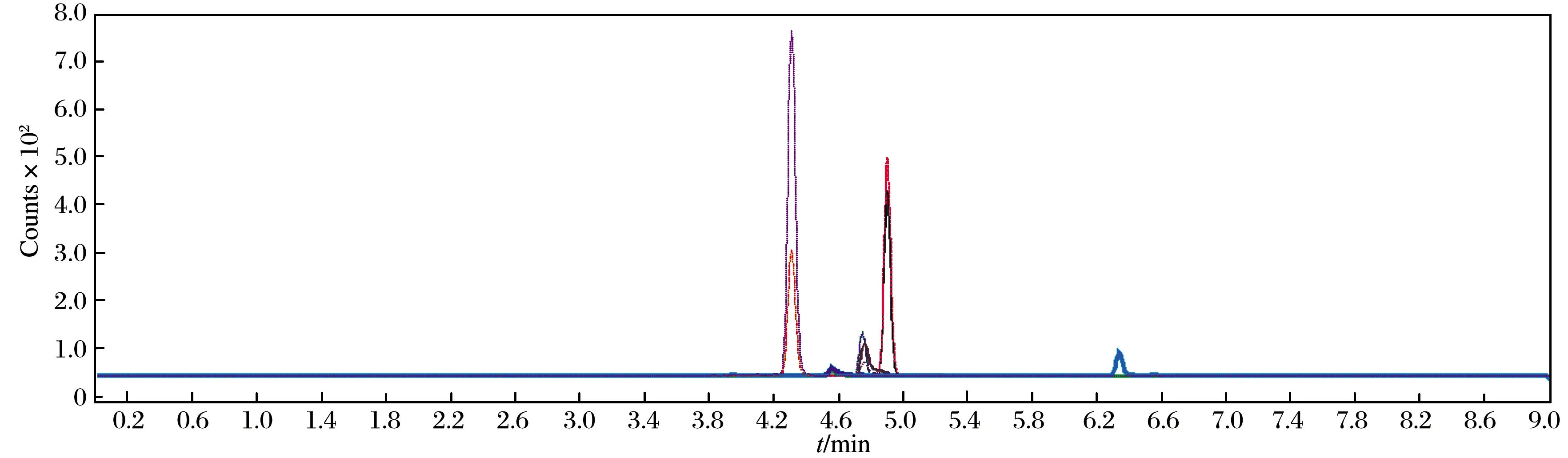
图1 黄曲霉毒素M1、B1、B2、G1、G2总离子流图
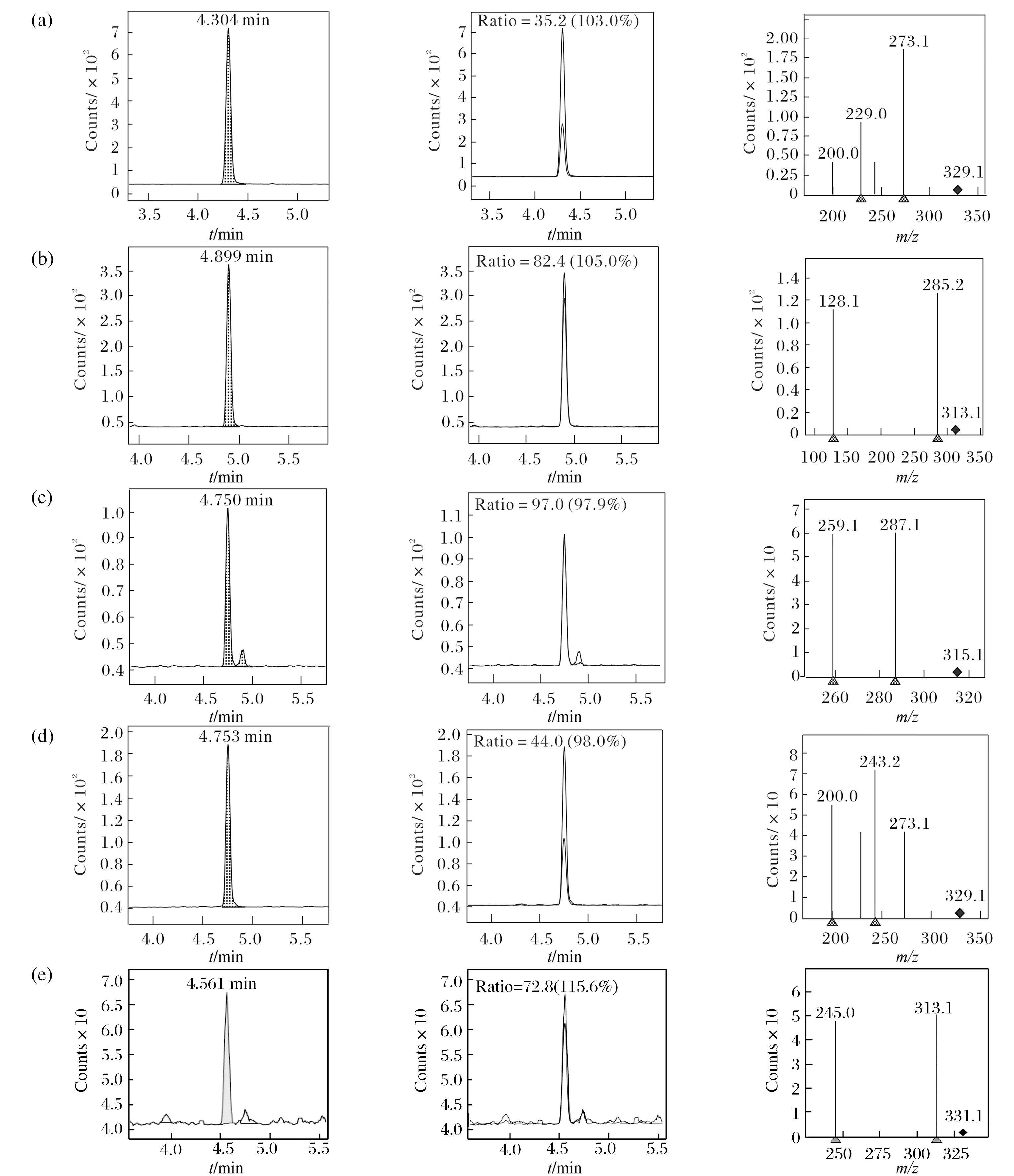
图2 黄曲霉毒素M1、B1、B2、G1、G2的MRM
2.3 基质效应
取空白基质样品,加入一定量的混合标准使用溶液,按“1.2.3”项下样品溶液制备方法同法处理,制备成质量浓度分别为0.1、0.2 ng/mL的基质标准溶液,与同浓度的纯溶剂标准溶液同时进样分析,计算两者分析物质谱响应值比值的百分比(matrix effect, ME).若ME值大于100%,则表示存在基质增强效应.若ME值小于100%,则表示存在基质抑制效应.若ME值接近100%,则表示基质效应影响小.结果显示,黄曲霉毒素B2的基质效应不明显,黄曲霉毒素G1、M1、G2随着浓度的增加,产生基质效应增强,黄曲霉毒素G2在低浓度下基质抑制效应明显(如图3所示).

图3 基质效应
2.4 线性关系、检出限及定量限
取混合标准使用溶液适量,使用乙腈稀释配制一系列的标准曲线溶液,外标法定量,以黄曲霉毒素的定量离子峰面积(Y)为纵坐标,质量浓度(X)为横坐标绘制标准曲线.以大于等于3倍信噪比确定各待测物的检出限(LOD),以大于等于10倍信噪比确定各待测物的定量限(LOQ),结果如表3所列.由表3可见,5种黄曲霉毒素在0~1.6 ng/mL范围内线性关系良好,相关系数r为0.996 4~0.999 1,检出限范围为0.04~0.20 ng/g,定量限范围为0.58~0.95 ng/g.

表3 5种黄曲霉毒素的线性关系、检出限、定量限
2.5 回收率与相对标准偏差
在阴性样品中分别加入质量约为1、2、4 ng 三个水平的混合标准使用溶液,按“1.2.3”进行处理,上机测试,每个添加水平平行制备3份试样,试验结果如表4所列.表4结果显示,5种黄曲霉毒素的回收率在81.9%~103.2%之间,相对标准偏差(relative standard deviations,RSD)在2.2%~4.5%之间.
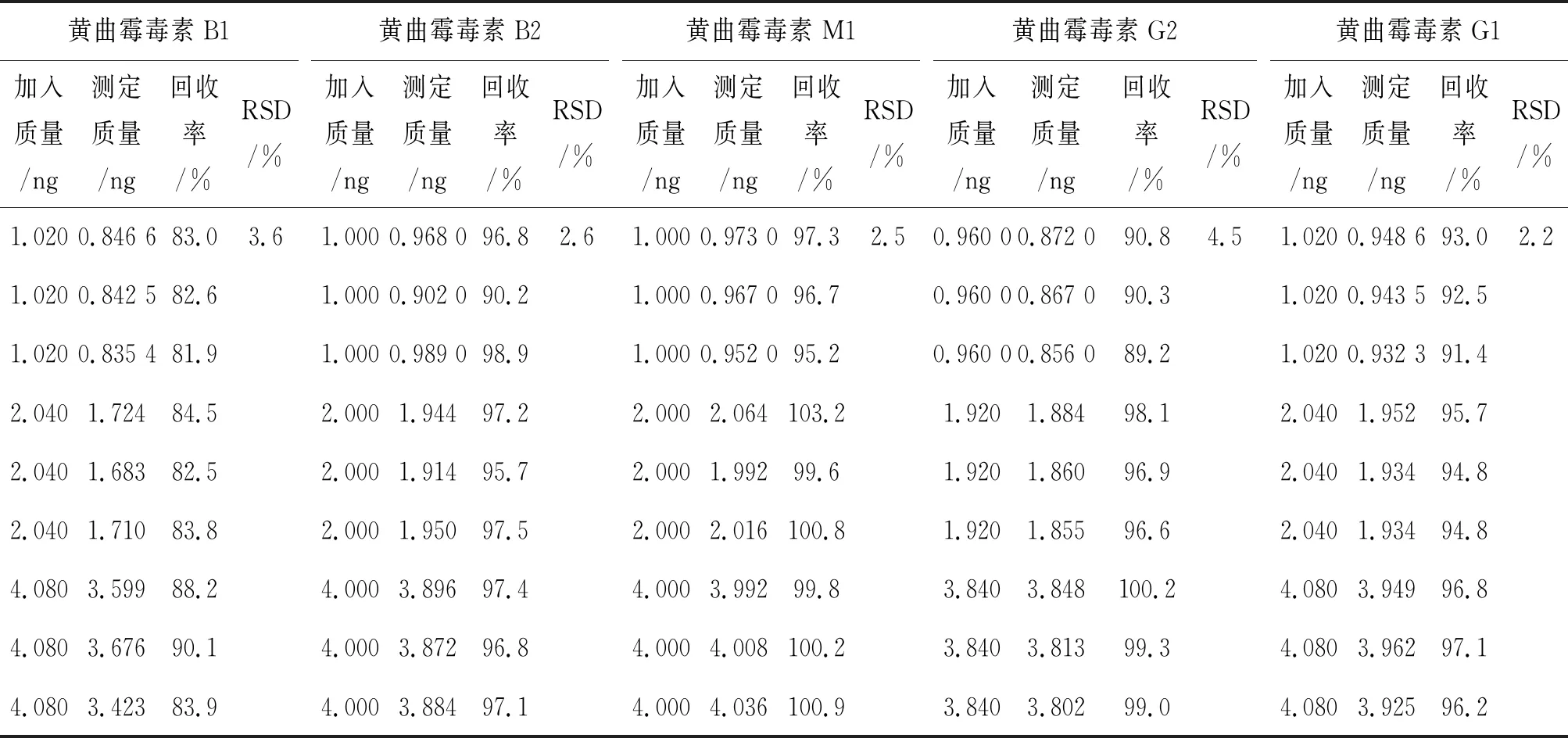
表4 5种黄曲霉毒素的回收率与相对标准偏差
2.6 实际样品测定
采用本研究建立的方法对市售10批次婴幼儿奶粉进行测定,结果均未检出5种黄曲霉毒素,阴性样品的总离子流图如图4所示.
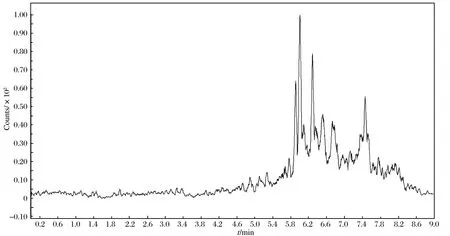
图4 阴性测试样品总离子流图
3 结论
本文建立了一种基于QuEChERS-超高效液相色谱串联质谱法同时测定婴幼儿奶粉中5种黄曲霉毒素的分析方法.该方法去除基质效果良好,操作简单便捷、灵敏度高、适用性强,通过方法学验证,该方法能够满足婴幼儿奶粉中5种黄曲霉毒素的检测要求,其能够为婴幼儿奶粉中黄曲霉毒素的监管提供技术支持.
