剪切波弹性成像联合MRI对干燥综合征涎腺病变的诊断价值
2022-04-06赵磊桑亮张震
赵 磊 桑 亮 张 震
干燥综合征(Sjögren’s syndrome,SS)属于自身免疫性疾病,早期主要以眼干、口干等症状为主,随着病情进展,可影响消化、神经、肺、皮肤等系统,严重时可导致肺间质纤维化合并感染、肺动脉高压、肾脏衰竭及中枢神经病变等,甚至危及患者生命,故需早诊断、早治疗[1]。临床早期多通过唾液腺流率、口腔症状、眼部症状等评估病情,但主观性较强,易受其他疾病影响,导致误判。唇腺活检是目前最客观的诊断SS的方法,具有较高的准确率,但其有创,不宜作为首选检查方法。剪切波弹性成像具有无创、定量、客观等优势,能够检测组织硬度,更好地分辨局灶性良恶性肿块,间接评估涎腺功能。MRI 具有多平面、多参数成像的特点,对软组织分辨率高,能够客观评价腮腺病变,且MRI 形态学和成像表现均可反映涎腺病变的严重程度。目前已有报道[2-3]证实剪切波弹性成像和MRI 分别在SS诊断中各有价值,本研究旨在探讨剪切波弹性成像联合MRI对SS涎腺病变的诊断价值。
资料与方法
一、研究对象
选取2019年3月至2020年10月我院收治的110例SS涎腺病变患者(观察组),其中男64例,女46例,年龄22~73 岁,平均(46.86±10.54)岁。纳入标准:①入组前无放、化疗史;②检查前未接受免疫抑制剂及激素剂治疗;③各项检查资料完整。排除标准:①合并其他影响唾液腺功能疾病、慢性炎症者;②有涎腺手术史者;③涎腺占位性病变、获得性免疫缺陷病、丙型肝炎病毒感染者。根据唇腺活检分级标准[4]判定病情严重程度,将观察组进一步分为轻度组69 例和重度组41 例,轻度组中男41 例,女28例,年龄22~72岁,平均(46.99±10.32)岁;重度组中男23 例,女18 例,年龄22~73岁,平均(46.61±10.33)岁。另选同期63 例健康体检者为对照组,其中男35 例,女28 例,年龄23~71 岁,平均(46.86±10.54)岁。各组性别比、年龄、体质量指数比较差异均无统计学意义。本研究经我院医学伦理委员会批准,所有受检者均知情同意。
二、仪器与方法
1.剪切波弹性成像检查:使用法国声科Aixplorer彩色多普勒超声诊断仪,L5-4线阵探头,频率4~15 MHz。受检者取平卧位,暴露颈部,避免颈部过度仰伸。首先使用二维超声多切面扫查双侧颌下腺和腮腺,观察腺体形态、大小及内部回声;然后切换至弹性成像模式,探头垂直于皮肤表面,避免过度施压,嘱咐患者屏住呼吸、放松颈部肌肉,设定取样框,大小约为腺体中央1 cm×1 cm,待填充完全后稳定3 s,测量定帧,于框内最大硬度值处测量双侧颌下腺中部和腮腺杨氏模量均值,重复测量3 次取平均值。由两名高年资超声医师共同进行图像分析。
2.MRI检查:使用GE SIGNA 1.5T MRI检查仪。患者禁食60 min,检查时避免吞咽动作;选择8 通道正交头线圈。调节FSE 参数,T1WI 扫描,TE 1.05 ms,TR 460 ms;T2WI 扫描:TE 101.30 ms,TR 3100 ms。然后行MRI 检查,采用二维短时反转恢复序列,层厚20~34 mm,反转时间160 ms,TE 550 ms,TR 6000 ms。于导管方向的斜矢状面采集参数:激励次数2 次,FOV 140 mm×140 mm,矩阵512×512。由两名高年资影像医师共同进行图像分析,比较各组不同信号强度标准差、脂肪信号分级及腮腺导管扩张分级情况。
3.分级标准:①腮腺导管扩张分级标准[5]。0 级,导管无扩张;1 级,导管直径<1 mm,呈弥漫性点状扩张;2 级,导管直径1~2 mm,呈弥漫性球状扩张;3 级,导管直径<2 mm,呈弥漫性腔洞样扩张;4级,腺体内主导管短缩,分布不均,末梢导管分布不均,数量少,大小不等,呈管腔状扩张。②脂肪信号分级标准[6]。0级,正常腺体,未见脂肪信号;1 级,腮腺内脂肪信号呈稀疏点条状分布;2 级,腮腺内脂肪信号呈网格状弥漫分布;3 级,腮腺内弥漫性脂肪面积<50%,脂肪信号呈斑片状,残留腺体呈多发结节状;4 级,正常腺体消失,腮腺内弥漫性脂肪面积≥50%,见大范围脂肪信号。
三、统计学处理
应用SPSS 22.0统计软件,计量资料以x±s表示,多组比较采用重复测量方差分析,两两比较行LSD-t检验。绘制受试者工作特征(ROC)曲线分析各指标单独及联合应用诊断SS涎腺病变的价值,曲线下面积(AUC)比较行Z检验。P<0.05为差异有统计学意义。
结果
一、剪切波弹性成像检查结果比较
重度组双侧颌下腺和腮腺杨氏模量值均高于轻度组和对照组,差异均有统计学意义(均P<0.05);轻度组双侧颌下腺和腮腺杨氏模量均高于对照组,差异均有统计学意义(均P<0.05)。见图1,2和表1。
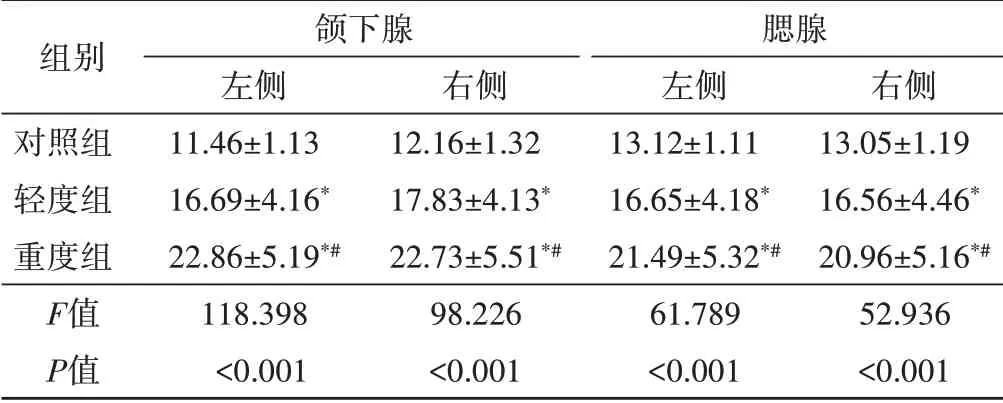
表1 各组双侧颌下腺及腮腺杨氏模量值比较(x±s) kPa
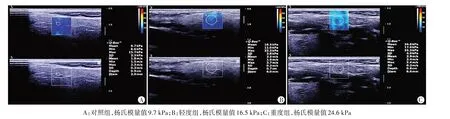
图1 各组左侧颌下腺剪切波弹性成像图
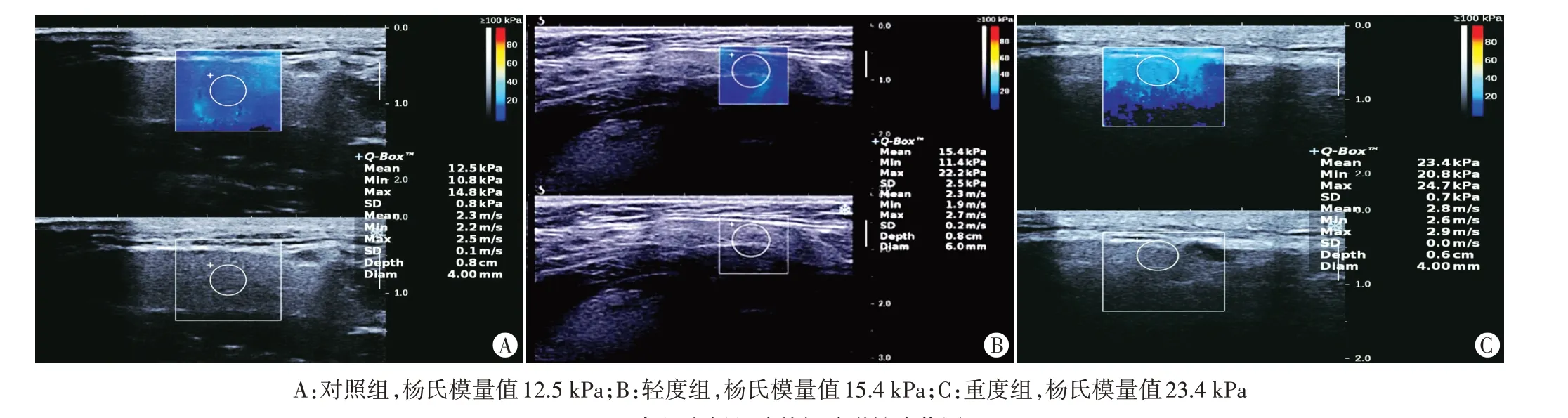
图2 各组右侧腮腺剪切波弹性成像图
二、MRI检查结果比较
重度组T1WI、T2WI、脂肪信号分级、腮腺导管扩张分级均高于轻度组和对照组,差异均有统计学意义(均P<0.05);轻度组T1WI、T2WI、脂肪信号分级、腮腺导管扩张分级均高于对照组,差异均有统计学意义(均P<0.05)。见表2和图3。
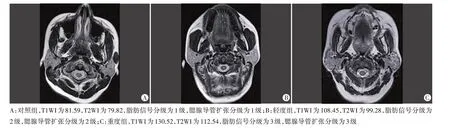
图3 各组MRI检查图
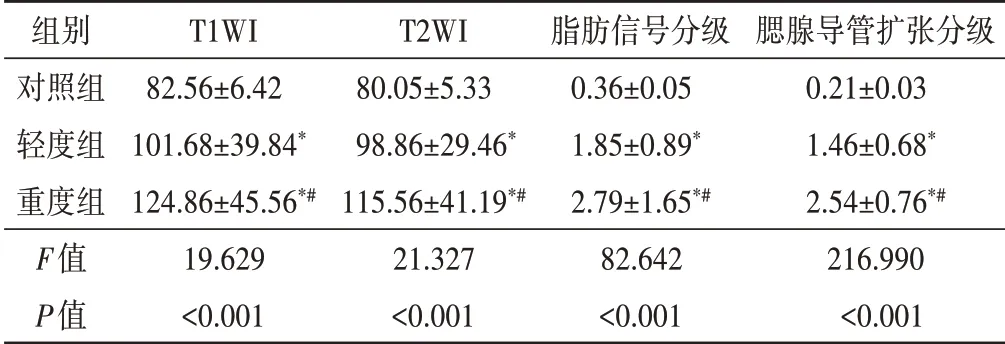
表2 各组不同信号强度标准差、脂肪信号分级、腮腺导管扩张分级比较(x±s)
三、ROC曲线分析
ROC 曲线分析显示,双侧颌下腺杨氏模量值、双侧腮腺杨氏模量值、T1WI、T2WI、脂肪信号分级、腮腺导管扩张分级诊断重度SS 涎腺病变的AUC 分别为0.805、0.743、0.732、0.745、0.647、0.670、0.659、0.832,将上述指标纳入Logistic回归分析,根据回归系数值拟合其联合诊断的计算公式:联合诊断=左侧颌下腺杨氏模量值+0.184/0.370*右侧颌下腺杨氏模量值+0.127/0.370*左侧腮腺杨氏模量值+0.073/0.370*右侧腮腺杨氏模量值+(-0.028)/0.370*T1WI+(-0.035)/0.370*T2WI+(-0.122)/0.370*脂肪信号分级+2.391/0.370*腮腺导管扩张分级,结果显示各指标联合应用诊断重度SS涎腺病变的AUC 为0.971。联合应用的AUC 与左侧颌下腺杨氏模量值、右侧颌下腺杨氏模量值、左侧腮腺杨氏模量值、右侧腮腺杨氏模量值、T1WI、T2WI、脂肪信号分级、腮腺导管扩张分级单独应用的AUC 比较差异均有统计学意义(Z=3.671、4.391、4.603、4.353、5.709、5.128、4.985、3.514,均P<0.001)。见表3和图4。
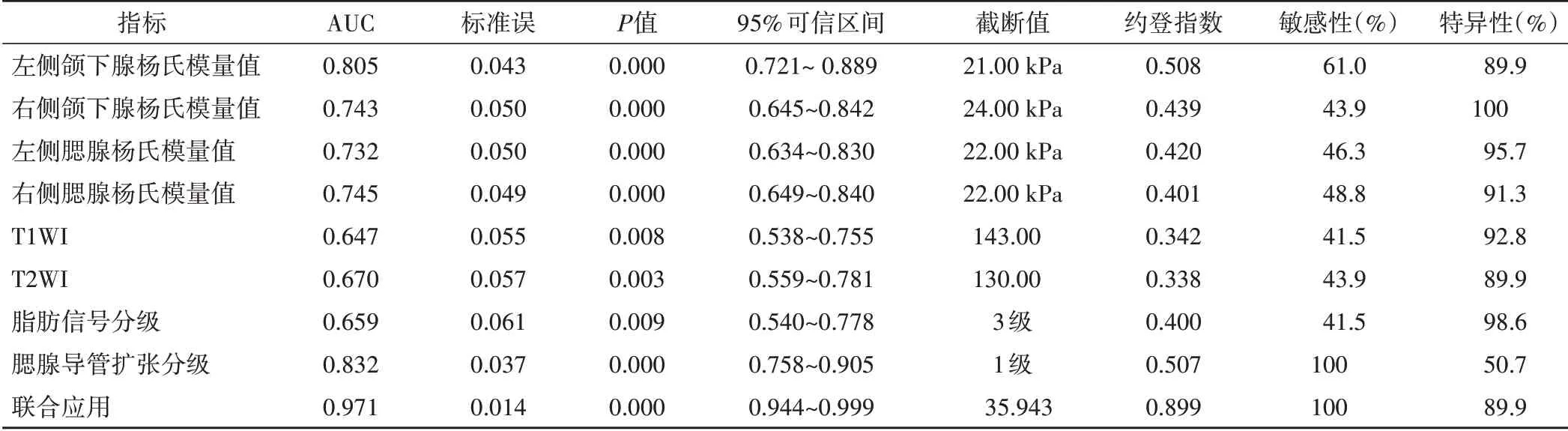
表3 各指标单独及联合应用诊断重度SS涎腺病变的ROC曲线分析
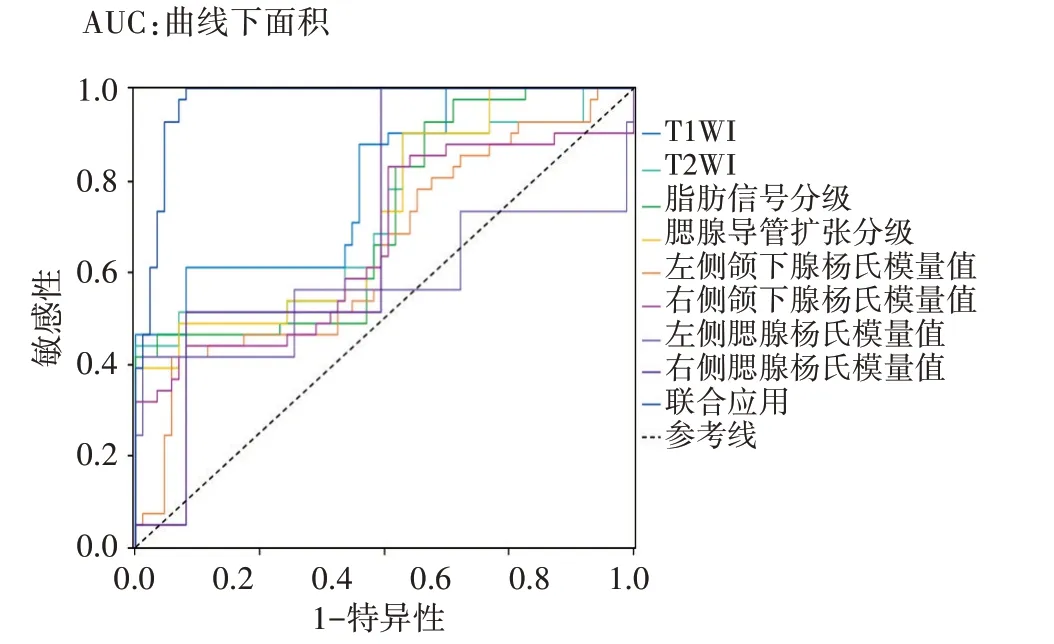
图4 各指标单独及联合应用诊断重度SS涎腺病变的ROC曲线图
讨论
SS 是一种慢性多发性疾病,可累及泪腺、腮腺等外分泌腺,其发病机制目前尚未明确,可能与上皮细胞抗原表达有关[7]。当机体出现SS 时,浆细胞和淋巴细胞可浸润泪腺和涎腺,导致腺体实质被破坏,出现系统性损害,影响其正常功能,最后发展为腺体萎缩纤维化。临床早期多使用超声、CT、唾液腺核素显像、X线等方法检查SS,虽有一定诊断价值,但也存在局限性,X线检查有辐射损伤;超声造影检查可因造影剂过敏应用受限;唾液腺核素显像、CT 误诊率较高。MRI具有组织分辨率高、无创伤等优势,不仅可显示腮腺大体形态,还可呈现导管影像,为临床诊断提供更多信息[8]。剪切波弹性成像是近年发展的超声新技术,可反映组织硬度,通过检测组织硬度进行定性诊断,可更客观地区分SS腺外包块和腺内包块,对病变鉴别诊断具有一定指导作用[9]。
本研究结果显示,观察组双侧颌下腺和腮腺杨氏模量值均高于对照组,差异均有统计学意义(均P<0.05)。说明SS可明显侵犯颌下腺和腮腺,且重度组双侧颌下腺和腮腺杨氏模量值均高于轻度组(均P<0.05),说明组织硬度可因腺体变硬、纤维化程度加重而增大,原因可能是早期淋巴细胞浸润,腺泡破坏不明显,随着病情进展,淋巴细胞大量聚集,纤维化加重,导致腺泡萎缩破坏,腺体质地变硬,引起腺体功能低下,使组织硬度明显增大[10]。剪切波弹性成像能较准确地反映局部病灶情况及严重程度,且不受操作者主观因素的影响,能较好地反映病灶与周围组织硬度的差异[11]。
研究[12]表明,SS 腮腺病变形成机制为唾液在腺泡或导管内聚集,腮腺排空功能下降,唾液分泌量减少。正常腮腺组织脂肪含量较少,在T1WI 和T2WI 中信号均匀;而SS患者因体内唾液积聚,T1和T2弛豫时间均延长。本研究结果显示,观察组T1WI、T2WI、脂肪信号分级、腮腺导管扩张分级均高于对照组,且重度组上述指标均较轻度组更高,差异均有统计学意义(均P<0.05)。说明MRI能够通过评估信号强度、信号分级及导管扩张分级判断机体是否存在涎腺病变及严重程度[13]。分析原因:一方面是腮腺导管水成像原理主要依据人体液体特性,正常人腮腺处无大量脂肪,因流动血液的留空效应表现为无信号或低信号,而SS涎腺病变患者含有唾液的腺泡、腮腺导管可产生较强对比,表现为高信号;另一方面当发现SS涎腺病变后,腮腺内可出现大量脂肪面积和管腔状扩张,通过观察脂肪信号分级和导管扩张程度可了解疾病发生、发展情况。虽然MRI对SS的诊断准确率较高,但也可能因导管内液体较少,无法反映扩张形态而出现假阴性,故建议联合检查进一步提高诊断准确率。
马光慧等[14]研究显示MRI 能很好地显示SS 的腮腺形态和信号改变,定量参数可直观反映腮腺各级导管扩张情况,为临床诊断提供客观依据。刘芳和任卫东[15]研究显示,实时剪切波弹性成像通过定量指标能够为临床诊断原发性SS腮腺病变提供可靠依据,具有便捷、无创等优势。为进一步探索MRI、剪切波弹性成像对SS涎腺病变的诊断效能,本研究将其进行ROC曲线分析,结果显示剪切波弹性成像、MRI检查指标联合应用诊断SS 涎腺病变的AUC 为0.973,高于各指标单独应用(均P<0.05),表明联合应用的价值更高,故建议临床在条件允许的情况下选择联合诊断,以达到降低假阴性率的目的。
综上所述,剪切波弹性成像能够反映SS涎腺病变局部病灶情况及严重程度,MRI 能够显示腮腺内腺泡及各级导管的改变,均有一定应用价值,两者联合应用临床价值更高。但本研究样本量有限,且未进行影像特征区分和定性评估,今后有待针对上述不足进一步探索。
