制霉菌素混悬剂的制备及质量评价
2022-04-02邹梅娟朴洪宇
黄 嵩,邹梅娟,朴洪宇
(沈阳药科大学 药学院,辽宁 沈阳 110016)
制霉菌素(nystatin, NYS)分子式为 C47H75NO17,分子量为 926.29,化学结构式见图 1。NYS是一种多烯型抗生素,具有共轭多烯大环内酯结构,常用于治疗皮肤与口腔感染的病原体念珠菌[1-2]。其作用机制为与真菌细胞膜上的麦角固醇结合,导致膜通透性改变,以致重要的细胞内物质外漏而达到杀灭真菌的目的[3-5]。与其他抗真菌药相比,NYS 具有更广泛的抗真菌谱,由于口服在胃肠道吸收差,肝毒性风险低,药物相互作用和不良反应未见报导[6-8]。
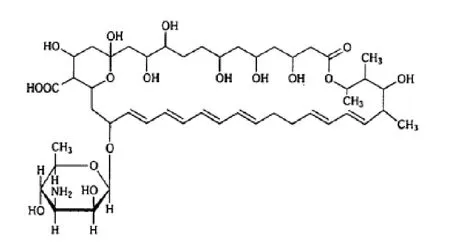
Fig. 1 Molecular formula of nystatin 图1 制霉菌素的化学结构式
制霉菌素混悬剂 1994 年在英国上市,商品名为 NystatinTMoral suspension(ready-mixed),国内尚未有同类制剂生产。且该混悬剂虽然生产工艺简单,但各批次制剂含量容易产生差异,制剂制备中 pH 易发生改变,制剂的稳定性易受到影响。本实验采用先将 NYS 分散于适宜介质中,再通过分散法制备 NYS 混悬剂,以提高制剂的稳定性,降低批次间差异。对 NYS 混悬剂的处方进行筛选,并研究各处方因素对 NYS 混悬剂稳定性的影响。
1 仪器和材料
BS110S 电子天平(德国 Sartorius 有限公司),FA25 型高速剪切匀质机(德国 Fluko 公司),L-2000 高效液相色谱仪(日本Hitachi公司),L-2420 UV-VIS 检测器(日本 Hitachi 公司),Rcz-6B 型药物溶出度仪(上海黄海药检仪器厂),pHS-25 精密 pH 计(上海雷磁仪器厂),UV-1800 紫外分光光度计(日本 Shimadzu 公司)。
制霉菌素(含量 6300 Units/mg,批号 C130556;Capua Bioservics S.p.A),甘油(P & G Chemicals),蔗糖(南宁糖业股份有限公司伶俐糖厂),羧甲基纤维素钠(Ashland Globle Holdings Inc.),磷酸氢二钠(湖南九典制药股份有限公司),对羟基苯甲酸甲酯(上野制药株式会社),对羟基苯甲酸丙酯(上野制药株式会社),香精(International Flavors & Fragrances Inc.)。
2 方法与结果
2.1 制霉菌素含量测定方法
临用新制。取本品,振荡 30 秒至均匀,静置 30 秒。用内容量移液管精密量取 1.0 mL,置200 mL 棕色量瓶中,用流动相分次洗涤移液管内壁,洗涤液并入量瓶中,继续加流动相至约 190 mL,超声 5 min,用流动相稀释至刻度,摇匀。用注射器吸取 5 mL,经 0.22 μm 有机滤膜滤过,弃去初滤液 2.5 mL,取续滤液 1 mL,作为供试品溶液,精密量取 10 μL 注入液相色谱仪中,记录色谱图;另取 NYS 对照品 50.0 mg,精密称定,置 50 mL 棕色量瓶中,加二甲基甲酰胺至48 mL,超声 2 分钟,用二甲基甲酰胺稀释至刻度,摇匀(对照品放置冷藏中 3 天稳定)。精密量取 1.0 mL,置 10 mL 棕色量瓶中,用流动 相稀释至刻度,摇匀,即得 NYS 对照品溶液,同法测定[9]。按外标法以峰面积计算。
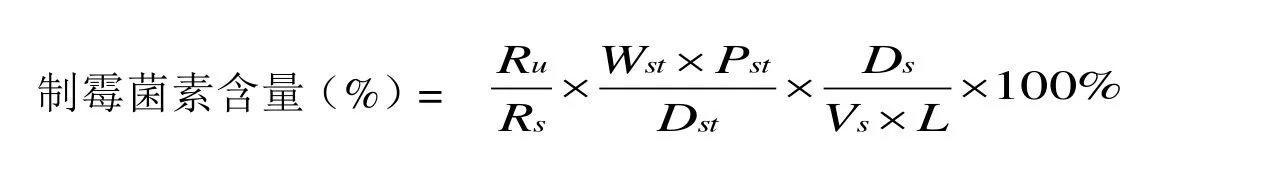
其中,Ru为供试品制霉菌素 A1及其异构体峰面积之和,Rs为对照品制霉菌素 A1及其异构体峰面积之和,Wst为对照品称样量(mg),Vs为供试品称样体积(mL),Dst为对照品稀释倍数,Ds为供试品稀释倍数,Pst为对照品纯度(units/mg),L 为供试品标示量(units/mL)。
高效液相色谱(HPLC)条件 色谱柱:Diamonsil C18ODS2(4.6 mm × 250 mm, 5 μm);流动相:甲醇-N, N-二甲基甲酰胺-0.1 M 醋酸铵溶液(550 : 150 : 270, v / v / v);检测波长:305 nm;柱温:25 ℃,流速:0.8 mL/min;进样量:10 μL。该色谱条件下,NYS 在 290.9~872.7 units/mL范围内峰面积和浓度线性关系良好,标准曲线为 A = 7 008.8C + 8 625.2(r2= 0.999 8)。NYS 回收率在 98~102% 之间,精密度 RSD < 2.0%,该方法专属性、精密度、稳定性良好(RSD < 2.0%)。
2.2 制霉菌素溶出度测定方法
取本品 0.5 mL(约相当于 NYS 50,000 Units),照溶出度与释放度测定法(《中国药典》2020年版四部通则 0931 第二法),以 0.1% SDS 溶液 900 mL 为溶出介质,温度 37 ± 0.5 ℃,转速为每分钟 50 转,依法操作。经 5 min 时,取溶液适量,滤过,取续滤液作为供试品溶液;另取NYS 对照品适量,加溶出介质溶解并定量稀释制成每 l mL 中约含 61.8 units 的溶液,作为对照品溶液。取上述两种溶液,照紫外分光光度法在 305 nm 测定其吸光度。溶出度应大于 50%,溶出度误差限度小于 15%,应符合规定。
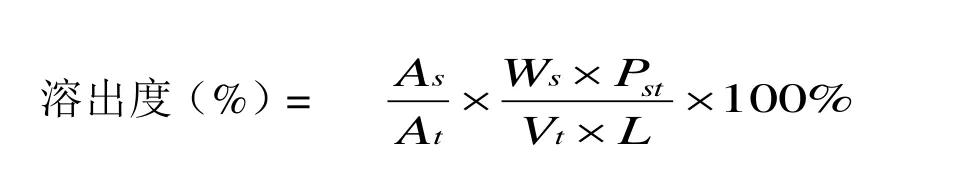
其中,As为对照品吸光度值,At为供试品吸光度值,Ws为对照品称样量(mg),Vt为供试品称样体积(mL),Pst为对照品纯度(units/mg),L 为供试品标示量(units/mL)。
溶出介质中,NYS 在 6.2~77.2 units/ml 范围内吸光度和浓度线性关系良好,标准曲线为A = 0.011 78C - 0.006 72(r2= 0.998 4)。NYS 回收率在 98~102% 之间,专属性良好,精密度良好(RSD < 2%)、稳定性良好。
2.3 沉降体积比
参照《中国药典》2020 年版四部通则 0123,用具塞量筒量取供试品 50 mL,密塞,用力振摇 1 min,记下混悬物初始高度 H0,静置 3 h,记下混悬物最终高度 H,按下式计算:
沉降体积比 = H / H0。沉降体积比不应低于 0.9。
2.4 原研制剂的初步分析
根据原研制剂说明书及对原研制剂的初步分析,制剂由制霉菌素、蔗糖、甘油、乙醇、羧甲基纤维素钠、磷酸盐、防腐剂、香精和纯化水组成。对原研制剂(批号:F203,标示量 100 000 units/mL)进行抽样分析。原研制剂为淡黄色或黄色混悬剂;制剂中制霉菌素为针状结晶,粒径在 50 微米左右;pH 在 6.95~7.05 之间;含量在 95%~115% 之间;5 min 时溶出度在 85%~95% 之间;沉降体积比为 1.0。
2.5 制霉菌素混悬剂的制备
蔗糖 30 g 与处方量羧甲基纤维素钠混匀,加适量水制成蔗糖溶液,备用。将 2.5 g 甘油加适量水配制成溶液,将 1.6 g NYS 分散在甘油水溶液中,慢慢加入上述蔗糖溶液中,边加边搅拌。加入 0.12 g 磷酸氢二钠,0.075 g 对羟基苯甲酸甲酯、0.015 g 对羟基苯甲酸丙酯和适量香精,补加水至 100 mL,高速剪切 10 000 r/min,约 10 min,至分散均匀,调节 pH 至 7,真空脱气后,过 100 目筛,即得。
2.6 处方筛选
2.6.1 制霉菌素分散介质的筛选
NYS 具有较强的疏水性,直接将 NYS 分散到蔗糖溶液中极易聚结[10],影响制剂的均匀性与物理稳定性。因此需要将 NYS 分散在合适的介质中,先搅拌制成分散均匀的液体,再将含药混悬液转移至糖浆中。甘油作为常见的助悬剂同时具有较好的润湿性,本身与水也可以任意比例互溶。乙醇具有良好的润湿效果,NYS 在乙醇溶解度低,因此乙醇水溶液也可用作分散介质。将相同量的 NYS 分别混入等体积下表所述三种分散介质中,通过观察分散后的状态与静置之后的沉降体积比考察以上三种分散介质,结果见表 1。

Table 1 Screening of dispersion media表1 分散介质的筛选
结果表明,当以水为分散介质时,NYS 几乎全部漂浮在水面上,经过较长时间搅拌后,逐渐分散在水中,但仍会聚集成大的团块,转移过程中容易附着在容器壁上。当以乙醇水溶液作为分散介质时,虽然 NYS 的分散效果与流动性较好,但是混悬液的物理稳定性较差,NYS 沉降速度快,也不利于转移。只有甘油水溶液作为分散介质时,NYS 分散良好的同时有较好的物理稳定性,其流动性也适于物料转移,因此选择甘油水溶液作为 NYS 的分散介质进行之后的处方筛选。
2.6.2 羧甲基纤维素钠用量的筛选
CMC-Na 易于分散在水中形成透明的胶体溶液,溶液具有一定粘度,能够长时间保持稳定,因此常用作助悬剂[11]。同时为了保证分散效果和分散速度,需要将粘度控制在合适的范围,因此对 CMC-Na 的用量进行了筛选。分别考察了 0.1%、0.15% 和 0.2% 的 CMC-Na 用量,结果见表 2。
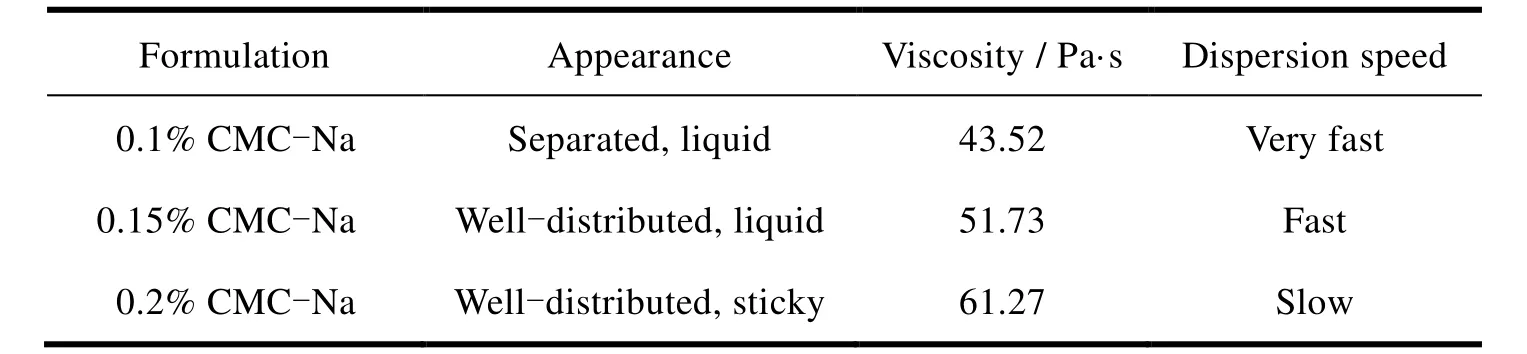
Table 2 Screening of the amount of CMC-Na表2 CMC-Na用量的筛选
结果表明,随 CMC-Na 用量的提高,混悬剂的粘度也会升高。当 CMC-Na 用量为 0.1% 时,制剂粘度偏低,虽然在水中可以以很快的速度分散,但制剂随放置时间会产生分层的现象,物理稳定性不好。当 CMC-Na 用量为 0.2% 时,混悬剂粘度较大,分散困难,在水中分散速度也较为缓慢,有可能进一步影响药物的溶出速度。因此选择添加 0.15% CMC-Na,物理稳定性良好,分散速度较快,但不足以完全掩盖 NYS 的苦味,考虑添加矫味剂进行弥补。
2.6.3 防腐剂对混悬剂 pH 的影响
蔗糖溶液作为基质时具有较好的粘度,物料也较为廉价,在混悬剂中应用广泛。而 NYS 有土腥味,蔗糖溶液能起到较好的掩味效果,一定程度上提高 NYS 的口服顺应性,因此选用蔗糖溶液作为制剂的基质。实际应用过程中,发现蔗糖溶液的 pH 值随时间会发生较大变化,由最开始的中性快速转变为酸性环境,对 NYS 的稳定性产生影响。根据文献与实际应用需要,选择添加防腐剂抑制 pH 值变化。对羟基苯甲酸甲酯与对羟基苯甲酸丙酯都是常用的医药防腐剂,由于具有酚羟基结构,抗细菌能力比苯甲酸、山梨酸要强,两者联用具有较好的加成性与协同性。将处方放置在 40 ℃ 条件下,分别在 5 天和 10 天时测定 pH 值,结果见表 3。
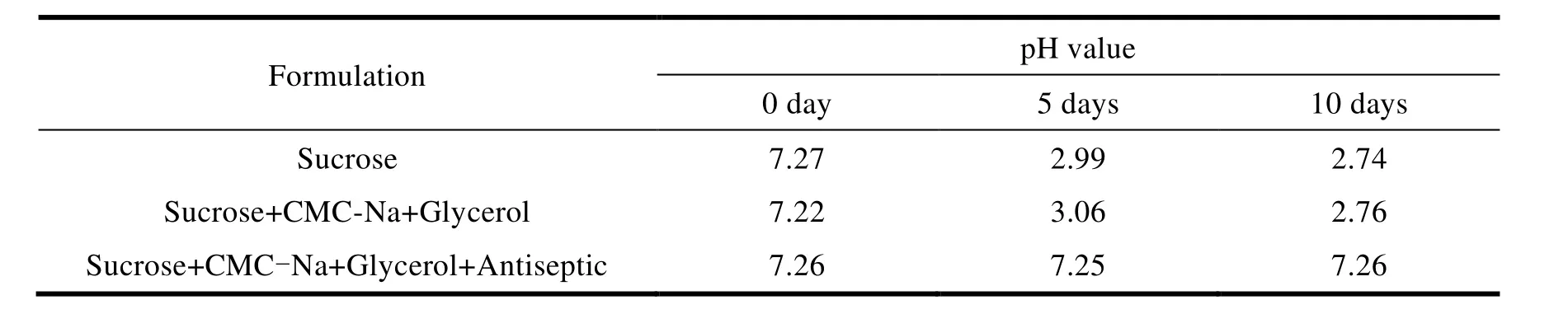
Table 3 Effects of preservatives on pH stability of the syrup表3 防腐剂对基质pH稳定性的影响
结果表明加入对羟基苯甲酸甲酯和对羟基苯甲酸丙酯可以有效提高混悬剂基质的 pH 稳定性。这是因为蔗糖在水中会分解为葡萄糖和果糖,高温和强酸条件都会加剧转化反应。分解得到的葡萄糖在微生物作用下生成葡萄糖酸及其它具有弱酸性的物质[12],影响制剂的 pH 稳定性。对羟基苯甲酸甲酯与对羟基苯甲酸丙酯可以有效杀菌,抑制葡萄糖转换为葡萄糖酸。当溶液 pH 值为 7 时,对羟基苯甲酸甲酯与对羟基苯甲酸丙酯杀菌活性也能维持较高的活性[13],适合本制剂使用。
2.6.4 矫味剂的筛选
由于 NYS 的味道难以通过基质完全掩盖,需要添加矫味剂使制剂的气味和味道易于接受,从而提高患者的顺应性。由于常用香精多为弱酸性,也可能与基质发生反应影响制剂的稳定性,选择了三种味道较好的香精制备成制剂,放置在高温环境下进行考察,结果见表 4。
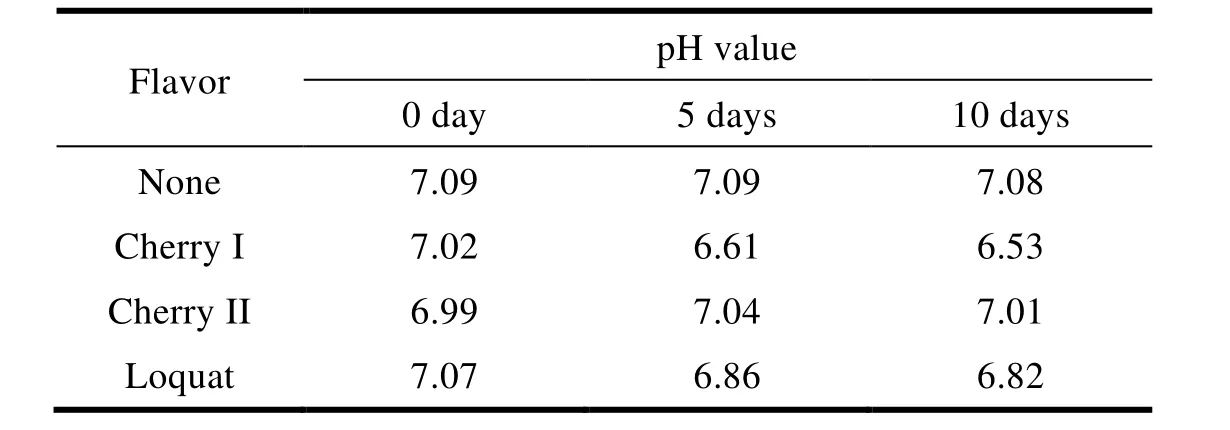
Table 4 Effects of the flavor on pH stability 表4 矫味剂对制剂 pH 稳定性的影响
结果表明,Cherry I 型香精和琵琶香精都会逐渐酸化,降低制剂的 pH 值,但 pH 的变化短时间不会对含量产生影响。Cherry II 型香精 pH 较为稳定。其中作用机制尚不明确,根据类似文献[14]推测原因为,两种香精中都含有大量酸、酯类化合物,容易使制剂 pH 降低。Cherry II 型香精相比之下,酸、酯类物质含量可能较少,能够在矫味的同时维持较好的 pH 稳定性,利于保持制剂的稳定性,因此,选用 Cherry II 型香精作为矫味剂。
2.7 制霉菌素混悬剂的表征
取 NYS 混悬剂 0.5 mL,加入纯化水 1 mL,以10 000 r/min 的速度离心 15 min,弃去上清液,将底层沉淀在 -60 ℃ 下减压冻干,即得 NYS 素冻干粉。以市售制剂作为参比,同法处理,用于之后的表征实验。
2.7.1 SEM 观察
通过扫描电镜(scanning electron microscope, SEM)观察原料药与制剂的形态与表面特性。方法为:将样品用导电的胶固定在铝制短柱上,表面喷金,采用 20 kV 的加速电压扫描器表面并拍照,结果见图 2。

Fig. 2 Scanning electron microphotographs of NYS (A), self-made preparation (B) and commercial preparation (C) 图2 制霉菌素原料药(A)、自制制剂(B)和市售制剂(C)的SEM电镜图
结果显示,NYS 原料药呈短柱状,粒径在 5 μm 左右,粒径分布较为均匀;制剂中的 NYS呈针状,粒径在 50 μm 左右,粒径分布比较均匀,与市售制剂一致。推测 NYS 晶体在放置过程中会逐渐生长,通过 DSC 与 XRD 判断 NYS 的晶型是否发生改变。
2.7.2 DSC
通过差示扫描量热法分析法考察原料药与制剂的晶型,称取样品 3.0~5.0 mg,氮气保护下,以 10 ℃/min 的速度从 35 ℃ 升至 280 ℃,图谱见图 3。
通过差热扫描量热法的结果可知,自制制剂冻干粉在 150 ℃ 和 170 ℃ 附近有两个吸热峰,与原料药相比位置并未发生明显的变化,说明制剂中药物的晶型与原料药一致,在制剂过程中没有发生改变。自制制剂的 DSC 曲线与市售制剂基本一致,说明两者晶型相同。
2.7.3 XRD
通过 X-射线衍射分析原料药与制剂的晶型,取适量原料药与制剂进行 X-射线粉末衍射分析,辐射源为 Cu-Kα,管压 40 kV,管流 30 mA,扫描角度 3~50°,步长 0.02,扫描速度 2°/min,衍射图谱同见图 4。
结果表明,NYS 在 2θ 为 5°~30° 内有明显的晶体衍射峰。自制制剂冻干粉与原料药的衍射峰位置没有明显差异,以上结果进一步说明了 NYS 在制剂过程中晶型没有发生改变。同时,自制制剂的 XRD 图谱与市售制剂基本一致,表明两者晶型相似。

Fig. 3 Differential scanning calorimetry cerves of NYS (A), self-made preparation (B), and commercial preparation (C) 图3 制霉菌素原料药(A)、自制制剂(B)和市售制剂(C)的DSC曲线
2.8 稳定性
由以上实验可知,稳定的 pH 值是制剂能够保持稳定的关键,结合 NYS 的自身特点,考察在实际储存条件下的稳定性情况。将三批模拟商品包装的样品与市售制剂置于相对湿度 60 ± 5%、温度为 25 ± 2 ℃ 的条件下存放,分别于第 3、6、9、12 月取样,以外观、含量、溶出度、pH值和沉降体积比为指标进行考察,结果见表 5。
结果表明,NYS 混悬剂在商品包装的条件下,存放 12 个月后,外观不变,溶出度与沉降体积比无明显变化,pH 值与药物含量略有减小,但在合格范围内。与市售制剂相比,制剂稳定性有所提高,说明自制 NYS 混悬剂稳定性良好。
3 讨论
3.1 剂型与处方选择
NYS 常制成片剂用以治疗消化道念珠菌病,也可制备成泡腾片,治疗白色念珠菌和其他念珠菌所引起的阴道感染。为了方便口腔用药和儿童用药,可以选择制成混悬剂。混悬剂口中释放快,直达患处,患者顺应性强。
然而,NYS 有浓重的土腥味,制成混悬剂时需要在保证制剂稳定性的前提下进行调味。NYS本身稳定性较差,混悬剂的物理稳定性也需要重点考察,是处方考察中的难点。
处方筛选中选择混悬剂的关键质量属性制剂性状、粘度、pH 稳定性侧重考察,为处方筛选提供了依据。当处方粘度较大时,制剂的物理稳定性良好,掩味效果也较好,但是分散较慢可能会影响药物的释放。NYS 在酸性条件和碱性条件下都不稳定,制剂应始终保持在中性环境,磷酸氢二钠起到了缓冲盐的作用,但当添加过量缓冲盐时,又会导致主药聚集,降低制剂的物理稳定性。香精的选用也会影响到制剂的 pH 稳定性。
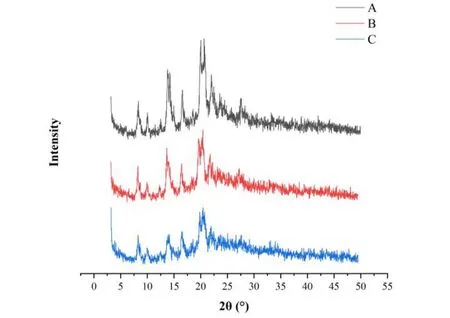
Fig. 4 X-ray diffraction spectra of NYS (A), self-made preparation (B) and commercial preparation (C) 图4 制霉菌素原料药(A)、自制制剂(B)和市售制剂(C)的XRD图谱
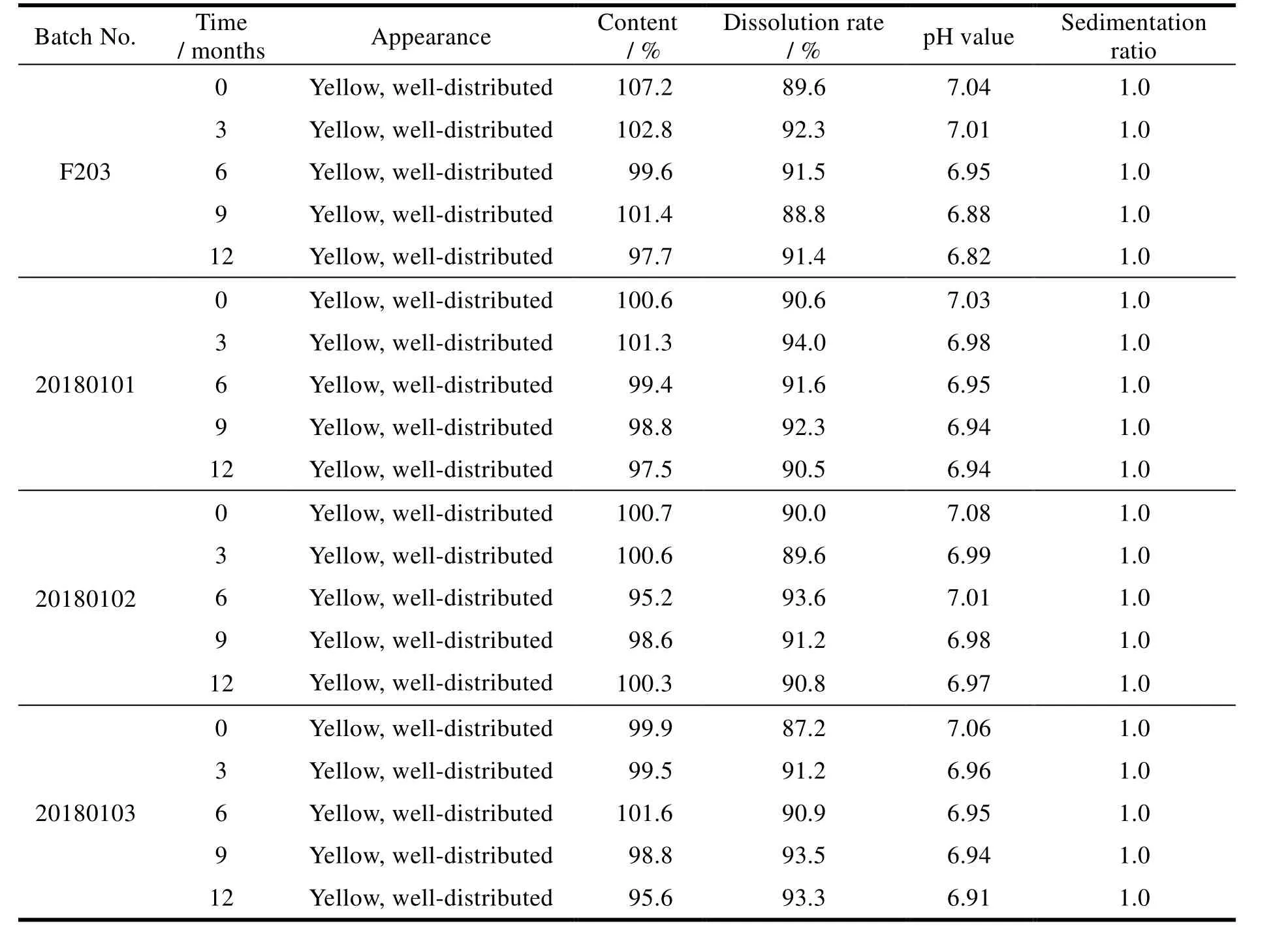
Table 5 Test results of long-term stability of nystatin suspension表5 制霉菌素混悬剂长期稳定性实验结果
3.2 制霉菌素晶体的成长
NYS 原料药的粒径较小,但在混悬剂体系中,原料药有增长的趋势并形成针状结晶,在室温1 个月内即可达到 50 μm 左右,与市售制剂相同,之后不再变化。晶体成长过程中,pH 值,沉降体积比,含量等均无明显变化,制剂稳定性良好。成长之后的 NYS 晶体与原料药具有相同的晶型和性质。这些针状结晶在混悬剂中能够形成稳定的架桥结构,避免聚结影响制剂的物理稳定性。NYS 晶体成长的机制有待下一步研究。
3.3 含量检测方法
NYS 作为抗生素常用含量测定法为效价测定法,通过管碟法测量抑菌圈直径衡量抑菌效果。该方法不能提供准确数据,且费时。因此参考 Phyllis Wilson 等人的方法,建立了高效液相色谱法来测定制剂含量的含量。验证表明,上述方法都满足检测要求,并且有省时省力、简单易行的优点。
3.4 稳定性试验考察
稳定性考察中,重点选择了性状、pH 值和含量作为考察重点,其中影响因素试验为处方调整提供了支持,同时对产品的贮存和有效期的制定提供了依据。
长期稳定性试验为产品的有效期提供了参考依据和数据。长期留样数据表明制剂在 12 个月内稳定性良好。
4 结论
成功制备了制霉菌素混悬剂,该制剂工艺简单,药物回收率高且批次间差异小。该制剂掩味效果好,能够提高患者,尤其是婴幼儿的顺应性。长期留样实验结果说明,该制剂具有良好的稳定性,有继续研究开发的必要和价值。
