磁共振成像与乳房X线摄影对乳腺簇状钙化病变的诊断价值比较
2022-04-01马金平朱荔刘紫朦杨丽刘丰源鲍宝石邢宁王建东
马金平,朱荔,刘紫朦,杨丽,3,刘丰源,鲍宝石,邢宁*,王建东*
1解放军总医院第一医学中心普通外科医学部,北京 100853;2烟台市蓬莱人民医院普外一科,山东烟台 265600;3北京市顺义区医院普通外科,北京 101300
早期诊断对提高乳腺癌患者的生存率至关重要[1],微钙化可能是早期乳腺癌最有价值的诊断标志物[2],乳房X线摄影(MG)是目前临床上针对乳腺微钙化病变的主要检查方法。微钙化在乳腺良恶性病变中均可出现,MG检出难以定性的微钙化时,常常建议进一步行组织活检,但创伤性检查会加重患者的生理和心理压力,因此寻求无创性的检查方法判断病灶性质是临床亟待解决的问题。乳腺磁共振成像(MRI)虽然难以显示乳腺的微小钙化,但可检测出恶性病灶的新生血管,并能观察到2~3 mm的病变,可很好地显示病灶的形态及血流动力学参数,对乳腺良、恶性病变的定性具有重要意义。但MRI检查价格昂贵且检查时间较长,其全面推广受到一定限制。MRI动态增强结合MG检查将乳腺可疑微钙化病变的形态学与血流动力学参数综合起来,可对乳腺微钙化病变的定性提供帮助。本研究比较了MRI与MG对乳腺簇状钙化病变的诊断价值,以明确MRI检查是否可提高诊断的准确性。
1 资料与方法
1.1 研究对象 收集2009年1月-2018年5月就诊于解放军总医院第一医学中心的62例乳腺簇状钙化病变患者的临床资料。纳入标准:(1)术前或穿刺前MG检查发现含簇状钙化病灶,同时行MRI检查;(2)女性患者;(3)术前未行乳房相关治疗;(4)于本院进行手术治疗,对于非肿块型钙化灶,术前行MG下导丝定位,术中切除病灶后行MG检查明确钙化灶完整切除;(5)临床病理资料完整。排除标准:(1)簇状钙化<5粒/cm2;(2)妊娠或哺乳期患者;(3)术前行新辅助治疗或有乳房手术史;(4)未行乳房全切者;(5)术后病理为特殊类型癌。
1.2 MG检查 采用全数字化乳腺摄影机(美国GE公司),所有患者行轴位(CC位)及侧斜位(MLO位)摄影,增加病变切线以及斜位和局部放大相,观察病灶位置、大小、形态、边缘、密度及钙化情况。簇状钙化计数标准:在钙化范围>1 cm2位置选择最密集处计数,钙化颗粒>5粒/cm2;在钙化范围<1 cm2位置钙化颗粒>5粒。
1.3 MRI检查 采用GE 1.5T和3.0T MRI扫描仪(美国金利公司),4通道或8通道相控阵乳腺专用线圈,扫描序列包括MR扩散加权成像(DWI)、T2加权成像(T2WI)、T1加权成像(T1WI)、动态增强4个序列。详细参数参照程流泉等[3]的研究。
1.4 图像评估 采用美国放射学院乳腺影像报告与数据系统(breast imaging reporting and data system,BI-RADS)对病灶进行分类,评估报告均由有经验的主治医师或(副)主任医师审核签署。
1.5 统计学处理 使用SPSS 22.0软件进行统计分析。MG与MRI检查的诊断一致性比较采用Kappa检验,采用ROC曲线分析比较两种检查的诊断效能。P<0.05为差异有统计学意义。
2 结 果
2.1 一般资料 共纳入62例乳腺簇状钙化病变患者,年龄49(29~65)岁,术前行MG和MRI检查。术后病理结果显示,良性20例,恶性42例[包括浸润性癌(IDC) 35例、导管原位癌(DCIS) 7例],病变性质及BI-RADS分类如表1所示。
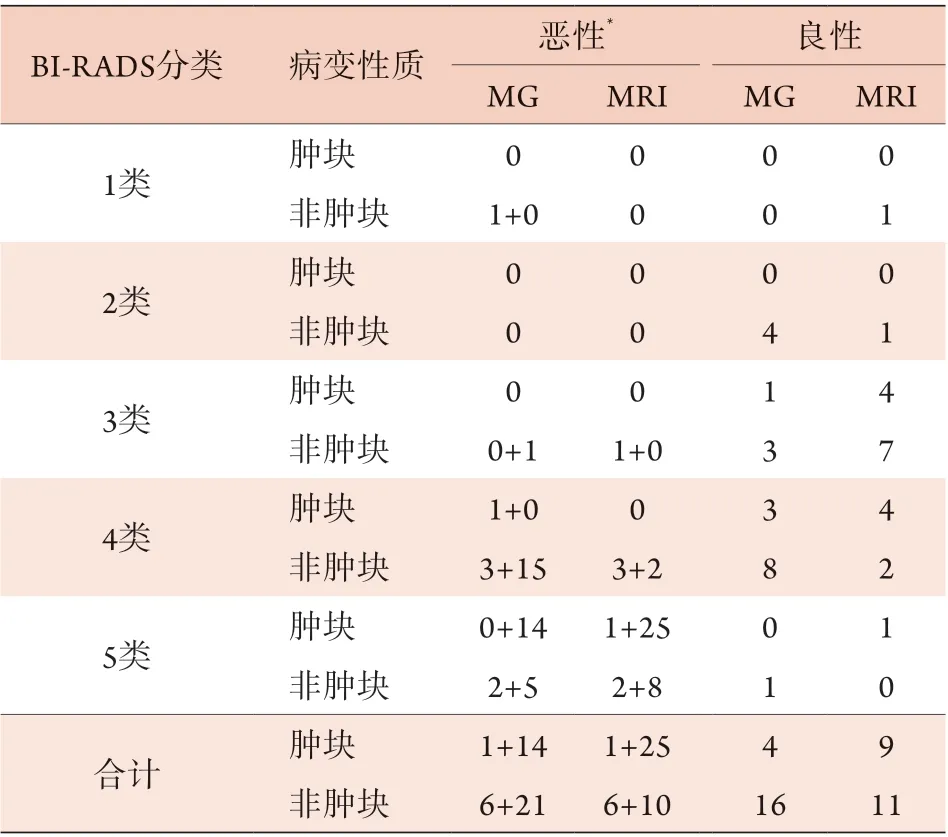
表1 62例乳腺簇状钙化病变患者的BI-RADS分类、病变性质与病理结果(例)Tab.1 Summary of BI-RADS, pathological morphology and mass nature of 62 patients with clustered calcification breast lesions (n)
20例良性患者中,MG检查BI-RADS分类为1-3类8例,其中1例为肿块样病变,7例为非肿块样病变;对应MRI检查BI-RADS分类为1-3类6例,4类2例,其中4例为肿块样病变,4例为非肿块样病变。MG检查BI-RADS分类为4-5类12例,其中3例为肿块样病变,9例为非肿块样病变;对应MRI检查BI-RADS分类为1-3类7例,4-5类5例,其中5例为肿块样病变,7例为非肿块样病变。
42例恶性患者中,MG检查BI-RADS分类为1-3类2例,均为非肿块样病变;对应MRI检查BIRADS分类为4-5类2例,其中1例为肿块样病变,1例为非肿块样病变。MG检查BI-RADS分类为4-5类40例,其中15例为肿块样病变,余25例为非肿块样病变;对应MRI检查BI-RADS分类为1-3类1例,4-5类39例,其中25例为肿块样病变,15例为非肿块样病变。
2.2 MG与MRI检查诊断乳腺簇状钙化病变的一致性 62例乳腺簇状钙化病变患者中,MG检查诊断为1-3类10例(16.1%,10/62),4类30例(48.4%,30/62),5类22例(35.5%,22/62);MRI检查诊断为1-3类14例(22.6%,14/62),4类11例(17.7%,11/62),5类37例(59.7%,37/62)。MG与MRI检查的诊断一致性较差,Kappa值为0.346(表2)。
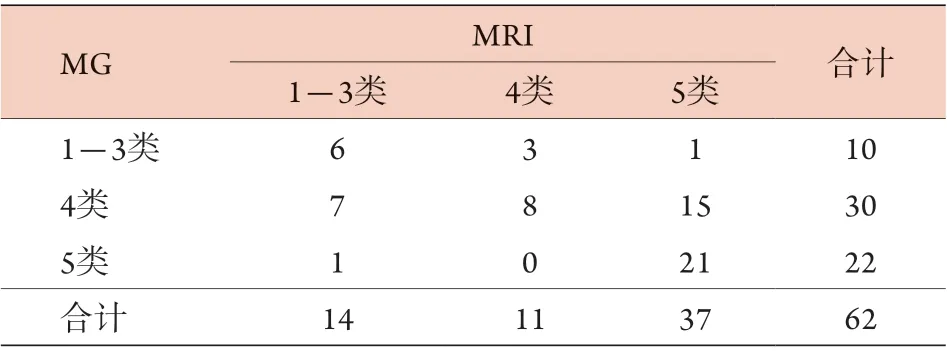
表2 MG与MRI检查诊断乳腺簇状钙化病变的一致性(例)Tab.2 Comparison of diagnostic consistency between MG and MRI in duster calcification of breast lesions (n)
2.3 MG与MRI检查对乳腺簇状钙化病变的诊断效能比较 MG检查鉴别乳腺良、恶性病变的截断值为4.5(AUC=0.800,95%CI 0.686~0.914),诊断乳腺簇状钙化恶性疾病的敏感度、特异度和约登指数分别为50.0%、95.0%和45.0%;MRI检查鉴别乳腺良、恶性病变的截断值为4.5(AUC=0.940,95%CI 0.850~1.000),诊断乳腺簇状钙化恶性疾病的敏感度、特异度和约登指数分别为85.7%、95.0%和80.7%。MRI检查诊断的准确率高于MG检查(88.7%vs. 64.5%,图1、表3)。
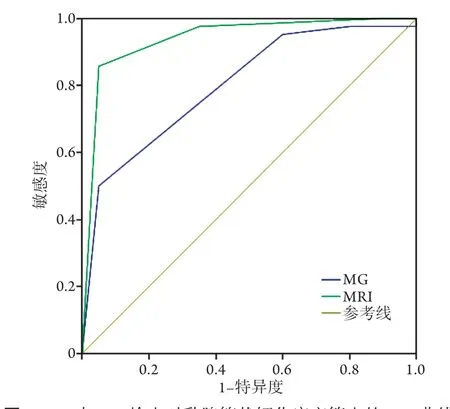
图1 MG与MRI检查对乳腺簇状钙化病变筛查的ROC曲线Fig.1 ROC analysis for breast screening of mammography and MRI
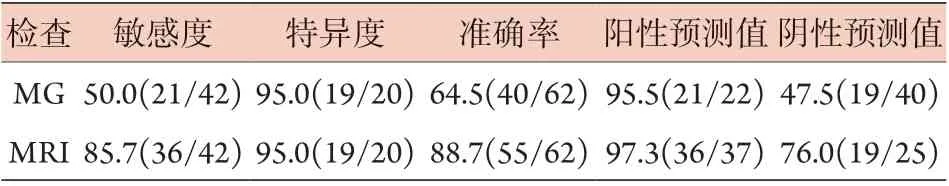
表3 MG与MRI检查对乳腺簇状钙化病变的诊断效能比较[%(n1/n2)]Tab.3 Comparison of diagnostic efficacy of MG and MRI in duster calcification of breast lesions [%(n1/n2)]
3 讨 论
乳腺微钙化是由各种原因引起的矿物质沉积,在乳腺良恶性肿瘤中均可出现。良性钙化一般是钙质沉积造成的,恶性钙化一般是肿瘤坏死残留形成的。根据钙化的大小、形状、分布及密度判断乳腺疾病的良恶性具有重要意义。乳腺微钙化是诊断早期乳腺癌的重要特征,也可能是乳腺恶性肿瘤早期的唯一指征[4]。有研究发现,微钙化是乳腺恶性肿瘤的独立预测因素[5]。最近Clauser等[6]使用微钙化形态、异型性和伴发癌症的标准,通过更广泛频谱的分层算法寻找潜在的恶性病变。但在实际临床工作中,良恶性钙化的形态存在重叠,常出现一些不易或不能定性的可疑钙化,尤以微钙化为著。研究发现,簇状微钙化是无法触及的乳腺癌的主要标志之一,有时甚至是唯一的阳性标志,因此准确判读簇状微钙化、筛选发现乳腺癌是临床亟待解决的问题。根据钙化灶的大小和形态差异,团簇状钙化可分为粗糙不均质钙化、粗大或爆米花样钙化和营养不良性钙化等[7]。研究发现,呈单发团簇状分布的粗糙不均质钙化灶的潜在恶性可能性为7%~15%[8-9]。MG检查操作简单、费用低、诊断较可靠,是目前乳腺筛查常用的影像学方法,特别是其可发现直径0.1~0.2 mm的钙化点,显著提高了含钙化乳腺病灶的检出率。有研究报道,约1/3的MG检查及多达40%的乳腺癌MG检查发现了钙化灶[10]。虽然MG检查在钙化灶的检出方面是其他检查无法替代的,但因其技术特点限制了MG检查的准确性,钙化点大小不一、形态多变、分布随机,与周围乳腺组织对比度低,且放射科医师个体经验存在差异,导致早期诊断的准确率较低[11]。MG检查的阳性预测值为27.4%~60.4%[12],具有相对较低的敏感度(67.8%)和特异度(75%)[13],因此单纯依靠MG检查判断簇状微钙化的性质存在一定缺陷。乳腺微钙化的过度活检率高达72.1%~75.0%[14-16],由于其假阳性率较高,导致许多良性疾病进行了不必要的活检,增加了患者的心理压力及经济负担。
目前,MRI技术得到了很好的推广,由于磁共振对比剂和快速成像序列的开发运用,乳腺MRI诊断水平逐渐增高。MRI可通过注射顺磁对比剂强化肿瘤细胞而对病变进行功能评估,提高诊断乳腺恶性疾病的敏感度和特异度。Pinker等[17]发现,动态增强MRI诊断乳腺癌的准确率为90.6%,但难以显示乳腺的微小钙化,所以在MG发现的钙化病灶中,MRI的评估作用仍存在争议。微小钙化灶虽较难发现,但肿瘤细胞生长较为迅速,致使周围血管增生,肿瘤组织早期血管生成所导致的血流变化,能够通过MRI增强扫描信号反映出来。时间-信号强度曲线为病灶血流灌注及流出等多种因素的综合反映,能够体现病灶情况[18-19]。研究发现,对于MG发现的BI-RADS 3类和5类含钙化病灶,不建议进一步使用乳腺MRI辅助诊断[20]。对于MG检查发现的BI-RADS 4类钙化病灶,可考虑行乳腺MRI检查进一步协助判断病灶性质。Bennani-Baiti等[21]分析了248例微钙化乳腺癌患者,发现MRI对MG分类为BIRADS 4a和4b类的钙化灶诊断更为精准,有可能避免不必要的活检;而对于4c类钙化灶,不论MRI结果如何,均应进行活检以避免恶性肿瘤漏诊。在Strobel等[22]的研究中,58%(45/78)的簇状微钙化患者通过进一步MRI检查避免了行病灶穿刺活检,且22例MG检查为BI-RADS 4类的簇状微钙化患者经MRI进一步评估后,考虑为恶性,术后病理证实均为导管原位癌。由此可见,MRI可指导后续治疗,且可协助确定手术切除范围。
本研究结果显示,MG对伴有微钙化的乳腺肿瘤诊断准确率为64.5%,MRI为88.7%,MRI对良、恶性肿瘤的诊断准确率均高于MG。由于微钙化可伴随乳腺肿块出现,也可单独存在,在非肿块样病变乳腺癌中,钙化常常是唯一的阳性征象。因此本研究进一步分析了肿块样病变和非肿块样病变中MG和MRI检查的诊断效能,发现在诊断良性微钙化肿块样和非肿块样病变时,二者的准确率均较高,MRI的诊断效能较MG检查无明显提高。但一些特殊病理漏诊情况应结合病史和临床体检,以提高准确性;而对于恶性微钙化非肿块样病变,其诊断难度增加,尤其是MG,此类患者应加做MRI进一步评估病变性质。此外,本研究发现,对于部分MG发现的非肿块样钙化,MRI能够发现肿块样强化,分析原因可能是致密型腺体遮挡了肿物边缘,而MRI断层扫描能很好地弥补这方面的不足。
综上所述,本研究结果表明,MG检查发现乳腺簇状钙化时,建议进一步行MRI检查,以提高诊断准确性。但本研究为回顾性研究,纳入样本数量相对较少,可能存在选择偏倚,且缺乏病灶的病理大小,未对病理结果进行细化分析,其结果有待进一步研究验证。
