早期自然流产胚胎染色体异常的危险因素分析
2022-03-31张哲慧薛吟霜何英明向卉芬曹云霞
张哲慧,薛吟霜,何英明,向卉芬,曹云霞
自然流产(spontaneous abortion,SA)是指孕周在28周内,胎儿体质量不超过 1 kg而妊娠终止,在所有临床妊娠中约占15%~20%[1-2]。孕周小于12周的SA称为早期SA。早期SA的病因较为复杂,免疫学因素、易栓因素、女性生殖道解剖异常以及内分泌异常是最重要的4种母体病因。胚胎染色体异常在早期SA病因中较为常见,约占50%~60%[3]。对于夫妻双方染色体正常情况下发生的胚胎染色体异常,国际上尚无较为详尽的危险因素分析。该研究通过回顾性分析胚胎染色体异常的早期SA患者的临床资料、生化指标及分布特征,探讨其与胚胎染色体异常的关系,为临床诊治提供参考。
1 材料与方法
1.1 一般资料选择2019年12月—2021年3月于安徽医科大学第一附属医院生殖中心门诊就诊的315例早期SA并接受绒毛组织染色体检测的患者。纳入标准:① 年龄20~42岁;② 被诊断为超声和组织学检查支持的临床意义上的SA。排除标准:① 男方和(或)女方染色体异常;② 供精和(或)供卵助孕等情况。
1.2 方法
1.2.1胚胎染色体检测 将新鲜绒毛组织用大量等渗氯化钠溶液冲洗3~5次,去除血液等杂质后,用组织剪剪取少量绒毛组织并浸泡入等渗氯化钠溶液中。染色体微阵列分析(chromosomal microarray analysis,CMA)检测采用染色体微阵列optima芯片,使用美国Affymetrix Genechip生物芯片检测系统。
1.2.2分组 根据胚胎染色体检测结果将315例早期SA患者分为正常组(150例)与异常组(165例)。
1.2.3临床资料收集 采用统一调查表对两组患者进行问卷调查,内容包括:① 基础信息:双方年龄、联系电话、籍贯、女方民族、文化程度、职业;② 生活史与既往史:家族近亲结婚史、女方吸烟饮酒情况、饮用咖啡因饮料情况、污染及辐射接触史、既往疾病史、手术史、过敏史等;③ 月经及生育史。
1.2.4体质量指数(body mass index,BMI)及生化指标检测 两组患者空腹禁食超过8 h后测量身高、体质量,计算BMI=体重/身高2(kg/m2)。同时,全部患者均需空腹抽取肘静脉血10 ml,测定血清各项生化指标,包括促甲状腺激素(thyroid stimulating hormone,TSH)、25羟维生素D[25-hydroxyvitamin D,25-(OH)D]、抗核抗体(antinuclear antibody,ANA)、抗心磷脂抗体(anticardiolipin antibody,ACA)、甲状腺过氧化物酶抗体(thyroid peroxidase antibody,TPOAb)、甲状腺球蛋白抗体(thyroglobulin antibody,TgAb)、空腹胰岛素(fasting insulin,FINS)、促卵泡激素(follicle stimulating hormone,FSH)、黄体生成素(luteinizing hormone,LH)、同型半胱氨酸(homocysteine,HCY)等。25-(OH)D采用化学发光免疫法检测,使用LIAISON XL-2210全自动化学发光免疫分析仪;TSH、TgAb、TPOAb、FINS采用化学发光免疫法检测,使用罗氏Cobas 601型电化学发光免疫仪器;ANA采用间接免疫荧光法,使用Sprinter XL型全自动间接免疫荧光操作/酶联免疫一体机;ACA采用化学发光免疫法,使用Werfen 3710-0344型全自动化学发光免疫分析仪;FPG采用氧化酶法,采用罗氏Cobas701型全自动生化仪及配套试剂;HCY采用循环酶法,使用贝克曼AU5800型全自动生化分析仪。性激素于月经周期第2~4天测定,采用化学发光免疫法检测,使用美国Beckman公司化学发光免疫仪器。
2 结果
2.1 早期SA患者异常胚胎染色体的分布早期SA的胚胎染色体异常率为52.38%(165/315)。在165例异常的胚胎染色体中,非整倍体、多倍体及染色体结构异常分别占71.52%(118/165)、8.48%(14/165)、20.00%(33/165)。在非整倍体中,X染色体单体占13.56%(16/118),常染色体三体占82.20%(97/118),其中16号染色体三体占比最高30.51%(36/118)。见图1。
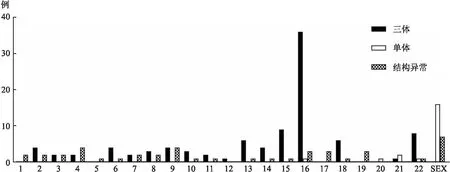
图1 早期自然流产患者胚胎染色体异常结果分布
2.2 两组基础资料的比较异常组与正常组的女方民族、文化程度、职业以及男方年龄分布情况,差异无统计学意义(P>0.05) ;异常组女方年龄(30.87±4.46)岁高于正常组(29.75±3.72)岁,差异有统计学意义(P<0.05);高龄组(≥35岁)胚胎染色体异常率(66.67%)高于非高龄组(<35岁,49.62%),差异有统计学意义(P<0.05)。见表1。
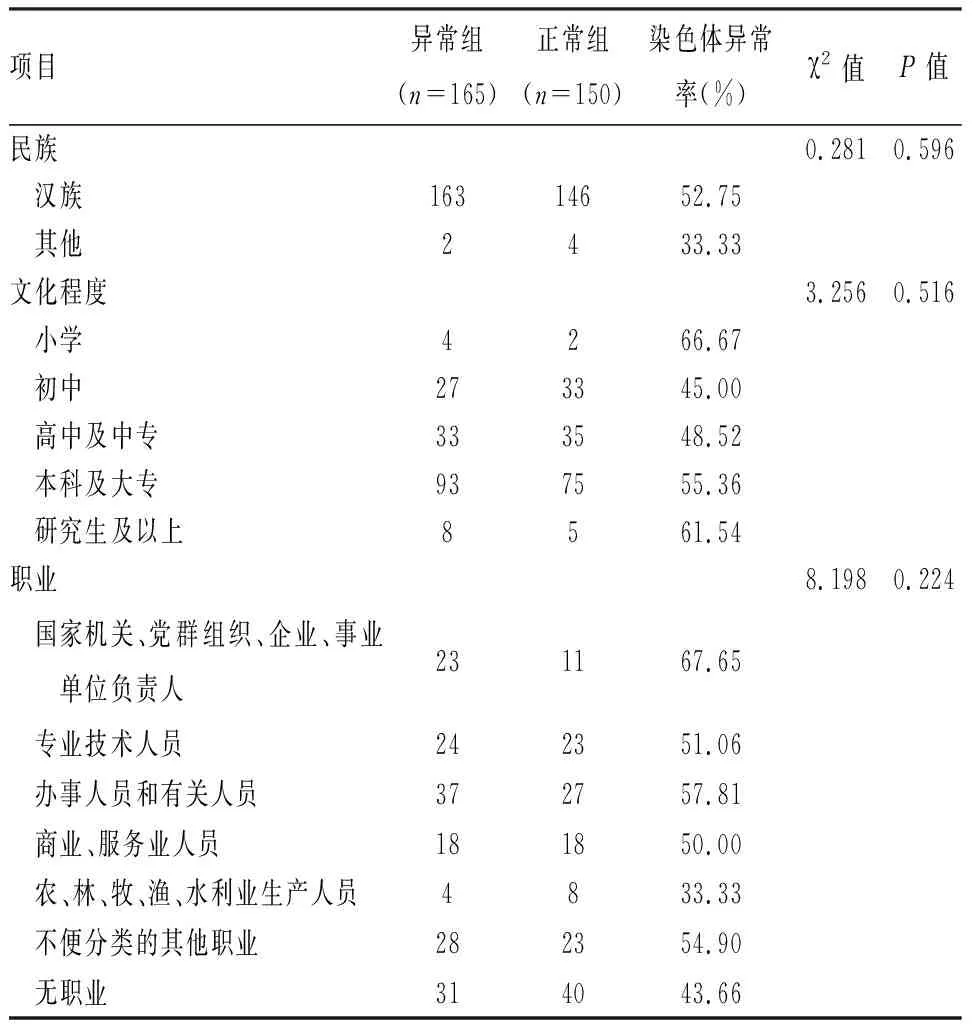
表1 两组患者基础资料的比较(例)
2.3 两组生活史与既往史的比较比较两组患者的近亲结婚情况、半年内吸烟饮酒饮用咖啡因饮料史、半年内污染辐射接触史,差异无统计学差异(P>0.05)。比较两组既往病史、手术史、过敏史、长期用药史,差异无统计学差异(P>0.05)。见表2。
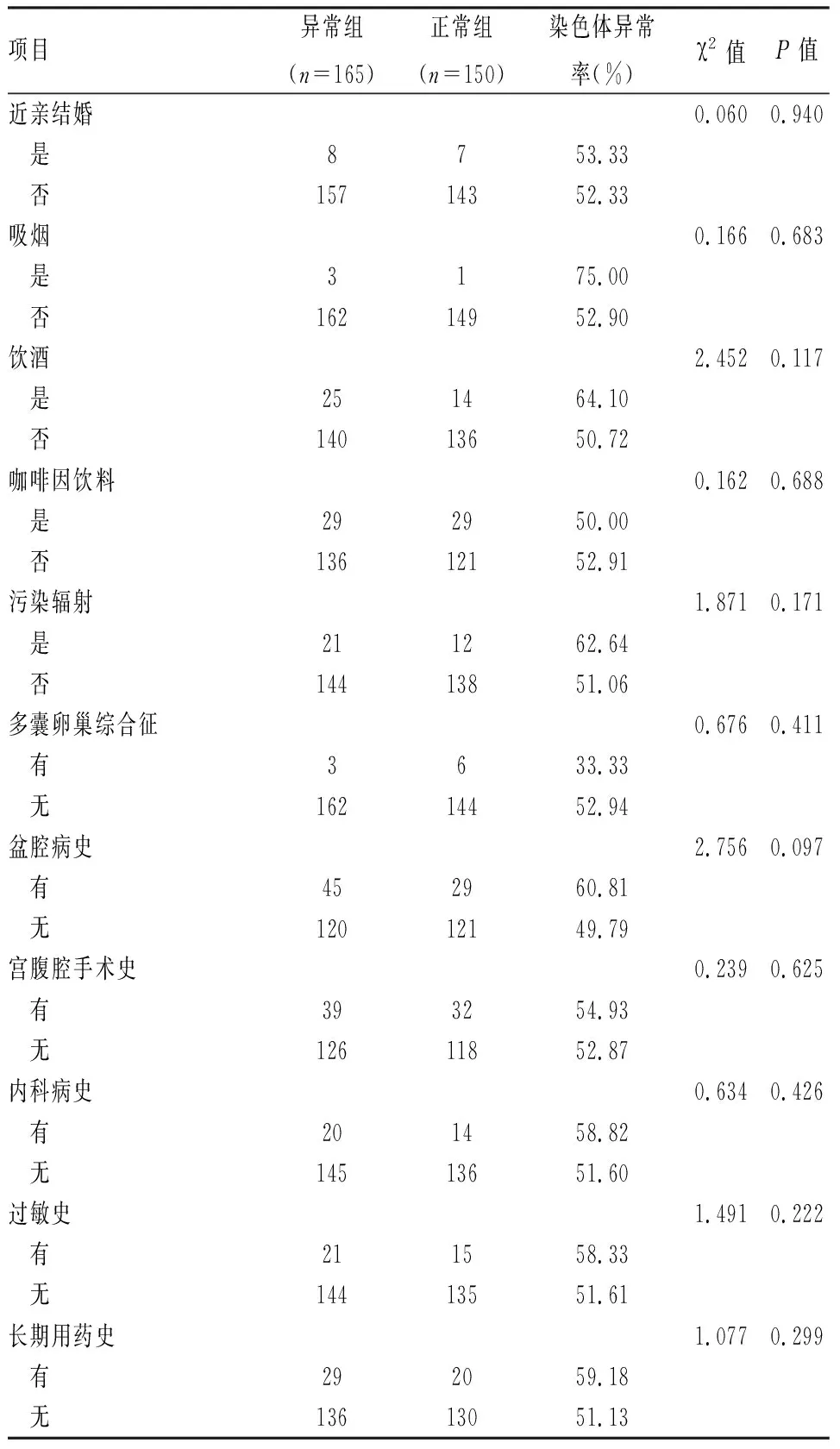
表2 两组患者生活史与既往史的比较(例)
2.4 两组患者月经史与生育史的比较通过统计比较发现,两组患者的月经初潮年龄、药物控制月经情况、既往孕次、不良妊娠史、计划外流产史、异位妊娠史、活产史差异无统计学意义(P>0.05);此次妊娠使用辅助生殖技术(assisted reproductive technique,ART)助孕的患者,胚胎染色体异常率低于自然妊娠患者,差异有统计学意义(P<0.05)。见表3。
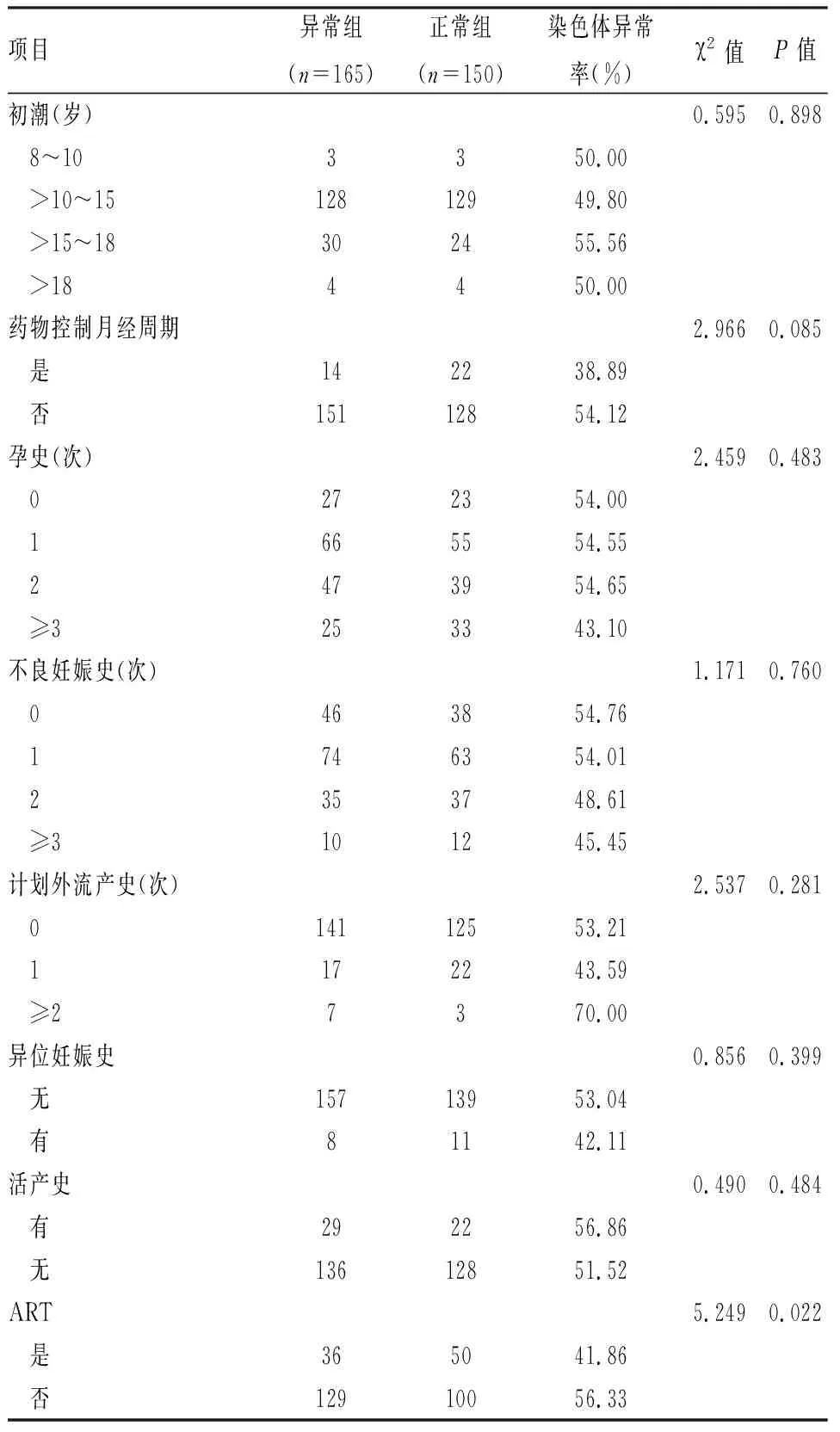
表3 两组患者月经史与生育史的比较(例)
2.5 两组生化指标的比较统计结果发现,两组BMI、TgAb、TPOAb、ANA、ACA、FPG、FINS、HCY、FSH/LH差异无统计学意义(P>0.05);异常组患者血清25-(OH)D含量(15.95±7.52 )μg/L低于正常组(17.93±7.87) μg/L,差异有统计学意义(P<0.05);早期SA患者维生素D缺乏率为70.79%,异常组维生素D缺乏率为75.15%,正常组为66.00%;维生素D严重缺乏[25-(OH)D<10 μg/L]患者胚胎染色体异常率高于维生素D轻度缺乏[10 μg/L≤25-(OH)D<20 μg/L]患者,维生素D轻度缺乏患者胚胎染色体异常率高于维生素D充足[25-(OH)D≥20 μg/L]患者,差异有统计学意义(P<0.05);异常组患者血清TSH含量高于正常组,差异有统计学意义(P<0.05)。见表4、5。
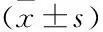
表4 两组患者生化指标的比较
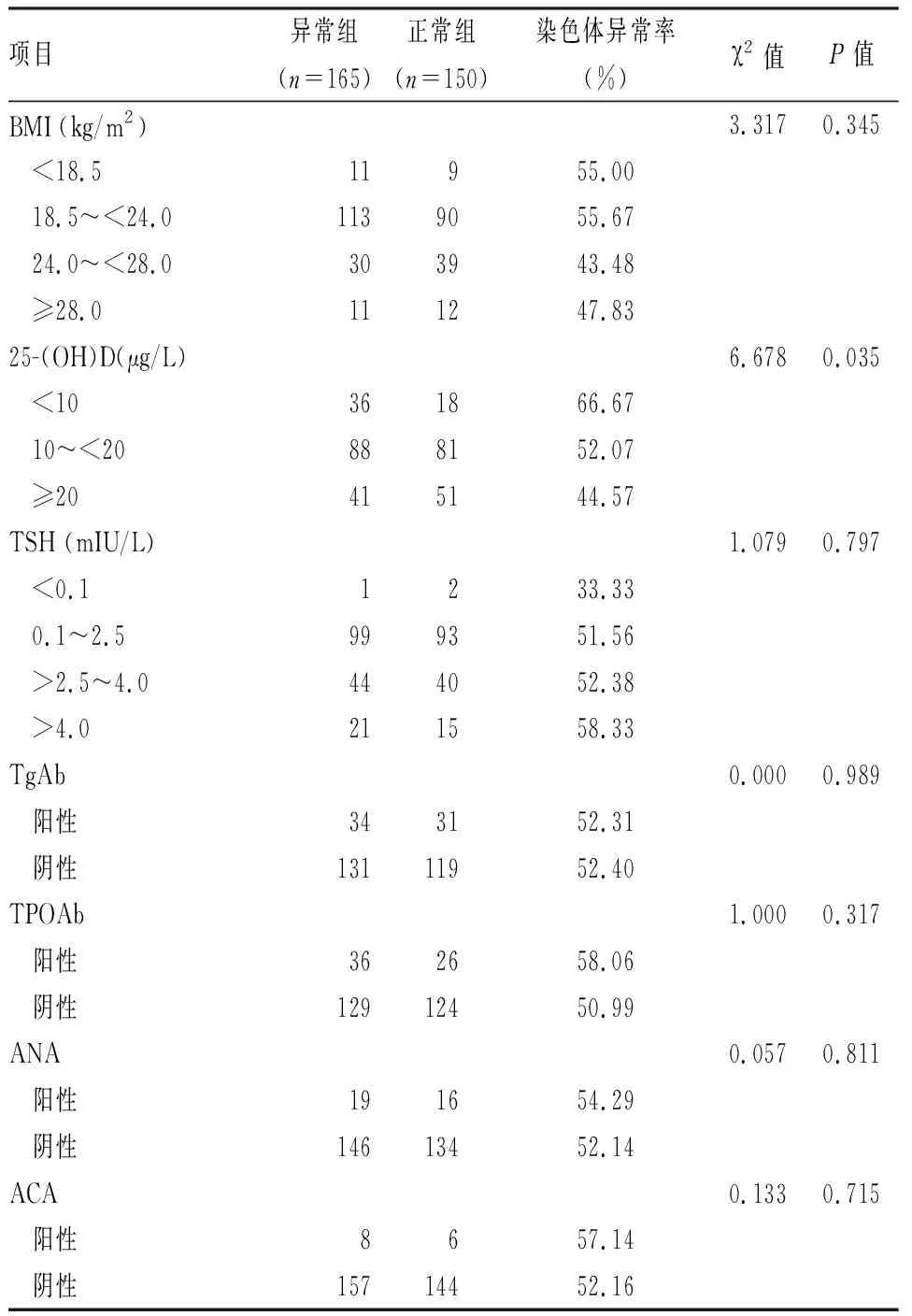
表5 两组患者生化指标的比较(例)
2.6 胚胎染色体异常的多因素Logistic回归分析在上述单因素分析的基础上,对两组间差异有统计学意义的指标进行多因素Logistic回归分析,结果表明,高龄以及低血清25-(OH)D水平是胚胎染色体异常的独立危险因素(P<0.05)。见表6。
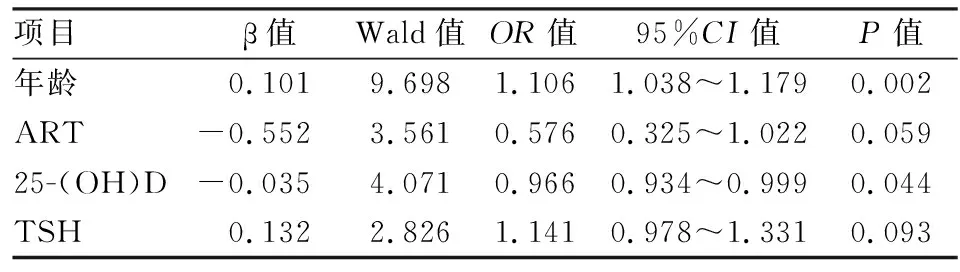
表6 胚胎染色体异常危险因素Logistic回归分析
3 讨论
目前,SA已是一个较为常见的生殖健康问题,其病因中胚胎染色体异常较为常见。因此,对早期SA患者进行胚胎染色体检测对病因诊断以及下一次妊娠有一定的指导意义。本研究在分析早期SA患者的临床资料、生化指标水平及其分布特征的基础上,发现女性高龄以及低血清25-(OH)D水平是胚胎染色体异常的独立危险因素。
有研究[4-5]分析常染色体三体在异常染色体中最为常见,约占60%,其中16号染色体三体作为致死性三体占异常染色体的20.00%。本次研究对象均为染色体正常的早期SA夫妻,胚胎染色体异常率为52.38%(165/315),常染色体三体占58.79%(97/165),其中16号染色体三体在异常染色体中占21.82%(36/165),这与相关研究一致[4-5]。胚胎染色体异常的原因包括生殖细胞减数分裂错误与受精卵细胞早期发育中有丝分裂错误,其中多数常染色体三体来源于母源减数分裂错误,大部分16号染色体三体都起源于卵子减数分裂Ⅰ[6]。在本研究中,女方年龄<35岁胚胎染色体异常率为49.62%,而年龄≥35岁的女方胚胎染色体异常率高达66.67%。随着女性年龄的增长,其生殖能力发生变化。在35岁后女性卵巢储备功能与卵子质量逐渐下降,卵母细胞的染色体非整倍体率明显上升,这可能与高龄女性卵母细胞端粒缩短、纺锤体老化导致减数分裂错误率提高有关[7]。女方年龄虽是至今唯一被证实与胚胎染色体异常相关的因素,但并非所有的染色体异常均与女方高龄相关。一项回顾性研究[8]发现,16号染色体三体与X单体的发生率在高龄组与非高龄组中并无统计学差异,这也从一定程度上证明了女方年龄并非唯一导致胚胎染色体异常的危险因素。
目前我国育龄期女性维生素D缺乏的现象较为普遍,且尚无维生素D分类的统一标准。在本研究中,维生素D缺乏的参考值采用美国医学研究院(IOM)推荐[9-10],即25-(OH)D < 20 μg/L。在早期SA的患者中维生素D缺乏率高达70.79%。胚胎染色体异常组的维生素D缺乏率(75.15%)高于正常组(66.00%),同时异常组中血清25-(OH)D水平低于正常组。维生素D作为人体必需的维生素,除了维持人体的钙磷平衡,调节细胞增殖、免疫、肌肉功能、皮肤分化、血管以及代谢水平,还参与生殖系统中多种功能的调节。在女性生殖系统中,维生素D受体存在于下丘脑、垂体、卵巢、子宫内膜、输卵管上皮、胎盘等组织,维生素D缺乏与不孕、子宫内膜异位症、多囊卵巢综合征、SA、先兆子痫以及妊娠期糖尿病有关[11]。本研究首次发现低血清25-(OH)D是导致胚胎染色体异常的独立危险因素,但目前母体血清维生素D在胚胎染色体中的风险机制尚不明确。Malloy et al[12]发现抗苗勒氏管激素(anti-mullerian hormone,AMH)的启动子包含一个功能性维生素D应答元件,维生素D通过这个应答元件直接上调AMH基因表达。AMH作为卵巢储备功能的预测指标,在卵泡发育与周期募集中起调节作用。维生素D缺乏可能通过下调AMH的表达来影响卵子质量,从而导致胚胎染色体异常。目前仍缺少维生素D影响胚胎染色体的直接证据,本次研究对象均来自就诊于安徽医科大学第一附属生殖中心的早期SA患者,纳入样本量较少,可能对结果造成偏倚,后期需扩大样本量并深入基础研究。
此外,在本研究中还发现异常组与正常组在妊娠方式和TSH水平上差异有统计学意义。自然妊娠患者胚胎染色体异常率(56.33%)高于ART助孕患者(41.86%),差异有统计学意义。方有燕 等[4]研究发现,自然妊娠组绒毛染色体异常发生率显著高于ART组(52.85%vs40.68%,P=0.033),而在郭楠 等[13]的研究中自然妊娠组的胚胎染色体异常率(43.75%)低于ART组(59.26%),差异无统计学意义。本研究与前者相符,在一定程度上说明ART可能并不增加胚胎染色体异常的风险。此外,本研究发现胚胎染色体异常组的TSH水平高于正常组[(2.75±2.13)mIU/Lvs(2.33±1.27) mIU/L,P=0.048],差异有统计学意义。亚临床甲状腺功能减退(subclinical hypothyroidism,SCH)在育龄期女性中发病率约为0.5%~5.0%,临床上针对复发性流产患者,常将TSH>2.5 mIU/L作为筛选标准。SCH可导致月经紊乱、不孕、流产及妊娠并发症等生殖系统疾病[14],可能影响颗粒细胞的生存率、类固醇的生成和卵母细胞的成熟[15],但目前尚无有价值的研究支持TSH对胚胎染色体有直接作用。
综上所述,女方高龄以及维生素D缺乏是胚胎染色体异常的独立危险因素。因此,对既往有早期SA史尤其是有胚胎染色体异常史的患者建议进行常规血清25-(OH)D的筛查,并积极诊断及治疗。这对防止下次妊娠再次出现胚胎染色体异常可能有积极意义。
