基于微滴式数字PCR技术对乙型肝炎低病毒血症患者血浆HBV DNA精准检测*
2022-03-30范子豪田原徐玲曹亚玲陈思思潘桢桢张向颖段钟平任锋首都医科大学附属北京佑安医院北京肝病研究所北京100069
范子豪,田原,徐玲,曹亚玲,陈思思,潘桢桢,张向颖,段钟平,任锋(首都医科大学附属北京佑安医院,北京肝病研究所,北京 100069)
低病毒血症是指HBV DNA定量持续或间歇大于检测下限但小于2 000 IU/mL的一类HBV持续感染[1-2]。美国肝病研究学会(American Association for the Study of Liver Diseases,AASLD)慢性乙型肝炎(Chronic hepatitis B, CHB)诊疗指南和我国CHB诊疗指南关于病毒学应答制定的标准均指出,低病毒载量血浆HBV DNA的精准检测十分重要[3-4]。随着抗病毒药物的广泛应用,乙型肝炎低病毒血症及隐匿性感染患者数量趋于增多,这对HBV DNA检测的灵敏度也提出了更高的要求[5-7]。故探求一种有效检测低病毒载量HBV DNA的方法,对临床抗病毒治疗效果的评价和治疗策略的调整具有重要意义。微滴式数字PCR(droplet digital PCR,ddPCR)技术作为新一代的PCR技术,能够对目标核酸进行绝对定量分析从而实现精准检测的目的。因此,本研究建立了检测HBV DNA的ddPCR方法并对乙型肝炎低病毒血症患者HBV DNA进行绝对定量分析。
1 材料和方法
1.1样本 收集2021年首都医科大学附属北京佑安医院19例乙型肝炎低病毒血症患者血浆样本进行临床检测分析,以及HBV、丙型肝炎病毒(hepatitis C virus, HCV)、丁型肝炎病毒(hepatitis D virus, HDV)和HIV感染患者血浆样本各5份进行特异性分析。乙型肝炎低病毒血症患者的纳入标准为:雅培M2000实时荧光定量PCR(quantitative real-time PCR, qRT-PCR)HBV DNA检测结果<10 IU/mL(含HBsAg阴性的隐匿型感染者)。本研究经首都医科大学附属北京佑安医院医学伦理委员会批准(文件批号: 京佑科伦意[2021]365号)且取得患者知情同意。
1.2主要试剂与仪器 病毒基因组DNA/RNA提取试剂盒(北京天根公司),ddPCR Super Mix、微液滴样本制备通用试剂盒(含微流控生物芯片)、微液滴检测通用试剂盒(北京新羿生物公司);T100热循环PCR仪(美国Bio-Rad公司),D-1微滴式数字PCR平台:Drop Maker样本制备仪、Chip Reader生物芯片分析仪(北京新羿生物公司)。
1.3引物和探针的设计与合成 ddPCR引物和荧光探针均由上海生工生物公司合成。引物及探针序列为:上游引物:5′-CTCTCTTTACGCGGTCTC-3′,下游引物:5′-GTCGTTGACATTGCTGAG-3′,荧光探针:5′-FAM-CCGTCTGTGCCTTCTCATCTGC-TAMRA-3′。
1.4构建HBV DNA阳性对照质粒 阳性对照质粒为构建的pUC57-HBV质粒。阳性对照质粒的构建、纯化和鉴定由北京博迈德基因技术有限公司完成,且质粒原液浓度为1 357 ng/μL(约为4.23×1011copies/μL),于-80 ℃保存备用。
1.5ddPCR反应体系和条件 在D-1微滴式数字PCR平台完成ddPCR反应。根据微液滴样本制备通用试剂盒说明书配制反应体系。ddPCR反应体系共30 μL,包括2×SuperMix 15 μL,模板5 μL,上、下游引物(10 μmol/L)各1.5 μL,探针0.6 μL,无酶无菌水6.4 μL。将30 μL PCR混合物和180 μL微液滴生成油在Drop Maker样本制备仪上反应,生成“油包水液滴”,然后用T100热循环PCR仪对微液滴样品进行扩增。PCR反应条件:95 ℃ 10 min;94 ℃ 30 s,60 ℃ 1 min,40个循环;12 ℃ 5 min。利用Chip Reader生物芯片分析仪检测FAM信号并分析结果。
1.6标准曲线和检出限分析 以梯度浓度稀释的HBV阳性对照质粒为模板,对该方法进行准确性和灵敏度的评价。构建的阳性对照质粒按1×105、1×104、1×103、1×102、1×101、1×100copies/μL的浓度进行梯度稀释和上机检测。通过阳性对照质粒的拷贝数和检测结果的拷贝数计算线性方程。
1.7特异性试验 对5例已知为HBV阳性临床样本按照病毒基因组DNA/RNA提取试剂盒说明书进行HBV DNA提取,浓度分别为1.8×103、2.3×103、1.7×103、1.1×102、3.5×102copies/μL。同时对已知为HCV、HDV、HIV阳性的临床样本(各5例)进行核酸提取后逆转录为cDNA,均对其进行ddPCR检测。
1.8重复性试验 选择低拷贝数的HBV阳性对照质粒(1×102、1×101、1×100copies/μL)进行ddPCR重复性检测。每一样品均重复检测3次,统计检测结果并计算变异系数(coefficients of variation,CV)。
1.9临床样本的检测 按照病毒基因组 DNA/RNA提取试剂盒说明书进行HBV DNA提取。采用ddPCR法对纳入研究的19例乙型肝炎低病毒血症患者的临床样本进行检测和结果分析。
2 结果
2.1标准曲线和检出限分析 ddPCR检测梯度稀释阳性对照质粒的结果见图1,线性范围在1×105~1×100copies/μL且检出限低至1 copy/μL(阳性质粒稀释法)。阳性对照质粒浓度与ddPCR检测结果浓度取对数作标准曲线,如图2所示,线性方程为y=1.039 2x+0.099 5(y为质粒浓度转换为log10,x为检测浓度转换为log10),R2值为0.999 5。
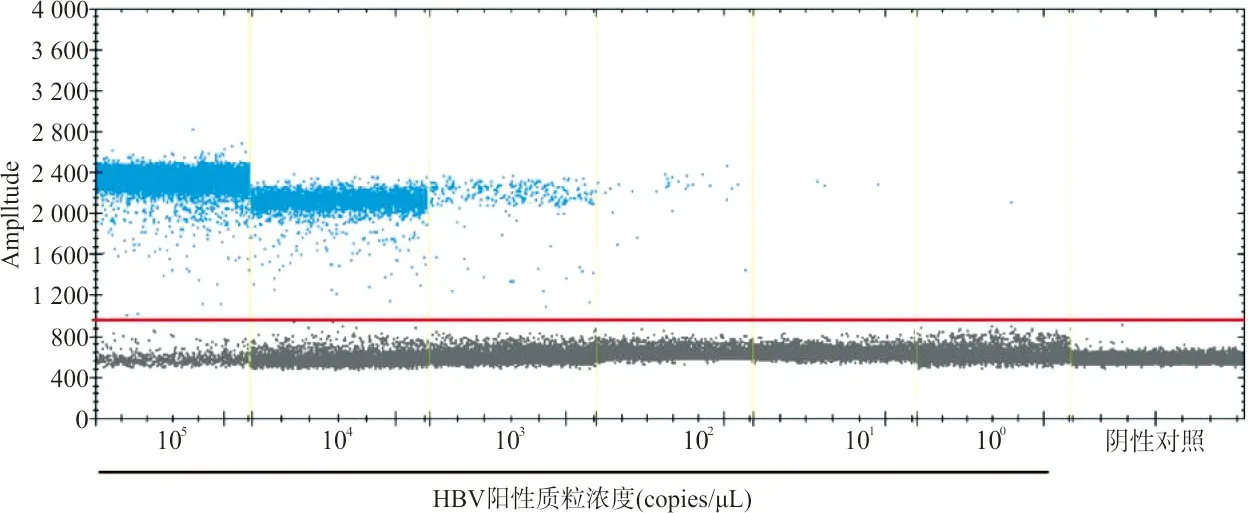
注:蓝色点代表阳性信号;红线代表阳性阈值判断。

图2 ddPCR检测阳性对照质粒标准曲线
2.2特异性分析 对已知为HBV阳性的临床样本进行ddPCR检测,结果均为阳性。同时对已知为HCV、HDV和HIV患者的临床样本进行核酸提取逆转录后的ddPCR检测,结果均为阴性,见图3。
2.3重复性分析 对低拷贝数的HBV阳性对照质粒1×102、1×101、1×100copies/μL进行ddPCR重复性检测,结果见表1,计算各自CV值分别为18.8%、9.9%、9.7%。
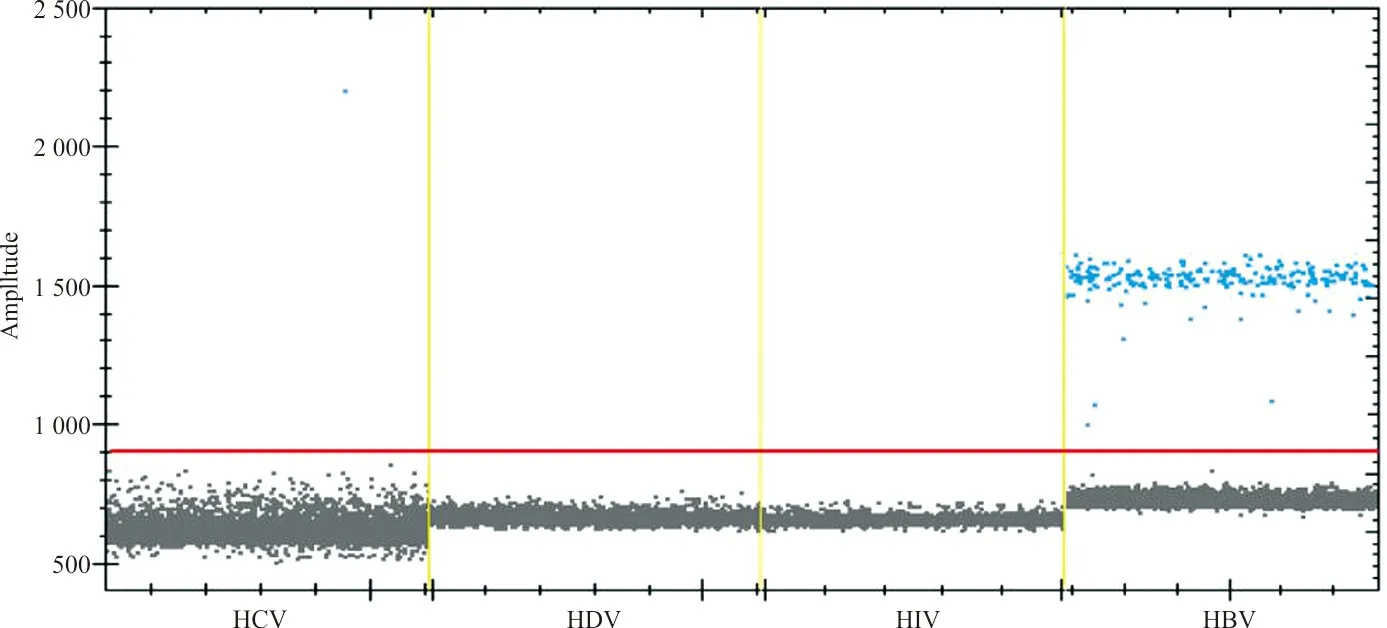
注:蓝色点代表阳性信号;红线代表阳性阈值判断。

表1 低拷贝数HBV阳性对照质粒重复性试验结果
2.4乙型肝炎低病毒血症患者HBV DNA临床样本的检测 采用ddPCR法对纳入研究的19例乙型肝炎低病毒血症患者的临床样本进行绝对定量检测,结果见图4。在低于qRT-PCR检测下限乙型肝炎低病毒血症患者血浆中均检测出一定量的HBV DNA,若以上述检出限结果1 copy/μL为临界值,19例乙型肝炎低病毒血症患者HBV DNA阳性13例,检出率为68.42%。
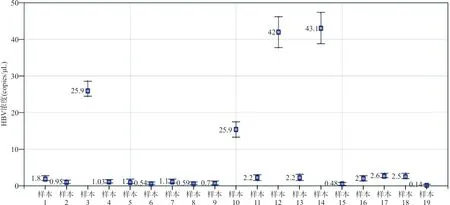
图4 乙型肝炎低病毒血症患者临床样本ddPCR检测结果
3 讨论
HBV DNA的定量检测在判断HBV的复制水平、传染性程度以及在评价抗病毒疗效等方面均有重要意义。但随着抗病毒药物的普遍推广和应用,长期进行抗病毒治疗的患者中往往存在低浓度的HBV DNA,病毒载量甚至低于现有检测方法的检出限[8]。与此同时,隐匿性感染者以及乙型肝炎低病毒血症患者数量不断上升,越来越多HBV感染患者体内存在不易检出的低浓度HBV DNA,这对输血、透析、移植等都造成严重的安全隐患[9-10]。近期有研究表明,低浓度的HBV DNA持续存在已经成为晚期肝病的独立危险因素[11]。
目前临床上常用的HBV DNA检测方法是qRT-PCR。而qRT-PCR定量是通过使用外标法来定量目标DNA的未知浓度,并获得循环定量(CQ)值。CQ值根据阈值设置的不同而不同,有主观或经验性,并且CQ值不能提供精确的临界值[12]。此外,qRT-PCR在HBV DNA拷贝数差异不大的样本中很难区分,特别是在拷贝数低的样本中,缺乏一定精确性[13]。因此,急需探寻一种灵敏度更高的技术来满足低病毒量的定量检测。
ddPCR作为新一代的PCR技术,是一种以核酸扩增为基础对目标核酸进行不依赖标准品和标准曲线的绝对定量分析技术[14]。其与需要标准曲线的qRT-PCR不同,ddPCR提供了绝对结果。通过对样品的微滴化处理将含有核酸分子的反应体系分成成千上万个纳升级的微滴,其中每个微滴不含或者含有一个至数个靶分子。经PCR扩增后,对微滴逐个进行检测,根据泊松分布原理及阳性微滴的个数与比例即可得出靶分子的起始拷贝数或浓度。目前ddPCR已经被用于多种临床样本及多种病原体的多样化检测[15-17]。在HBV检测方面,也利用其高灵敏的特点应用于长期抗病毒治疗患者的HBV DNA分析[18]。尽管如此,ddPCR针对HBV DNA的检测研究还是相对缺乏。
本研究首先评估了ddPCR对HBV DNA绝对定量的能力,对构建的阳性对照质粒的检测在具有较高的拟合优度(R2=0.999 5)的同时具有较高准确度和特异性,证明其可以成为一般病毒学研究可靠、准确和灵敏的工具。在方法的建立中,通过对HBV阳性质粒梯度稀释得到ddPCR检测HBV DNA的检出限低至1 copy/μL,但该检出限有待进一步的研究和验证。在ddPCR检测梯度稀释的HBV阳性质粒过程中,当模板量大于105copies/μL时检测结果的实际值偏离理论值(该部分结果未展示),这可能是由于高目标浓度下的液滴饱和度使泊松统计量失效所造成[19],进一步说明ddPCR更适用于低病毒载量的检测。对低于临床检出限的乙型肝炎低病毒血症患者HBV DNA绝对定量后发现,均检测出一定量的HBV DNA。当以1 copy/μL为临界值,患者HBV DNA的检出率为68.42%,且这一数值极有可能随着标本基数的增加而增加。由此可见,在隐匿性感染或HBsAg血清学转换这类乙型肝炎低病毒血症患者中,仍存在一定量的HBV DNA,这为部分患者发生病毒学突破提供了有力的理论支撑。
总之,本研究建立并评估了ddPCR检测低病毒载量HBV DNA的方法,其能够高准确、高灵敏和高特异地对乙型肝炎低病毒血症患者HBV DNA实现绝对定量。这将有助于开展乙肝精准抗病毒治疗,保证乙肝低病毒血症治疗的安全有效。
