五种抗菌药物对革兰阴性菌体外抗菌活性比较*
2022-03-28王雪婷嵇金如应超群刘志盈王培培陈云波沈萍肖永红
王雪婷,嵇金如,应超群,刘志盈,王培培,陈云波,沈萍,肖永红
(浙江大学医学院附属第一医院传染病诊治国家重点实验室、国家感染性疾病临床医学研究中心、感染性疾病诊治协同创新中心,杭州 310003)
革兰阴性菌血流感染是临床最常见的血流感染类型,近年来,全球革兰阴性菌血流感染的发病率呈上升趋势,其中大肠埃希菌、肺炎克雷伯菌、铜绿假单胞菌以及鲍曼不动杆菌为主要致病菌[1]。在我国,上述细菌同样为主要的致病革兰阴性菌。2014—2019年全国血流感染细菌耐药监测报告(BRICS)显示,碳青霉烯耐药肺炎克雷伯菌从7.2%上升至20.6%,碳青霉烯耐药铜绿假单胞菌(carbapenem-resistant pseudomonas aeruginosa,CRPA)从10.4%上升至18.8%,碳青霉烯耐药鲍曼不动杆菌(carbapenem-resistant acinetobacter baumannii,CRAB)一直处于40%左右甚至更高水平。产超广谱β-内酰胺酶(extended-spectrum β-lactamase,ESBL)大肠埃希菌、肺炎克雷伯菌作为重要的多重耐药菌检出率则呈轻微下降趋势,2019年度检出率分别为49.7%,19.6%[2-3]。寻找合适而有效的抗菌药物成为当前的难题,β-内酰胺类/β-内酰胺酶抑制剂复方制剂通过抑制超广谱β-内酰胺酶活性恢复细菌对β-内酰胺类抗菌药物的敏感性,临床常用药物包括头孢哌酮/舒巴坦、哌拉西林/他唑巴坦、哌拉西林/舒巴坦,是我国医保目录产品,常用于治疗各种革兰阴性菌引起的中重度感染。同时各种复方制剂由于其配伍情况差异,体外抗菌作用存在一定差异。本研究比较了哌拉西林、哌拉西林/他唑巴坦(他唑巴坦固定浓度4 mg·L-1)、哌拉西林/舒巴坦(2:1和4:1)以及头孢哌酮/舒巴坦(2:1)对肠杆菌科细菌、鲍曼不动杆菌和铜绿假单胞菌的体外抗菌活性,从而为临床用药提供一定的参考。
1 材料与方法
1.1实验材料
1.1.1菌株 实验菌株为2018—2019年BRICS收集的肠杆菌科细菌(非碳青霉烯类耐药菌株)5664株(其中大肠埃希菌3621株,肺炎克雷伯菌1328株,阴沟肠杆菌249株)、鲍曼不动杆菌292株(非碳青霉烯耐药菌116株)以及铜绿假单胞菌363株(非碳青霉烯耐药菌280株)。全部菌株来源于临床血培养。质控菌株为大肠埃希菌ATCC 25922,为本实验室保存菌株。
1.1.2抗菌药物及培养基 头孢哌酮(效价:99%,批号:130420-201105,购于中国食品药品生物制品检定院),哌拉西林(效价:95%,批号:P1200717,购于苏州二叶制药有限公司),他唑巴坦(效价:95%,批号:03191203,购于山东二叶制药有限公司),舒巴坦(效价:91%,批号:03191203,购于山东二叶制药有限公司)。Mueller-Hinton琼脂(MHA),购于英国OXOID公司,批号:2989738。
1.2实验方法
1.2.1产ESBL菌株的确定 应用美国临床与实验室标准研究所(CLSI)推荐的纸片扩散法进行细菌产ESBL的确定。头孢他啶与头孢他啶/克拉维酸两者抑菌圈相比增加≥5 mm时,判定为产ESBL。
1.2.2最低抑菌浓度测定 应用CLSI推荐琼脂二倍稀释法测定哌拉西林、哌拉西林/他唑巴坦、哌拉西林/舒巴坦(2:1和4:1)及头孢哌酮/舒巴坦(2:1)对实验菌株的最低抑菌浓度(minimum inhibition concentration,MIC)。含舒巴坦复方制剂按照比例配制,哌拉西林及其复方制剂中起始浓度256 mg·L-1,最低浓度0.5 mg·L-1;头孢哌酮起始浓度128 mg·L-1,最低浓度0.125 mg·L-1;他唑巴坦固定浓度4 mg·L-1。而后进行倍比稀释,将倍比稀释后不同浓度的抗菌药物与加热溶解后的MH琼脂混匀制成含药琼脂平板。从孵育了16~20 h新鲜培养物的平板上,用一次性无菌接种环挑取菌落,混悬于无菌0.9%氯化钠溶液中制成浓度相当于0.5麦氏单位浊度的菌悬液,再以1:10稀释后以多点接种仪(日本SAKUMA公司)接种于含药琼脂平板上,每个接种点细菌量约为104CFU,接种后于35~37 ℃培养箱内培养16~20 h,判读结果。将平板置于黑色、无反光物体上读取结果,以抑制细菌生长的最低药物浓度为MIC。
1.3结果统计 以抑制细菌生长的最低药物浓度为MIC,抑制50%细菌生长的最低药物浓度为MIC50,抑制90%细菌生长的最低药物浓度为MIC90;统计各种药物对实验菌株的MIC范围、MIC50和MIC90;按照CLSI折点标准计算敏感/耐药率,比较各种抗菌药物的体外抗菌活性;哌拉西林/舒巴坦对肠杆菌科细菌折点参考哌拉西林标准,含舒巴坦的复方制剂对鲍曼不动杆菌敏感性折点参照氨苄西林/舒巴坦复方中舒巴坦的标准,敏感、中介和耐药分别设定为≤ 4,8和≥16 mg·L-1。头孢哌酮/舒巴坦对肠杆菌、铜绿假单胞菌的折点标准参考药品说明书,敏感、中介和耐药分别为头孢哌酮≤16,32和≥64 mg·L-1[4]。
2 结果
2.1临床菌株的5种抗菌药物MIC值及敏感性比较 对肠杆菌科细菌,β-内酰胺酶抑制剂复方制剂的体外抗菌活性均优于哌拉西林单药,哌拉西林/他唑巴坦、哌拉西林/舒巴坦2:1和4:1的MIC90均为64 mg·L-1(以哌拉西林浓度计),较哌拉西林的MIC90降低3个浓度梯度。其中哌拉西林/舒巴坦2:1活性优于4:1,敏感率分别为79.3%,67.5%。头孢哌酮/舒巴坦的MIC90为32/16 mg·L-1,敏感率为85.9%。各肠杆菌科细菌对5种抗菌药物的MIC详见表1。
哌拉西林/他唑巴坦、头孢哌酮/舒巴坦、哌拉西林舒巴坦(2:1)对产ESBLs大肠埃希菌具有较强的体外抗菌活性,MIC90分别为128/4,64/32和64/32 mg·L-1,敏感率分别为75.9%,72.1%和66.2%。对产ESBLs肺炎克雷伯菌,β-内酰胺酶抑制剂复方制剂体外抗菌活性欠佳,敏感率均低于50%。
对于其他肠杆菌(除沙门菌属外),哌拉西林具有一定的抗菌活性,敏感率均高于50%。对阴沟肠杆菌复合体、产气肠杆菌、沙门菌属、沙雷菌属及变形杆菌属,4种β-内酰胺酶抑制剂复方制剂均具有强大的体外抗菌活性,尤其对沙雷菌属和变形杆菌属,4种复方制剂的敏感性均高于90%。
对碳青霉烯类耐药鲍曼不动杆菌(carbapenem-resistance acinetobacter baumannii,CRAB),5种抗菌药物抗菌活性不佳。对非CRAB,头孢哌酮/舒巴坦及哌拉西林/舒巴坦2:1和4:1的体外抗菌活性较强,MIC90分别为16/8、16/8和32/8 mg·L-1,敏感率分别为76.7%、82.8%和83.6%,其中哌拉西林/舒巴坦2:1和4:1的体外抗菌活性相似(表1)。哌拉西林复方制剂对铜绿假单胞菌具有良好抗菌活性,对非碳青霉烯耐药铜绿假单胞菌,4种复方制剂敏感率菌超过90%,头孢哌酮/舒巴坦、哌拉西林/舒巴坦2:1和4:1的活性相似,MIC90为16/8、16/8和16/4 mg·L-1,敏感性分别为91.8%、93.9%和92.5%(表1)。
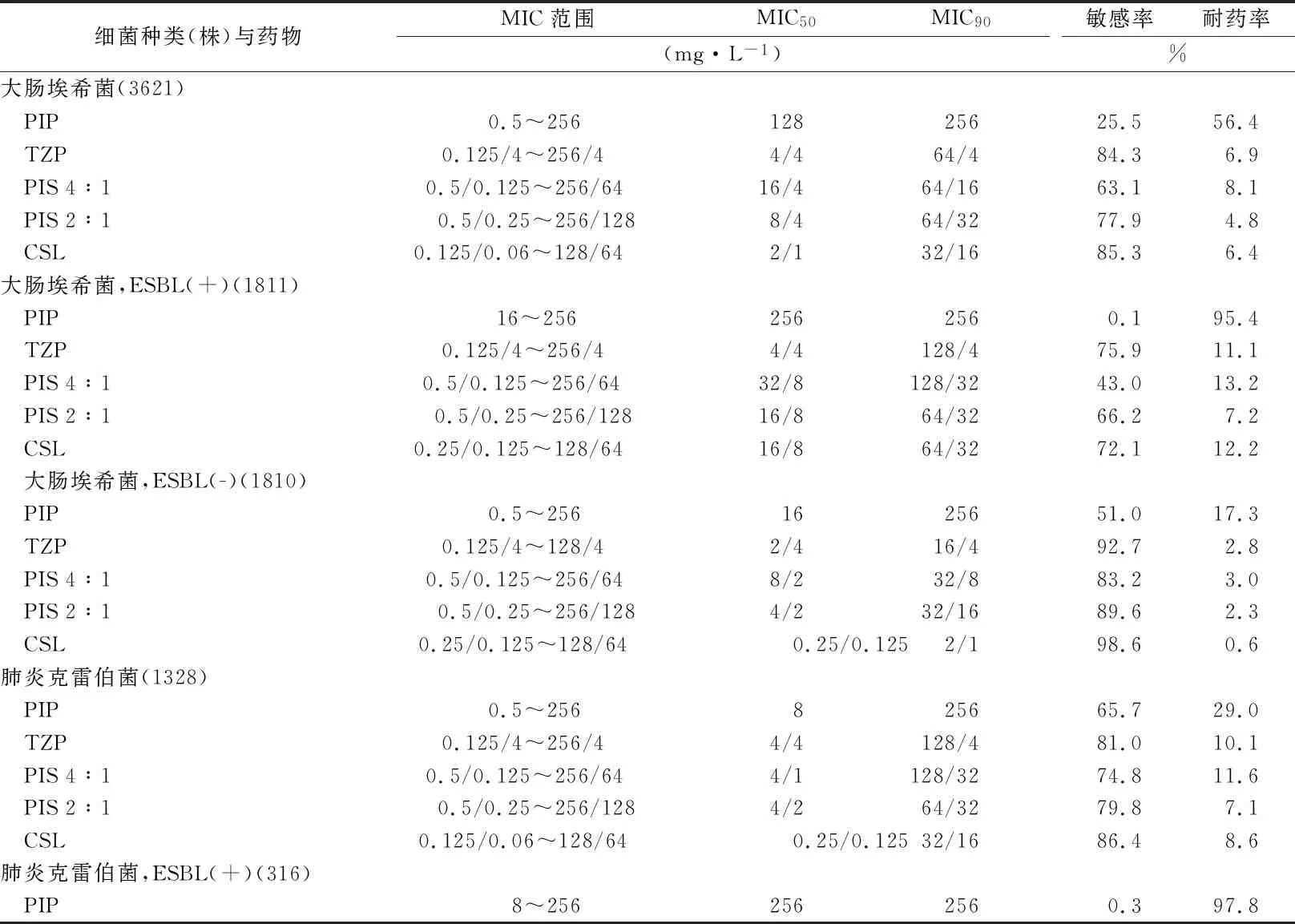
表1 5种抗菌药物对革兰阴性菌体外抗菌活性比较Tab.1 Comparison of in vitro antibacterial activity of five antibiotics against Gram-negative bacteria
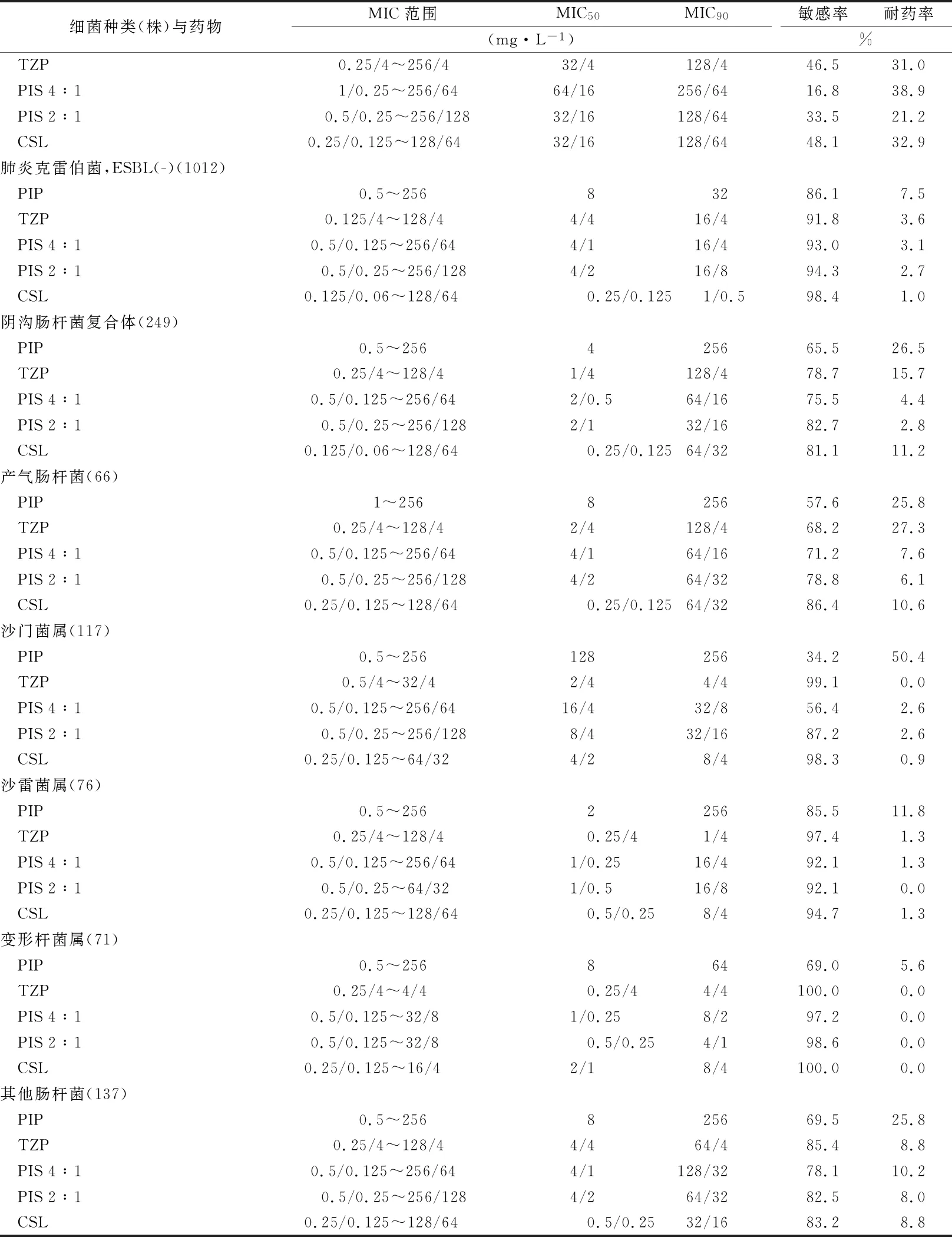
续表1 5种抗菌药物对革兰阴性菌体外抗菌活性比较Tab.1 Comparison of in vitro antibacterial activity of five antibiotics against Gram-negative bacteria
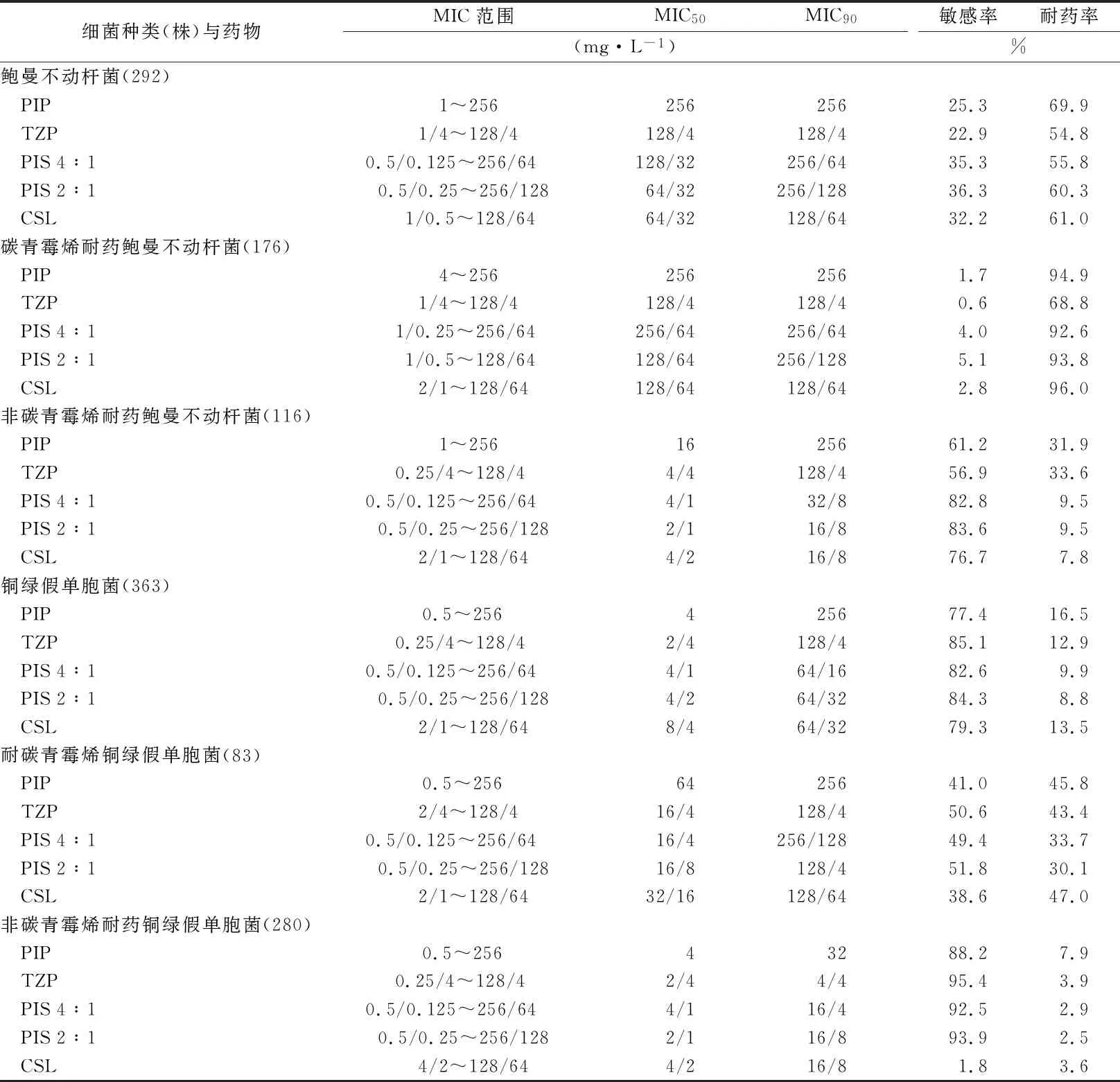
续表1 5种抗菌药物对革兰阴性菌体外抗菌活性比较Tab.1 Comparison of in vitro antibacterial activity of five antibiotics against Gram-negative bacteria
2.25种抗菌药物对主要细菌的累计抑菌百分率曲线 对肠杆菌,4种β-内酰胺酶抑制剂复方制剂累积抑菌百分率曲线较哌拉西林左移,其趋势相似,哌拉西林/舒巴坦(2:1,4:1)和哌拉西林/他唑巴坦MIC90相近(图1)。

PIP.哌拉西林;PIS.哌拉西林/舒巴坦;TZP.哌拉西林/他唑巴坦;CSL.头孢哌酮/舒巴坦。图1 5种抗菌药物对肠杆菌的累积抑菌率曲线PIP.Piperacillin;PIS.Piperacillin/Sulbactam;TZP.Piperacillin/Tazobactam;CSL.Cefoperazone/Sulbactam.Fig.1 Cumulative inhibition rate curves of five antibiotics against Enterobacteriaceae
对大肠埃希菌,4种β-内酰胺酶抑制剂复方制剂的累积抑菌百分率曲线较哌拉西林明显左移。对产ESBLs大肠埃希菌,哌拉西林/他唑巴坦、头孢哌酮/舒巴坦、哌拉西林/舒巴坦2:1的累积抑菌百分率曲线相近。对不产ESBLs大肠埃希菌,哌拉西林/他唑巴坦、哌拉西林/舒巴坦2:1和4:1三者曲线相近,头孢哌酮/舒巴坦的累计抑菌百分率曲线较另三种β-内酰胺酶抑制剂复方制剂左移(图2)。
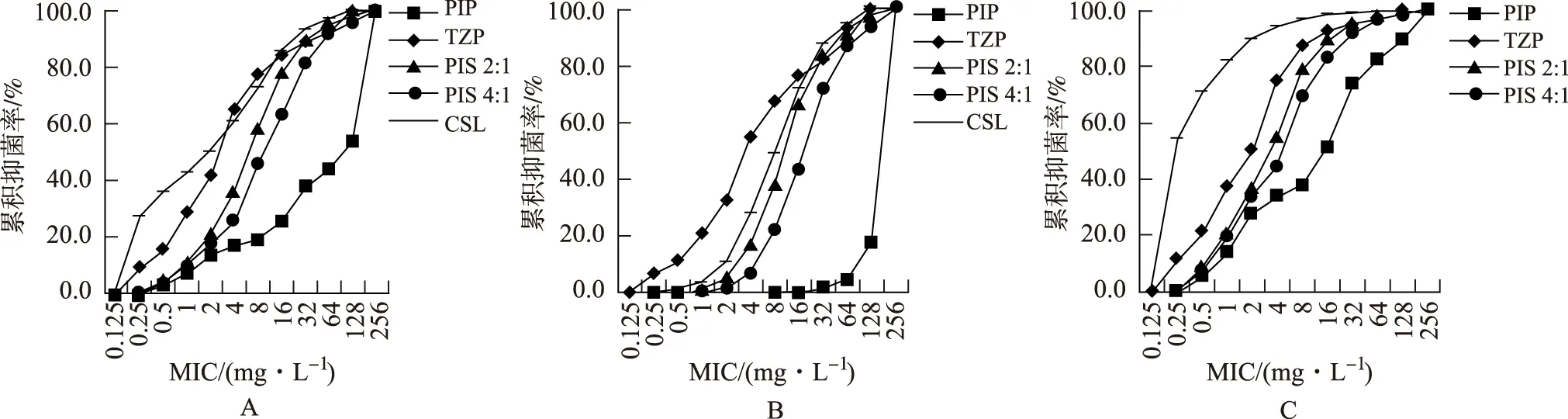
PIP.哌拉西林;PIS.哌拉西林/舒巴坦;TZP.哌拉西林/他唑巴坦;CSL.头孢哌酮/舒巴坦。图2 5种抗菌药物对大肠埃希菌(A)、产ESBLs大肠埃希菌(B)和不产ESBLs大肠埃希菌(C)的累积抑菌率曲线PIP.Piperacillin;PIS.Piperacillin/Sulbactam;TZP.Piperacillin/Tazobactam;CSL.Cefoperazone/Sulbactam.Fig.2 Cumulative inhibition rate curves of five antibacterial agents against E.coli(A),ESBL-producing E.coli (B)and non-ESBL-producing E.coli(C)
对肺炎克雷伯菌,4种β-内酰胺酶抑制剂复方制剂较哌拉西林曲线左移。对产ESBLs肺炎克雷伯菌,3种含舒巴坦复方制剂较哌拉西林/他唑巴坦累积抑菌百分率曲线左移,但增效作用不明显。对不产ESBLs肺炎克雷伯菌,哌拉西林/他唑巴坦、哌拉西林/舒巴坦2:1和4:1的累积抑菌百分率曲线存在相近,头孢哌酮/舒巴坦相对于前三者的累积抑菌百分率曲线左移(图3)。

PIP.哌拉西林;PIS.哌拉西林/舒巴坦;TZP.哌拉西林/他唑巴坦;CSL.头孢哌酮/舒巴坦。图3 5种抗菌药物对肺炎克雷伯(A)、产ESBLs肺炎克雷伯菌(B)和不产ESBLs肺炎克雷伯菌(C)的累积抑菌率曲线PIP.Piperacillin;PIS.Piperacillin/Sulbactam;TZP.Piperacillin/Tazobactam;CSL.Cefoperazone/Sulbactam.Fig.3 Cumulative inhibition rate curves of five antibacterial agents against K.pneumoniae (A), ESBL-producing K.pneumoniae (B) and non-ESBL-producing K.pneumoniae (C)
对非碳青霉烯耐药鲍曼不动杆菌,头孢哌酮/舒巴坦及哌拉西林/舒巴坦较哌拉西林累积抑菌百分率曲线左移,哌拉西林/他唑巴坦累积抑菌百分率曲线与哌拉西林相近(图4)。对铜绿假单胞菌及非碳青霉烯耐药铜绿假单胞菌,5种抗菌药物累积抑菌百分率曲线均相近(图5)。

PIP.哌拉西林;PIS.哌拉西林/舒巴坦;TZP.哌拉西林/他唑巴坦;CSL.头孢哌酮/舒巴坦。图4 5种抗菌药物对鲍曼不动杆菌(A)和非碳青霉烯耐药鲍曼不动杆菌(B)的累积抑菌率曲线PIP.Piperacillin;PIS.Piperacillin/Sulbactam;TZP.Piperacillin/Tazobactam;CSL.Cefoperazone/Sulbactam.Fig.4 Cumulative inhibition rate curves of antibacterial agents against A.baumannii(A)and non-carbapenem-resistant A.baumannii(B)
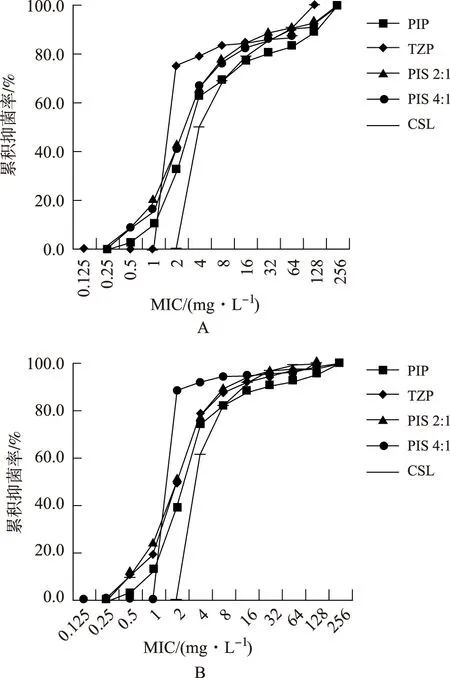
PIP.哌拉西林;PIS.哌拉西林/舒巴坦;TZP.哌拉西林/他唑巴坦;CSL.头孢哌酮/舒巴坦。图5 5种抗菌药物对铜绿假单胞菌(A)和非碳青霉烯耐药铜绿假单胞菌(B)的累积抑菌率曲线PIP.Piperacillin;PIS.Piperacillin/Sulbactam;TZP.Piperacillin/Tazobactam;CSL.Cefoperazone/Sulbactam.Fig.5 Cumulative inhibition rate curves of antibacterial agents against P.aeruginosa(A) and non-carbapenem-resistant P.aeruginosa (B)
3 讨论
产ESBLs肠杆菌科是临床常见病原体。目前,碳青霉烯类抗生素是治疗产ESBLs肠杆菌感染的主要药物,但广泛使用可能导致碳青霉烯类抗生素耐药性的产生及迅速传播。将β-内酰胺酶抑制剂复方制剂作为产ESBLs肠杆菌科细菌感染的治疗选择,可以减缓碳青霉烯类单一使用可能导致的耐药选择性压力。本研究发现头孢哌酮/舒巴坦、哌拉西林/他唑巴坦、哌拉西林/舒巴坦(2:1)对ESBLs大肠埃希菌的活性良好。4种β-内酰胺酶抑制剂复方制剂对产ESBLs肺炎克雷伯菌的抗菌活性明显弱于产ESBLs大肠埃希菌,这可能与产ESBLs肺炎克雷伯菌同时合并其他耐药机制有关。关于β-内酰胺酶抑制剂复方制剂与碳青霉烯类治疗感染的疗效具有争议[5-7],但一项Meta分析发现,在治疗产ESBLs肠杆菌科细菌引起的血流感染时,哌拉西林/他唑巴坦等β-内酰胺酶抑制剂复方制剂与碳青霉烯类在30 d全因死亡率方面不具有显著差异[8]。
含舒巴坦复方制剂对非CRAB展现出很强的活性,哌拉西林/舒巴坦2:1和4:1两者体外抗菌活性相似,此与舒巴坦的抗菌活性有关。舒巴坦对鲍曼不动杆菌抗菌活性主要归因于其内在活性,通过结合鲍曼不动杆菌的青霉素结合蛋白2发挥作用[9]。与此前研究相似,包括哌拉西林在内的各抗菌药物对铜绿假单胞菌展现出较强的活性[10-12]。一项回顾性研究表明,β-内酰胺酶抑制剂复方制剂治疗铜绿假单胞菌引起的血流感染的疗效不逊于碳青霉烯类药物,并且使用复方制剂可减少CRPA的产生[13]。因此,在体外敏感的前提下,β-内酰胺酶抑制剂复方制剂也许可作为治疗铜绿假单胞菌感染的一个选择。
体外抗菌活性对抗菌药物选择具有参考价值,但临床用药还需要依据药动学/药效学(PK/PD)研究结果。哌拉西林与他唑巴坦体内具有相似代谢过程,蛋白结合率相似,分别为20%~30%和20%~23%;半衰期分别为1.17 h和1.81 h[14],并且输注方法对哌拉西林和他唑巴坦药动学无影响。目前,临床上常用的给药方式为哌拉西林/他唑巴坦4.5 g(8:1)每8小时给药一次,每次静脉输注30 min,对于目标细菌感染能获得有效的PK/PD目标值。
哌拉西林和舒巴坦在人体内分布、代谢、排泄基本保持同步。健康受试者静滴哌拉西林/舒巴坦6.0 g(2:1)后,两者血药峰浓度(Cmax)分别为 (420.4±266.3) mg·L-1和(139.1±104.6) mg·L-1;AUC分别为 (473.6±187.0) mg·h·L-1和(152.63±66.8) mg·h·L-1;消除半率期分别为(1.04±0.10) h和(1.28±0.38) h[15]。药物主要通过肾脏排泄,用药后8 h内47.5%~85.5%的哌拉西林以原型自尿中排出;50.1%~100.0% 的舒巴坦经尿排出[15]。根据上述研究结果,临床上常用给药剂量为哌拉西林/舒巴坦1.5 g(2:1)或3.0 g,q12h,对于严重感染者,剂量可增加至6.0 g。此前有临床研究表明注射用哌拉西林/舒巴坦(2:1)与哌拉西林/他唑巴坦(8:1)对照治疗呼吸和泌尿系统中、重度细菌性感染疗效相当[16];作为国产酶抑制剂复方,值得进一步开展临床应用研究。
本研究表明,4种β-内酰胺酶抑制剂复方制剂对产ESBLs大肠埃希菌具有突出抗菌活性,头孢哌酮/舒巴坦及哌拉西林/舒巴坦(2:1)对非CRAB和CRPA具有较强抗菌活性;对肠杆菌科细菌,哌拉西林/舒巴坦(2:1)的体外抗菌活性优于哌拉西林/舒巴坦(4:1),对鲍曼不动杆菌及铜绿假单胞菌,两者活性相似。有必要进行深入PK/PD和临床研究,为感染治疗药物选择提供支持。
