生物质纤维医用敷料研究进展
2022-03-28刘方恬曹孟杰崔金海邓红兵
吴 洋, 刘方恬, 曹孟杰, 崔金海, 邓红兵
(1. 武汉大学 资源与环境科学学院, 湖北 武汉 430079; 2. 武汉大学 生物质资源化学与环境生物技术 湖北省重点实验室, 湖北 武汉 430079; 3. 奥美医疗用品股份有限公司, 湖北 宜昌 443200)
在全球范围内,急性和慢性伤口,如烧伤和糖尿病溃疡,对患者和医疗保健系统造成了巨大的负担[1-2]。针对该问题,目前研究人员正在进行广泛的研究以开发能够在短时间内有效治疗伤口的技术。适当的治疗策略包括使用愈合率高的医用敷料,既可以阻碍感染、防止不良结果产生,还可以降低成本。通常,急性伤口是一种皮肤损伤,指在一个可预测的时间范围内能完全愈合的敞口,这取决于伤口的深度、大小和损伤的程度;与之相对的慢性伤口则是皮肤损伤不能及时愈合,并可能有复发的风险[3-4]。因此,不同伤口对医用敷料的需求不同,选择适应于特定类型伤口的材料对伤口愈合至关重要。
到目前为止,已经开发了多种医用敷料用于治疗不同种类的伤口,根据其形式可以分为纱布、水凝胶、海绵、纳米纤维膜等[5]。其中,纤维类医用敷料可以减轻疼痛感,促进伤口愈合,在治疗慢性伤口方面十分有优势[6]。纳米纤维作为一种相对较新的医用敷料材料,正受到越来越多的关注[7-8]。纳米纤维网由许多小到几微米或几百纳米的纳米纤维交叉组成,提供了相对较大的接触表面积和微纳米孔,该结构可以模拟细胞外基质结构,增强伤口上细胞的黏附和爬行,促进细胞生长[8]。从组分上看,天然聚合物和合成聚合物均可用于制备医用敷料,而天然聚合物因其生物相容性、生物降解性、高仿生水平和物理化学性质而被广泛应用于医用敷料[9]。特别是基于天然聚合物的医用敷料,其降解速率可以与伤口愈合过程同步,确保了活性物质的有效释放,避免了伤口的二次伤害。目前已研究的作为医用敷料的天然聚合物材料包括海藻酸钠、透明质酸、甲壳素、壳聚糖、卡拉胶、纤维素、果胶、淀粉、胶原蛋白等[10-13]。
理想的医用敷料要具有良好的生物相容性和抗菌性,较高的渗液管理能力、透气性及有效的屏障功能[14]。生物质纤维敷料具有高孔隙率和可控的孔径尺寸,可保证良好的透气性,且与天然细胞外基质高度相似,有利于细胞的爬行和黏附[15]。生物质纤维形貌及其集合体结构还赋予敷料良好的阻隔性和多功能性,其可负载多种活性成分,增加抗菌性能,提升舒适度[5,16-17]。由此可见,生物质纤维有应用于理想医用敷料的巨大潜力,亟需对其进行系统地分析和讨论,促进该领域的进一步发展。
本文旨在简要介绍生物质纤维伤口敷料的研究进展,对来源于生物质的不同原料如甲壳素/壳聚糖、纤维素、胶原蛋白、丝素蛋白、海藻酸、透明质酸及其衍生物的纤维制备方式进行讨论;并对目前文献报道的生物质纤维敷料的功能性应用进行综述,为医用敷料的发展提供参考。
1 用于医用敷料的生物质纤维的制备
1.1 壳聚糖/甲壳素
甲壳素是自然界中唯一带正电的生物质碱性多糖,常见于甲壳类、真菌类动物中,如虾蟹壳、昆虫外壳以及真菌细胞壁等,是世界第二大生物质资源[18]。制备甲壳素纤维用于医用敷料的研究已有不少报道,常见的制备方法包括湿法纺丝、干法纺丝、静电纺丝、干喷-湿法纺丝、液晶纺丝、发酵法等(见图1)[19-20]。其中:湿法纺丝最为常见;由液晶纺丝和干喷-湿法纺丝制备的纤维强度较好;由熔融纺丝得到的纤维结构均匀致密。采用不同方法得到的纤维各有优势,可依据实际需求选用[21]。例如,Huang等[22]通过湿法纺丝制备了纯甲壳素纤维,并通过丙酮处理及热压湿纤维制备了甲壳素非织造布,其纤维结合紧密,纤维直径大约为40 μm。
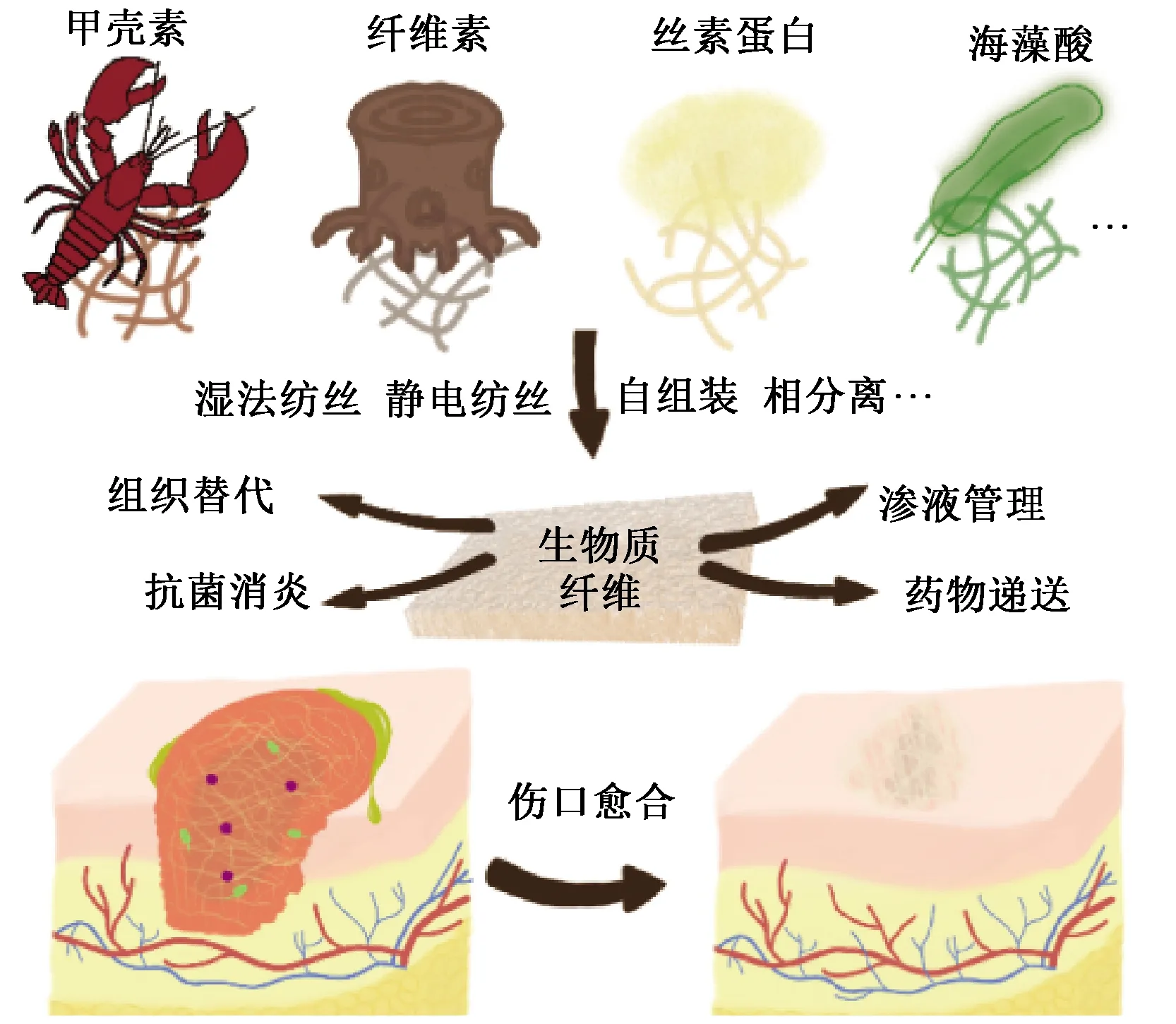
图1 生物质纤维敷料的制备和应用Fig.1 Preparation and application of biomass fiber medical dressings
壳聚糖为甲壳素的脱乙酰衍生物,其生物相容性好,可与细胞表面负电基团发生非特异性吸附,还可阻断神经末梢从而减轻疼痛;其生物可降解性良好,在人体内能很好地被代谢吸收,当其缓慢解聚时,可释放出N-乙酰-β-D-葡糖胺,刺激成纤维细胞增殖,利于胶原沉积和天然透明质酸合成,有助于促进伤口愈合[23]。已有研究证明,壳聚糖纤维敷料相较于海绵敷料和膜敷料表现出更好的细胞附着力、增殖力和生物相容性,可作为促进伤口愈合的理想材料[24]。壳聚糖可溶解在浓醋酸中制备得到纳米级纤维。然而,制备的纯壳聚糖纤维强度通常不佳,影响其应用,将壳聚糖与其他生物可降解性和生物相容性良好的聚合物混合可以提高力学强度,同时保持良好的生物相容性[25]。Wang等[26]将壳聚糖、聚乙烯醇和铜金属有机框架结合,有效地发挥了不同材料的抗菌性、力学性能、生物相容性,制备出拥有良好物理性能和抗菌性能的功能医用敷料,纤维直径大约为400 nm,拉伸强度可达4.5 MPa。
1.2 纤维素
纤维素是自然界储量最丰富的生物质,在木材、棉花、秸秆等农作物以及细菌、藻类中均有存在。纤维素纤维可以促进组织再生,对感染的伤口比较有效[27]。木材基纤维素纳米原纤维敷料可较好地附着在伤口上,不会引发过敏或炎症反应,在治疗烧伤病人伤口方面具有很好的效果[28]。细菌纤维素生物相容性好,其三维结构纤维材料不仅可以作为载药载体,还能保持高孔隙率,负载抗菌消炎物质后还可加速伤口愈合[29]。醋酸纤维素也有助于细菌性伤口愈合,且其强度、稳定性高[30]。
使用静电纺丝技术是制备纤维素纳米纤维较为常见的手段,还可通过调节工艺参数制备可控的多孔结构,且热稳定性好,还易于被化学改性,但力学性能较差[31],可通过混合其他原料改善这一缺陷,提高复合材料的力学性能。例如:醋酸纤维素与明胶混合模仿正常皮肤的形态和结构特征,有利于细胞增殖,并具有良好的生物相容性[32];将聚己内酯和醋酸纤维素共混,通过静电纺丝制备纤维,同时将壳聚糖和胶原蛋白自组装于纤维表面,所制纤维的平均直径约为500 nm,拉伸强度可达7.95 MPa[33]。
总之,纤维素纤维因其良好的生物相容性和适应性十分适合用于医用敷料制备,其在传统医用敷料中占有主要地位,应用也相当广泛,未来新型的纤维素纤维还将在医用敷料领域发挥更大的作用。
1.3 胶原蛋白
胶原蛋白是构成细胞外基质的主要物质,其生物相容性好,可被机体降解吸收,同时为创面修复提供支持[34],在伤口愈合期间可以减少过多的蛋白酶活动,帮助伤口愈合[35],有利于细胞的爬行和增殖。胶原蛋白是哺乳动物体内含量最多、分布最广的一类蛋白,且与组织器官功能联系紧密[36]。
目前胶原蛋白纤维的制备方式较单一,常用技术为静电纺丝技术。例如,以六氟异丙醇为溶剂制备聚乳酸-聚乙二醇/胶原蛋白纳米纤维,其纤维平均直径为250 nm,拥有较高的孔隙率[37]。但胶原蛋白自身的降解速度快,强度低[38],需要进一步处理,较为常用的方法是制备复合纤维。将聚己内酯和胶原蛋白静电纺丝,制备的复合纤维可负载肠杆菌噬菌体T4,具有很好的拉伸强度[39]。此外,还可通过交联弥补这一不足,常使用的交联剂包括化学交联剂戊二醛、植物化合物种子多糖及肉桂等[40]。胶原蛋白还具有一定的免疫原性,可以通过使用戊二醛等阻断其具有抗原性的侧基、将胶原蛋白制成明胶使蛋白质分子分解为肽、去除芳香族自由基等方式降低其免疫原性[1]。
1.4 丝素蛋白
丝素蛋白,主要由非极性氨基酸组成,不溶于水,生物相容性好且无毒性,在体内外均表现出可促进细胞增殖分化的作用,有利于伤口创面的愈合。良好的可降解性、柔韧性及透水透气性使其具有作为医用敷料的天然优势[41],被广泛用于各种急性慢性伤口修复[12]。
虽然丝素蛋白在伤口创面修复中具有很大的潜力,但应用中仍存在很多问题。如静电纺丝时,溶解丝素蛋白的溶剂六氟异丙醇具有一定的毒性,且仅靠单一的丝素蛋白纤维难以满足创伤修复的要求,其抗菌性和本身力学性能也有待进一步加强[42]。目前常采用制备复合敷料的方法进行改进,以提高创伤修复效果,如双层纤维膜敷料、纤维凝胶复合敷料等[43]。
一般来说,丝素蛋白纤维可通过自组装、湿法纺丝、干法纺丝、静电纺丝等方法制备,较多的研究均集中在湿法纺丝和静电纺丝上。由静电纺丝制备的丝素纳米纤维医用敷料透气性良好,可促进伤口的愈合[44],但由静电纺丝制备的纤维通常是水溶性的,需要交联才可应用,且力学性能较差,而采用纤维层层自组装改性可以一定程度上提高丝素蛋白纤维的力学性能[45]。Zhang等[46]使用湿法纺丝制备了微米级多糖和丝素蛋白混合的纤维,多糖的羟基和丝素蛋白的氨基之间形成氢键,在具有良好生物相容性的同时还具有良好的力学性能,适于制备医用敷料。
总之,将丝素蛋白纤维有效处理,开发出高修复性、多功能化的医用敷料是未来的发展方向之一。然而还需要进一步探索丝素蛋白的作用机制,并有效解决创伤修复的安全性和普适性问题。
1.5 海藻酸
海藻酸纤维具有良好的吸湿性能[47],可有效吸收伤口渗液,保持适宜伤口愈合的环境,有效避免二次感染。海藻酸不溶于水,在一定程度上限制了其应用;但海藻酸盐是水溶性的,而且海藻酸盐纤维同样具有良好的液体吸收能力[48],因此,这类纤维受到了越来越多的关注,有望广泛应用于医用敷料领域。
有许多方法可用于制备海藻酸盐纤维,通过混纺,可强化材料的优良性能,弥补纤维自身的劣势。王建坤等[49]将海藻酸钙纤维与棉纤维混纺,有效提高了纤维的可纺性,解决了纺纱过程中海藻酸钙纤维抱合力弱的问题。房乾等[50]采用湿法纺丝将海藻酸盐制成纤维,然后通过针刺工艺制备海藻纤维/粘胶/涤纶纤网新型复合医用敷料,其具有高的液体吸收量和透湿量,可促进伤口愈合,并缓解敷料揭除时的疼痛感。
用湿法纺丝方法制备的海藻酸盐纤维的力学性能欠佳,但通过添加氧化石墨烯可明显提高纤维的强度[51],且对细胞无毒。静电纺丝也是制备海藻酸盐纤维的方法之一,海藻酸自身的可纺性欠佳,但可将具有良好可纺性的聚乙烯醇与具有良好吸湿性、生物相容性及止血功能的海藻酸钠纤维复合,制备出功能性医用敷料。该材料可以为细胞的生长提供良好的支持,且细胞的黏附和增殖情况良好,使伤口愈合期间的炎症反应有所减轻[52]。
1.6 透明质酸
透明质酸是一种天然非免疫性线性聚阴离子多糖,其生物相容性和在人体中的生物可降解性好,具有非免疫性、靶向性、高持水性和黏弹性,在生理条件下通常会以钠盐聚电解质形式存在。透明质酸广泛用于生物医药领域,其可以吸收伤口渗液,为细胞的爬行和迁移提供支持,在伤口愈合过程中,透明质酸可促进伤口再生,有利于皮肤修复重建[53]。
利用静电纺丝技术可将透明质酸制备成纤维形貌,有效发挥其促进细胞爬行迁移的优势,所得到的纳米级透明质酸纤维膜平均厚度为0.041 cm[54]。但单一透明质酸的自身稳定性差,限制了其进一步应用,且透明质酸溶于水时由于反离子的存在会导致其水溶液黏度增加,链缠结不充足,为确保稳定性,常溶解于有毒有机溶剂中。为解决这一问题,可通过添加聚乙烯醇和羟丙基-β-环糊精实现在水溶剂下制备[55]。将透明质酸与其他化合物混合,可提高材料的力学性能。将姜黄素、尿素、透明质酸混合通过静电纺丝技术制备纤维,其直径大约为298 nm,拓宽了透明质酸作为纤维在敷料方面的应用[56]。除静电纺丝外,通过逐层组装技术也可制备含有透明质酸的纤维医用敷料[57]。
2 生物质纤维医用敷料的功能化应用
2.1 抗菌消炎
伤口感染是阻碍伤口正常愈合过程的主要障碍之一,感染会延长炎症反应,阻碍再上皮化和胶原蛋白的合成,并延迟愈合过程,从而增加住院时间和治疗费用,而具有抗菌活性的医用敷料成为重要的解决途径。
壳聚糖/甲壳素类医用敷料因其良好的抗菌性能,在抗菌敷料领域一直受到研究人员的广泛关注[11,58-59]。随着科技的发展,甲壳素和壳聚糖微/纳米纤维的制备成为可能,赋予了其更广的应用空间,也有利于抗菌医用敷料的进一步发展[60]。Abdel-Mohsen等[61]从裂褶菌中提取了一种甲壳素/壳聚糖-葡聚糖的复合物,并将其溶解在预冷的碱尿素体系中,并通过干喷-湿法纺丝技术制备了非织造超细纤维膜。该纤维直径从几十微米到几百微米不等,与普通壳聚糖纤维相比,无需交联剂即可获得高孔径和孔隙率,且形态均一,可作为三维支架结构材料。抗菌实验结果表明,该敷料对革兰氏阳性菌的抗菌活性明显优于革兰氏阴性菌,说明带正电的壳聚糖发挥了重要的抗菌作用。目前,关于壳聚糖衍生物的研究也趋于成熟,已知具有季铵基的壳聚糖衍生物对细菌和真菌具有较高的功效。Ignatova等[62]制备了含壳聚糖季铵盐的光交联纳米纤维膜,可以有效抑制革兰氏阳性菌和革兰氏阴性菌的生长,表明了该材料作为抗菌医用敷料的潜力。
除了直接制备甲壳素/壳聚糖纤维用于医用敷料,利用具有抗菌能力的物质对生物质纤维进行改性赋予其抗菌能力,是应用生物质纤维解决伤口感染的另一种思路。Ma等[45]利用带正电的壳聚糖与带负电的丝素蛋白之间的静电力作用,在丝素蛋白纳米纤维表面负载壳聚糖,实现了纳米纤维膜抗菌能力从无到对大肠杆菌和金黄色葡萄球菌98%以上抑菌率的跨越,既保留了丝素蛋白纤维优良的生物相容性,又在一定程度上降低了该材料应用于医用敷料时受到污染的风险。一些无机物,如银、四氧化三铁、二氧化钛和氧化锌制成的纳米颗粒,可以作为与生物质纳米纤维结合的抗菌剂。例如,Cai等[63]开发了壳聚糖/明胶杂化纳米纤维,并通过添加四氧化三铁纳米颗粒来增强力学性能,这种纳米复合材料策略形成了具有高鲁棒性和抗菌功能性的纳米纤维敷料。然而,纳米颗粒的团聚及其在纳米纤维中的保存是该类材料应用于人体的2个瓶颈,因为其可能会降低该类纳米复合材料体系的抗菌性能。纳米颗粒在纳米纤维表面的沉积还可能导致它们被释放到人体中,到达内部敏感器官、改变细胞生化途径,并产生副作用[9]。海藻酸纤维自身的抗菌性与医用敷料的抗菌标准存在差距,也需要在制备过程中添加部分抗菌成分[64]。王海楼等[65]制备的载银海藻酸钙纤维水刺非织造布对金黄色葡萄球菌和大肠杆菌的抑制效果良好;Miraftab等[66]制备的海藻酸钠/碳酸银/车前草复合纤维,具有持久有效的抗菌性能及缓慢的银释放率,其作为敷料的效果可达到市售级的敷料水平。
生物质纤维的抗菌属性可以由抗菌生物质原料纤维自带,也可以通过在生物质纤维上负载其他抗菌组分赋予。无论何种方式,其最终目的就是构建既具有抗菌性能,又具有良好生物相容性的生物质纤维医用敷料,以促进伤口愈合和减少炎症发生。
2.2 药物递送
伤口愈合的过程复杂,包括止血、血管生成和恢复皮肤屏障功能。这些过程的正常发生需要生长因子和细胞因子的存在,然而,在某些情况下,这些因子没有充分存在或转化信号没有显著上调,可能导致愈合过程脱离其正常的级联或完全停止。生长因子、细胞因子、抗菌剂、蛋白质、小分子和生物活性药物等可以提高伤口愈合速度,与全身给药相比,这些药物在伤口的局部给药更有利于伤口愈合。这是因为局部给药可以降低药物的毒性或减少给药次数等[67]。药剂学和微/纳米技术的发展使研究人员能够制造药物传递系统,控制药物在伤口环境中的释放,或直接将药物递送到愈合组织或细胞中,使伤口愈合过程趋于正常[68]。
Scheneider等[69]利用静电纺丝技术开发了负载表皮生长因子的丝素蛋白纳米纤维膜用于促进伤口修复,其具有良好的强度、优异的生物相容性和易于控制的膜结构。被掺入丝素蛋白纤维中的表皮生长因子随着时间缓慢释放,170 h内的释放量仅为25%,表皮生长因子的加入大大缩短了愈合时间,证实该材料具有应用于慢性不愈合伤口的潜力。进一步,Miguel等[70]制备了一种双层纳米纤维敷料。其中顶层为丝素蛋白与聚己内酯的混纺膜,以模拟表皮的致密性和防水能力;底层为仿生真皮的丝素蛋白与透明质酸纤维膜,并在其中负载了百里香酚。这种双层膜敷料具有适合愈合过程的孔隙性、润湿性、力学性能和生物相容性,百里香酚的加入有效提高了材料的抗氧化和抗菌能力,提升了其在伤口修复中的适应性。
利用静电纺丝制备纳米纤维的技术已趋向成熟,但是在医用敷料应用中仍存在瓶颈,特别是在制备生物质纳米纤维时,低毒性的溶剂体系一直是难题,例如丝素蛋白、甲壳素、醋酸纤维静电纺丝技术常常需要利用六氟异丙醇、丙酮等有机溶剂来溶解,虽然可以通过后续处理使残留溶剂挥发,但其制备过程仍然存在风险。为此,已有研究人员致力于开发无毒溶剂体系来制备生物质纤维敷料,Seon-lutz等[71]以纯水为溶剂制备了具有生物相容性的不溶性透明质酸基纳米纤维,并以非甾体抗炎药萘普生为模型药物,探讨了透明质酸基纳米纤维在水溶液或超临界二氧化碳下对药物的负载情况。结果表明,该纳米纤维膜在几天内显示出有规律的药物释放,且没有失去纤维结构,促进了安全的功能性医用敷料的发展。
2.3 渗液管理
使用常规的医用敷料通常会导致敷料与伤口之间的伤口渗出物过度残留,愈合的首要任务是管理伤口的渗出液,因为过多的渗出物会使伤口过度水化,从而不利于伤口的愈合,因此,具有耐液态水和透湿、透气性能的柔性纳米纤维膜在医用敷料中越来越受到关注。从本质上讲,具有随机取向纤维的纳米纤维膜具有通孔结构,允许湿气从伤口中逸出;此外,小孔径和可调节的亲水性保证了纳米纤维膜的防水性。静电纺纤维的高表面积允许渗出物积累,而相互连接的纳米孔允许气体渗透。Li等[72]制备了一种具有不对称润湿性的多尺度复合纳米纤维膜,将丝素蛋白和聚己内酯通过静电纺在多巴胺处理的亲水聚乙烯醇纳米纤维膜表面形成多尺度疏水纳米纤维,形成单向水传导的不对称可润湿性复合膜。该复合膜有助于清除伤口上的渗液,有利于医用敷料的单向水传导。Adeli等[73]制备了聚乙烯醇/壳聚糖/淀粉纳米纤维膜,然后将制备的纳米纤维膜交联以提高耐水性,并优化生物降解率。由其制成的敷料具有适当的孔隙率和平衡的吸水率及水蒸气传输速率,可有效地处理伤口渗出物,为伤口提供合适的潮湿环境。
除了在生物质纤维材料结构上改进外,亦有生物质原料改性以提高材料吸湿性的研究。纤维素结构中有较多的极性基团,可吸收伤口渗出物,多孔的结构有利于增加透气性,但其遇水后溶胀度不高,这也是纤维素用于制备传统敷料的不足。经过功能化处理后,纤维素衍生物吸湿性提高。例如,通过氯乙酸处理纤维素纤维可以制备羧甲基纤维素纤维,其可以吸收大量的伤口渗出液,同时在伤口上形成一个适合创面愈合的潮湿环境[74]。
生物质原料(如海藻酸钠、壳聚糖等)的吸湿能力,可以赋予其纤维材料在伤口处理中的渗液管理能力。同时,还可以通过设计生物质纤维敷料的特殊结构,利用原料属性与结构特点协同促进材料吸水透湿能力,使其更加趋近理想敷料的要求。
2.4 组织替代
传统医用敷料的主要作用是保护伤口,为促进伤口愈合提供良好的环境,然而,这些产品不能替代丢失的组织,如严重受损的真皮组织[75]。组织工程皮肤替代品目前正在发展为一个潜在的解决方案,逐渐成为治疗全皮肤损伤的一种有效选择[76-78]。这些替代品可以与细胞一起接种以形成工程皮肤,也可以植入细胞内以招募局部细胞并促进其生长。组织工程皮肤替代品能够通过在伤口上提供一个安全的覆盖物来实现皮肤的生物功能,其易于处理,还可以减少愈合过程中患者的疼痛和不安。作为皮肤移植物的生物材料应具有兼容性、可生物降解性、细胞相容性,并应符合皮肤组织的物理化学特性。由可生物降解的纳米纤维支架组成的组织工程皮肤移植物正在得到广泛的研究,因为它们具有一些独特的优势,胶原蛋白、透明质酸、壳聚糖等生物活性物质的应用已成为该领域目前研究的重点[67,79]。
在过去的几十年里,皮肤组织工程应用的功能性生物替代品的开发已经取得了一些进展。目前,智能细胞外基质模拟支架通过诱导细胞-基质通信、组织重塑和体内平衡,发展成为一种有前景的范例。通过静电纺丝技术开发的生物质纳米纤维材料,可以模拟细胞外基质中天然胶原纤维的结构。由于胶原纤维在维持皮肤组织的完整性和强度方面发挥着关键作用,静电纺丝产品可以提供一个仿生的纳米纤维结构支架,以促进伤口愈合[80]。然而,静电纺天然胶原纳米纤维的力学性能差、酶降解控制弱,造成了支架的不稳定性,是阻碍其应用的显著缺点[81]。
除了胶原蛋白纳米纤维外,多糖基纳米纤维也被广泛用于皮肤组织的替代研究中。Noh等[82]的研究表明:在甲壳素纳米纤维支架上,正常人类成纤维细胞和角质形成细胞显示出了良好的附着和扩散行为,而I型胶原蛋白涂层可以进一步提高纳米纤维支架对细胞附着和增殖的支持有效性;甲壳素纳米纤维支架在大鼠皮下移植中在28 d内完全降解,无任何炎症反应,说明了甲壳素纳米纤维在尺度上的优势有利于其应用于皮肤替代物支架。同时,已有研究证实了壳聚糖-聚乙烯醇纳米纤维具有良好的细胞相容性,并能促进体内伤口愈合[83-84];且由于壳聚糖的抗菌特性和明胶的细胞黏附特性,壳聚糖-明胶混合物的纳米纤维支架也被认作皮肤再生的潜在支架[85]。另外,Singh等[86]开发了一种仿生κ-角叉菜胶包覆的醋酸纤维素三维纳米纤维支架,可促进皮肤细胞外基质的形成。κ-角叉菜胶是一种天然的硫酸化藻类多糖,与皮肤细胞外基质的天然葡萄糖氨基多糖非常相似。此外,静电纺醋酸纤维素纳米纤维类似于细胞外基质的三维纳米形貌结构。在涂层形式下,κ-角叉菜胶可以在纳米纤维支架上提供细胞功能所需的生化条件,从而模拟皮肤细胞外基质的天然三维微环境。
由于生物质原料的生物相容性、生物降解性和与人体识别大分子的相似性,其被广泛用于组织工程皮肤替代品中。生物质纤维,尤其是纳米纤维结构,因其可以模拟皮肤细胞外基质而更具优势。但是人体皮肤组织结构复杂、功能特殊,目前关于组织替代的研究还达不到真正替代的目的,仍需依赖工程技术的进一步发展。
3 展 望
伤口修复是一个受多种因素影响的生理过程,其复杂性往往会导致一些不确定性,如伤口愈合缓慢、继发性感染和炎症等。生物质纤维材料是一种很有应用前景的医用敷料材料,因其具有良好的生物相容性和优异的结构特点,可以为伤口营造适宜的愈合环境。尽管对生物质纤维医用敷料开发的研究由来已久,但值得注意的是,已批准的伤口护理治疗产品很少。尤其在国内市场上,具有自主知识产权的功能性医用敷料产品屈指可数。虽然目前的制造技术显现出许多优点,但生物质纤维材料的制备和应用仍存在一些限制,包括原料的纯度、溶剂的选择等。例如:甲壳素自身含有微量蛋白极难去除,有可能引起免疫反应,如何有效地进一步降低甲壳素中的蛋白质含量,提高敷料的普适性关系着甲壳素纤维敷料未来的发展,也是亟待解决的问题之一。另外,生物质纤维材料的力学强度也使其发展受限,目前需要与一些合成高分子结合或引入交联剂来改善这些问题,但仍需探索更加简易安全的方法。目前,单一的纤维敷料已不再满足人们的需求,将生物质纤维与其他形式的材料结合,如多层膜复合材料、纤维复合水凝胶、纤维气凝胶等,既可以保留生物质纤维的优良特性,还将更有利于其对不同伤口的定制化处理。
