活性炭负载TiO2吸附与光催化降解甲醛研究进展
2022-03-25惠世恩朱新伟王登辉刘长春
惠世恩,朱新伟,王登辉,刘长春
(1.西安交通大学 能源与动力工程学院,陕西 西安 710049; 2.西安科技大学 安全科学与工程学院,陕西 西安 710054)
0 引 言
现阶段,装修材料大都含有甲醛(HCHO)等污染物[1-3]。甲醛危害性大、释放周期长,释放累计超过一定阈值时,会产生室内空气污染[4-6],严重危害身体健康[7]。因此,处理甲醛等室内环境污染物刻不容缓。室内甲醛污染物的去除方法大体上分为2类:① 源头治理,使用不含甲醛的装修材料或用品,该方法比较方便,但生产不含甲醛的装修材料的技术手段有限,从源头上去除甲醛不太现实;② 后期治理,如换气法、植物吸收法、等离子净化法、吸附剂吸附法和光触媒降解法等。由于甲醛释放周期长、易受季节影响,一些寒冷地区不太适用通风换气法去除甲醛。绿色植物能去除低浓度的甲醛[8],但在高浓度室内,绿色植物吸附甲醛见效甚微。低温等离子法是一种新兴的除甲醛方法,是利用离子与甲醛分子结构发生复杂反应,从而催化降解甲醛。研究表明[9],低温等离子法能将甲醛完全降解为CO2和H2O,快捷高效,但会产生O3和CO等物质,技术经济消耗大,有待进一步发展。
活性炭是由天然或合成的含碳物质经加工制得的产品,原料包括生物质材料、不同变质程度的煤、石油焦等。与其他原料相比,煤炭价格低廉、来源广泛,煤基活性炭化学稳定性强、机械强度高。煤基活性炭的工艺流程包括煤炭破碎、炭化、活化及后处理等。制备方法分为3种:① 化学活化法[10],将酸、碱、盐等活化剂加入煤炭,在惰性气氛中加热蒸发,同时进行炭化和活化制取活性炭。② 物理活化法[11],将煤炭低温热解后,用CO2或水蒸气进行热破坏,获得相应的结构。③ 物理化学活化法[12],将活化剂添加到煤炭中,再经气体活化制得具有特殊结构性能的活性炭。吸附法是利用活性炭纤维(ACF)[13]、活性炭(AC)[14]等多孔吸附剂的孔径分布和表面官能团对甲醛等污染物进行处理,具有材料易得、操作方便等优点。光催化降解技术是利用一定波长的光照射光触媒材料以产生参与反应的活性物种,将甲醛降解为CO2和H2O,具有净化空气的效果[15]。TiO2无毒无害、安全绿色、光催化效率较高,是公认较理想的光催化降解甲醛等室内污染物的材料[16-17]。但TiO2光谱响应范围窄,需通过金属离子、非金属离子掺杂等手段[18-19]提高光子利用效率和光催化活性。此外,TiO2难以回收再利用[20],因此研究者探索不同催化剂载体以提高光催化效率,而活性炭作为吸附载体,具有稳定性强、比表面积大等优势[21],有利于TiO2的负载。
笔者结合国内外研究现状综述了活性炭吸附机理及改性、光催化反应原理、提高光催化活性途径、TiO2负载等内容,分析比较活性炭和TiO2/AC对甲醛的吸附降解性能,以期为甲醛高效降解提供指导。
1 活性炭及改性
1.1 活性炭吸附甲醛
活性炭具有比表面积大、吸附速率快、孔径分布适中等特点,在吸附、分离甲醛污染物方面具有显著优势[22]。按照吸附方式不同,活性炭吸附分为物理吸附和化学吸附。物理吸附过程中,孔径梯度分布决定吸附容量和速率,大孔和中孔发挥输送甲醛分子的作用,微孔具有巨大的比表面积,能为污染物提供足够停留场所,活性炭表面利用在不对称偶极矩作用下产生的范德华力吸附甲醛分子[23]。化学吸附是活性炭的羧基、酚羟基等官能团与甲醛吸附质分子发生化学反应,吸附较稳定,具有不可逆性[24]。从活性炭的物理吸附和化学吸附过程可知,活性炭的孔径分布和表面官能团对吸附质吸附过程极为重要。
汤进华等[25]研究了活性炭微孔和中孔对甲醛吸附性能的影响,发现活性炭吸附效果与微孔占比呈正相关;当中孔比表面积增大时,达到吸附平衡的时间缩短。宋剑飞[26]基于孔径分布研究了有机污染物在活性炭上的吸附,发现较好的孔梯度分布会加速污染物在活性炭孔径中的内扩散,提高吸附容量。虽然活性炭微孔能提供巨大的比表面积,但需大孔和中孔等输送孔,孔径梯度影响活性炭的吸附容量与吸附速率。
林莉莉等[27]通过动态穿透试验研究了椰壳和木质活性炭表面官能团对甲醛吸附性能的影响。结果表明,椰壳炭对甲醛的吸附性能最好,这得益于椰壳炭表面较多的酚羟基和含氮官能团。KOWALCZYK等[28]研究了活性炭表面官能团与甲醛的反应机理,甲醛不仅可与官能团形成氢键,还能与孔径中的羧基和酚羟基发生氧化反应。
活性炭表面官能团含量决定化学吸附、氧化反应的程度,较大的微孔比表面积为污染物提供足够的物理吸附位点,孔径分布影响甲醛分子的内扩散能力。然而活性炭以物理吸附为主,吸附不稳定,在一定压力、温度条件下会发生脱附,造成二次污染。通过氧化还原方法,改变活性炭表面化学官能团数量和类型,将物理吸附转变为物理-化学联合吸附,可有效提高甲醛分子在活性炭表面的吸附。
1.2 活性炭改性吸附甲醛
甲醛属于极性分子,通过改性增加活性炭表面的酸性含氧官能团,能为极性分子提供更多的化学吸附活性位点。

极性吸附质可稳定吸附在经酸性改性的活性炭表面,归因于官能团含量增加。刘雪梅等[31]研究经磷酸改性和氮气活化后的活性炭对甲醛的吸附性能,发现磷酸质量分数40%,氮气活化温度550 ℃时,改性活性炭对甲醛的吸附容量为4.78 mg/g。刘耀源等[32]发现活性炭经H2SO4改性后,甲醛饱和吸附量增加了近50%,脱附峰面积和峰高均有一定程度提高。酸化可改变活性炭的孔径分布和表面酸性官能团含量,活性炭对甲醛的吸附容量增加,可能是物理吸附和化学吸附协同作用的结果。
处理甲醛的方法除了活性炭吸附法外,TiO2光催化降解甲醛无毒无害,引起广泛关注。
2 TiO2光催化甲醛
2.1 光催化降解甲醛机理
纳米TiO2属于由Ti3d和O2p轨道杂化形成的不连续能带结构[33]的半导体,由价带、导带和禁带组成。
根据光电效应[34-35](图1,Eg为带隙宽度),低能价带中的电子(e-)被光照激发越过禁带进入导带空穴(h+)[36]。价带中电子受激发后,还存在另外2种形式[37]:① 一部分被TiO2的缺陷位捕获;② 一部分激发光电子被空穴捕获,此时以热能形式释放能量,降低电子和空穴的分离效率,从而影响光催化效率。

图1 能带结构示意[34-35]Fig.1 Energy band theory schematic[34-35]
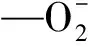

图2 TiO2光催化降解机理[38]Fig.2 Photocatalytic mechanism of TiO2[38]
1)电子(e-)和空穴(h+)的形成:
(1)

(2)

(3)
(4)
3)—OH的形成:
① 吸附空气中的水分子形成:

(5)
② 借助中间物H2O2形成:
H2O2的形成:
(6)

(7)
(8)
(9)
—OH的形成:

(10)
(11)
(12)
③ 与OH-反应形成:

(13)
4)空穴-电子对的复合:

(14)
杨建军等[39]通过程序升温脱附(TPD)、电子自旋共振(ESR)等物理方法研究了甲醛氧化过程中的中间物种和反应机理,认为甲醛被氧化成CO2、H2O的反应过程为

(15)

(16)

(17)

(18)
(19)
除了试验探究甲醛光催化反应机理外,谢鹏涛等[40]通过密度泛函理论的B3LYP方法和MP2方法在6-311++G(d,p)层面上研究了反应势能面上的反应物与中间物种之间的连接关系,模拟表明中间产物为甲酸(HCOOH)的异构体形式(HOCOH)。
e-、h+和—OH在甲醛氧化降解过程中至关重要。ISHIBASHI等[41]分别比较了反应过程中—OH、h+的产率和光催化的量子产率,结果发现,空穴产率和光催化的量子效率在同一个数量级,空穴在光催化过程中具有重要作用,应尽可能抑制电子、空穴的复合,使更多空穴参与到反应中形成活性物种。
因为价带中的e-会与h+复合、被缺陷位点捕获、迁移至半导体不同位置发生反应,所以电子、空穴的寿命很短,只有皮秒级。YANG和TAMAI[42]测量发现电子被捕获的时间为260 fs,而空穴的捕获时间更短,只有50 fs。TAMAKI等[43]研究发现电子的浅捕获时间为100 fs左右,深捕获时间为150 fs,浅捕获到深捕获时间为50 fs。
电荷运输能力也是影响光催化效率的重要因素[44],HOFFMANN等[45]研究了TiO2颗粒的紫外光激发过程,光催化反应过程及其特征时间见表1,界面电荷转移时间的特征时间长于载流子的生成、捕获、复合。黄晓俊[46]认为光生电子和空穴的复合比电荷转移快得多,很大程度降低了光生电子和空穴参与反应的数量,因此,有效降低电子和空穴的复合也是光催化研究领域的重要研究内容。

表1 TiO2半导体光催化反应的基本过程和特征时间范围[45]
2.2 光催化高效降解甲醛途径
朱琴等[47]探究不同波长的光照射TiO2对甲醛降解效果的影响,发现无紫外光照射时,甲醛的降解率约为29%。TiO2作为一种光催化材料,能降解甲醛等有毒害的气体或液体,具有安全、高效、节能、处理效果佳且不会产生二次污染等优点。但TiO2在光催化领域的弊端使其并未得到大规模工业应用。
纳米级TiO2在光催化领域的弊端[48],表现在:① 纳米级TiO2的分散性较差,易发生团聚现象,因此比表面积降低,减少了与甲醛分子接触面积,影响光催化性能。② 电子和空穴的寿命短,反应过程中需源源不断产生空穴与电子,使其迁移至半导体不同位置,并参与反应产生活性物种。③ TiO2对光照利用率较低。综上所述,TiO2存在粒径小、分散性差、电子-空穴对复合率高、太阳光利用率低等弊端,为提升其催化性能,需深入研究。
2.2.1贵金属沉积
朱晓兵等[49]研究了Au/TiO2光催化脱除气相甲醛的效果,结果表明相对湿度和蓝光光强分别为13%、38.5 mW/cm2时,光反应条件下甲醛降解率为77%,远高于暗反应时的转化率。
贵金属改性TiO2的作用原理[50]:
1)贵金属沉积在TiO2后,因费米能级存在差异能产生贵金属-TiO2异质结,TiO2中的光生电子被光照激发跃迁后,从TiO2表面转移到贵金属表面,当费米能级达到一致时,形成了空间电荷层,不平衡的电荷分布造成能带弯曲形成肖特基势垒[51],如图3所示(Ef为费米能级;E0为贵金属的表面势能;Ex为内建电场;Φb为肖特基势垒高度;Φs为TiO2的功函数)。价带中受激发的电子可被肖特基势垒捕获。
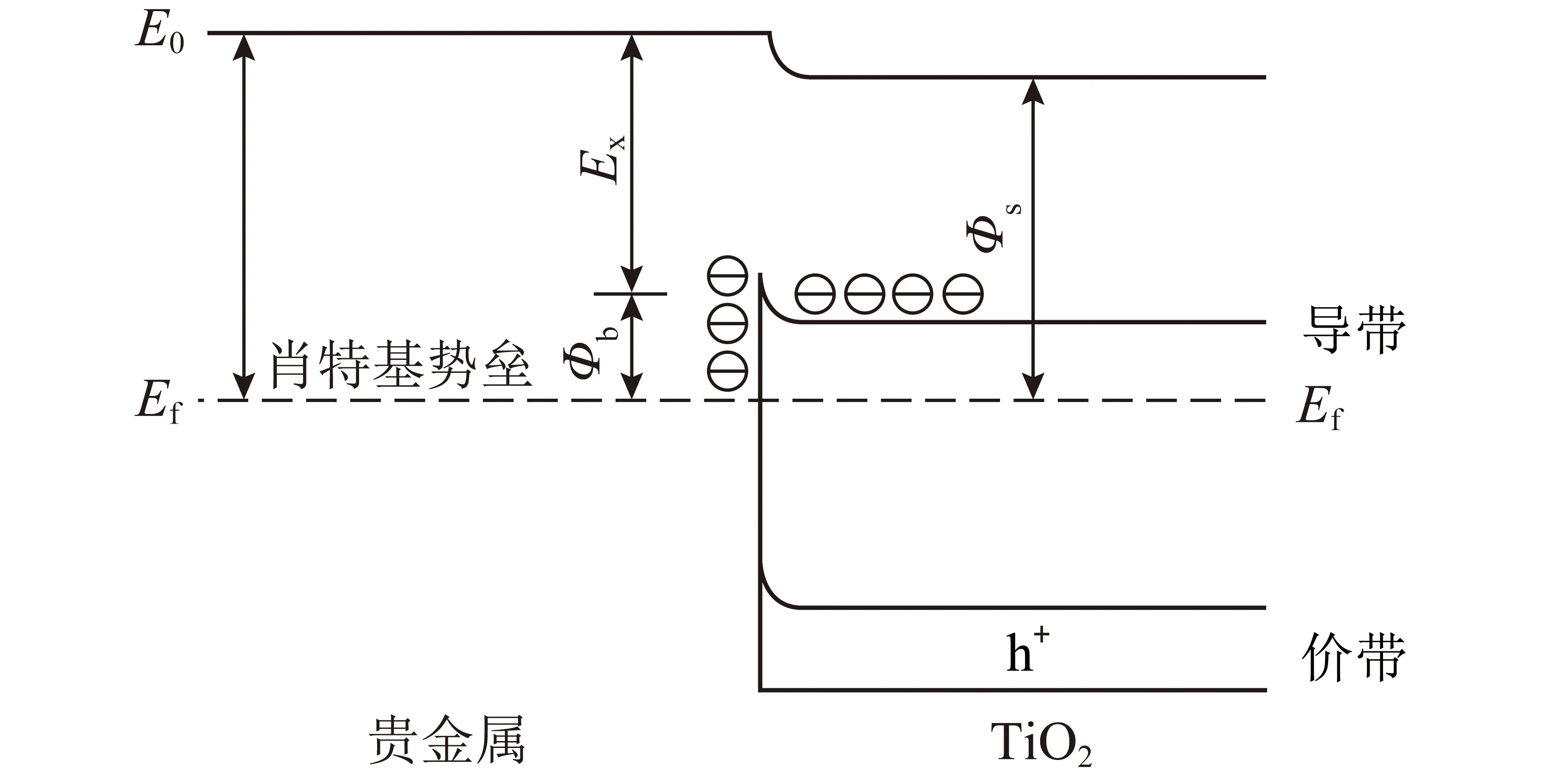
图3 肖特基势垒示意[51]Fig.3 Schematic of schottky barrier[51]
2)当贵金属掺杂入TiO2晶格中,会形成晶格畸变,一定程度上抑制电子-空穴对的复合,提高纳米TiO2光催化性能。
贵金属沉积到TiO2表面,并不影响TiO2的比表面积。研究发现,在TiO2表面沉积10%的Pt时,对纳米级TiO2的影响仅为6%。如果贵金属在TiO2的沉积量较大时,会增加电子-空穴对的复合率。研究[52-55]表明,沉积在TiO2表面的贵金属主要是Pt、Pd和Ag。ZHANG和HE[56]分别评估Pt、Rh、Pd、Au沉积在TiO2后的催化活性,甲醛的降解率依次是Pt/TiO2>Rh/TiO2>Pd/TiO2>Au/TiO2>TiO2。HUANG等[57]研究发现Pd的负载量为0.1%的Pd/TiO2时,室温下可将甲醛完全降解为CO2和H2O。
2.2.2表面光敏化
表面光敏化[58]是将TiO2的吸收光谱拓宽至可见光区的有效途径之一,分为染料敏化和复合敏化2种。
染料敏化是通过物理或化学方式将激发态电势比TiO2能级更负的有机染料吸附于TiO2表面,光生电子e-转移至不同位置,并与TiO2表面的氧气等发生反应,作用机理如图4[59]所示。研究表明,光敏化剂改性TiO2可提高光催化活性,光子的利用效率可提高30%~80%[60]。具有一定稳定性的光敏化剂主要有玫瑰红、叶绿素、曙红B、硫堇曙红、紫菜碱等。
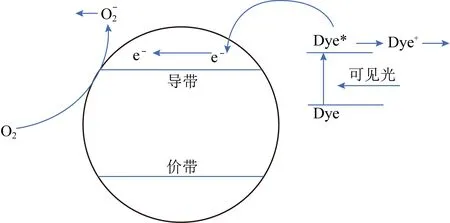
图4 染料敏化TiO2光催化反应机理[59]Fig.4 Mechanism of dye-sensitized TiO2 photocatalytic reaction[59]
复合敏化是将禁带宽度小的半导体与TiO2半导体组合形成一个异质结,由异质结的工作原理可知,与TiO2复合半导体价带中的电子被激发输运到TiO2导带中[61],如图5所示。一般选择与TiO2能带结构相近且禁带宽度较窄的半导体(如CdS、SnO、Fe2O3、WO3等)与TiO2复合。利用2种组分匹配的能带结构之间的协同效应可拓宽复合催化剂的光谱响应范围,在一定程度上提高光生载流子的寿命,构建异质结是光催化领域新的研究方向[62-65]。CdS-TiO2复合体系的能带图[66]如图6所示,CdS的禁带宽度约为2.4 eV,CdS在光照条件下,首先被激发,其中光生电子输运到TiO2导带中,实现了光生载流子分离[67]。杜晶晶等[68]发现CdS-TiO2的复合效果较好。杜玉[69]认为Ag2O-TiO2材料有利于光生载流子的分离与迁移,能有效降解甲醛。

图5 TiO2和钙钛矿的能级[61]Fig.5 Energy level of TiO2 and CH3NH3PbI3[61]
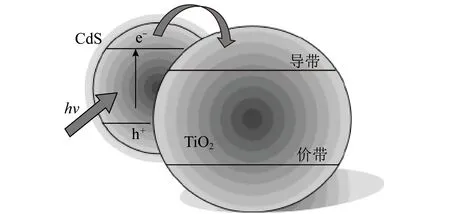
图6 CdS-TiO2 复合体系的能带[66]Fig.6 Energy band of CdS-TiO2 composite system[66]
2.2.3金属离子掺杂
SITENG等[70]研究表明,Fe3+、Mn2+掺杂进纳米TiO2后,其吸收光谱可以产生红移,提高其光催化活性。这一发现迅速带动了金属离子改性TiO2的研究。李慧芳[71]制备Ag掺杂的TiO2用以降解甲醛,发现Ag/TiO2用量为40 g时,甲醛的降解率可达93%以上。IWASAKI等[72]研究发现Co2+的掺杂量为3%时,甲醛降解速率在可见光和紫外光下均最快。KUBACKA等[73]对阳离子(如V、Mo、W)改性后的TiO2催化降解甲苯进行研究,发现经V、W改性的TiO2光催化活性较高。研究[74-75]发现,Mo5+、Ce4+、Fe3+等19种金属离子改性TiO2可提高光催化活性,而经Co3+和Al3+掺杂会一定程度上促进电子、空穴的复合,降低其光催化活性。黄晓俊[46]研究La、Ce等掺杂改性TiO2,结果表明,La、Ce掺杂量分别为1.5%、0.5%时,能较大程度抑制TiO2由锐钛矿向金红石相的转变。刘岩崑[37]研究了Fe3+掺杂量对TiO2降解甲醛性能的影响,结果表明当掺杂0.5%的Fe3+时,甲醛降解率最大为92.5%。
金属离子掺杂TiO2的作用原理[76]为:① Ti4+的位置被金属离子取代,造成晶格畸变,TiO2产生了更多的缺陷,以捕获自由电子,一定程度上提高了光催化活性;② 金属离子掺杂到TiO2后,能作为自由电子的受体将其捕获,阻碍了载流子的复合;③ 金属离子能在TiO2中形成一个杂质能级,一定程度上缩短禁带宽度,拓宽光谱响应范围。
当金属离子掺杂TiO2满足以下条件时,才能提高光催化活性:① 金属离子掺杂进TiO2后要能够形成电子、空穴的浅捕获势阱。如Fe3+能级既靠近TiO2的价带又靠近其导带,所以TiO2经Fe3+掺杂后,形成了浅捕获势阱,有效俘获了电子、空穴[77-78];研究人员利用稀土元素掺杂改性[79]TiO2取得了明显进展,原因是稀土元素的5d空轨道为电子的迁移提供了场所。② 使用与Ti4+离子半径(74.5 pm)相近的金属离子(如Fe3+、Co3+、Ni3+和Cr3+离子半径分别为69.0、68.5、70.7和75.5 pm[38])掺杂。因为离子半径相近的金属离子较易取代Ti4+,改变TiO2的能带结构,形成浅捕获势阱,提高光催化活性。掺杂金属离子的浓度与光催化性能之间是抛物线关系[80-81],所以掺杂适宜浓度的金属离子才能提高光催化活性。
2.2.4非金属离子掺杂
研究[82-83]显示,N掺杂纳米TiO2能拓宽其光谱响应范围。刘彦东[84]以尿素为氮源制备氮掺杂的光催化材料N/TiO2用以降解甲醛,结果显示甲醛降解率为69.3%。李小红[85]认为在溶液pH为5,煅烧温度500 ℃得到的TiO2-xNx材料的甲醛降解率可达70.18%,降解反应符合一级动力学规律。LIU等[86]采用sol-gel法制备氮掺杂的TiO2薄膜用以降解甲醛,研究表明,甲醛降解率在24 h内达到了90%,并具有优异的稳定性和重复使用性。WANG等[87]认为TiO2经氮掺杂后,位于价带附近的N2p态是催化性能得以提高的原因。PALGRAVE等[88]研究了TiO2经氮掺杂后的禁带宽度,认为TiO2带隙变窄的主要原因是间隙氮不对称扩散到本体中。ZHANG等[89]研究了先后在NH3和H2中煅烧得到的TiO2产品的光催化性能,发现氧空位与N杂质协同作用可以提高其降解污染物效率。
非金属离子掺杂TiO2的作用原理为:① TiO2氧位被非金属阴离子取代后,结构的畸变程度发生改变,一定程度上减少了电子-空穴对的复合,有更多的电子、空穴可参与反应[90];② O的轨道与非金属离子(如N3-、C4-等)的轨道杂化后,引起TiO2导带下移,减小了TiO2的禁带宽度,拓宽了光谱响应范围;③ 非金属阴离子进入TiO2晶格取代间隙位,形成深杂质能级,拓宽了光谱响应范围,但同时在深杂质能级处,电子、空穴会发生复合,解决这一竞争性关系对于提高光催化活性至关重要。常见的TiO2掺杂改性的非金属阴离子有N3-、P3-、C4-、S2-,其中以N3-的掺杂效果最好[91]。
综上,拓宽纳米TiO2光谱响应范围、提高光催化性能的主要方法有贵金属沉积、表面光敏化、金属离子掺杂、非金属离子掺杂等。
3 TiO2/AC吸附-光催化协同降解甲醛
研究发现,将纳米TiO2负载在载体(如二氧化硅、活性炭等)上,制得TiO2/AC复合材料可有效解决TiO2粉体难以回收的问题,增加了TiO2的光催化活性;活性炭负载后,可提高催化剂周围的局部浓度,增加污染物与TiO2的接触面积,将中间产物等完全降解[92]。
黄文耀等[93]采用电喷雾的方法研究了光触媒TiO2和活性炭在电纺纤维上的逐层沉积,得到NF-P/C多层复合膜。复合薄膜与空气污染物具有较大接触面积是由于具有大比表面积的电纺纳米纤维作为光触媒载体。吴凌姗[80]制备了无光触媒/ACF复合材料,将吸附和催化结合,加快降解甲醛等室内污染物的速率。孙和芳等[94]研究了TiO2/ACF吸附催化材料对甲醛的降解效果,结果显示,协同材料对甲醛的降解率可达94.06%,活性炭对甲醛的吸附量为60 mg/g,远高于单独活性炭的吸附率。可知甲醛经过吸附—传质—降解过程后,可大幅提高降解速率。催化剂将负载体浓缩的甲醛降解,ACF可实现脱附再生。
陈玉娟等[95]研究了活性炭的孔结构和比表面积对吸附催化协同材料的催化性能影响,结果显示,协同材料的光催化活性随活性炭平均孔径和比表面积的增大而提高。与此同时,卢辛成等[96]通过溶胶-凝胶法分别将不同孔径和比表面积的活性炭负载到TiO2上降解甲苯,比表面积大的活性炭负载TiO2对甲苯的降解率可达97%,催化剂的失活时间明显延迟。可知活性炭的比表面积和孔径对吸附催化协同材料的催化降解性能影响显著,具有中孔和大孔的的活性炭负载能明显提高光催化性能。
罗清清等[97]研究了TiO2在协同材料中的分散性,发现TiO2分散性良好,平均粒径约为40 nm,催化剂活性位点均匀分布,因此协同性能明显提高。王舜[98]通过电子显微镜研究了TiO2在TiO2/AC材料表面的分散性,结果如图7所示,TiO2较均匀地负载在活性炭表面,也有较少部分TiO2呈团聚颗粒,这是由于粒子通过团聚能降低体系的自由能,以提高负载稳定性。XING等[99]通过控制TiO2在活性炭表面的负载次数,有效控制了催化剂颗粒的团聚。

图7 TiO2 /AC协同材料的SEM图[98]Fig.7 SEM of TiO2/AC synergistic materials[98]
马晓军和李冬娜[100]探究纳米TiO2负载量对降解甲醛影响,研究表明,随着纳米TiO2负载量的增大,甲醛降解率先增大后减小。李小红等[101]研究发现活性炭表面TiO2负载浓度增大时,透光率降低,因此甲醛降解率下降。同时,研究了吸附催化协同材料的重复实用性,结果见表2,TiO2/AC材料连续使用6次时,甲醛降解率仍达92.79%。

表2 TiO2 /AC使用次数与甲醛降解率的关系[101]
胡校冬和邓桦[102]通过扫描电镜研究TiO2负载在活性炭孔径中的位置,如图8所示,可知催化剂负载达到一定阈值时,活性炭的过渡孔被堵塞,影响吸附性能。

图8 活性炭表面负载前后SEM图[102]Fig.8 SEM of activated carbon before and after surface loads[102]
TiO2负载量达到一定阈值时,会堵塞活性炭的大孔和中孔,影响污染物的迁移速率,从而降低降解效率。因此,应调整吸附剂和催化剂的复合比例,以达到最佳的催化降解活性。
4 结语与展望
按照吸附方式的不同,活性炭吸附可分为物理吸附和化学吸附,较好的孔梯度分布能加速甲醛在活性炭孔径中的内扩散,提高物理吸附容量,增加活性炭表面酸性含氧官能团的数量,有利于提升甲醛极性分子的化学吸附。然而,中孔活性炭应用范围广,调控难度大是目前煤基活性炭制备技术亟待解决的问题。TiO2催化剂在污染物治理方面提供了新的发展方向,但量子效率低、可见光吸收范围窄等问题普遍存在,在制备过程中,通过金属离子/非金属离子掺杂改性等手段,可有效拓宽光谱响应范围,在一定程度上抑制电子和空穴的复合。将TiO2负载在活性炭上制得TiO2/AC吸附催化协同材料,有利于解决催化剂难以回收利用的问题,通过活性炭对甲醛的吸附与浓缩,为光催化提供良好的反应环境,提高降解速率。
TiO2/AC吸附降解甲醛未来研究方向主要集中在以下方面:
1)活化剂与活性炭孔形状之间的关系尚未清晰,需优化不同制备方法,开发具有特殊结构性能的活性炭。
2)通过控制活化与炭化过程,调节不同尺寸孔在总孔容中的比例,以开发具有特异吸附能力的活性炭。
3)探究改性方法与活性炭官能团的关系,制得具有最大吸附能力的活性炭。
4)制备形貌可控、便于回收利用和可见光吸收率高的新型TiO2催化剂将成为今后的发展方向。
5)随着对TiO2机理的深入探究,制备去除效率高、吸附容量大、能耗低、具有选择性的TiO2/AC材料,提升吸附催化协同材料的制备水平,TiO2/AC材料将具有更广阔的应用前景。
