龙柏衍生碳点的合成及其对Fe3+、抗坏血酸的连续检测
2022-03-24程雨丹杨诗译程德燚王艺霏刘学瑞
程雨丹,杨诗译,程德燚,王艺霏,刘学瑞,徐 慧,
(1.湖州学院 理工学院,浙江 湖州 313000;2.鲁东大学 化学与材料科学学院,山东 烟台 264025)
碳点(Carbon dots,CDs),又称碳量子点,是一种正在迅速发展的碳纳米材料,表面富含官能团,易溶于水,稳定性高,具有良好的生物相容性.CDs的合成有多种方法[1-2],其中水热法具有操作简单、产物粒径均匀、成本低且无污染等优点,是目前应用最广泛的制备方法.如,Pei等[3]利用不同的氨基酸作为原料制备出不同性质、粒径的CDs,由于其结构各异,在不同领域发挥了不同的作用.CDs在医学成像[4]、化学和生物分析[5]、光催化[6]、太阳能电池[7]等领域具有较好的应用前景.
Fe3+是人体必需的微量元素之一,人体内如果缺乏铁则会出现各种各样的疾病,如贫血、肠损伤、癌症等[8-9].但人体内Fe3+的含量是有限量的,并非越多越好.铁在自然界中也广泛存在,河水中存在适量的铁会调节藻类群落组成,甚至会改善藻类品质,但铁一旦过量,则会造成水体污染.因此,铁含量的检测对人体健康和生态环境十分必要.
抗坏血酸(AA),又称维生素C,是维持人体正常生命活动所必需的维生素之一,具有水溶性和抗氧化性,也是胶原蛋白合成的重要原料.从食物中摄取AA还可以治疗贫血、预防动脉硬化.近年来,多种方法被运用到食物和药品的AA检测中,其中荧光分析法具有灵敏度高、简单易操作的特点.
龙柏(拉丁学名:Sabinachinensis(L.) Ant. cv.Kaizuca),又名刺柏、红心柏、珍珠柏等,是圆柏(桧树)的栽培变种,其长到一定高度,枝条开始螺旋盘曲向上生长,呈盘龙姿态,故名“龙柏”,常被用于园林绿化.目前,许多生物质基的碳点得到报道[10-11].龙柏是一种常见的生物质,分布广泛,原料易得且成本低廉.龙柏富含萜烯类、烷烃类、酯类[12]、黄酮、苯丙素苷、大豆脑苷和甾醇类等[13],是制备CDs的极好原料.以其为前驱体,一步水热法制备CDs,无需其他化学试剂,方法简单,绿色环保,将其应用于Fe3+和AA的连续检测,操作简单,灵敏度高且无污染.CDs具有较高的生物相容性、较长的荧光寿命、相对较宽的吸收光谱、较窄的荧光光谱等,在荧光分析中展现出较多优势.本文以龙柏枝叶为碳源,通过一步水热法制备CDs,并实现Fe3+和AA的荧光法连续定量测定,同时将该方法应用于实际样品的检测.
1 材料与方法
1.1 材料与表征
氯化锌、六水氯化钴产自天津博迪化工股份有限公司;AA、氯化钠产自天津市瑞金特化学品有限公司;葡糖糖(Glu)、谷胱甘肽(GSH)产自成都艾科达化学试剂有限公司;半胱氨酸(Cys)、氯化钾产自国药集团化学试剂有限公司;氯化钡产自天津市苏庄化学试剂厂;氯化镉产自天津市科密欧化学试剂有限公司;氯化铜产自莱阳经济技术开发区精细化工厂;无水氯化锂产自天津市福晨化学试剂厂;尿酸(UA)产自Alfa Aesar ;多巴胺(DA)产自Sigma-Aldrich.所有试剂均为分析纯试剂.龙柏取自鲁东大学校园.
CDs的形貌和尺寸大小由高分辨透射电镜(Talos F200X G2,美国 Thermo Fisher Scientific 公司)表征;表面官能团由傅里叶变换红外光谱仪(MAGNA 550,美国 Nicolet 公司)测定;表面元素和存在状态由X 射线光电子能谱(XPS,ESCALAB Xi+,美国 Thermo Fisher Scientific 公司)表征;紫外可见吸收光谱由紫外可见分光光度计(UV-2550,日本 Shimadzu 公司)获得;所有荧光光谱由荧光分光光度计(LS-55,美国 PerkinElmer 公司)测得.
1.2 样品制备
称取20.1 g龙柏枝叶,洗净后加入400 mL超纯水碾碎,并将其转移至聚四氟乙烯衬里的反应釜中,200 ℃ 下反应5 h;反应釜自然冷却至室温,15 000 rpm离心10 min,去除大颗粒,上清液用0.22 μm过滤膜过滤后置于4 ℃下保存备用.取CDs溶液冷冻干燥后称量,再溶于一定体积的超纯水中得到其准确浓度.
1.3 Fe3+检测
将30 μL CDs(5 mg/mL)置于2 970 μL醋酸-醋酸钠缓冲溶液(0.05 M,pH=5.0)中,然后加入不同浓度的Fe3+,在室温下测定其荧光强度.
1.4 AA检测
在Fe3+和CDs的混合溶液中加入不同浓度的AA溶液,反应3 min后测定其荧光强度.
2 结果与讨论
2.1 CDs表征
CDs 的大小、形态及分布状态通过透射电镜获得.如图1所示,CDs 近似球形,直径约 5.1 nm,且分散均匀,证明CDs 制备成功.图2中高分辨电镜所标出的晶格间距为0.23 nm,与石墨碳(100)面的晶格间距相当,证明碳点制备成功.

图1 龙柏枝叶衍生CDs的透射电镜图Fig.1 Transmission electron microscopy image of CDs

图2 单个CDs的晶格条纹Fig.2 Lattice fringes image of single CDs
图3为以龙柏枝叶为碳源,通过水热法制得的CDs的XPS表征图.从图3可以看出,CDs有3个明显的峰,分别在286.4 、399.8 、535.0 eV处,与之相对应的是C1s、N1s和O1s.由此可见,该CDs主要由C、O、N三种元素组成.
对C1s进行分峰,得到图4,据此可判断出4种不同的表面化学键:C-C (284.8 eV)、C-O (286.2 eV)、C=O (287.6 eV) 和 O-C=O (288.7 eV).XPS分析结果表明,CDs表面含有丰富的官能团,水溶性较好.
为进一步研究CDs表面的官能团,本文对CDs进行红外吸收光谱测定,结果如图5所示.在3 420、 1 774 cm-1处的吸收带源自O-H和C=O基团的伸缩振动[14].在1 621、1064 cm-1处的吸收带源自C=C和C-O基团的拉伸振动.红外光谱数据与上述XPS分析一致,证明CDs表面含有羟基和羧基,含氧官能团赋予CDs优异的水溶性.图6为CDs的Zeta电位图,其电位为-13 mV,进一步证明碳点表面含有羧基,解离后使其表面带负电,在溶液中能稳定存在.
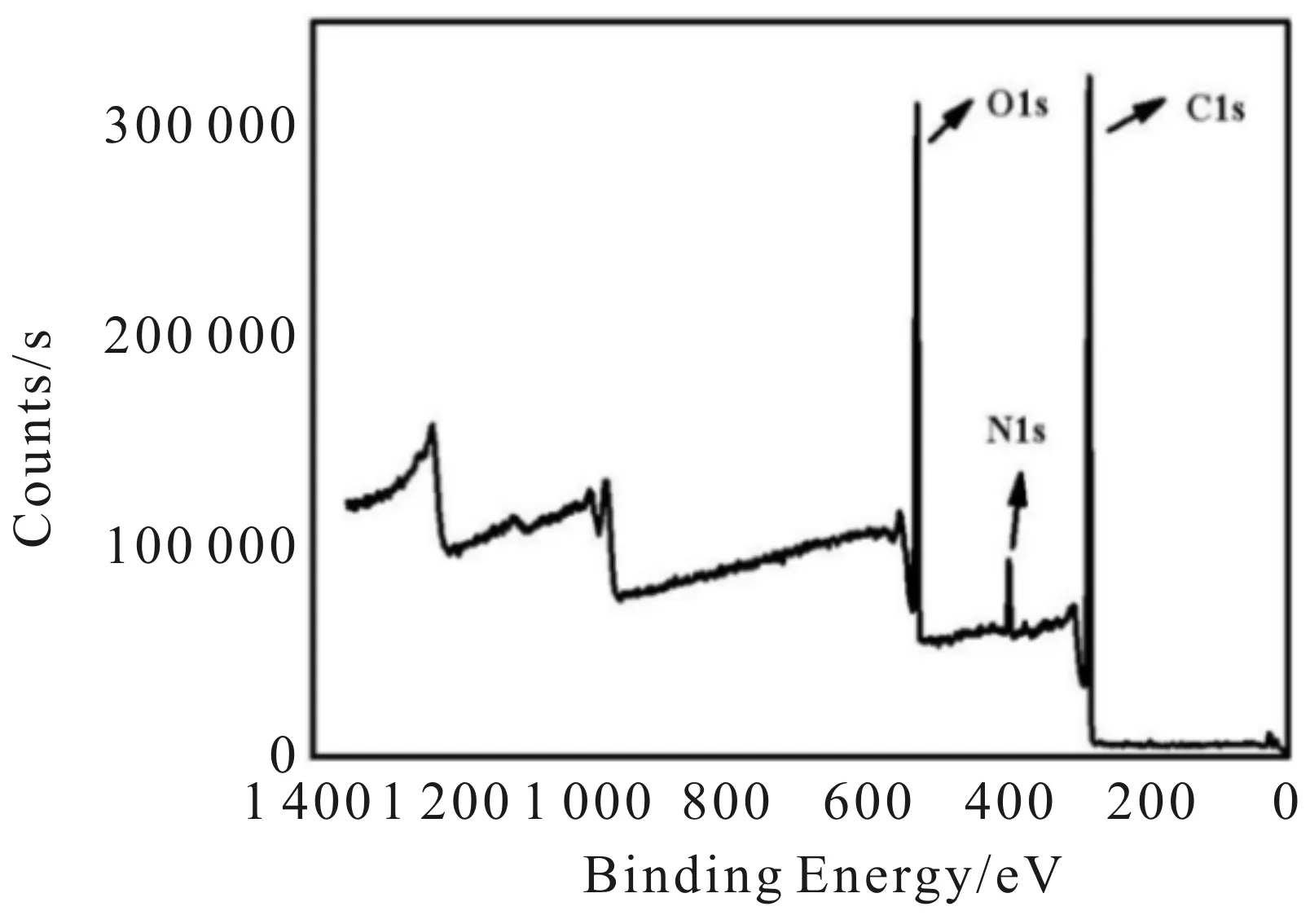
图3 CDs的X射线光电子能谱图Fig.3 XPS spectra of CDs
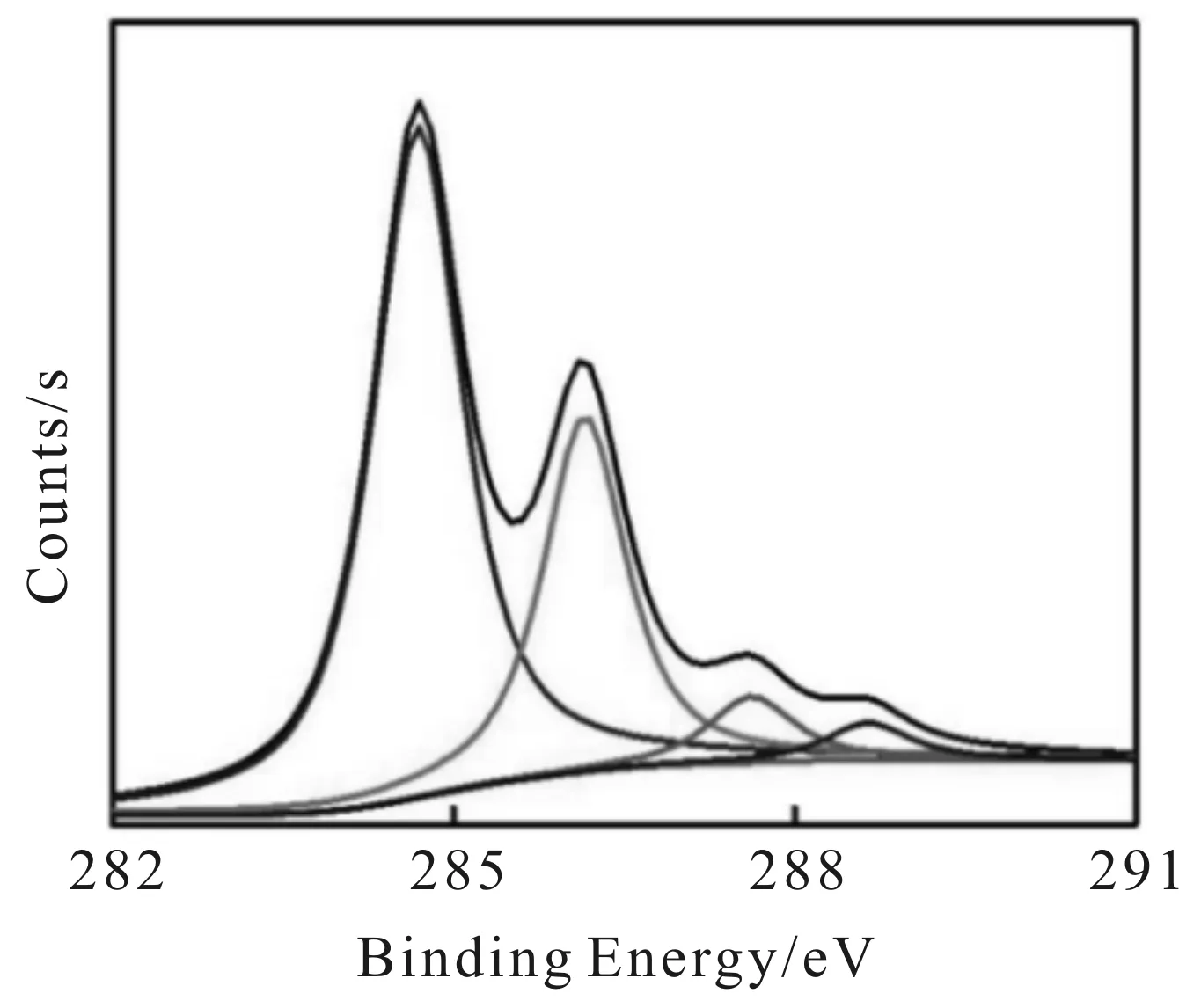
图4 C1s分峰图Fig.4 C1s XPS
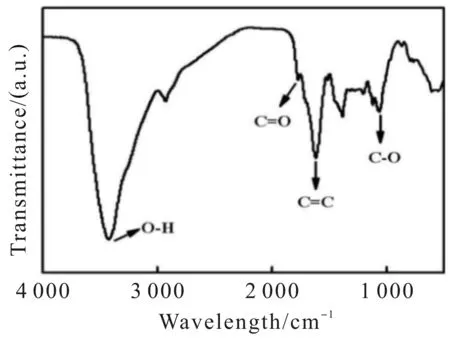
图5 傅里叶变换红外光谱图Fig.5 Fourier transform infrared spectrum of CDs
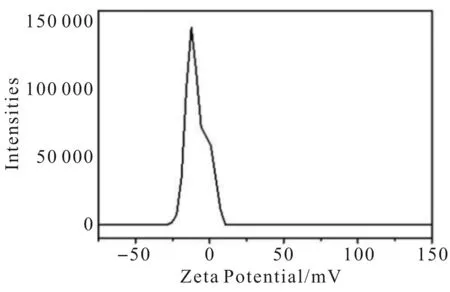
图6 Zeta电位图Fig.6 Zeta potential of CDs
2.2 碳点荧光性能
图7为在不同激发波长下CDs的发射光谱图.在290~380 nm范围内改变激发波长,荧光发射峰的位置只有微小移动,具有激发波长不依赖性,荧光强度呈先增加后降低的趋势,在330 nm时强度达最高值.因此,本文选择330 nm作为最适宜的激发波长.
CDs具有较稳定的荧光性质.本研究通过测量CDs溶液的荧光强度随保存时间、离子强度及pH的改变来证明这一特性.
图8为碳点荧光强度随时间的变化图.CDs合成后,对其荧光强度进行测量,之后每隔5天对CDs的荧光强度再次测量,共测6次.结果发现,CDs的荧光强度在保存1个月后没有发生明显改变,说明CDs的荧光性质较稳定.离子强度也是影响荧光强度的一个重要因素.本研究以NaCl为例,探究离子强度对以龙柏枝叶为碳源一步水热法制备出的CDs荧光强度的影响.首先测量CDs溶液的荧光强度,然后分别在CDs溶液中加入0.2 、0.4 、0.6 、0.8 、1 M NaCl溶液,测其荧光强度.结果如图9所示,荧光强度几乎未发生变化,说明离子强度不会影响溶液的荧光强度.该方法制备的CDs可推广应用到高离子强度溶液的检测中.
本文还研究了pH对CDs荧光强度的影响.取不同pH的醋酸-氢氧化钠溶液,向其加入等量的CDs,结果如图10所示.随着pH的增加,荧光强度总体较稳定,只有微小的起伏,表明在不同酸度溶液中,CDs的性质也较稳定.以上研究结果表明,所制备的CDs具有很好的稳定性.

图7 不同激发波长的碳点荧光发射谱Fig.7 Fluorescence emission spectra of CDs under different excitation wavelength
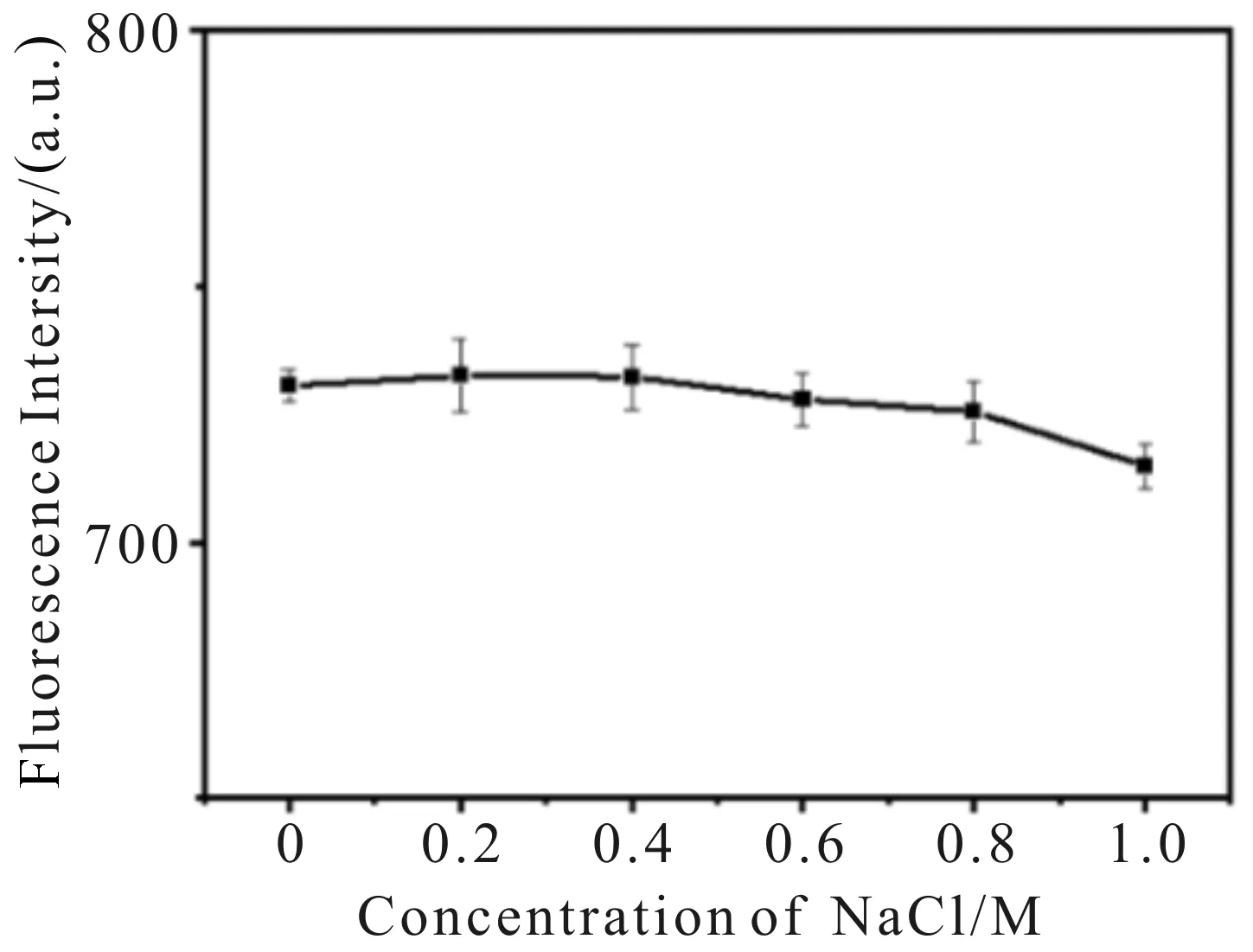
图8 时间对碳点荧光强度的影响Fig.8 The effect of time on the fluorescence intensity of CDs
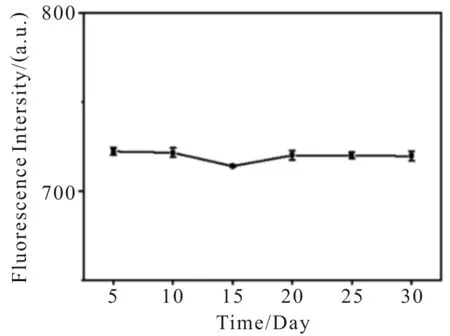
图9 NaCl浓度对碳点荧光强度的影响Fig.9 The effect of NaCl concentration on the fluorescence intensity of CDs
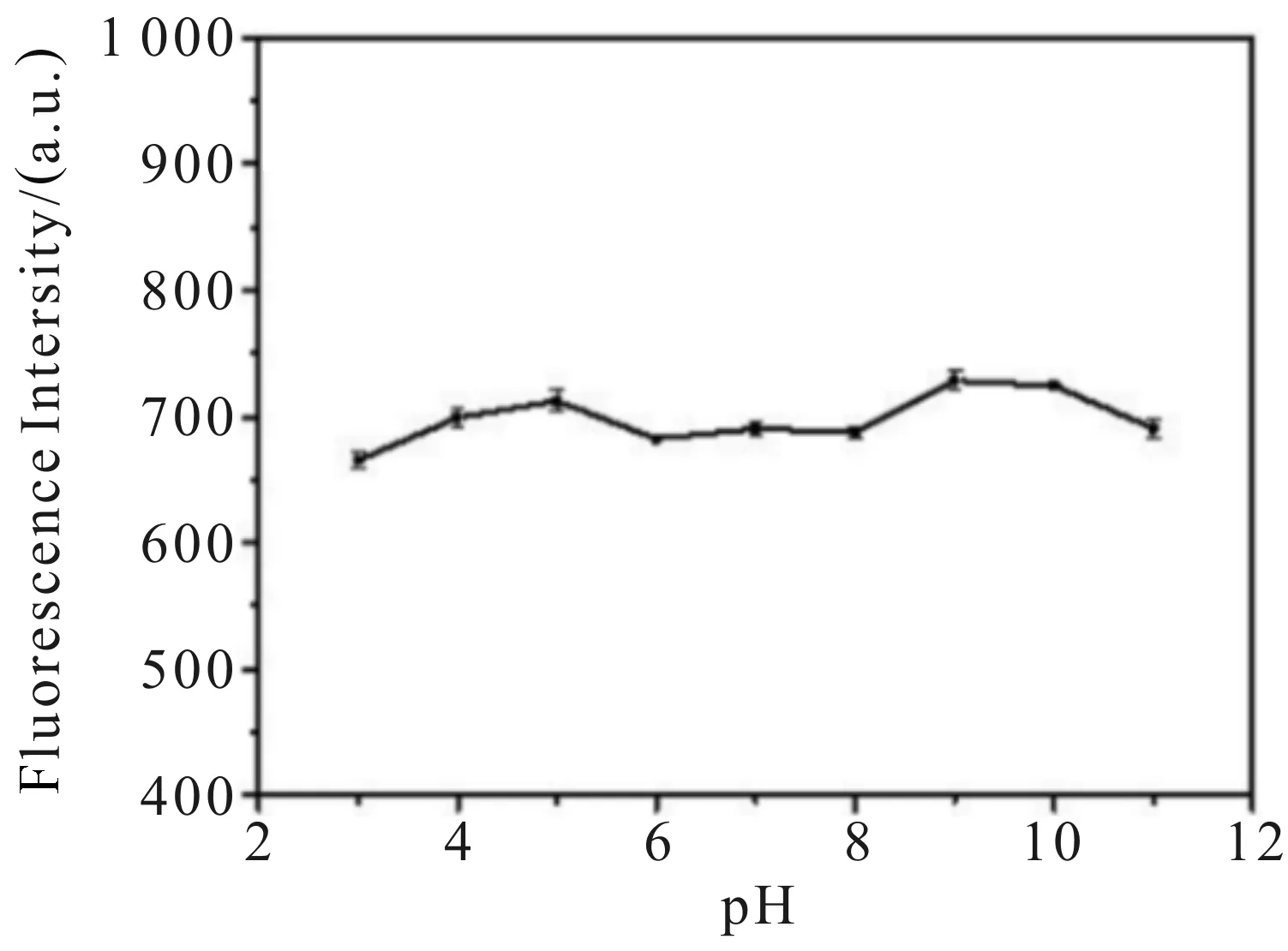
图10 pH对碳点荧光强度的影响Fig.10 The effect of pH on the fluorescence intensity of CDs
2.3 Fe3+检测
2.3.1 优化反应条件
实验发现,Fe3+对CDs的荧光强度具有很强的猝灭作用.为优化实验条件,探究反应时间、pH和CDs浓度对CDs荧光猝灭效率的影响.结果表明:Fe3+的加入可引起CDs荧光的明显猝灭,1 min后强度达到稳定,表明Fe3+对CDs的猝灭可快速完成,Fe3+的检测可快速实现.当pH=5.0、CDs浓度为 0.05 mg/mL 时,荧光强度比值(F/F0,其中F为Fe3+存在时的荧光强度,F0为未加Fe3+时的荧光强度)为最低值,因此将此作为定量检测的最佳条件.
2.3.2 金属离子猝灭的选择性
图11为不同金属离子对CDs荧光强度比值的影响.由图11可知,只有Fe3+会使荧光强度大幅下降,其余各种离子如Cd2+、Zn2+、Hg2+、Li+、Ba2+、Cu2+、Co2+、Ca2+、Sn4+、K+、Mg2+、Pb2+、Ni2+和Na+对荧光强度几乎没有影响(Cu2+和Hg2+有极其轻微的干扰),说明Fe3+对CDs的荧光猝灭具有极高的选择性.其原因可能是:与其他金属离子相比,Fe3+与CDs表面的羧基和羟基的亲和力更强.
为探究Fe3+对CDs荧光强度的猝灭机理,本文对CDs的荧光寿命进行测定.在加入Fe3+的前后,CDs的荧光寿命分别为5.4 ns和 5.6 ns (图13),两者接近,说明当Fe3+存在时CDs的荧光猝灭为静态猝灭,即Fe3+与CDs形成非荧光络合物[15].此外,Fe3+的紫外可见吸收光谱与CDs的荧光激发光谱部分重叠(图14),说明当Fe3+与CDs共存时发生了内滤效应[16].由此推测:Fe3+对CDs的猝灭机制是非荧光络合物的形成和内滤效果共同作用的结果.
研究发现,在CDs溶液中同时加入干扰离子和Fe3+,荧光猝灭的程度与不加干扰离子时相比几乎没有变化,结果如图12所示.这进一步证明干扰离子不会使CDs发生荧光猝灭,该方法具有极好的选择性.
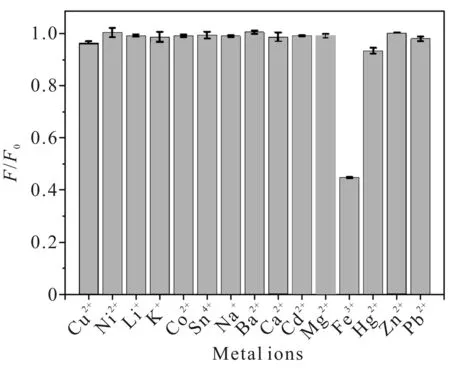
图11 不同金属离子对CDs荧光强度比值的影响(碳点浓度为0.05 mg/mL)Fig.11 Fluorescence intensity ratio of CDs in the presence of different metal ions (the concentration of CDs is 0.05 mg/mL)
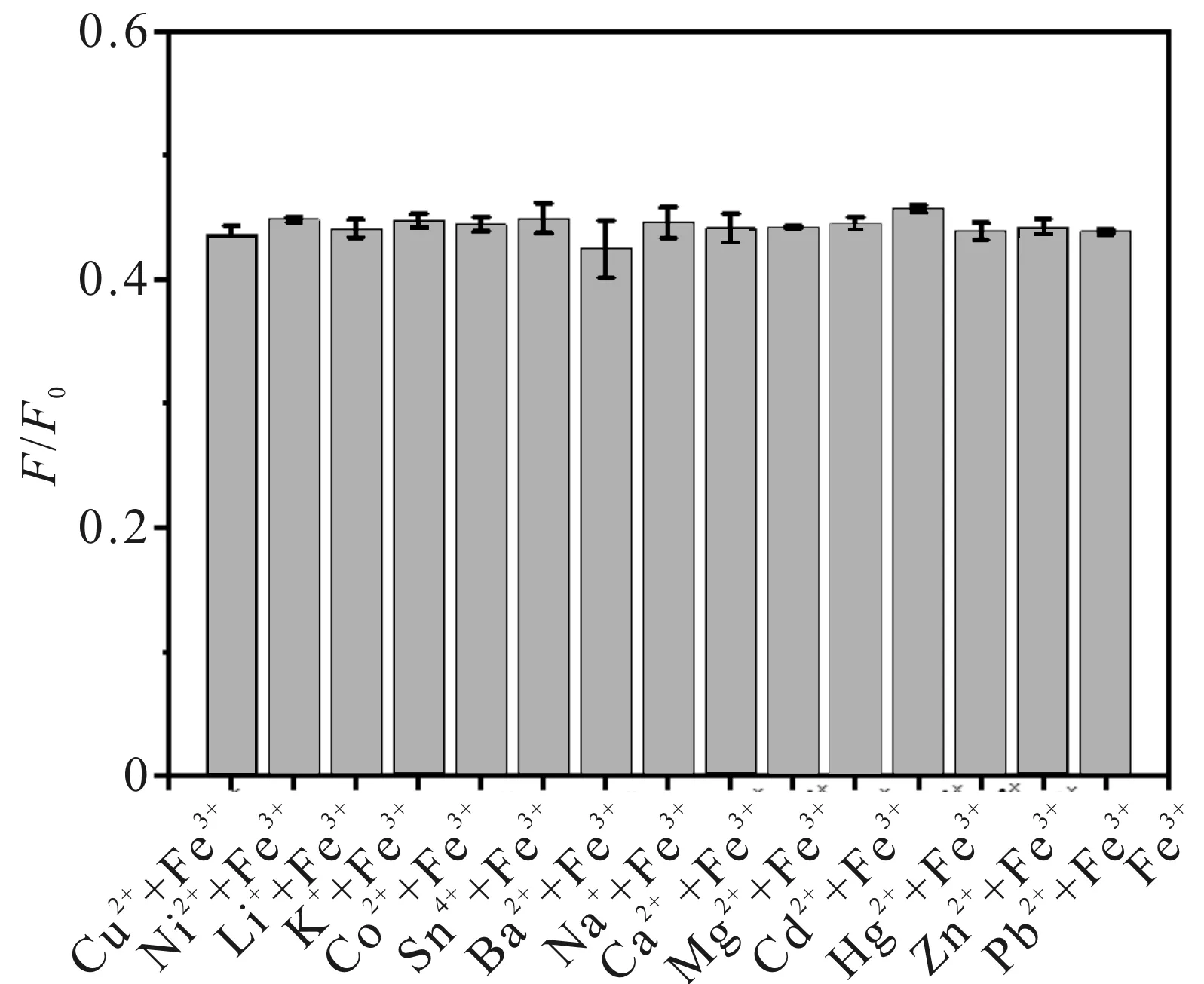
图12 同时加入干扰离子和Fe3+的荧光强度比值图Fig.12 Fluorescence intensity ratio in the presence of interfering ion and Fe3+
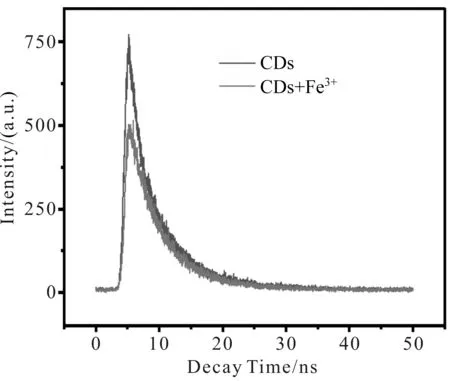
图13 Fe3+加入前后CDs的荧光寿命图谱Fig.13 Fluorescence lifetime before and after addition of Fe3+
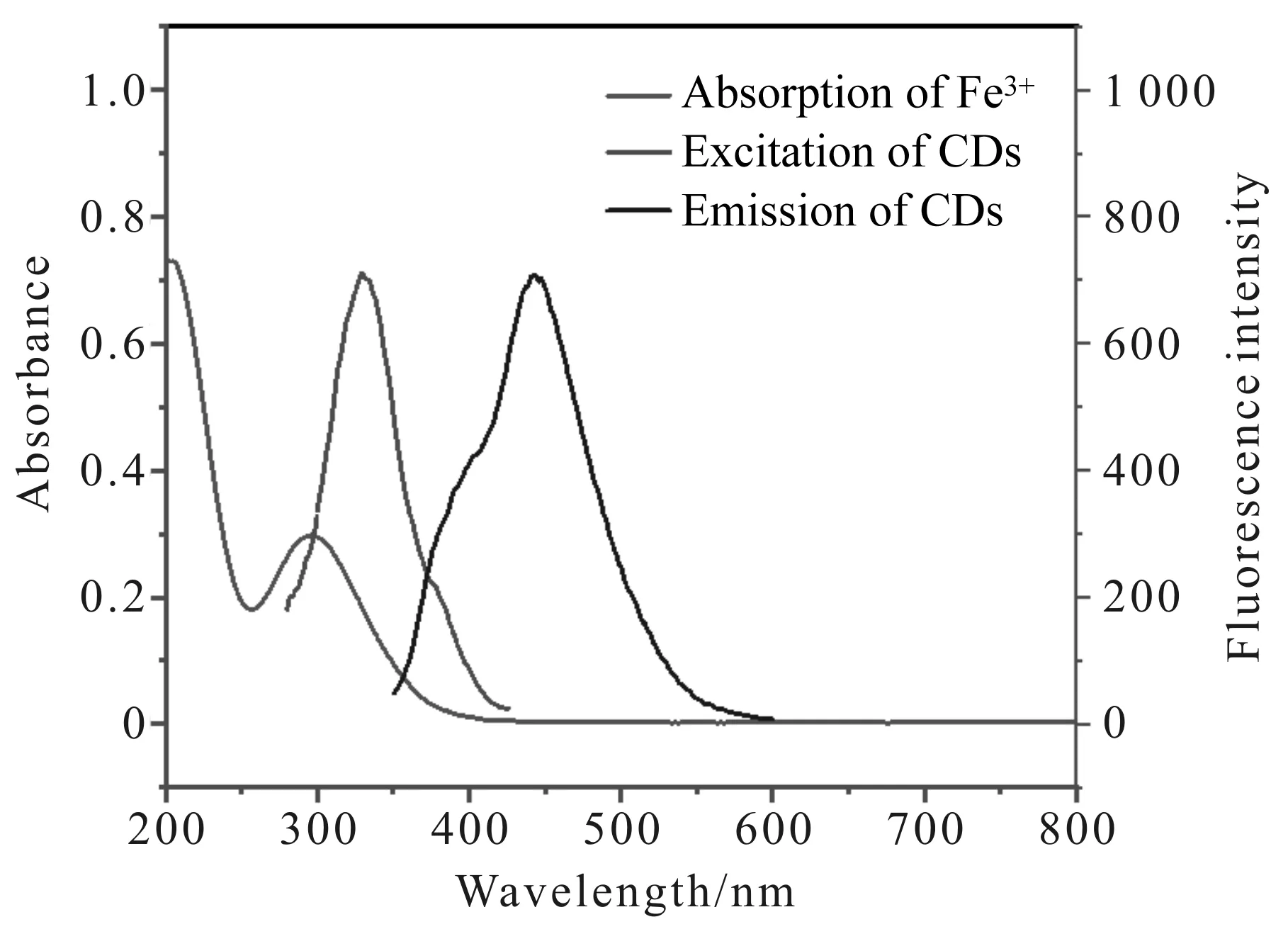
图14 Fe3+的吸收光谱、CDs的激发和发射图谱Fig.14 The absorption spectrum of Fe3+, excitation and emission spectra of CDs
2.3.3 线性相关性与检出限测定
由图15、图16可知,CDs的荧光强度随Fe3+浓度的降低而降低.分析数据得知,Fe3+浓度在1~80 μM (图17)和80~200 μM(图18)范围内与荧光强度呈线性响应.线性方程分别为F=672.793 6-2.473 6C铁离子(R2=0.994 1)和F=574.079 0-1.327 8C铁离子(R2=0.991 4),具有较高的灵敏度.根据检出限的计算公式(3Sbl/S,其中Sbl为空白样品多次测定的标准偏差,S为线性方程的斜率),可得Fe3+的检出限为0.65 μM.显然,利用该CDs检测Fe3+的方法,具有较低检出限和较宽线性范围的优点,且简单方便.
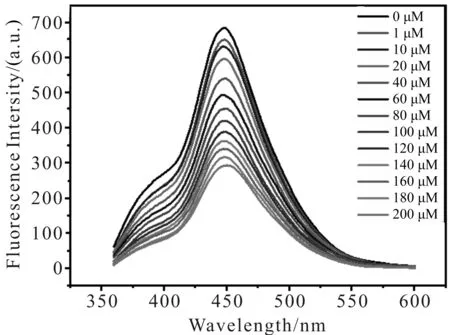
图15 不同浓度Fe3+存在下CDs的荧光图谱Fig.15 Fluorescence spectra of CDs in the presence of various concentrations of Fe3+
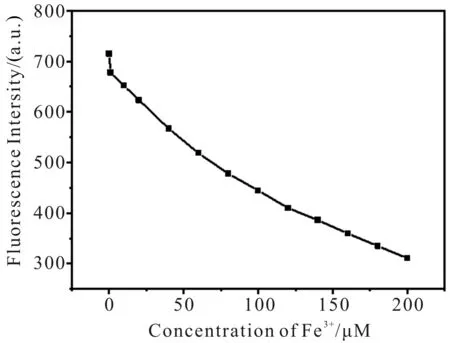
图16 Fe3+与荧光强度关系图Fig.16 The relationship between fluorescence intensity and the concentration of Fe3+
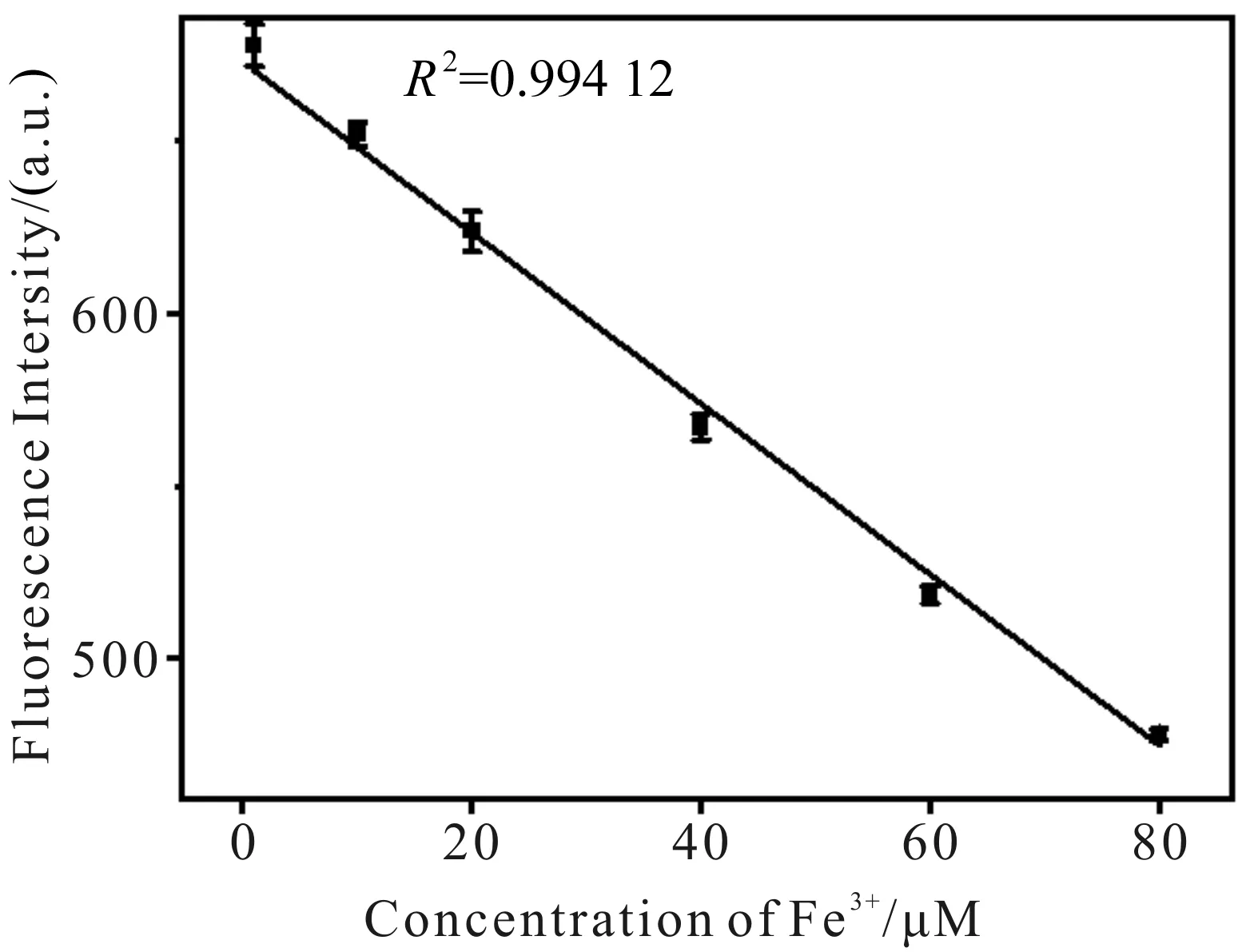
图17 1~80 μM时Fe3+和荧光强度的线性关系Fig.17 The linear detection range for Fe3+at 1~80 μM
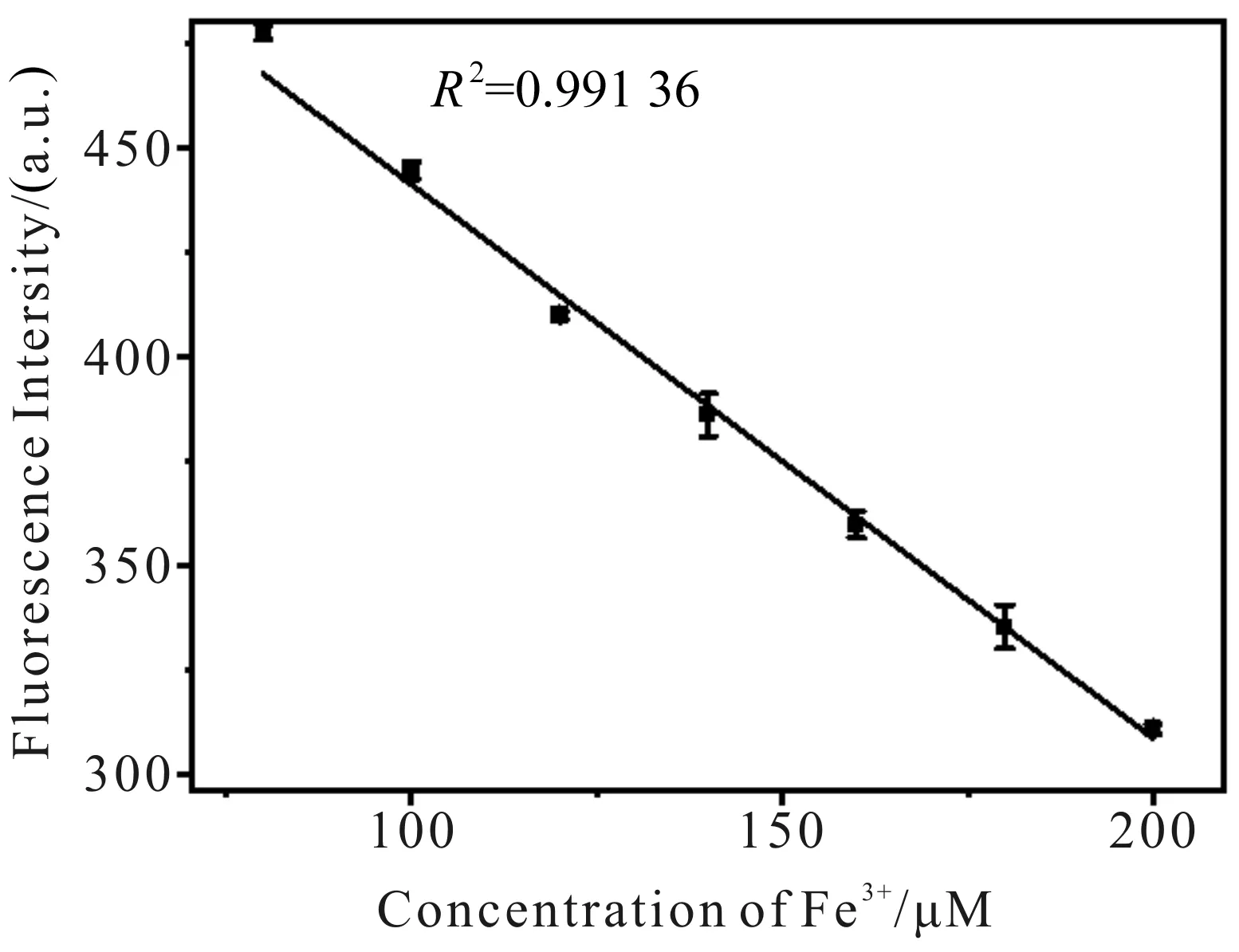
图18 80~200 μM时Fe3+和荧光强度的线性关系Fig.18 The linear detection range for Fe3+ at 80~200 μM
2.3.4 实际样品检测
为测试该方法的准确性和实用性,本研究将测试方法应用到实际样品测量中,包括自来水和湖水.所有样品经静置和过滤后除去悬浮颗粒,取1 500 μL实际样品、1 470 μL pH 5.0缓冲溶液与0.05 mg/mL CDs混合,其荧光强度与单独pH 5.0缓冲溶液相比无明显差距,说明实际样品对测定没有干扰.分别加入40、80、200 μM 标准Fe3+,回收率在91.4%~95.4%之间,证明该方法的适用性很强,能够推广到实际样品的检测中.
2.4 AA检测
2.4.1 时间优化
前期研究发现,Fe3+可以猝灭CDs的荧光.进一步研究发现,在已经发生荧光猝灭的溶液中加入AA后,CDs的荧光强度得到了恢复.这是因为AA具有很强的还原性,能将Fe3+还原为Fe2+,而Fe2+不能猝灭CDs的荧光.研究反应时间与荧光强度恢复程度的关系发现,反应3 min后,进一步延长反应时间,荧光强度几乎保持恒定,表明AA与CDs和Fe3+的反应达到平衡.因此,本研究选择3 min作为定量检测的反应时间.
2.4.2 线性相关性与检出限检测
如图19所示,CDs的荧光强度随着AA浓度的升高而升高.根据分析数据得知,AA浓度在0~220 μM内与荧光强度呈线性响应(图20).线性方程为F=277.788 8+1.529 1CAA(R2=0.993 8),灵敏度较高.将平行测量得到的具体数值代入检出限的计算公式,可得到AA的检出限为0.74 μM.
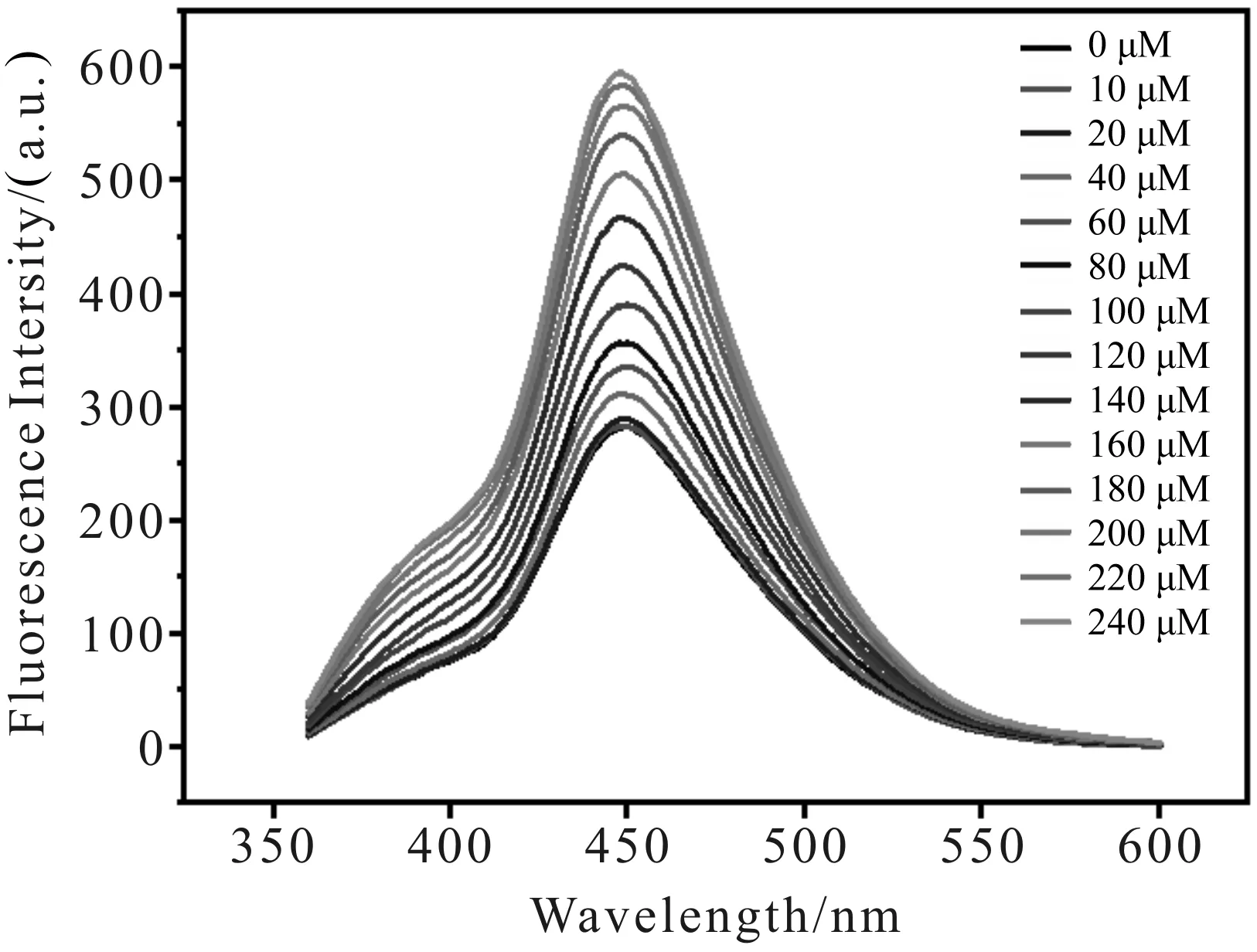
图19 不同浓度AA存在下CDs的荧光图谱Fig.19 Fluorescence spectra of CDs in the presence of various concentrations of AA
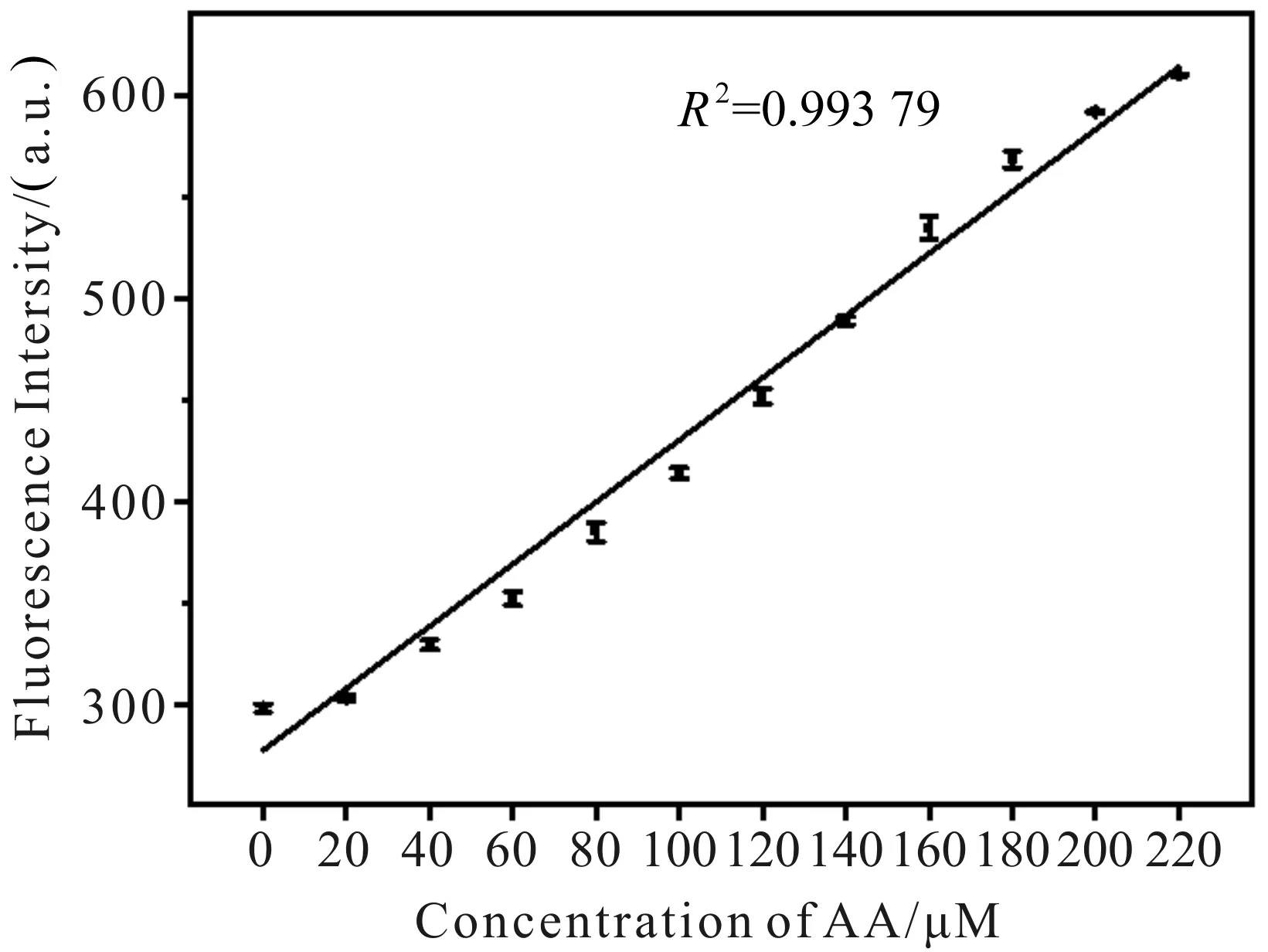
图20 AA浓度与荧光强度线性关系Fig.20 The linear relationship curve between fluorescence intensity and the concentration of AA
2.4.3 干扰物质检测
关于AA对荧光强度恢复的选择性实验,可以通过引入干扰物质(GSH、Cys、Glu、UA、DA)来验证.将浓度为220 μM 的GSH、Cys、Glu、UA、DA溶液加入0.05 mg/mL已被200 μM Fe3+猝灭的CDs溶液中,结果发现(图21),AA可使荧光强度大幅恢复,Cys对CDs荧光强度有小幅恢复,其他物质对CDs荧光强度的恢复并无明显影响.将终浓度为220 μM 的AA溶液加入上述干扰物质溶液中,结果发现(图22),其荧光强度均升高,且升高的程度与只加AA时无明显差别.由此证明,其他物质对CDs荧光强度的恢复无显著影响,AA对CDs荧光强度的恢复具有极高的选择性.众所周知,AA可与Fe3+发生氧化还原反应,把Fe3+氧化为Fe2+,使荧光恢复.这间接证明了只有Fe3+可使CDs发生荧光猝灭,Fe2+不能使CDs发生荧光猝灭.
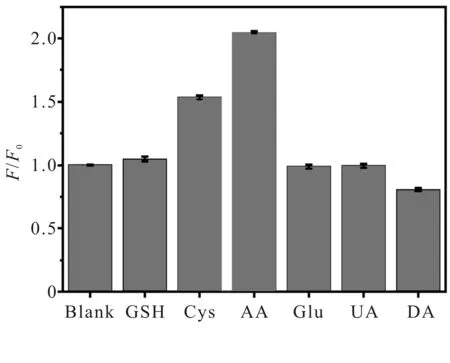
图21 不同物质对CDs荧光强度的恢复图Fig.21 Effects of the fluorescence recovery of CDs by different substances
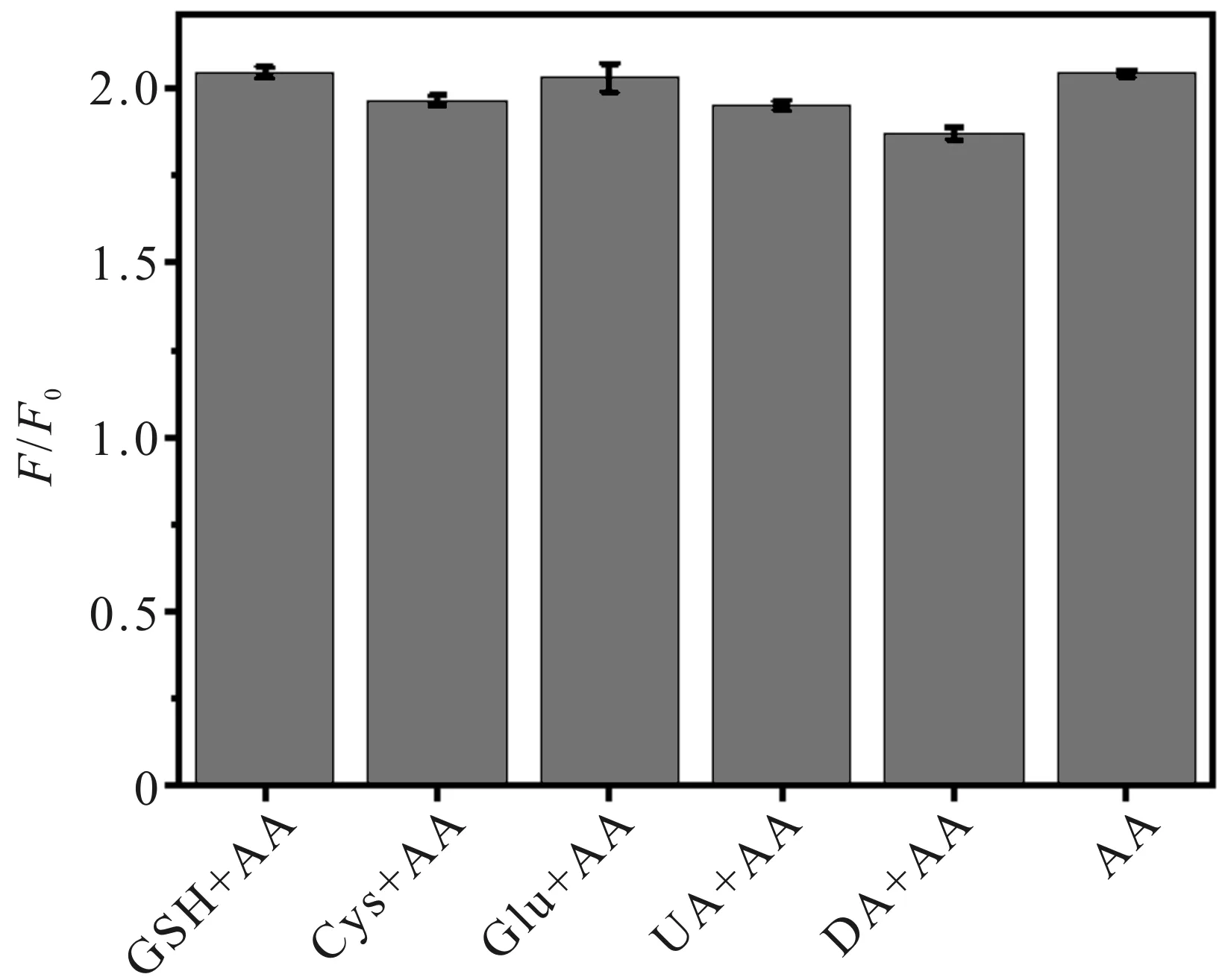
图22 不同物质对荧光强度恢复的干扰Fig.22 Interference of different substances on the fluorescence recovery of CDs
2.4.4 实际样品检测
为检验该方法的准确性和实用性,将该方法应用到实际样品如牛奶和酸奶的测定中.将所有样品经静置和过滤后除去悬浮颗粒,取300 μL实际样品、2 670 μL pH 5.0缓冲溶液与0.05 mg/mL CDs混合,荧光强度与纯pH 5.0缓冲溶液相比无明显差距.这说明在实际样品中不存在同类物质的干扰.在实际样品中分别加入50 μM、100、200 μM AA后,测其荧光强度.结果显示,回收率为84.2 %~106 %,RSD小于6.05%.由此说明,该方法可灵敏地检测实际样品中的AA,具有较好的应用前景.
3 结 语
以龙柏枝叶作为前驱体,利用水热法一步制备CDs.结果发现,Fe3+能猝灭该CDs的荧光,且具有很好的特异性.据此,可建立灵敏的Fe3+浓度检测传感器,并将其应用到实际的样品检测中.AA可使发生荧光猝灭的溶液恢复荧光.利用这一特点可建立快速的AA浓度检测传感器,并将其应用到实际样品的检测中.实验证明,该方法可以连续高灵敏度、高选择性地检测Fe3+和AA.
