微波消解-电感耦合等离子体发射光谱(ICP-OES)法测定生物质中的碱金属和碱土金属
2022-03-23王树加陈晓丽关进安陈佩丽苏秋成
王树加 陈晓丽 关进安 陈佩丽 付 娟 苏秋成
(中国科学院 广州能源研究所,广州 510640)
生物质作为一种环境友好,成本实惠,直接或间接取之植物光合作用的一种绿色生物可再生生物能源,越来越受到各国政府开发和利用的重视[1]。生物质含量丰富,地球上每年存储的生物质遍布各地,主要包括生物秸秆和农作物废料[2],林业和林木加工废料、城市生活垃圾[3],人畜粪便、水生植物等[4]。随着国际社会对环境保护、能源保障安全的提出,加快开发可再生生物能源是国际社会普遍共识,对于缓解能源危机及环境问题有着重要的意义。生物质是一种清洁燃料,氮硫含量较低,灰分含量也少,因此对环境的影响也小。然而碱金属和碱土金属AAEMs(Alkali and Alkaline Earth Metallic Species)[5]K、Na、Ca和Mg元素是生物质中最富含的元素,对其开发利用过程中产生较大的影响。一方面,燃烧过程中,AAEMs会与相关的化合物发生反应[6],形成聚团、烧结、沉积等现象[7],部分AAEMs会粘附在换热器等表面,造成设备腐蚀,给生产带来不利[8]。另一方面,在某些过程中AAEMs可以作为催化剂,对生物质的热转化过程起到催化作用,即使是少量的AAEMs加到纤维素中,也能够减少碳氢化合物的产率[9]。通过对生物质内强催化剂AAEMs的不同,减少预处理方法可以提高木质素纤维素左旋葡萄糖的产率,以及从软木中最大限度地生产糖和超细木质素颗粒[10]。生物质内不同形态的K、Na、Ca和Mg元素都可以降低样品的热解活化能,去除掉这些AEMs后,大大提高活化能,而且这些影响着生物质热解特性,其中Ca元素可以影响热解过程中焦的生成,Mg元素影响热解失重形式[11]。因此,研究生物质中AAEMs含量的分析方法,对后续生物质的开发利用具有重要的意义。
测量K、Na、Ca和Mg含量元素主要的仪器有原子吸收光谱法[12-13]、X射线荧光光谱(XRF)法[14]、离子色谱(IC)法[15 ]和电感耦合等离子质谱(ICP-MS)法[16]。原子吸收光谱法由于分析速度慢,不能同时分析多元素,X射线荧光光谱存在矿物效应,制备标准样品复杂等特点,离子色谱存在分析时间长等都不是首选的分析仪器。电感耦合等离子体(ICP)是一种优越的发射光源,它给原子发射光谱法(AES)带来了很多的发展空间[17-19]。利用ICP-OES测K、Na、Ca和Mg含量已有相关的文献报道[20],但生物质来源广泛,样品成分复杂,共存元素干扰多,目前还没有对其测定干扰的相关研究。因此,亟需针对伴生元素对K、Na、Ca和Mg含量分析测定干扰进行研究,建立多元素共存时ICP-OES精准测定生物质AAEMs的分析方法。
1 实验部分
1.1 主要仪器
Optima 8000电感耦合等离子体发射光谱(美国PerkinElmer公司),Multiwave PRO 微波消解仪(奥地利Anton Paar公司),Milli-Q Synergy超纯水系统(美国Millipore公司),BHW-09A16 电热板赶酸器(上海博通化学科技有限公司),BSA224S-CW电子分析天平,感量为0.1 mg(德国 Sartorius 公司)。
1.2 主要试剂及标准溶液
硝酸(优级纯)、过氧化氢(优级纯),实验用水为超纯水(18.2 M·cm)。
各元素标准储备溶液,国家有色金属及电子材料分析测试中心。
灌木枝叶成分分析标准物质GBW07603(GSV-2):青海省锡铁山铅锌矿区。
1.3 实验方法
1.3.1 微波消解方法
称取0.10 g(精确至0.000 1 g)生物质样品于微波消解罐中,加入4 mL HNO3+1 mL H2O2然后按微波消解程序:5 min功率爬坡至600 W,保持功率600 W 5 min,5 min功率爬坡至1 200 W,保持功率1 200 W 15 min,最后冷却到70 ℃。冷却后取出消解罐,将消解液转移到容量瓶里面,用去离子水多次冲洗消解管转移到容量瓶并定容备用。
1.3.2 样品测定
用ICP-OES分别测定标准工作溶液和处理好的溶液,仪器工作条件如表1所示。

表1 PE Optima 8000 工作参数
2 结果与讨论
2.1 样品前处理条件优化
分别使用3 mL HNO3+1 mL HCl和4 mL HNO3+1 mL H2O2两种处理方法对生物质样品按上面消解程序进行微波消解前处理,发现两种酸的混合体系进行消解都能把样品消解完全,本程序的微波消解最高温度均能达到230 ℃左右,由于盐酸体系会导致挥发性的次氯酸、氯气、氯化氢等气体,综合考虑实验过程的环保安全,因此,本实验选择使用4 mL HNO3+1 mL H2O2消解生物质。
2.2 分析谱线波长的选择
通过选择元素周期表中钾、钠、钙、镁的所有谱线进行筛选,钠元素的分析波长有589.592、330.237、588.995、330.298、288.114 nm,钾元素的分析波长有766.49、404.721、769.896 nm,钙元素的分析波长有317.933、315.887、393.366、396.847、422.673、227.546 nm,镁元素可以使用仪器推荐的285.213 nm。先用2 mg/L的钠元素单标准溶液对钠元素分析波长进行准确度的验证,用5 mg/L的钾、钙元素单标准溶液分别对钾、钙元素分析波长进行准确度的验证。测试的相对误差结果如表2所示,由表2可以看出,钠元素的5条谱线中589.592 nm的谱线分析相对误差最小,灵敏度高,干扰小;钾元素的3条谱线中766.49 nm谱线相对误差小,干扰小;钙元素分析谱线中弃掉灵敏度太高的393.366和396.847 nm两条饱和谱线,虽然315.887 nm的谱线相对误差小,但是干扰元素的谱线多,所以本次钾选用317.933 nm谱线;镁元素由于没有干扰,所以选用仪器推荐的谱线。综上分析,钾、钠、钙、镁的分析谱线为766.49、589.592、317.933、285.213 nm。

表2 钠钾钙分析谱线的相对误差
2.3 不同酸体系对测试的影响
分别用1%、2%、5%、10%和20%的硝酸溶液配制1 mg/L的钾、钠、钙、镁混合标准溶液,然后对不同体系的酸进行三次测量取平均值,最后计算回收率。考察了不同类型的酸体系对样品中各待测元素回收率的影响,结果如图1所示。由图1可以看出当采用HNO3(1%)配制的标准系列溶液拟合的标准曲线时,用HNO3(1%)测试时各元素的回收率接近100%,随着待测溶液体系中酸浓度的增加,各元素的回收率逐渐偏大,当体系为20%的硝酸溶液时,各待测元素的回收率在114%~121%,测试结果与参考标准值之间的误差较大,因此待测样品进行分析检测时,要选择接近待测样品酸体系的浓度进行标准曲线点的配制。

图1 不同的酸体系对钾、钠、钙和镁回收率的影响Figure 1 The effect of different acid systems on the recovery rates of K,Na,Ca and Mg.
2.4 共存元素对碱金属碱土金属测定的影响
筛选生物质中常见的Ni、As等15种金属元素,考察了常见金属元素对K、Na、Ca、Mg测定时的影响。首先用标准溶液配制2 mg/L的K、Na、Ca、Mg混合标准溶液,对其进行平行测定 6次,以平均值作为本次测量的真值,同时在相同的仪器条件以及人员条件下,分别配制2 mg/L的K、Na、Ca、Mg混合标准溶液,20 mg/L的Ni、As等15种金属元素,采用本实验研究的谱线对K、Na、Ca、Mg进行测定,每个样品测试6次,取平均结果为最终结果,计算求得的相对误差如图2所示。从图2中实验结果可以看出,当被测样品中碱金属碱土金属K、Na、Ca、Mg浓度为2 mg/L时,生物质中常见15种共存金属元素含量为20 mg/L时,Pb、In、Ti、Mn对Na元素的影响比较大,Al对K元素的影响比较大,As、Cu、Cd对Ca元素的影响比较大,相对误差都超过5%。所有考察元素对Mg的影响不大,相对误差都小于5%。因此,当生物质样品中有高含量的Pb、In、Ti、Mn四种元素或其中一种的时候,测量钠元素时需要考虑共存元素干扰;当生物质样品中含有高含量Al时,测量钾元素需考虑共存元素干扰;当生物质样品中含有高含量的As、Cu、Cd三种元素或其中一种时,测量钙元素需考虑共存元素干扰;对于生物质样品中的镁元素,共存元素对其干扰较小,因此测定镁可以忽略其干扰。
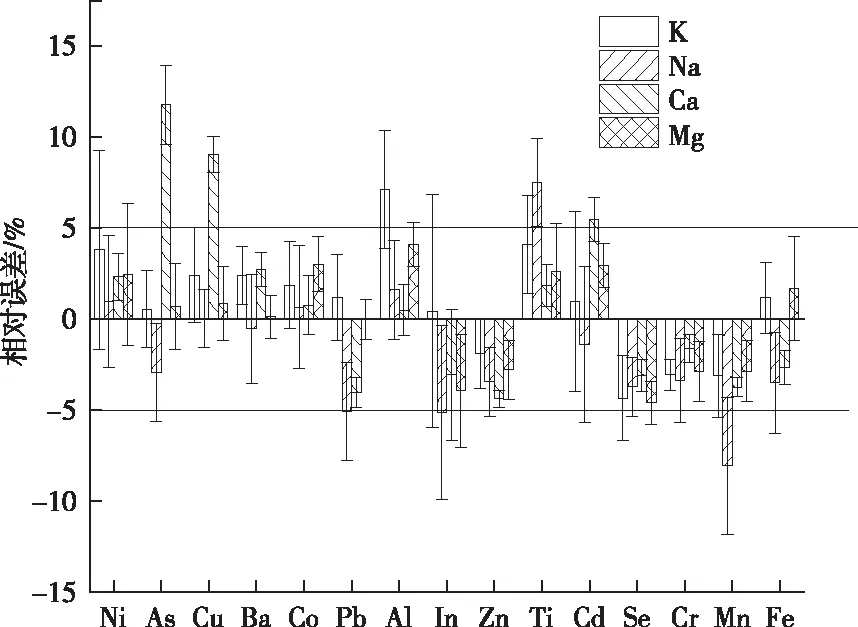
图2 不同共存元素对碱金属碱土金属 测量相对误差影响Figure 2 The influence of different coexisting elements on the relative error of alkali metal alkaline earth metal measurement.
2.5 干扰系数法减少共存元素干扰
分别配制干扰浓度20 mg/L的Mn、Ti、In、Pb为基体的Na标准溶液(2 mg/L),用ICP-OES外标法测得Na的质量浓度,分别求出Mn、Ti、In、Pb对Na的干扰系数;同理,配制干扰浓度20 mg/L的Al为基体的K标准溶液(2 mg/L),以及分别配制干扰浓度20 mg/L的As、Cd、Cu为基体的Ca标准溶液(2 mg/L),按式(1)分别求出Al对K的干扰系数以及As、Cd、Cu各元素对Ca的干扰系数,计算结果见表3。表4列出了当干扰物元素为10 mg/L的时候,用式(2)干扰系数法进行校准后的测量数据,由表4可以看出,干扰系数法可以使各干扰元素对待测元素的误差降低,校准后测量误差在-0.50%~6.65%。
K=C/Cn
(1)
式中:C为干扰元素在分析元素波长处所贡献的浓度,mg/L;Cn为方法研究确定的干扰元素的浓度,mg/L;
C校=C仪-KC干
(2)
式中:C校为经过干扰系数法校正后的元素浓度,mg/L;C仪为仪器测量分析的浓度,mg/L;C干为分析样品中干扰元素浓度,mg/L。
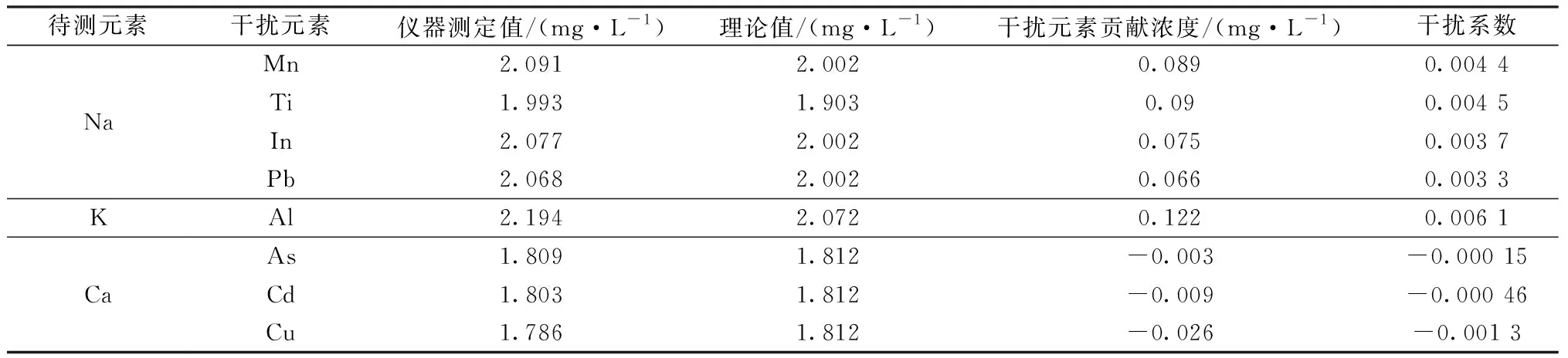
表3 各分析元素不同干扰元素的干扰系数

表4 各分析元素不同干扰元素校准前后误差值
2.6 线性方程及检出限
按照设定的仪器参数条件,对各标准系列浓度点进行测定,以各元素仪器响应信号强度为纵坐标,浓度点为横坐标,进行线性相关拟合。对样品空白进行测量10次,以10次空白强度测定值标准偏差(s)的3倍所对应的浓度作为方法检出限(DL=3s/b,b为斜率)。测定结果如表5所示

表5 工作曲线的波长、线性方程、相关系数和检出限
2.7 质控标准样品的分析
称取3份0.1 g(精确至0.000 1 g)灌木枝叶成分分析标准物质,按照本方法进行样品前处理测定,因标准样品中常见的重金属元素含量较低,所以直接用本研究的碱金属碱土金属谱线进行分析检测,计算3次测定的相对标准偏差,结果见表6。由表6可以看出,各元素测定值与标准参考值一致,相对标准偏差在1.7%~2.9%(n=3),方法回收率在94.3%~106%,说明本研究测试方法适合生物质样品检测。
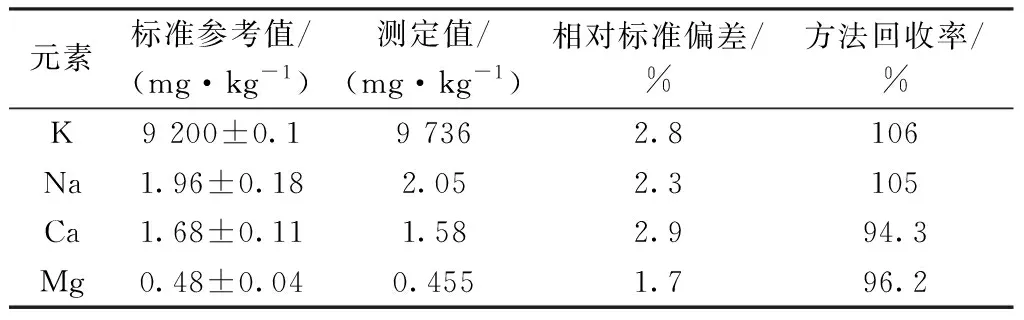
表6 标准物质分析结果
2.8 样品精密度和准确度实验
分别处理6份0.10 g(精确至0.000 1 g)的玉米芯和西瓜皮样品,经过微波消解,定容至20 mL,按实验方法的仪器测量参数进行测试,并计算其平均值和相对标准偏差,结果见表7;同时另取3个测试样品,分别对其中加入等体积10 mg/L的钾钠钙镁混合标准溶液,进行加标回收率实验,结果见表8。由此可见,玉米芯各元素的精密度为0.98%~1.9%,加标回收率为80.2%~106%;西瓜皮的各元素精密度为0.91%~2.3%,加标回收率为85.3%~106%。说明本实验的方法精密度和加标回收率良好。

表7 玉米芯和西瓜皮的精密度实验
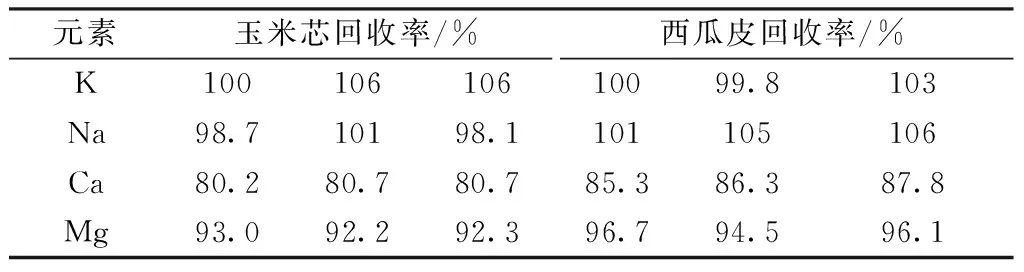
表8 玉米芯和西瓜皮的加标回收率
2.9 比对实验
微量验证样品检测过程中的干扰情况,保证分析数据的准确性,选用过氧化氢消解法对玉米芯和西瓜皮进行样品前处理,并采用离子色谱法和本研究方法对钾、钠、钙、镁进行分析,测定方法数据结果比较采用t检验法,结果如表9所示。查理化表可知,t0.05,5=2.571,由表9可以看出,t试验值 表9 本方法与离子色谱法分析结果的比较 建立微波消解-ICP-OES法测定生物质中常见的碱金属和碱土金属元素K、Na、Ca和Mg等4种元素。通过对分析谱线元素波长的选择,样品消解前后酸体系以及常见共存元素对K、Na、Ca和Mg元素测定干扰的研究,提出了标准曲线酸体系和样品分析体系尽量一致以及干扰系数法可以降低共存元素对分析的干扰。通过对玉米芯和西瓜皮样品进行重复性实验以及加标回收率实验,验证了该分析方法的精密度和准确度,采用国家标准参考物质GBW07603(GSV-2)灌木枝叶成分进一步分析验证了该分析方法的准确性,通过t检验法对该实验方法和离子色谱法测定进行对比,验证了该方法的准确可靠性。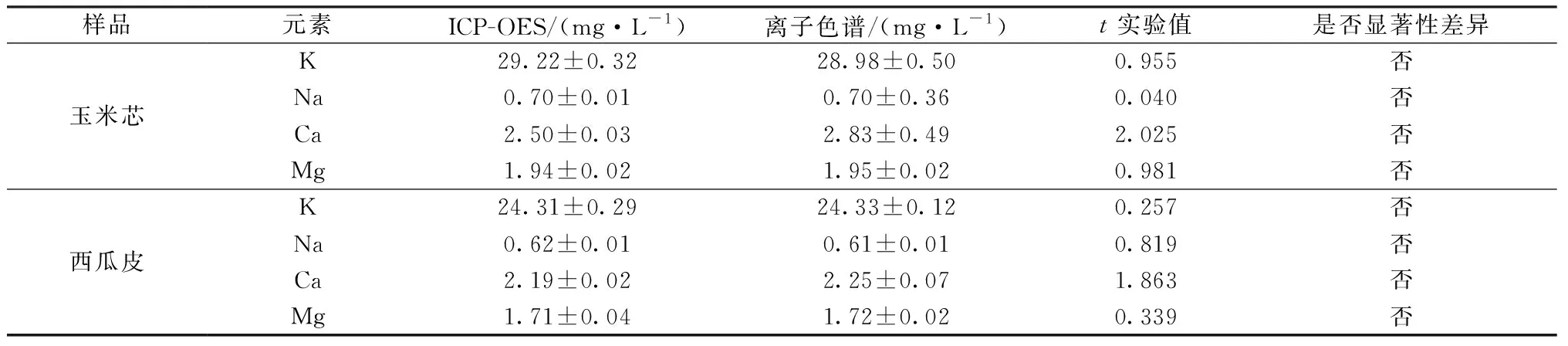
3 结论
