单一屋尘螨与双螨变应原免疫治疗的安全性分析*
2022-03-23刘书楠傅远瑜曾小丽周维康
蒲 西,周 薇,曾 越,刘书楠,傅远瑜,曾小丽,李 双,田 静,周维康△,曾 丹▲
(1.西南医科大学附属医院皮肤科,四川泸州 646000;2.重庆市人民医院过敏反应科 400010)
过敏性疾病影响着患者社会生活、睡眠、学习和工作,已经成为全球健康问题[1]。变应原特异性免疫治疗(AIT)作为过敏性疾病一线治疗方案,是目前唯一有可能通过免疫调节作用改变过敏患者免疫机制及自然进程的治疗方法[2]。基础和临床研究均证实了AIT治疗过敏性疾病的有效性和安全性,但其最大缺点是在治疗过程中可能发生过敏反应,严重的全身不良反应可出现过敏性休克,威胁患者生命安全。由于AIT的方案各不相同,且受地区、环境、人种的影响,不同研究报道的全身不良反应发生率也有很大差异[3]。变应原提取物、治疗方案和伴随的疾病/药物、注射后观察时间不足等都可能成为全身不良反应发生的危险因素[4]。
尘螨(HDMs)是我国最常见的吸入性变应原,HDMs的两个主要种类是屋尘螨和粉尘螨,大多数HDMs过敏患者对这两种变应原都是共同致敏的,HDMs也是引起过敏性鼻炎(AR)和过敏性哮喘的重要原因[5-6]。目前市面上有多种脱敏制剂可供选择,其中单一屋尘螨(100%屋尘螨疫苗)与双螨(50%粉尘螨、50%屋尘螨混合制剂)变应原注射液使用最为广泛。WHO认为,当患者同时对两种存在交叉反应的变应原过敏时,选取单一变应原制剂或两种变应原混合制剂进行AIT,其长期疗效没有显著差异[7],故在选择脱敏制剂时,安全性就显得极为重要。本研究通过观察对比在重庆市人民医院过敏反应科使用单一屋尘螨与双螨变应原注射液的尘螨脱敏患者在治疗过程中的不良反应,分析可能与不良反应发生的相关因素,了解其安全性。
1 资料与方法
1.1 研究对象
患者来自2016年1月至2020年1月就诊于重庆市人民医院过敏反应科的尘螨过敏患者。根据AR及其对哮喘的影响(ARIA)指南[8],经过敏专科医生诊断为过敏性疾病且为AIT适应证患者,所有患者血清屋尘螨特异性IgE(sIgE)检测均高于0.7 ku/L(2级以上,CAP Pharmacia,Uppsala,Sweden),皮肤点刺试验呈阳性反应(风团直径至少3 mm;ALK,Hørsholm,Denmark)且症状评分为中重度。
1.2 方法
单一屋尘螨变应原注射液的皮下脱敏患者,使用丹麦ALK-ABELL公司生产的标准化屋尘螨变应原疫苗(Alutard SQ),按照常规皮下脱敏方案进行治疗。起始阶段有4种浓度:1号瓶100 SQ-U/mL、2号瓶1 000 SQ-U/mL、3号瓶10 000 SQ-U/mL、4号瓶100 000 SQ-U/mL,维持阶段浓度为100 000 SQ-U/mL。使用双螨变应原注射液的皮下脱敏患者采用德国默克集团Allergopharma公司生产标准化双螨变应原疫苗(NHD),按其常规皮下脱敏方案进行治疗。起始阶段有3种浓度,1 号瓶50 TU/mL、2号瓶500 TU/mL、3号瓶5 000 TU/mL,维持阶段5 000 TU/mL。起始治疗阶段每周上臂外侧皮下注射疫苗1次,连续治疗至维持治疗阶段,维持阶段一般是每4~6周注射1次。如注射时出现较重的局部不良反应或全身不良反应,则根据过敏专科医生评估减量或按上次注射剂量重复注射1次。患者须在注射前0.5~2.0 h口服氯雷他定片,每次注射前需完善呼气峰值流速(PEF)并记录,观察患者注射部位皮肤情况,每次注射后,患者须在科室观察30 min,并再次完善峰流速,对比注射之前的数值以避免发生气管痉挛,以防止不良反应的发生。若患者发生不良反应,则需详细记录不良反应情况。
脱敏治疗前患者完善皮肤点刺试验(SPT)、sIgE、总IgE(tIgE)的检测,根据点刺试验判断患者是否多重敏感,屋尘螨sIgE≥17.5 ku/L被认为是强致敏反应。本研究已获得重庆市人民医院伦理委员会的批准[伦审(科研)第S2020-115-01],并通过免除知情同意书申请。
1.3 不良反应
按照欧洲变态反应和临床免疫学学会(EAACI)不良反应判定标准由专业人员对不良反应进行判断[9]。不良反应分为局部和全身不良反应,局部不良反应主要包括注射部位局部皮肤瘙痒、红晕、肿胀、硬结、坏死等。全身不良反应分为5级,0级:无症状;Ⅰ级:轻度全身不良反应,局限性荨麻疹、鼻炎或轻度哮喘(PEF较基线下降小于20%);Ⅱ级:中度全身不良反应,发生缓慢(>15 min),出现全身荨麻疹和(或)中度哮喘(PEF下降20%~40%);Ⅲ级:严重(非致命)的全身不良反应,发作迅速(<15 min)出现全身荨麻疹、血管性水肿或严重哮喘(PEF下降大于40%);Ⅳ级:过敏性休克,迅速出现全身瘙痒、潮红、红斑、全身荨麻疹、喘鸣(血管性水肿)、哮喘发作、低血压休克等,需要抢救治疗。Ⅴ级:死亡。注射后30 min内发生为即刻反应,30 min后为延迟反应。
1.4 统计学处理
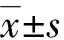
2 结 果
2.1 纳入患者基本情况
本研究共纳入单一屋尘螨组AIT患者64例,双螨组AIT患者50例。单一屋尘螨AIT患者,男35例,女29例;平均开始治疗年龄(21.0±11.5)岁;tIgE为238.0(101.0~480.0)ku/L,sIgE为31.4(18.0~87.3)ku/L,sIgE/tIgE为(14.8±7.6)%;47例患者为sIgE强致敏;46例患者为变应原多重敏感;22例患者合并有过敏性哮喘。双螨AIT患者中,男32例,女18例;平均开始治疗年龄(20.0±12.7)岁;tIgE为399.5(172.0~648.0)ku/L,sIgE为43.3(10.2~83.5)ku/L,sIgE/tIgE为(12.4±7.3)%;37例患者为sIgE强致敏;40例患者为变应原多重敏感;14例患者合并有过敏性哮喘。两组患者基本情况差异均无统计学意义(P>0.05)。
2.2 单一屋尘螨和双螨发生不良反应情况及对比
64例单一屋尘螨AIT患者共接受2 726次注射,40例患者共出现过局部不良反应120次;其中有26例患者共发生96次AIT全身不良反应,76次(79.17%)为Ⅰ级反应,17次(17.71%)为Ⅱ级反应,仅有3次(3.09%)为Ⅲ级反应;另外,96次全身不良反应中,77次(80.21%)为即刻反应;起始阶段发生不良反应42次,其中34次(80.95%)是在注射4号瓶浓度期间,54次发生在维持阶段。50例双螨AIT患者共接受1 534次注射,18例患者共出现过局部不良反应48次;有8例患者共发生过13次全身不良反应,Ⅰ级反应5次(38.46%),Ⅱ级反应2次(15.38%),Ⅲ级反应6次(46.15%);另外,13次全身不良反应中,即刻反应11次(84.62%);有4次发生在起始阶段注射期间,均为3号瓶浓度,9次发生在维持阶段,见表1。

表1 不良反应发生情况
2.3 全身不良反应的具体症状
单一屋尘螨AIT患者全身不良反应临床表现主要为咳嗽咳痰、胸闷和鼻部症状,其中1例患者在注射后出现3次胃部不适。 而值得注意的是双螨AIT患者中,出现局部或全身荨麻疹症状最为常见。大部分患者给予雾化吸入糖皮质激素和短效β2受体激动剂后可得到缓解,见表2。
2.4 不良反应发生的危险因素
性别、tIgE、sIgE、sIgE/tIgE、sIgE强致敏、敏感状态、伴哮喘史与发生全身不良反应无显著相关性,单一屋尘螨AIT患者中,儿童(P=0.010)、局部不良反应(P=0.049)与全身不良反应发生有相关性,见表3。进一步对年龄(儿童)、性别(男)、sIgE(强致敏)、多重敏感 (多敏)、诊断(伴哮喘)、伴有局部不良反应等因素进行logistic回归分析发现,儿童是单一屋尘螨AIT患者发生全身不良反应的危险因素(OR=3.927,P=0.011),对其全身不良反应的发生有预测价值;局部不良反应(OR=4.200,P<0.001)是双螨AIT患者发生全身不良反应的危险因素,其他因素未发现相关性。
2.5 发生全身不良反应的时间分布
单一屋尘螨AIT发生全身不良反应月份分布较广泛,主要集中在5-7月(34.40%),其次在10-11月(24.00%);在双螨AIT的全身不良反应中,5-7月(46.20%)和11月(23.10%)为全身不良反应高发时期,见图1。

表2 全身不良反应的具体表现[ n(%)]

表3 发生全身不良反应与未发生全身不良反应患者的差异
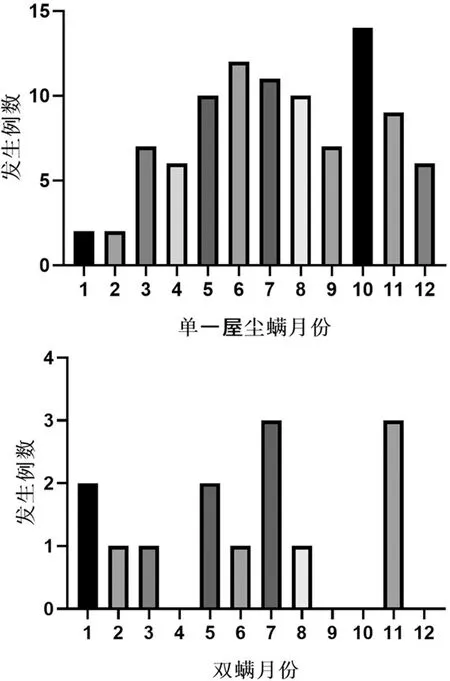
图1发生全身不良反应的时间分布
3 讨 论
AIT在我国已有50多年的应用历史,基础和临床研究均证实了其有效性及安全性,但因为可能会出现严重的过敏反应,引起了患者和过敏专科医生高度关注。尽管这2种HDMs变应原制剂已经在临床试验中证明了它们的有效性和安全性,但通常是与安慰剂或甚至自我对照组进行比较[10-12],两者安全性进行对比的研究较少。一项对比单一屋尘螨和双螨AIT儿童AR疗效的研究中认为使用这两种疫苗进行AIT,其长期疗效并没有实际上的差别[13],故在选择脱敏制剂时,两种脱敏制剂的安全性就显得极为重要。
在本研究中,单一屋尘螨AIT全身不良反应发生率(40.63%)远高于双螨(16.00%),其中以Ⅰ级反应为主(79.17%)。此前一项对129例中国尘螨患者使用单一屋尘螨AIT的调查中,其全身不良反应发生率为43.40%[14],与本研究结果相近。本研究中双螨AIT虽然较少发生全身不良反应,但更易发生严重的过敏反应,Ⅲ级反应发生率为0.39%,13次全身不良反应中有6次为Ⅲ级反应(46.15%),其发生Ⅲ级反应的概率约为单一屋尘螨的4倍。一项纳入217例使用双螨AIT患者的研究中,Ⅲ级及以上全身不良反应率为0.43%[15],与本研究结果相似。本研究统计结果中,单一屋尘螨AIT患者全身不良反应症状以鼻部症状和哮喘发作为主,双螨AIT患者以局部或全身荨麻疹症状为主,与之前研究结果相似[16-17];另一项使用双螨AIT患者的研究中,全身不良反应症状则主要以鼻部症状为主[18]。在注射后应特别注意观察患者症状,特别是双螨治疗患者,一旦患者出现全身不良反应早期症状和体征,就应警惕是否发生了严重的过敏反应,提前做好抢救措施。
在两者的相同点上,单一屋尘螨和双螨AIT患者均超过80%为即刻反应,且即刻反应往往比延迟反应更为严重,故在注射后观察30 min是极为重要的,这需要患者的积极配合,须告知患者其重要性。本研究结果显示在起始阶段发生的全身不良反应易发生在注射最高浓度瓶号期间,单一屋尘螨起始阶段发生的全身不良反应中80.95%发生在4号瓶期间,双螨起始阶段全身不良反应均发生在3号瓶期间,此前研究也发现在最高浓度注射期间易发生全身不良反应[19-20]。因此,在患者进行高浓度瓶号注射前需做好安全评估,注射后严密观察。
本研究结果显示,单一屋尘螨AIT的患者,儿童(OR=3.927,P=0.011)是其发生全身不良反应的危险因素;双螨AIT患者发生过局部不良反应(OR=4.200,P<0.001)的患者更易发生全身不良反应。此前的研究中,使用单一屋尘螨AIT的研究也提出全身不良反应在儿童中比在成人中更常见[14]。考虑患儿可能对过敏原更敏感,对过敏原提取物的耐受性较低,容易过敏,且患儿在注射时更易紧张,医师及家长应对患儿进行心理疏导及健康教育指导。本研究结果表明,局部不良反应是发生全身不良反应的预测因子,这与之前许多研究的结果相一致[11,21]。还有研究认为发生过大局部不良反应的患者可能会增加未来发生全身不良反应的风险[22]。但也有研究报道局部不良反应不能预测全身不良反应[23],因此目前关于局部不良反应是否能预测全身不良反应的发生尚无定论。EAACI过敏原免疫治疗指南建议如果注射部位出现扩大的局部不良反应[直径大于10 cm的红色和(或)肿胀],过敏专科医师可酌情调整下一次注射的给药方案,当局部不良反应发生时,可以使用H1-抗组胺药物来减少局部不良反应的频率和严重程度(A级推荐),但这种预防性治疗不能预防以后全身不良反应的发生[24]。局部不良反应是否是全身不良反应发生的危险因素,还需要进一步研究评估研究。但在临床治疗过程中,对于发生过局部不良反应的患者,过敏专科医生应予以更多的观察,并对患者做好安全教育。
在本研究中,5-7月、10-11月发生全身不良反应频率较高。一项中国的流行病学调查显示,气候因素可能通过对当地过敏原的影响间接影响过敏性疾病患病率,重庆地区最主要的过敏原为尘螨[25],且重庆地处盆地,空气湿润,5-7月、10-11月时降雨量大,给尘螨繁殖提供了良好的环境,这可能是导致该时间段不良反应发生率较高的原因。在梅雨潮湿季节应提醒患者做好防护措施,尽量减少过敏原的接触。
哮喘一直被认为是全身不良反应发生的关键危险因素,特别是失控的哮喘显然与严重甚至致命的全身不良反应有关[3]。但在本研究中未发现其相关性,这可能与本研究纳入的患者哮喘症状较轻,且哮喘均已控制有关。同时本研究也没有发现性别、tIgE、sIgE、sIgE/tIgE、sIgE强致敏、敏感状态与发生全身不良反应发生的相关性。
皮下脱敏患者全身不良反应的发生与多种因素相关,故在治疗前对患者自身情况进行详细了解,对患者脱敏治疗的安全进行评估,以及对患者的严格管理,细心指导显得极为重要,这需要过敏专科医生和患者共同参与。
本研究存在一些局限性,由于为回顾性研究,病例数量较少,得出的结论可能存在误差,目前关于单一屋尘螨和双螨AIT的安全性研究较少,因此要探究AIT不良反应的危险因素还需要更多大样本、多中心的研究。
综上所述,单一屋尘螨AIT发生全身不良反应发生率较双螨高,但双螨AIT更易发生严重过敏反应;全身不良反应大部分为即刻反应,在最高浓度瓶号注射期间更易发生;儿童为单一屋尘螨AIT全身不良反应的危险因素;局部不良反应为双螨AIT全身不良反应的危险因素;梅雨潮湿季节为尘螨过敏患者全身不良反应的高发期。
