复方苦参注射液联合奥希替尼治疗T790M突变型非小细胞肺癌的临床疗效及安全性
2022-03-20吕齐法杨小琼
江 山,吕齐法,李 辉,杨小琼
(1.都江堰市人民医院呼吸与危重医学科,四川 成都 611830;2.南昌大学附属第四医院呼吸与危重医学科,江西 南昌 330000;3.西南医科大学附属医院呼吸与危重医学科,四川 泸州 646000)
肺癌是发生于支气管腺体或黏膜的恶性肿瘤,发生率为19.90%,严重影响国民健康[1]。其中85%为非小细胞肺癌(NSCLC),是肺癌中最常见的类型。然而NSCLC早期无明显症状,确诊时多丧失手术机会,且经过第一代表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKIs)治疗后产生获得性耐药,T790M突变率为60%,第三代EGFR-TKIs奥希替尼是治疗临床NSCLC晚期T790M突变的首选方案,可有效延长患者生存期[2-3]。然而临床证据表明,奥希替尼治疗过程中间质性肺炎致死率达4%,且腹泻及皮疹等毒副作用较第一代EGFR-TKIs明显,降低了患者的医疗效果[4]。因此优化以奥希替尼为基础的药伍方案,降低毒副反应,对提高临床NSCLC的治疗效果具有重要意义。苦参注射液是含有生物碱和黄酮类物质的复方药物,可提高机体免疫力,减少放化疗期间患者的毒副反应,广泛应用于临床癌症的辅助治疗[5]。然而复方苦参注射液联合奥希替尼治疗T790M突变型 NSCLC的报道较少,故本研究针对T790M突变型NSCLC的临床患者,探究复方苦参注射液联合奥希替尼的临床疗效和安全性,旨在为临床应用提供参考。
1 资料与方法
1.1一般资料:连续纳入2017年4月~2020年12月本院以及西南医科大学附属医院呼吸与危重医学科确诊的T790M突变型 NSCLC患者80例,本次研究经过本院医学伦理委员会同意。纳入标准:①经影像学及病理学资料确诊为 NSCLC者;②一代EGFR-TKIs治疗后影像学资料提示疾病进展者;③基因学检测提示T790M突变(EGFR第20号外显子发生错义突变)者;④心肝肾功能正常,且耐受化疗者;⑤可评价的靶病灶≥1个。排除标准:①合并其他部位原发性肿瘤者;②基因学检测提示合并C797S突变;③存在免疫系统疾病者;④流动人口且随访困难者。将采用奥希替尼治疗纳入对照组(38例),采用复方苦参注射液联合奥希替尼治疗的纳入观察组(42例),其中对照组男25例,女13例;年龄29~77岁,平均(63.34±7.83)岁。观察组男31例,女11例;年龄30~76岁,平均(64.73±6.92)岁。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2治疗方法:对照组患者均采用甲磺酸奥希替尼片(批准号:H20170167,阿斯利康制药有限公司)口服治疗,剂量为80 mg/次·d。观察组在对照组的用药基础上加用复方苦参注射液(批准号:Z14021231,山西振东制药股份有限公司)静脉滴注治疗,12 ml/次·d。两组患者均安排定期门诊或病房复诊,通过影像学资料跟踪患者疾病的进展情况。
1.3疗效指标
1.3.1近期疗效评价:两组患者分别接受不同方案治疗28 d后,采用美国肿瘤放射治疗协作组编制的临床肿瘤疗效评价标准[6]评价近期疗效。标准如下:完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。疾病控制率(DCR)=(CR例数+PR例数+SD例数)/总例数×100%,客观缓解率(ORR)=(CR例数+PR例数)/总例数×100%。
1.3.2远期疗效评价:采用首次无进展生存时间(PFS-1)评价T790M突变型NSCLC治疗的远期疗效。PFS-1定义为:患者接受奥希替尼治疗至病情首次出现进展的时间。
1.4安全性评价
1.4.1免疫指标评价:两组患者分别于治疗前及治疗28 d后,抽取患者空腹静脉血2 ml,采用Ficoll密度梯度离心得到外周血单核细胞,用CD4+及CD8+的流式抗体标记,然后采用流式细胞仪检测CD4+和CD8+数值。
1.4.2毒副反应评价:记录两组患者在治疗过程中腹泻、皮疹、恶心纳差、骨髓移植以及间质性肺炎等毒副反应的发生情况。采用世界卫生组织抗肿瘤药物毒副反应分级标准[6-7]评价两组患者治疗过程中毒副反应,该标准分为0~Ⅵ级,分级越低提示毒副反应越轻。

2 结果
2.1近期疗效:观察组患者DCR(78.95% vs 90.48%)以及ORR(34.21% vs 66.67%)与对照组相比均显著增加,差异有统计学意义(P<0.05)。见表1。

表1 患者近期临床效果的比较[n(%)]
2.2远期疗效:随访过程中两组患者均未存在失访者。由Kaplan-Meier 曲线发现对照组患者中位PFS-1为12个月,试验组患者中位PFS-1为12个月,二者PFS-1比较,差异无统计学意义(Log-rank检验:χ2=0.023,95%CI:0.668~1.606,P>0.05)。见图1。
2.3免疫系统指标结果:治疗前两组患者的CD4+、CD8+以及CD4+/CD8+计数差异无统计学意义(P>0.05),治疗后观察组与对照组相比CD4+计数升高,CD8+计数降低,CD4+/CD8+比值升高,二者具有统计学意义(P<0.05)。见表2。
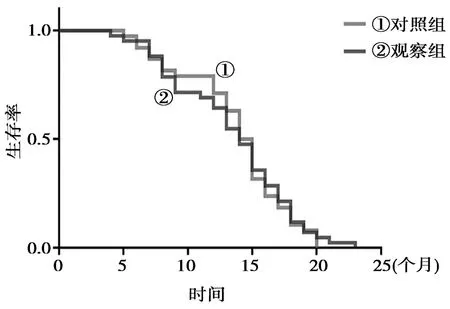
图1 患者无进展生存时间比较(个月)

表2 患者治疗前后T淋巴细胞亚群变化比较
2.4毒副反应比较:治疗期间观察组患者腹泻、皮疹、恶心纳差、骨髓抑制以及间质性肺炎等毒副反应的发生情况与对照组相比显著降低(P<0.05),而Q-T间期延长的发生情况与对照组差异无统计学意义(P>0.05)。见表3。观察组患者治疗期间毒副反应分级与对照组相比显著降低,差异有统计学意义(P<0.05)。见表4。
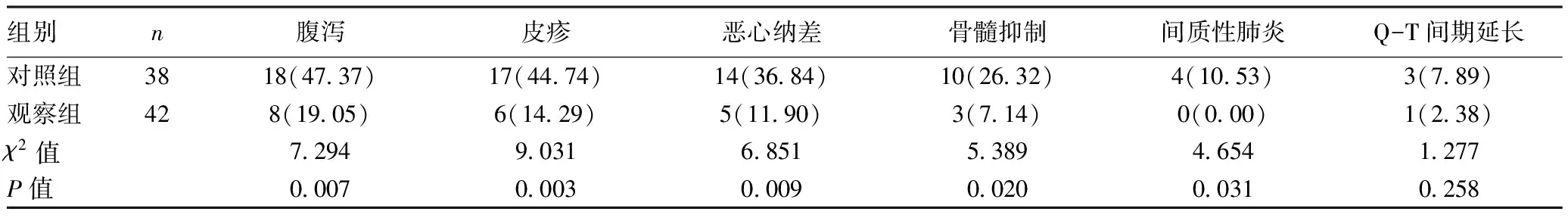
表3 患者毒副作用比较[n(%)]
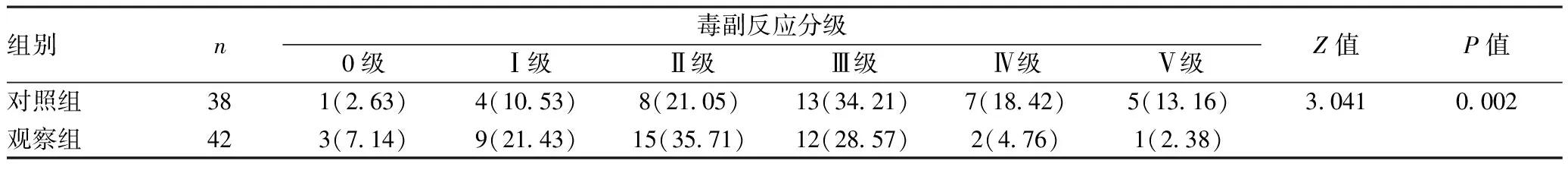
表4 患者毒副反应分级[n(%)]
3 讨论
以EGFR-TKI为基础的靶向药物是晚期NSCLC精准治疗的主要方法,奥希替尼作为第三代EGFR-TKI,可通过与T790M突变的EGFR基因催化域进行不可逆的结合,阻断EGFR同源二聚化和EGFR下游信号的表达,促进癌细胞降解[7-8]。Ⅲ期临床试验表明奥希替尼治疗T790M突变患者的PFS(中位PFS为10.1个月),相比传统铂类化疗(中位PFS为4.4个月)显著延长[4]。而本研究中发现奥希替尼治疗T790M突变型NSCLC的中位PFS为12个月,这与王洁等[4]研究较为一致。提示奥希替尼在治疗T790M突变型NSCLC具有积极的临床效果。然而不可否认的是,奥希替尼在有效控制疾病进展的同时,大量临床证明奥希替尼的毒副反应十分明显,腹泻发生率高达47%,约有32%患者出现3级及以上的毒副反应,7%的临床患者因毒副反应而被迫停药[9]。因此优化药伍,降低治疗毒副反应,是提高奥希替尼治临床应用效果的重要研究课题。
复方苦参注射液是由苦参和白土苓等中药提炼合成的具有降低癌症治疗期间毒副反应,加强临床治疗效果的中成药[10]。本研究中采用复方苦参注射液联合奥希替尼治疗T790M突变型NSCLC发现患者DCR以及ORR均增加,提示联合用药的近期临床疗效显著,可迅速抑制肿瘤的发生发展,缓解临床症状。结合有关文献发现复方苦参注射液中的苦参碱以及脱氢苦参碱等活性成分可作用于肿瘤细胞核酸序列,将肿瘤细胞阻滞在G0/G1期,抑制其向M期分化,达到抑制肿瘤细胞增殖的临床效果[11]。而张小文等[12]则发现复方苦参注射液可通过抑制PI3K/Akt通路,发挥诱导肿瘤细胞凋亡的药理作用。但是在本研究的随访过程中,发现两组患者的PFS-1无显著差异,提示复方苦参注射液作为辅助用药,在短期内控制NSCLC的进展,提高近期临床疗效的同时,无法延长患者的远期疗效。
CD4+和CD8+细胞是机体监视并杀伤肿瘤细胞的主要免疫细胞。研究表明NSCLC化疗期间CD4+/CD8+比值下降,提示T淋巴细胞免疫功能失调,机体免疫力降低[13]。本研究与段哲萍等[14]人研究一致。这提示复方苦参注射液对于维持化疗期间机体免疫水平具有重要作用。同时本研究发现复方苦参注射液联合奥希替尼可减轻T790M突变型NSCLC治疗期间的毒副反应,对于防止因毒副反应而减药或被迫停止治疗具有积极的临床意义,因此提高机体免疫力,降低毒副反应也是复方苦参注射液联合奥希替尼增强T790M突变型NSCLC 近期疗效的潜在原因。查阅相关报道发现复方苦参注射液具有激活CD4+细胞的增殖,增强机体免疫功能,同时具有清热解毒、凉血立湿之功效[15],在肺癌、肝癌以及乳腺癌等辅助用药中均具有减毒增效的作用[16]。
综上所述,本研究针对临床T790M突变型NSCLC患者,发现复方苦参注射液联合奥希替尼可提高患者的近期疗效,提高化疗期间的免疫功能,减轻化疗期间的毒副反应,具有积极的临床效果和安全性。
