神经内镜与显微镜下经鼻蝶垂体瘤切除术治疗垂体瘤近期疗效的对比
2022-03-20秦小春
秦小春,贾 琦,游 洪,刘 祺
(石河子大学医学院第一附属医院神经外科,新疆 石河子 832000)
垂体瘤是发生于垂体前叶、后叶与颅咽管上皮残余细胞处的内分泌性肿瘤,以往的流行病学统计报道显示其人群发生率约为1/10万,发病率仅次于脑胶质瘤和脑膜瘤[1]。垂体瘤是一种良性肿瘤,经积极治疗后可获得良好的预后[2]。其主要治疗方法有药物治疗、手术治疗和放射治疗,其中手术治疗是垂体瘤患者的优先选择方案,大部分垂体瘤患者选择经鼻蝶垂体瘤切除术治疗[3-4]。随医疗技术、微创技术和影像技术日趋发展,神经内镜[5]及显微镜下[6]经鼻蝶垂体瘤切除术治疗均得到了较好的发展,两者各有各的优势、劣势。有关两种方式对垂体瘤患者的具体疗效一直存在争议。本研究通过比较神经内镜与显微镜下经鼻蝶垂体瘤切除术治疗垂体瘤近期疗效,以期为临床垂体瘤患者的治疗提供参考。
1 资料与方法
1.1一般资料:回顾性选取2016年1月~2020年12月本院收治的垂体瘤患者72例的临床资料,本研究已经过本院医学伦理委员会同意。纳入标准:①满足2015年中国垂体腺瘤外科治疗专家共识制定的诊断标准患者[7];②循证医学评估符合手术指征者,择期给予经鼻蝶垂体瘤切除术处理;③术后病理结果均为垂体腺瘤,并均未行其他方案治疗处理。排除标准:①合并垂体瘤卒中、肾上腺占位或甲状腺功能亢进患者;②服药所致高泌乳素血症患者;③复发性垂体瘤或存在远期失访风险患者;④鼻腔鼻窦严重感染者;⑤存在凝血功能障碍者;⑥合并精神疾患者。根据手术方式的不同将患者分为对照组(n=32,显微镜下)和研究组(n=40,神经内镜),其中对照组男15例,女17例,年龄19~74岁,平均(52.25±5.38)岁;病程1~24个月,平均(6.28±5.11)个月;肿瘤最大直径1.0~3.8 cm,平均(2.49±0.27)cm。研究组男22例,女18例,年龄22~75岁,平均(53.45±4.97)岁;病程1~24个月,平均(6.25±5.20)个月;肿瘤最大直径1.1~3.7 cm,平均(2.42±0.35)cm。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2方法:术前3 d连续口服泼尼松片(TID),患者手术之前均清洁鼻腔,剪除鼻毛。
1.2.1对照组:给予显微镜下经鼻蝶垂体瘤切除术治疗,患者取仰卧位,常规气管插管全身麻醉,碘伏纱布消毒面部,碘伏棉片消毒鼻腔,铺单。Hardy扩张器扩张术侧鼻孔直抵蝶窦前壁,扩张鼻道,撕裂蝶窦前壁与鼻中隔根部转折处黏膜,显微镜下找到蝶窦开口,剥离黏膜后暴露骨性开口与前壁,将蝶窦前壁凿除,咬除蝶窦分隔,去除蝶窦黏膜,鞍底喉部凿开鞍底,穿刺针穿刺鞍内,十字切开鞍底硬膜,用垂体瘤钳、刮匙及吸引器清除肿瘤,切除肿瘤后可用明胶海绵或止血纱填塞瘤腔,复位骨性鼻中隔与黏膜,用油砂条或纳吸绵填塞鼻腔。
1.2.2研究组:给予神经内镜经鼻蝶垂体瘤切除术治疗,患者取仰卧位,常规气管插管全身麻醉,碘伏纱布消毒面部,碘伏棉片消毒鼻腔,铺单。右侧鼻腔入路,在内镜直视下逐步进入鼻腔,从蝶窦开口内上缘,用直镰状刀弧形切口鼻黏膜,用枪状剪刀剪开鼻黏膜和蝶窦黏膜的连接部分,显露蝶窦前下壁和骨性鼻中隔。磨除蝶窦前壁形成1.5 cm左右骨窗,开放蝶窦腔,刮除黏膜暴露鞍底,置入30°内镜确认蝶窦腔内骨性隆起。穿刺针穿刺鞍内,抽吸排除动脉瘤,切除肿瘤的顺序应先从前下切向后下,再从后上到前上,切除肿瘤后鞍内明胶海绵止血,生物胶和人工硬膜封闭鞍底,用油砂条或纳吸绵填塞鼻腔。
1.3观察指标:①观察两组术中出血量、术后住院时间;②比较两组术中出现脑脊液漏的概率以及术后并发症发生情况,包括颅内感染、电解质紊乱及术后脑脊液漏;③于术前、术后1周检查视野平均缺损(MD)和视力等;④观察两组患者术后1周的临床疗效情况。其中优:临床症状均显著好转,肿瘤全部或基本消失;良:肿瘤细胞减少>50%,临床症状有一定的改善;可:临床有轻微的改善,肿瘤细胞较治疗前可减少>20%;差:临床症状与治疗前后无变化或者出现恶化。优良率=(优例数+良例数)/总例数×100%[8]。

2 结果
2.1两组优良率比较:研究组优良率明显高于对照组,差异有统计学意义(P<0.05)。见表1。
2.2两组术中出现脑脊液漏的概率以及术后并发症发生情况比较:研究组术中脑脊液漏的概率低于对照组,差异有统计学意义(P<0.05),两组术后并发症总发生率组间比较,差异无统计学意义(P>0.05)。见表2。
2.3两组手术前后视野情况比较:两组术前MD、视力组间比较差异无统计学意义(P>0.05),两组术后1周MD均较术前下降,视力较术前升高,差异有统计学意义(P<0.05),研究组术后1周MD低于对照组,视力高于对照组,差异有统计学意义(P<0.05)。见表3。
2.4两组围术期指标比较:研究组术后住院时间短于对照组,术中出血量少于对照组,差异有统计学意义(P<0.05)。见表4。

表1 两组优良率对比[n(%)]
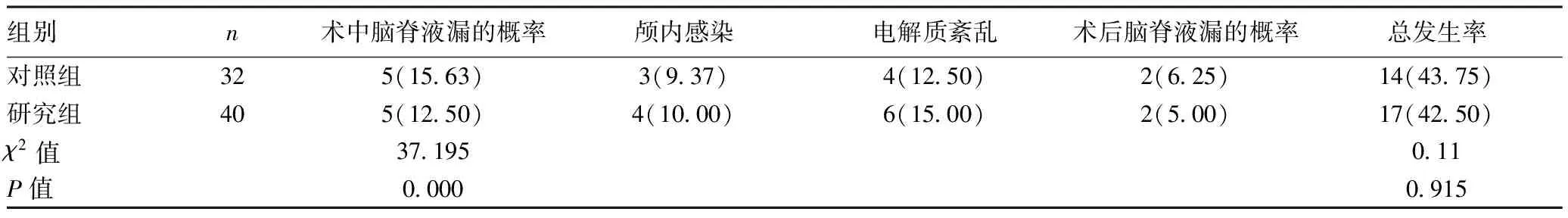
表2 两组术中出现脑脊液漏的概率以及术后并发症发生情况对比[n(%)]

表3 两组手术前后视野情况对比

表4 两组围术期指标对比
2.5相关案例分析:入院后行显微镜下经鼻蝶垂体瘤切除术治疗。见图1。入院后行神经内镜下经鼻蝶垂体瘤切除术治疗。见图2。

术前垂体MRI平扫
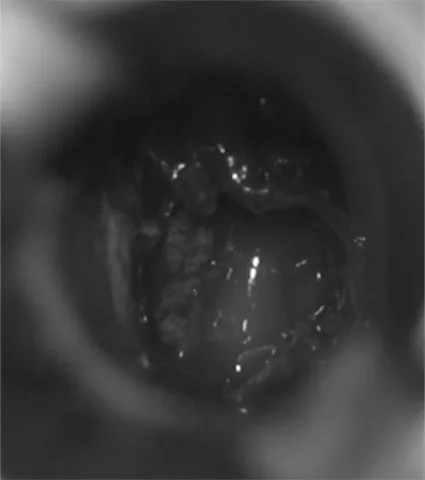
术中显微镜
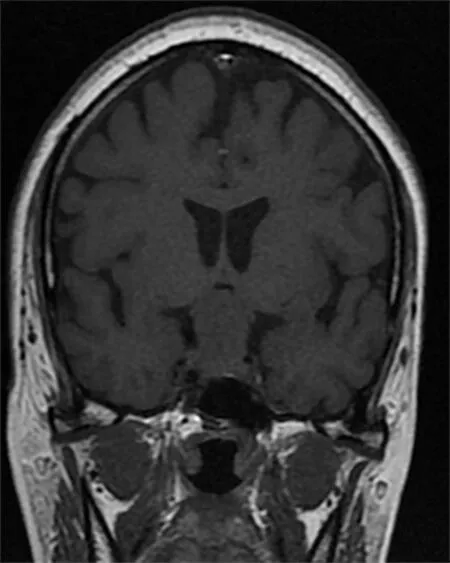
术前垂体MRI平扫

术中内镜
3 讨论
垂体腺瘤是一种分泌型肿瘤,目前临床上仍然以药物、手术以及放疗为主。然而,放疗的并发症较多,故逐渐被弃用;部分患者常常对药物反应不佳,故也多为辅助医治手段,因此,手术已成为主流方案[9-10]。以往的外科手术包括开颅手术[11]、经鼻蝶垂体瘤切除术[12]等,其中经鼻蝶垂体瘤切除术拥有恢复快、创伤小与并发症少的特点,深受患者与临床工作者的欢迎,在这之中以显微镜下和神经内镜下手术为主。但是,这两种手术入路方法各有优缺点。
显微镜下经鼻蝶垂体瘤切除术的优势在于:显微镜下提供的是三维视野,可增强术者双侧视野空间立体感[10]。也与常见手术类似,术者在显微镜下可以双手操控器械,有利于及时彻底止血,这些是神经内镜下单手较难完成的动作[13]。此外,显微镜下手术操作开展较早,手术操作已较为成熟,学习曲线时间短,有大量丰富的临床经验可供借鉴[14]。而显微镜下操作的缺点则在于:显微镜下需使用鼻窥器,对鼻中隔以及黏膜损伤较大,术中出血较多[15]。此外,显微镜为管形视野,对于瘤腔及毗邻组织无法做到完整细致的观察,容易出现肿瘤组织切除不干净以及脑脊液漏等[16]。神经内镜经鼻蝶垂体瘤切除术治疗的优势则在于:神经内镜下可以360°全方位观察,具有视野广以及照明清晰广角照明和全景视野等特点;同时,该类手术术中还可以调节内镜在术区的位置,进一步调节术野的距离,也可以调整角度镜面,以便于更清晰地观察术区视野[17]。此外,神经内镜体积较小,对鼻中隔、鼻黏膜的损伤相对较小,且不需要联合鼻窥镜进行手术,可较好地保护鼻腔正常结构[18]。然而神经内镜也存在一些缺点,如手术器械是利用人体自然通道进入术区,操作空间相对狭窄,提高了手术难度指数。并且要求术者对解剖结构、操作熟练程度较为苛刻[19-20]。其次,神经内镜成像为二维图像,视野缺乏深度感和立体感,术中若出血会导致视野模糊,止血困难。再次就是神经内镜开展较晚,定位困难,学习曲线相对较长[21-22]。
本研究结果显示,相比于显微镜下经鼻蝶垂体瘤切除术治疗,神经内镜治疗垂体瘤的优良率明显更高,可优化围术期指标,降低术中脑脊液漏的概率,且不增加术后并发症的发生风险。显微镜技术可提供三维图形,可在术中有效止血,但其对鼻腔组织的破坏力也相对较大,出血量相对更多[21]。而神经内镜治疗下,可全方位观察蝶窦内的情况,降低组织受损出血的概率,减少术中出血量,缩短手术时间[23]。同时在神经内镜下,不需要扩张鼻腔,可避免鼻黏膜、鼻中隔受损,减少治疗痛苦,使患者尽快恢复,缩短住院时间,提高其近期疗效[24]。垂体瘤患者常因瘤体压迫神经结构导致视野损害及视力减退,其中MD表示全视网膜光敏感度下降程度,视力表示总体视功能。既往不少研究均证实垂体瘤患者伴有视力与视野损害,且其视野损害程度与瘤体大小息息相关[25-26]。本研究中,观察组的术后视野功能改善效果明显优于对照组,可能与神经内镜下清除垂体瘤肿瘤组织更为彻底有关。神经内镜镜头照明度良好,灵活性高,准确性更高,可辨认颈内动脉隆起、双侧视神经管与鞍底凹陷,可有效切解决显微镜管状视野无法克服的局限性,具有切除更多瘤体的潜能[27-28]。目前,临床神经内镜手术还无法彻底取代显微镜手术,但是两者优点逐渐融合是趋势,只要通过临床医师扎实的理论知识和系统的训练,再通过集成应用现代高科技技术,神经内镜技术仍将会是显微神经外科主要的发展方向之一。本研究的不足主要在于为回顾性研究,样本量偏小,且未设置随访观察患者远期预后,仍有待进一步的大样本量、前瞻性、多中心研究来论证结论。
综上所述,相比于显微镜下经鼻蝶垂体瘤切除术治疗,神经内镜治疗垂体瘤的优良率明显更高,可优化围术期指标,改善患者视野情况,降低术中脑脊液漏的概率。
