聚对苯二甲酸丁二醇酯切片中游离四氢呋喃含量的测定
2022-03-19薛月霞李顶松
薛月霞,李顶松
(中国石化仪征化纤股份有限公司,江苏 仪征 211900)
聚对苯二甲酸丁二醇酯(PBT)是以精对苯二甲酸和1,4-丁二醇(BDO)为原料聚合而成的一种高聚物,被广泛应用于工程塑料和纺丝领域[1-2]。在PBT生产过程中,由于BDO容易环化生成四氢呋喃(THF), 因此PBT切片中或多或少地夹杂有THF,对下游应用造成一定的影响。在工程塑料领域,PBT切片中的THF会随着加热而部分释放出来,对操作人员的身心健康造成伤害,另外产品中残留的THF又会使工程塑料产品的两个重要指标50%乙醇提取物及3%乙酸提取物超标,不能满足美国食品安全相关标准的规定[3],从而造成产品不合格。在纺丝领域,PBT切片中的THF含量超标同样会影响到下游产品的染色均匀性。因此,近年来PBT切片生产厂家越来越重视对PBT切片中游离THF含量的控制。
目前,测定PBT切片中游离THF含量的方法均为气相色谱法,不同之处在于样品的前处理及进样方式。宋玉玲等[4]报道了用顶空进样气相色谱法测定PBT切片中游离THF含量的方法,该方法要使用顶空进样器,而大多数的PBT生产厂家并没有配备价格昂贵的顶空进样器。苏凤仙等[5]研究了用萃取法处理样品,再用气相色谱测定PBT切片中游离THF含量的方法,但该方法采用水作萃取剂,萃取时间需要5 h左右,且样品还需要人工用剪刀剪碎,操作时间长,且不方便。作者研究了用乙二醇作萃取剂处理样品,再以异丙醇做内标,用气相色谱测定PBT切片中游离THF含量的方法。该方法不需要剪碎样品,萃取时间只要2.5 h,且方法的精密度及加标回收率均能满足要求,可应用于实际生产。
1 实验
1.1 主要试剂
乙二醇:分析纯,国药集团化学试剂有限公司产;异丙醇:色谱纯,国药集团化学试剂有限公司产;四氢呋喃:色谱纯,国药集团化学试剂有限公司产;高纯氮气:纯度大于等于99.99%,自产。
1.2 主要仪器
GC-2014C气相色谱仪:日本岛津公司制;EH35B微控数显电热板:北京莱伯泰科仪器有限公司制;BSA1245电子天平:瑞士梅特勒托利多公司制;TH-500氢气发生器:北京中惠普分析仪器公司制;CP-Sil 8 CB气相色谱柱:美国安捷伦公司制。
1.3 色谱柱及色谱条件
毛细管色谱柱: 50 m×0.32 mm ×1.2 μm。柱温:初始60 ℃,保持5 min,升温速度10 ℃/min,升温至250 ℃,保持10 min。汽化室温度250 ℃,监测器温度250 ℃,N2载气流量1.8 mL/min,H2载气流量30 mL/min,空气流量300 mL/min,尾吹气(N2)流量28 mL/min,进样量0.4 μL,分流比60:1。
1.4 实验方法
1.4.1 配置内标溶液
准确称取1.0 g(准确至0.000 1 g)异丙醇于100 mL容量瓶中,用乙二醇定容至刻度。该溶液内标物浓度为10 mg/mL。
1.4.2 制作标准曲线
(1)准确称取1.0 g(准确至0.000 1 g)THF于100 mL容量瓶中,用乙二醇定容至刻度。该溶液THF浓度为10 mg/mL。
(2) 分别从(1)中移取0.1,0.2,0.3,0.4,0.5,0.6 mL于6个50 mL的容量瓶中,再依次加入0.5 mL的内标溶液,并充分摇匀备用,分别标记为1#~6#标准溶液。
(3)按照设置的气相色谱仪条件,分别测试(2)中的6个标准溶液。
(4)根据色谱分析结果,以THF与内标物的峰面积比为横坐标,以两者的浓度比为纵坐标,绘制标准曲线,见图1。

图1 THF溶液标准曲线Fig.1 Standard curve of THF solution
1.4.3 试样分析
准确称取5.0 g(准确至0.000 1 g)PBT切片样品于100 mL三角烧瓶中,加入20 mL乙二醇,并置于已经提前调整好温度的电热板上,加热回流2.5 h,冷却后取下。用移液管移出10 mL样品溶液于50 mL烧杯中,加入内标溶液0.4 mL,充分摇匀后进行色谱测试。根据THF与内标物的峰面积之比,从工作曲线查得THF与内标物的质量比,按式(1)计算切片样品中THF含量(x)。
x=ymv/wv1×1 000
(1)
式中:y为由标准曲线查得的THF与内标物的质量比;m为加入的内标物的质量;v1为从处理后的溶液中吸取的体积;v为处理样品时加入的乙二醇体积;w为称取的PBT切片样品质量。
2 结果与讨论
2.1 萃取溶剂的选择
THF为极性物质,根据相似相容原理,所以萃取剂应该选择极性试剂。
THF夹杂在PBT高聚物中,必须达到一定的温度,才能使其从PBT高聚物中挥发出来。实验以乙醇为萃取剂考察了THF的分离效果,结果表明,用乙醇沸腾加热回流5 h后, PBT切片中游离的THF被萃取出来的量不到实际含量的一半。这说明甲醇、乙醇等沸点低于水的试剂不适合作萃取剂。综上,本研究选用沸点较高的乙二醇作为萃取剂。
2.2 内标物的选择
萃取剂及待测物THF均为极性物质,要使内标物与萃取剂及待测物THF成为均相体系,内标物必须为极性物质。另外,为使内标物不影响测试结果,内标物不能是样品中含有的组分,按照此原则,本研究选择异丙醇为内标物。
2.3 萃取温度的选择
在不同电热板加热温度下加热回流2.5 h,PBT切片中THF含量测试结果见图2。

图2 不同加热温度下PBT切片的THF含量Fig.2 THF content of PBT chip under different heating temperature
从图2可以看出:温度低于140 ℃,PBT切片中THF含量测试结果随着温度的升高而提高;加热温度在145~160 ℃,测试结果趋于一致;当温度升高至沸腾状态下回流时,测试结果又明显升高。这是因为温度低于140 ℃时,PBT切片中游离THF运动速度慢,不容易从固相转入液相,所以2.5 h内并不能将切片中游离THF完全萃取到液相。而当温度在145~160 ℃时,切片中游离THF运动速度加快,容易从固相转入液相,加热回流2.5 h已经使PBT切片中游离THF完全萃取出来,所以结果趋于一致。但当温度升高至沸腾加热回流(乙二醇沸点197 ℃),测试结果反而升高,这可能是因为温度太高, PBT切片内部发生固相缩聚反应, 其固相缩聚反应的产物BDO和水等小分子从切片颗粒内部扩散出切片[6],BDO在高温下又进一步发生环化失水反应,生成THF,从而使测定结果偏高。所以本研究选用150 ℃作为萃取温度。
2.4 萃取时间的选择
萃取温度150 ℃时,不同萃取时间下PBT切片的THF含量测试结果见图3。
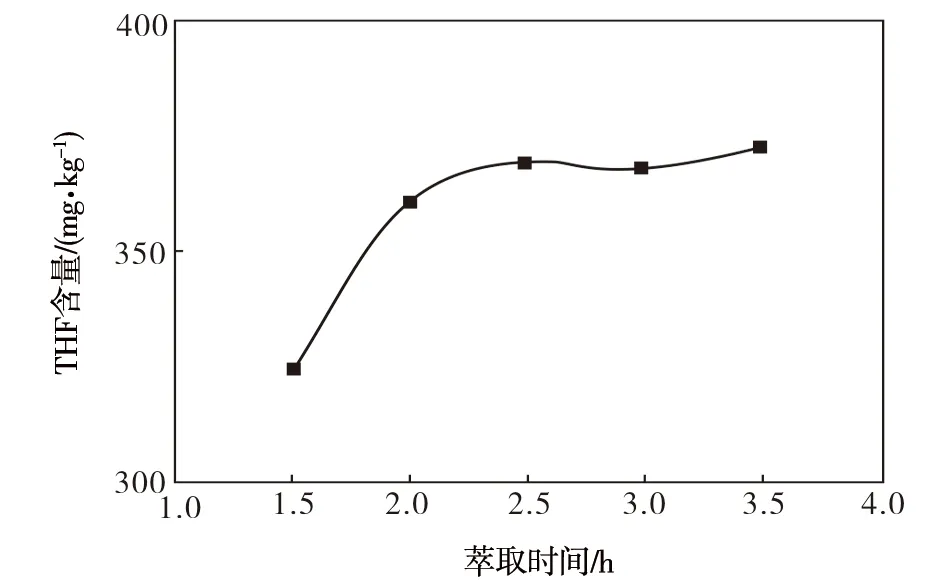
图3 不同萃取时间下PBT切片的THF含量Fig.3 THF content of PBT chip at different extraction time
从图3可知,当萃取温度设置为150 ℃时,萃取时间达到2 h以上,PBT切片中的游离THF可以完全萃取。所以,本研究萃取时间选用2.5 h。
2.5 方法的加标回收率
在已知含量样品中分别加入一定量的THF标准溶液,再按照2.4.3所给定的方法进行测试,结果见表1。

表1 加标回收率分析结果Tab.1 Analysis results of standard addition recovery rate
从表3可知,方法的加标回收率为96.3%~98.6%,满足国家标准规定的对化学分析方法正确度的要求[7],即当浓度水平大于等于100 mg/kg时,加标回收率应满足95%~105%。
2.6 方法的精密度
对同一样品,按照2.4.3所给定的方法测试6次,测定结果见表4。
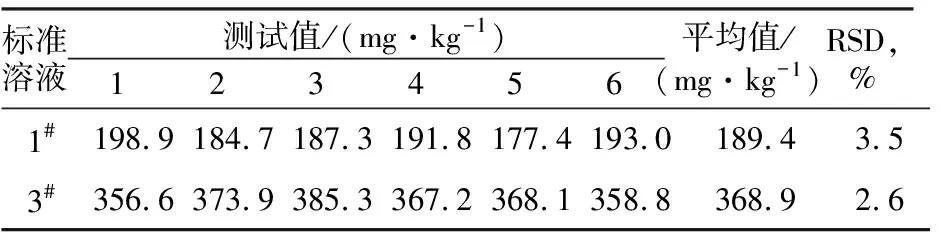
表2 精密度实验结果Tab.2 Precision experimental results
从表4可知,方法的实验室内相对标准变差(RSD)为2.6%~3.5%,满足国家标准[7-8]对化学方法精密度的要求,即在重复次数不小于6次时,被测组分含量在100~1 000 mg/kg,实验室内RSD应满足3.8%~5.3%。
3 结论
a.采用气相色谱仪,选用50 m×0.32 mm ×1.2 μm毛细管色谱柱测定PBT切片中游离THF含量,最佳萃取剂为乙二醇,萃取温度为150 ℃,萃取时间为2.5 h。
b.本方法的加标回收率为96.3%~98.6%,RSD为2.6%~3.5%,均符合国家标准对化学方法的准确度和精密度的要求。与现有的方法相比,本方法不需要使用昂贵的顶空进样器,PBT切片不需要粉碎剪切等复杂的处理操作,具有操作简便、结果可靠等优点,完全可以应用于PBT实际生产中。
