基于传感技术测定空气中氧气的含量
2022-03-17田磊
田磊

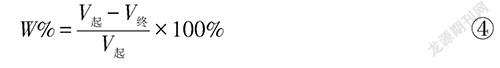

摘要:测定空气中氧气的含量是初中化学的入门级实验,在该实验过程中,在空气中点燃红磷会对空气造成污染,实验中导管内存在的水的体积无法测得。针对这些问题笔者采用数字化传感技术并将原教材中的耗氧剂进行替换,使得测量结果更加精确。
关键词:氧气含量;数字化;传感技术
文章编号:1008-0546(2022)03x-0083-02 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2022.03x.021
一、研究背景
测定“空气中氧气的含量”,是人教版初中化学第二单元课题一“空气的组成”的一个基本实验。教材中的实验是将法国著名科学家拉瓦锡的实验“利用金属汞定量研究空气成分”进行了改进而得到的。但原教材中的实验也存在诸多不足之处,如:在集气瓶外点燃红磷会造成空气污染。如何将这个实验进行优化改进,以达到更加精确地测定氧气含量是我们研究的目的。当前教育时代提倡多学科融合的思想,利用创客教育的开源性能否与化学学科的实验进行有效整合,值得我们去研究。利用python中小学创客教育程序内容,编制温度压强测定程序,进行测定空气中氧气含量,具有一定的可行性。
二、问题提出
通过对近10年中国知网关于“测定空气中氧气含量的实验改进”方案的文章分析可以发现,测定空气中氧气含量的主要分为:燃烧法、铁粉氧化法,常温氧化法。教材中的实验是利用红磷进行燃烧法消耗氧气,这种方法的缺点是在氧气含量低于一定浓度时,红磷会停止燃烧。无法将氧气完全消耗完,而且利用水测量气体消耗的体积,会因水中溶解有部分氧气造成实验误差。
针对以上问题,我们对原教材的实验中存在的问题进行归纳分析,并提出实验改进意见:
1.将原教材中的红磷燃烧替换成利用铁粉氧化的方法;
2.将利用水位变化测定消耗气体的体积改用温度、压强传感器进行测定。
三、实验原理:
1.实验药品与器材
药品:铁粉5.0 g、碳粉0.1 g、氢氧化钠溶液、氯化钠溶液。
器材:锥形瓶、BMP280温度压强传感器、电脑。
2.药品与器材的选择
通过九年级化学第八单元“金属和金属材料”课题3的学习和探究,学生已经知道了铁在潮湿的空气中能与氧气发生反应,利用这个原理可以消耗空气中的氧气,进而进行测定。在初中的学习过程中,对于铁的锈蚀我们不做过多的深究,但在高中阶段我们都知道,铁的锈蚀分为析氢腐蚀和吸氧腐蚀。
在酸性条件下,铁可以发生析氢腐蚀,其反应如下:
负极:Fe-2e===Fe
正极:2H+2e===H↑
总反应:Fe+2H===Fe+H↑
在中性条件下,铁可以发生吸氧腐蚀,其反应如下:
负极:Fe-2e===Fe
正极:2HO+O+4e===4OH
总反应:2Fe+O+2HO===2Fe(OH)
如果水中存在中性盐类物质,可以增加溶液的导电性,加快铁锈蚀的速度。根据吸氧腐蚀的结果可以看到,生成物为Fe(OH),这种物质容易与氧气结合形成Fe(OH),因此在碱性条件下,铁锈蚀的速度可以更加迅速。
活性炭作为一种吸附剂,其表面具有疏松多孔的结构,可以吸附气体。将碳粉和铁粉混合以后可以有效富集氧气,提高反应效率。同时,铁粉与碳粉混合以后可以构成原电池装置,加快反应的速率。
BMP280温度压强传感器是创客教育常用的一种开源硬件。可以广泛应用于中小学教学中,常用来测定温度和压强的变化。根据理想气体状态方程:PV=nRT,在温度和压强一定的情况下,压强和气体体积成反比。根据传感器的数据测出反应前后的温度和压强的变化值,进行计算即可得出气体变化的体积。
四、实验步骤
步骤一:连接仪器检查装置气密性。
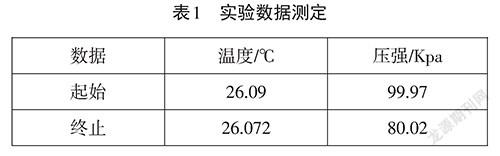
步骤二:打开温度压强控制程序,将温度压强传感器与橡胶塞连接密封。放入锥形瓶内5分钟,待温度和压强示数稳定后记录初始数据,初始温度为26.09℃,压强为99.97 kPa(避免因传感器自身通电后受热引起的温度变化造成实验误差)。
步骤三:将5.0 g铁粉和0.1 g碳粉混合均匀后装入锥形瓶中,滴入10滴左右氢氧化钠溶液和氯化钠溶液,迅速塞上橡胶塞,开启监测系统(见图1)。
步骤四:待温度和压强示数趋于稳定后,将程序中的温度压强数据导出并绘制成折线图。
五、结果分析
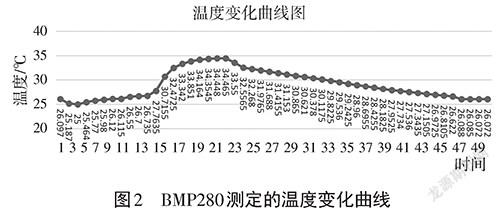
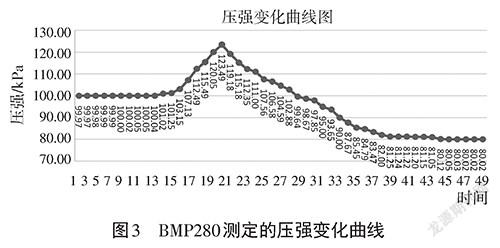
在操作過程中,铁粉反应的时间大概在15~16分钟左右。数据按照每1秒返回一次,共测得温度和压强数据各1051个,剔除无效数据后。按照每20个数据求平均值共得50组数据,将50组数据进行处理得到下图2和图3。
在实验开始前,传感器放在锥形瓶内5分钟,防止因传感器自身受热导致的实验误差。起初铁粉反应较慢,温度上升较慢,随着铁粉发热以后反应速度越来越快,在第20组数据左右,温度达到最大值34.465℃。此时锥形瓶的氧气被消耗完,由于锥形瓶未做保温措施,故温度开始下降。到室温26.072℃趋于稳定。
在实验开始后,铁粉放热,瓶内气体减少。温度在缓慢上升,但是压强几乎不变,在第13组数据开始,温度和压强都迅速上升。在第20组数据左右,压强达到最大值123.49kPa。随后温度下降,压强迅速下降至80.02kPa并趋于稳定。
我们取温度和压强的初始值和最终稳定值进行计算。
根据理想气体状态方程PV=nRT(P代表压强、V代表体积、n表示物质的量,R为常数,T代表温度)。将表格数据带入分别可得:
P×V=n×R×T(起始状态) ①
P×V=n×R×T(终止状态) ②
P×V=n×R×T(若终止状态温度和压强不变) ③
则消耗气体的体积占总气体体积的19.95%,与教材中数据21%相比偏小。分析其原因:
①传感器自身通电后会产生热量,造成温度测定有一定误差,锥形瓶未做保温措施,无法精确地恢复到原来的温度进行测定。若是忽略温度的变化代入数据测得变化量为19.90%。
②锥形瓶内有液体存在,会使得一部分氧气溶解在水中,造成实验数据偏差。
针对上述问题,今后可做适当改进继续进行实验。
六、结语
利用传感器技术测定空气中氧气含量,可以提高实验结果的准确性。当前数字传感已经被广泛应用于各个学科及各个领域,化学作为一门以实验为基础的学科,更加注重数据的准确性和有效性,因此,普及和大力发展数字化实验具有潜在意义。
参考文献
[1]王培明,徐宝刚.利用电烙铁引燃白磷测定空气中氧气的含量[J].实验教学与仪器,2020,37(02):41-43.
[2]郭涛,孙汝中,王臣珠.测定空气里氧气含量实验的探究与创新[J].化学教学,2019(12):55-57.
[3]陆春华.测定空气中氧气含量实验的创新设计[J].中国现代教育装备,2019(22):35-38.
[4]梁雪峰.运用“学习进阶”理论优化初中化学实验教学——以“空气中氧气体积含量的测定”实验为例[J].亚太教育,2019(05):75.
[5]赵娟.空气中氧气含量测定实验的改进[J].中学化学教学参考,2018(22):59.
[6]谢作如.创客教育和STEM教育的2020展望[J].中国信息技术教育,2020(01):10-12.
2620501705323
