建立研究无机物性质的思路与方法
2022-03-17郭瑞云陈红硕王璐
郭瑞云 陈红硕 王璐


摘要:从燃烧条件出发,引出生活中常见的灭火剂,提出常见灭火剂的局限性,引导学生辩证看待问题。从物质类别和化合价角度,对钠的氧化物的化学性质进行预测、分析并验证,建立研究物质性质的思路与方法,运用化学知识解释常见灭火剂的局限性。并通过观察到“酚酞褪色”这一异常现象进一步探究,运用以实验为基础的实证研究方法进行验证。通过物质性质的研究分析钠的氧化物在生活与生产实际中的应用,感受化学的魅力,发展社会参与意识。
关键词:钠的氧化物;物质类别;化合价角度;思路与方法
文章编号:1008-0546(2022)03x-0029-03 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2022.03x.007
一、问题的提出
《关于新时代推进普通高中育人方式改革的指导意见》指出:积极探索基于情境、问题导向的互动式、启发式、探究式、体验式等课堂教学,注重加强课题研究、项目设计、研究性学习等跨学科综合性教学,认真开展验证性实验和探究性实验教学[1]。《普通高中化学课程标准》指出:学科核心素养是学科育人价值的集中体现,是学生通过学习而逐步形成的正确价值观、必备品格和关键能力。其中,“证据推理与模型认知”要求能初步学会收集各种证据,建立证据意识,能基于证据对物质组成、结构及其变化提出可能的假设,通过分析推理加以证实。“科学探究与创新意识”要求能发现和提出有探究价值的问题;能依据探究目的设计并优化实验方案,运用化学实验、调查等方法进行实验探究;善于合作,敢于质疑,勇于创新[2]。基于以上指导思想与理论依据,本案例从物质类别和化合价角度,对钠的氧化物[3]的化学性质进行预测、分析并验证,其核心价值在于利用分类观与价态观指导学生形成基于元素认识物质性质的核心观念与关键能力,建立研究物质性质的思路与方法。从根据钠的氧化物的化学性质辩证的分析常见灭火剂的局限性,引导学生从化学的视角看待问题和解决实际问题,促进学生辩证地看待问题,培养学生参与社会决策的意识。
通过对第一章“物质及其变化”的学习,掌握了分类研究的方法,学生能从分类角度考虑物质的转换,并初步能通过价态变化认识氧化剂与还原剂。但是,学生对从物质类别和化合价角度来研究物质这一过程缺乏感性认识材料。本案例通过对灭火剂局限性讨论,促进学生辩证的看待问题。通过以分类观与价态观对物质化学性质进行研究,为研究物质性质提供一般思路(见图1)。通过验证酚酞褪色原因,初步形成验证物质性质的基本思路。
二、教学过程
1.引入新课
【提问】物质燃烧需要哪些条件?生活中有哪些物质可以灭火?
【回答】可燃物、氧气、达到着火点。水、二氧化碳、沙子。
【过渡】水和二氧化碳一定能灭火吗?
【分组讨论】一部分同学认为可以,一部分同学认为不可以。
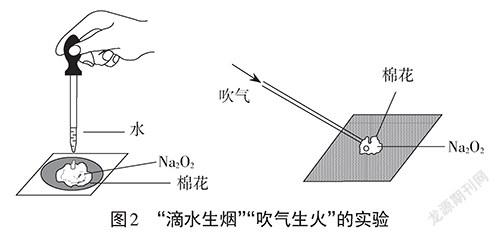
【演示实验】“滴水生烟”“吹气生火”(见图2)。
设计意图:创设真实问题情境,激发求知欲和探索欲,增强学习化学的兴趣和动机。
2.推测钠的氧化物的化学性质(任务一)
【投影】钠的氧化物。
【提问】从物质分类角度分析氧化钠的性质。
【分组讨论】氧化钠属于碱性氧化物,能与水反应,与酸性氧化物反应,与酸反应。
【投影】
Na2O+H2O===2NaOH
Na2O+CO2===Na2CO3
Na2O+2HCl===2NaCl+H2O
【展示】類比碱性氧化物得出化学性质。
【提问】过氧化钠与氧化钠有什么不同?从元素价态的角度分析过氧化钠的性质。
【分组讨论】O为-1价,既能被氧化又能被还原。
【引导】从元素化合价变化的角度出发,同学们判断一下:过氧化钠与水反应的产物。
【分组讨论】过氧化钠中氧元素的化合价为-1,化合价降低,生成氢氧化钠,化合价升高,生成氧气。
设计意图:引导学生从物质分类与元素价态的角度考虑物质的性质,形成分类观与价态观。
【问题解决】如何设计实验检验预测的产物是否正确?
【展示】研究物质性质的思路:
预测性质→设计方案→实验验证
【分组实验】过氧化钠与水反应(见图3)。
现象:固体溶解,有气泡产生,试管壁发热,带火星的木条复燃,滴加2滴酚酞后酚酞先变红后褪色。
【引导】你能根据实验现象写出过氧化钠与水反应的化学方程式吗?
【结论】2Na2O2+2H2O===4NaOH+O2↑,氧气使带火星木条复燃,生成氢氧化钠使酚酞变红。
设计意图:形成验证物质性质的思路,培养学生的证据意识。通过控制变量排除干扰,培养学生严谨求实的科学态度。
【问题解决】为什么酚酞变红后会褪色?
【介绍】资料:酚酞在浓的碱溶液中因生成钠盐而呈无色。
【分组讨论】(1)因为反应后试管很热,所以可能是溶液温度较高使红色褪去。(2)实验所加水较少,红色褪去可能是生成的NaOH浓度较大的缘故。(3)过氧化钠具有强氧化性,生成物中O2、H2O(可能产物)也具有强氧化性,可能使红色物质被氧化漂白。
设计比较性实验进行验证(图4)。
【观察】(1)、(2)变红不褪色,(3)中直接通入氧气变红不褪色,但是加入二氧化锰的试管中,生成使木条复燃的氧气,继续滴加酚酞,溶液变红。
【结论】中间产物过氧化氢使酚酞褪色。
设计意图:进一步培养学生的证据意识以及学生严谨求实的科学态度。
3.学以致用
【问题解决】怎么理解“滴水生烟”的实验?
【回答】反应放热,达到棉花着火点,同时生成氧气有利于燃烧。
【引导】水为非金属氧化物,二氧化碳也属于非金属氧化物,根据过氧化钠与水反应的化学方程式,能写出过氧化钠与二氧化碳反应的化学方程式吗?
【回答】2Na2O2+2CO2===2Na2CO3+O2↑
【问题解决】怎么理解“吹气生火”的实验?
【分组讨论】人体呼出气体主要是CO2。
【投影】
2Na2O2+2H2O===4NaOH+O2↑
2Na2O2+2CO2===2Na2CO3+O2↑
【提問】过氧化钠有什么用途?
【回答】供氧剂与漂白剂。
【提问】燃烧都能用水和二氧化碳灭火吗?过氧化钠着火怎么办?
【回答】用沙土盖灭。
【展示】过氧化钠的用途:供氧剂与漂白剂。
设计意图:燃烧不一定能用水和二氧化碳灭火,使学生能够从物质性质理解其相应的应用。
三、教学反思
1.基于真实情境组织教学,问题层层递进,知识螺旋式上升,在不断反思中实现深度学习。
2.引导学生从化学视角看待和解决实际问题,促进学生辩证看待问题,鼓励学生参与社会决策的意识。
将物质性质的学习融入有关的生活现象和社会问题的分析解决活动中,体现其社会应用价值,充分体现元素化合物与自然界和社会生活的密切联系。
参考文献
[1]国务院办公厅.关于新时代推进普通高中育人方式改革的指导意见[EB/OL]. http://www.gov.cn/zhengce/content/2019-06/19/content5401568.htm.
[2]中华人民共和国教育部.普通高中化学课程标准(2017年版2020年修订)[S].北京:人民教育出版社,2020.
[3]人民教育出版社,课程教材研究所,化学课程教材研究开发中心.普通高中教科书(化学必修第一册)[M].北京:人民教育出版社,2019.
