碳纳米纤维负载铁镍合金在锌空气电池中的应用
2022-03-16刘元震王春琼邹肖肖梅至远蒋静雯刘婷婷
蔡 胜 刘元震 王春琼 邹肖肖 梅至远 蒋静雯 刘婷婷*, 郭 洪*,
(1云南大学材料与能源学院,昆明 650500)
(2云南省烟草质量监督检测站,昆明 650106)
发展和制备高效、经济、稳定的电催化剂是实现高效能源转化和储存的有效途径之一。锌空气电池(ZABs)具有理论能量密度高(1 353 Wh·kg-1)、成本低、安全性良好等优点[1-3],其主要由4部分构成:空气电极(包括涂覆催化剂的气体扩散层)、碱性电解质、隔膜和锌负极[4]。放电时,空气电极处发生氧还原反应(ORR)释放电能;充电时,发生析氧反应(OER)来存储电能[5]。因此,OER是实现可充放电ZABs必不可少的过程,发展和制备高效、经济、稳定的OER催化剂至关重要。
目前常用的OER催化剂多为贵金属材料,如RuO2和Ir/C等,然而其储量少、成本高,严重限制了大规模的商业化应用[6-7],所以,迫切需要开发新型非贵金属OER催化剂。研究表明,过渡金属元素衍生物及其与碳的复合材料具有良好的催化活性[8-13],尤其是基于双金属间的协同效应的催化剂,其催化活性明显高于单金属[14]。Ma等[15]制备的FeNi/NiFe2O4-NC在1 mol·L-1KOH中表现出优异的OER催化活性,当电流密度为10 mA·cm-2时,过电势为316 mV,Tafel斜率为60 mV·dec-1,并且经计时电流法测试后,依然保持优于商用Ir/C的催化活性。此外,为了减少过渡金属纳米颗粒在制备和使用过程中的自发团聚,通常将其负载于多孔碳基纳米材料上[16-21],一般可通过静电纺丝法、无模板法或强碱蚀刻法等实现[22-24]。生物质(如鼠尾草[25]、柳絮[26]、纤维素[27]、蚕丝[28]、废咖啡渣[29])合成的多孔碳纳米材料由于具有制备简单且价格低廉等优点,被广泛用于电催化。Wu等[30]采用无模板法制备了一种由二元FeNi合金/氮化物纳米晶与生物质衍生氮掺杂碳(NC)组成的新型非贵金属基复合催化剂,该催化剂在1.0 mol·L-1KOH条件下表现出良好的OER活性(电流密度为 10 mA·cm-2时,过电势为 310 mV)。然而生物质材料在合成时重复性差,同时薄的二维碳层容易层层叠加,导致碳层基底的活性位点被覆盖,影响了OER催化活性[31-32]。碳纳米纤维具有合成重复性高、导电性好以及耐酸碱腐蚀等优点,因此受到广泛关注[33]。使用静电纺丝技术,通过对聚合物浓度进行有效调控,可以制备不同直径的碳纳米纤维[34-37]。Mo等[38]将通过静电纺丝和磷化处理制备的FeNiP-NCNF复合材料在1.0 mol·L-1KOH电解液中进行OER测试,电流密度为10 mA·cm-2时,过电势为300 mV,塔菲尔斜率为47 mV·dec-1,且经过40 000 s稳定性测试后,仍有92%容量保持率。
我们利用简捷的静电纺丝法,制备了碳纳米纤维负载 FeNi合金的复合催化剂 NiδFe4-δ-CNF(δ=1、2、3)。将该催化剂应用于OER时展现出较好的电催化性能。优异的催化活性主要得益于:(1)双金属之间的协同作用;(2)聚乙烯吡咯烷酮(PVP)在形成三维网状结构之后的碳化过程中,转变成了具有高导电性的碳纳米纤维;(3)嵌入碳纳米纤维中的双金属合金在碳结构的保护下能有效避免电解液带来的腐蚀。将Ni1Fe1-CNF+Pt/C组合作为ZABs的空气阴极催化剂时,展现出比商业Pt/C+RuO2更加优异的功率密度和充放电稳定性。
1 实验部分
1.1 实验药品
PVP(Mw=45 000~58 000,K30)、N,N-二甲基甲酰胺(DMF,99.8%)、乙酸镍(Ⅱ)四水合物(>98%)、乙酸亚铁(Ⅱ)四水合物(>95%)、Nafion 溶液(5%)购自 Aldrich公司,RuO2(99.9%)和20%Pt/C购自英国Johnson Matthey公司,玻璃微纤维滤膜购自Whatman公司。以上药品均为分析纯,使用前无需进一步纯化。
1.2 NiδFe4-δ⁃CNF(δ=1、2、3)的合成
纺丝液的配制:分别称取1.493 g乙酸镍(Ⅱ)四水合物和0.610 g乙酸亚铁(Ⅱ)四水合物、0.995 g乙酸镍(Ⅱ)四水合物和1.220 g乙酸亚铁(Ⅱ)四水合物、0.498 g乙酸镍(Ⅱ)四水合物和1.831 g乙酸亚铁(Ⅱ)四水合物3组乙酸盐。将3组乙酸盐分别溶于25 mL DMF中超声30 min直至完全溶解。然后分别称取4 g PVP加入上述3组溶液中。室温下磁力搅拌24 h直至溶液分散均匀,制得镍、铁物质的量之比分别为3∶1、1∶1、1∶3的纺丝液。
前驱体的制备:用针管抽取纺丝液,使用静电纺丝机进行纺丝,调整推进泵进料速率为1 mL·h-1,高压电源设置为20 kV,铝箔收集滚筒转速为90 r·min-1,喷丝针头与滚筒之间距离为16 cm。纺丝结束后,取下无纺布状前驱体,将前驱体放入真空干燥箱中,120℃干燥24 h。
催化剂的制备:把不同比例前驱体置于氩气流动的管式炉中,热解程序为25~800℃,升温速率为10℃·min-1,在800℃下保持2 h。所得样品根据对应比例分别标记为Ni3Fe1-CNF、Ni1Fe1-CNF和Ni1Fe3-CNF,即NiδFe4-δ-CNF(δ=1、2、3)。同时,将比例为1∶1的前驱体以10℃·min-1的升温速率分别升温至700、900℃并保持2 h,最终制得的样品分别标记为Ni1Fe1-CNF-700、Ni1Fe1-CNF-900。
1.3 电化学表征
所有电催化测试均使用CHI 760E辰华电化学工作站和旋转环盘(PINE公司)在25℃的三电极体系中测得,以Ag/AgCl电极作为参比电极,铂丝作为对电极,玻碳电极作为工作电极(d=5 mm,几何表面积 A=0.196 25 cm2),1.0 mol·L-1KOH 为电解液。测试时,将3 mg催化剂加入1 mL Nafion溶液(0.5%)中并超声分散20 min,取30µL分散液滴涂在干净的玻碳电极上自然风干(负载量为0.459 mg·cm-2)。同时使用商业RuO2催化剂修饰电极作为对照。循环伏安(CV)曲线扫描电位区间为-0.1~0.5 V,扫描速率50 mV·s-1。线性伏安(LSV)曲线扫描电位区间0~1 V,扫描速率5 mV·s-1,工作电极转速1 600 r·min-1。计时电流法测量稳定性时,电压值为0.60 V,时间为35 000 s。为了直观地对比数据,所有电势值均为相对可逆氢电极(RHE)电势(E),计算公式:E=EAg/AgCl+0.059 1 pH+0.197,其中 EAg/AgCl是 Ag/AgCl电极的电势。文中所有的LSV曲线都未经过iR矫正。
1.4 ZABs的组装
ZABs包括阴极、隔膜、阳极、电解液4个部分。将1.5 mg 20%Pt/C和1.5 mg的Ni1Fe1-CNF混合分散在100µL Nafion溶液和900µL去离子水中超声20 min制备得到催化剂分散液(Ni1Fe1-CNF+Pt/C)。取70µL催化剂分散液均匀地涂在碳纸上作为阴极,抛光锌片作为阳极,6 mol·L-1KOH溶液和0.2 mol·L-1Zn(Ac)2作为电解液。碳纸上催化剂的负载量为0.21 mg·cm-2。作为对照,在碳纸上滴加相同负载量的20%Pt/C和RuO2(质量比为1∶1)混合分散液(RuO2+Pt/C)作为阴极。利用Land CT2001A系统测试了ZABs的性能。
1.5 样品表征方法
采用X射线衍射仪(XRD,型号D8 VENTURE,德国布鲁克)对样品进行物相鉴定,测试时使用Cu Kα射线(λ=0.154 18 nm),扫描角度为10°~90°,步长0.02°,管电压40 kV,管电流30 mA。采用场发射扫描电子显微镜(FESEM,型号GeminiSEM 500,德国蔡司)和透射电子显微镜(TEM,型号JEM-2100,日本电子)对样品进行微观形貌表征,测试时工作电压分别为10和200 kV。采用X射线光电子能谱仪(XPS,型号K-Alpha+,赛默飞世尔科技)分析样品表面元素类型和价态,测试时使用单色化Al靶Kα辐射(hν=1 486.6 eV)作为激发源。
2 结果与讨论
2.1 形貌与结构分析
采用静电纺丝法制得碳纳米纤维前驱体,进一步对前驱体高温烧制得到 NiδFe4-δ-CNF(δ=1、2、3)。通过XRD对最终产物进行表征(图1a),煅烧后样品Ni3Fe1-CNF和Ni1Fe3-CNF对应的物相分别为FeNi3(PDF No.38-0419)和 FeNi(PDF No.03-1109)。 样 品Ni1Fe1-CNF的物相为Fe0.64Ni0.36(PDF No.47-1405),其合金相特征峰位于43.763°、50.835°和74.551°处,分别对应(111)、(200)和(220)晶面。26.135°处的特征峰归因于PVP的高温碳化。通过SEM对其进行形貌表征可以发现,静电纺丝法制备的前驱体(图1b)呈现出表面光滑的碳纳米纤维结构,碳化后的Ni1Fe1-CNF(图1c)具备3D网状的碳纳米纤维结构,在纤维表面可以看到FeNi合金颗粒。进一步使用TEM观察Ni1Fe1-CNF合金颗粒和碳层结构(图1d、1f)。图1d中的深色颗粒状物质为FeNi合金,其粒径分布如图1e所示,可以看到粒径主要分布在100~200 nm之间,大部分的粒径大小在100 nm左右。图1f清晰展示了FeNi的晶格,可以看到其晶面间距d=0.2 nm,这与XRD图中FeNi合金相最强峰所对应的(111)晶面间距一致。此外,在合金相边界发现石墨壳层,说明过渡金属被壳层良好包覆。这种结构增强了传输电子的能力,并且石墨外壳的疏水性质,使其在碱性介质中可以有效抵御电解质离子的吸附和渗透,保护内部的过渡金属颗粒不被碱性溶液腐蚀,提高过渡金属颗粒的稳定性[39]。
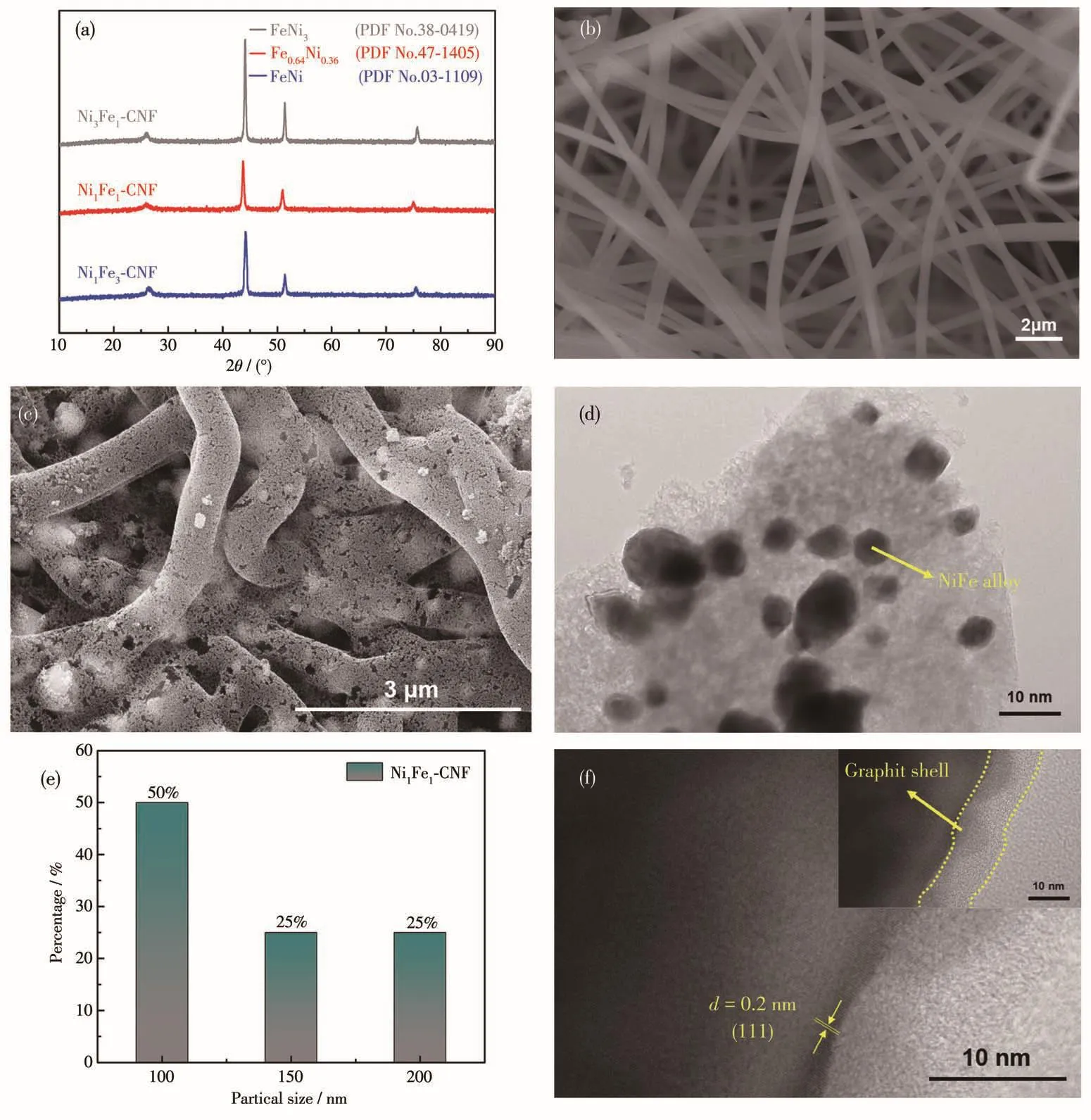
图1 (a)NiδFe4-δ-CNF的XRD图;(b)Ni1Fe1-CNF的前驱体的SEM图;Ni1Fe1-CNF的(c)SEM图、(d、f)TEM图和(e)粒径分布图Fig.1 (a)XRD patterns of NiδFe4-δ-CNF;(b)SEM image of the precursor of Ni1Fe1-CNF;(c)SEM image,(d,f)TEM images,and(e)particle size distribution of Ni1Fe1-CNF
为进一步分析Ni1Fe1-CNF的元素构成,对样品进行了XPS(图2)测试。图2a为Ni1Fe1-CNF的XPS全谱图,可以看出样品中存在C、N、O、Ni、Fe元素,其中C、N、O主要来自PVP。图2b的C1s谱图中有归属于C—C键(284.8 eV)、C=O(288.4 eV)和C—N(285.8 eV)键的特征峰[17]。Fe2p谱图如图2c所示,706.5和717.5 eV处的结合能对应Fe0,710.2和721.1 eV处结合能证明Fe2+的存在,713.3和725.9 eV归属于Fe3+的特征峰。Ni2p谱图如图2d所示,其中结合能为852.6和872.1 eV的2处特征峰对应Ni0,854.6和872.4 eV处的特征峰证明样品中Ni2+的存在。Ni和Fe的氧化态的存在是由于在空气的作用下,FeNi合金纳米颗粒发生了氧化使其表面形成了钝化膜[40]。

图2 Ni1Fe1-CNF的(a)XPS全谱图及(b)C1s、(c)Fe2p和(d)Ni2p高分辨XPS谱图Fig.2 (a)XPS survey spectrum,(b)C1s,(c)Fe2p,and(d)Ni2p high-resolution XPS spectra of Ni1Fe1-CNF
2.2 电催化OER性能研究
对 NiδFe4-δ-CNF(δ=1、2、3)进行 CV 测试,结果如图3a所示,3种催化剂呈现出一定的可逆性,Ni1Fe1-CNF拥有更高的电流密度和更低的起始电位。众所周知,LSV曲线中起始电位(ηonset)及电流密度值(j)达到10 mA·cm-2时对应的过电势值(η10)是研究催化剂OER活性最重要的2个参数。因此,我们测试了NiδFe4-δ-CNF(δ=1、2、3)和商用 RuO2催化剂样品的LSV曲线(图3b),可以看出Ni1Fe1-CNF拥有更小的起始电位,这与CV曲线结果是一致的。图3c显示4种样品的 ηonset和 η10。对比 ηonset和 η10,虽然 Ni1Fe1-CNF的ηonset比RuO2低10 mV,但Ni1Fe1-CNF的η10=280 mV明显优于商用RuO2(η10=310 mV),RuO2表现出更迅速的性能衰减。Tafel斜率反映了催化动力学速率的快慢,由图3d可知,Ni1Fe1-CNF的Tafel斜率值为51.64 mV·dec-1,优于商用RuO2和其他比例的样品,说明Ni1Fe1-CNF催化OER的动力学过程迅速、效率高。电化学双层电容值(Cdl)是衡量催化剂反应效率标准的另一重要参数,其与材料的电化学活性面积呈正比关系[41]。为更加深入地了解各催化剂的反应效率,通过在不同扫速下测试CV曲线进一步拟合了它们的 Cdl值。如图 3e 所示,NiδFe4-δ-CNF(δ=1、2、3)和 RuO2在电压为 1.35 V时 Cdl大小关系 为 Ni1Fe3-CNF(8.65 mF·cm-2)<Ni3Fe1-CNF(11.14 mF·cm-2)<RuO2(20.23 mF·cm-2)<Ni1Fe1-CNF(21.32 mF·cm-2),显然Ni1Fe1-CNF的Cdl优于商业的RuO2和其他比例的催化剂,这说明Ni1Fe1-CNF催化剂拥有更大的电化学活性面积和更多的活性位点。另外,Ni1Fe1-CNF在0.6 V电压下测试35 000 s后依然有83.6%的电流保持率,远优于RuO2的51.3%(图3f)。这得益于石墨壳层的保护,使得内部的过渡金属合金颗粒不被碱性溶液腐蚀,提高了活性中心过渡金属颗粒的稳定性。

图3 在1 mol·L-1饱和O2的KOH电解液中NiδFe4-δ-CNF和RuO2电催化剂的(a)CV曲线、(b)1 600 r·min-1时的LSV曲线、(c)ηonset和η10柱状图、(d)Tafel斜率和(e)Cdl图;(f)Ni1Fe1-CNF和RuO2的稳定性Fig.3 (a)CV curves,(b)LSV curves at 1 600 r·min-1,(c)ηonset,η10histograms,(d)Tafel slopes,and(e)Cdlgraph of NiδFe4-δ-CNF and RuO2electrocatalysts in O2saturated 1 mol·L-1KOH electrolyte;(f)Stability of Ni1Fe1-CNF and RuO2
此外,我们对最佳比例的前驱体在不同烧结温度(700、800、900℃)下进行烧制,将得到的催化剂进行了LSV测试。由图4a可知,Ni1Fe1-CNF的ηonset=260 mV,η10=280 mV,拥有比700和900℃时制备得到的样品更低的过电势,证明了其OER活性最优。综上所述,双金属掺杂比例为1∶1、煅烧温度为800℃时制备的Ni1Fe1-CNF具有最佳的OER催化活性。

图4 不同烧结温度制备的催化剂的(a)LSV曲线和(b)ηonset、η10柱状图Fig.4 (a)LSV curves and(b)ηonset,η10histograms of catalysts prepared at different sintering temperatures
2.3 ZABs性能研究
分别将Ni1Fe1-CNF、RuO2与Pt/C混合作为空气阴极组装ZABs(图5d左上角插图)进行性能研究。Ni1Fe1-CNF+Pt/C组装的ZAB开路电压为1.357 V(图5a),2个ZAB串联后点亮了发光二极管(工作电压1.8~2.2 V,图5c)。图5b的充放电LSV曲线测试结果表明Ni1Fe1-CNF+Pt/C ZAB具有更低的充电电压,这主要得益于Ni1Fe1-CNF优异的OER性能。另外,Ni1Fe1-CNF+Pt/C ZAB在172 mA·cm-2下的功率密度达到了峰值(122 mW·cm-2),明显优于贵金属基RuO2+Pt/C ZAB的功率密度(109 mW·cm-2)。Ni1Fe1-CNF+Pt/C ZAB和RuO2+Pt/C ZAB的充放电循环测试(图5d)表明,二者具有十分接近的放电电压,Ni1Fe1-CNF+Pt/C ZAB在循环了120 h后依然具有较好的稳定性,在经过720个循环(10 min一个循环)后,该电池的充放电电压间隙依然保持在0.80 V左右,充电电压约稳定在1.97 V(图5d右上角插图)。相比之下,贵金属基的催化剂在60 h以后充电电压急剧升高(约2.20 V)。上述结果表明,Ni1Fe1-CNF作为可充放电ZABs的阴极材料时具有较低的充电电压和充放电循环稳定性。

图5 (a)ZAB开路电压;(b)Ni1Fe1-CNF+Pt/C ZAB和RuO2+Pt/C ZAB的放电LSV曲线和功率密度曲线;(c)ZABs点亮发光二极管照片;(d)Ni1Fe1-CNF+Pt/C ZAB和RuO2+Pt/C ZAB充放电循环曲线Fig.5 (a)Open circuit voltage of ZAB;(b)Discharge LSV curves and power density curves of Ni1Fe1-CNF+RuO2and RuO2+Pt/C;(c)Photo of ZAB lighting up leds;(d)Charge/discharge cycle curves of Ni1Fe1-CNF+RuO2ZAB and Pt/C+RuO2ZAB
3 结 论
将FeNi二元合金负载于碳纳米纤维上制备得到的Ni1Fe1-CNF催化剂展现出优异的OER性能(ηonset=260 mV,η10=280 mV)。以Ni1Fe1-CNF+Pt/C作为空气阴极催化剂组装成ZAB,该电池实现了高达122 mW·cm-2的功率密度,经过720圈循环后依然拥有约0.80 V的充放电电势差。其优异的性能主要源于双金属间的协同作用及碳纳米纤维的高导电性,而且嵌入碳纳米纤维中的双金属合金在碳结构的保护下有效地提升了Ni1Fe1-CNF的稳定性。总之,采用双金属纳米颗粒嵌入导电基底上构筑一体化自支撑电极的方法,可以明显提高纳米颗粒载量并实现两者良好的接触,增强电子转移,降低内部电阻,从而延长电极的使用寿命。
致谢:感谢云南大学现代分析测试中心提供的样品检测服务。
